16.6:
Расчеты титрования: сильная кислота - сильное основание
16.6:
Расчеты титрования: сильная кислота - сильное основание
Расчет pH для титрационной растворов: Сильная кислота/сильная основание
Титрование выполняется для 25.00 мл 0.100 M HCl (сильная кислота) с 0.100 M сильного основание NaOH. PH в различных объемах добавленного основание раствор может быть рассчитан следующим образом:
(A) объем титранта = 0 мл. PH раствор обусловлен ионизацией HCl кислотой. Поскольку это сильная кислота, ионизация завершена, а молярность ионов гидрония составляет 0.100 M. pH раствор является следующим:

(b) объем титранта = 12.50 мл. Так как кислотный образец и титрант основание являются как монопротическими, так и одинаково концентрированными, это титрантное добавление включает в себя меньше, чем стехиометрическое количество основание, и поэтому оно полностью потребляется реакцией с избыточной кислотой в пробе. Концентрация оставшейся кислоты вычисляется путем вычитания потребленной суммы из первоначальной суммы и деления на объем раствор:
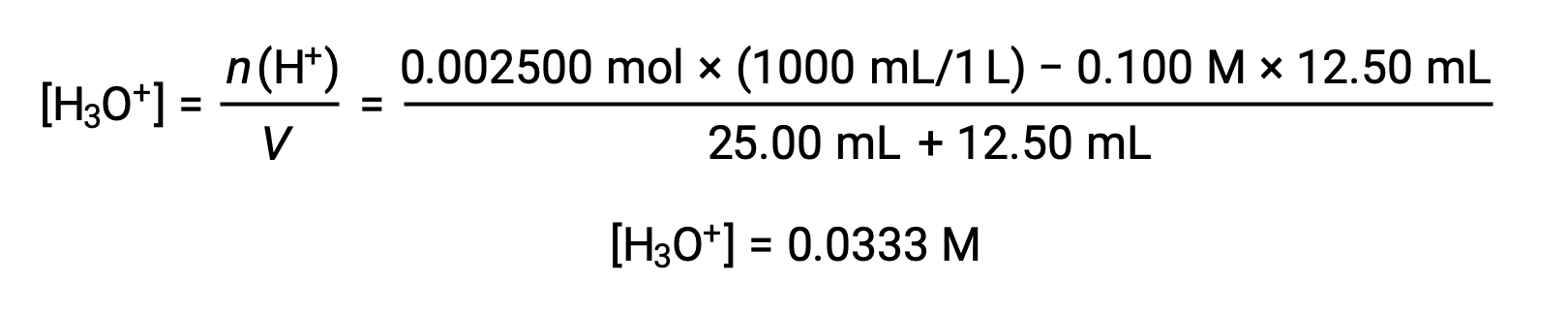
(c) объем титранта = 25.00 мл. Это титрантное добавление включает стехиометрическое количество основание (точка эквивалентности), и поэтому только продукты реакции нейтрализации находятся в раствор (вода и NaCl). Ни катион, ни анион этой соли не подвергаются ионизации кислотно-основная; единственным процессом, генерирующим ионы гидрония, является аутопротеолиз воды. раствор находится в нейтральном положении, с pH = 7.00.
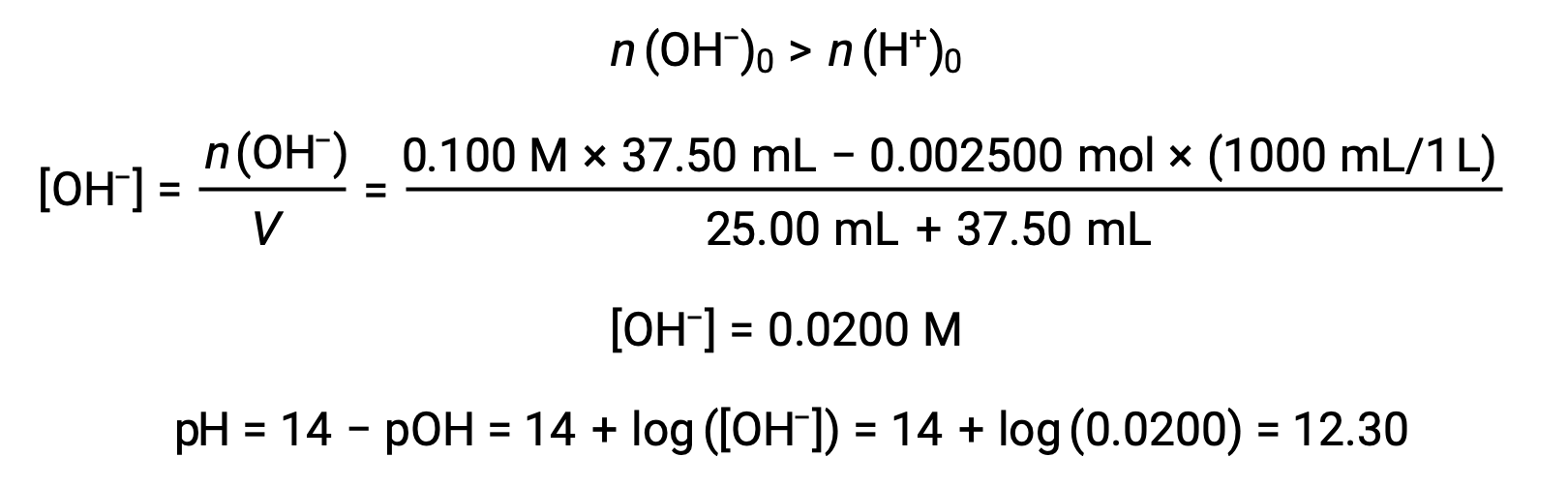
(d) объем титранта = 37.50 мл. Это предполагает добавление титранта, превышающего точку эквивалентности. Затем pH раствор рассчитывается с использованием концентрации ионов гидроксида:
Этот текст адаптирован из Openstax, Химия 2е изд., раздел 14.7: Титраки кислотно-основная.
