9.5:
放射性減衰及び放射性年代
9.5:
放射性減衰及び放射性年代
放射性崩壊は、不安定な核種の自然崩壊であり、試料中のすべての原子核が同時に崩壊するわけではないので、ランダムな過程です。単位時間あたりの崩壊数を放射能(A)といい、試料中の原子核の数に比例します。崩壊定数(λ)は、単位時間における原子核あたりの崩壊の平均確率です。
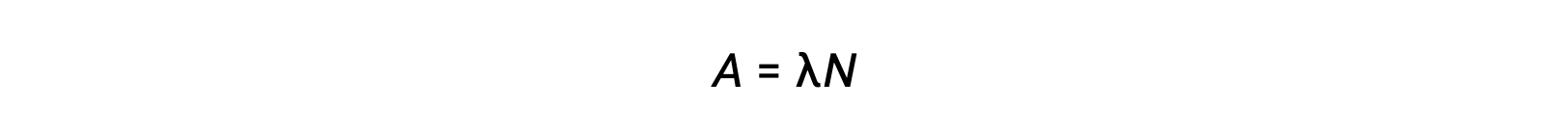
放射能のSI単位はベクレルで、これは1秒間に1回の崩壊を意味します。放射能の別の単位はキュリーで、370億ベクレルに相当します。異なる放射性核種の放射能と時間をプロットすると、崩壊速度が異なることがわかります。放射能がある値からその値の半分になるまでの時間を半減期といい、t1/2と表記されます。
放射能は放射性原子の数に比例するため、時間とともに放射性試料が減ると減少します。数学的には、放射性核種の放射能は指数関数的な式で示されます。
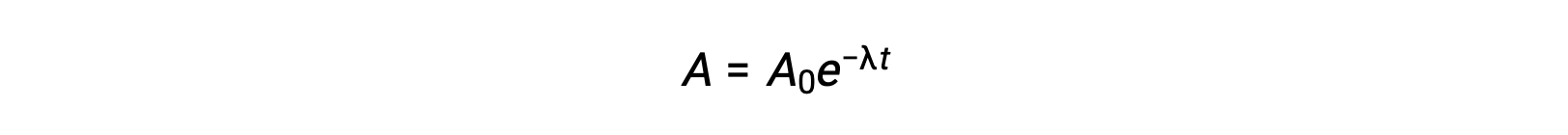
このように、活性が半分になると、式を並べ替えることで半減期を計算することができ、半減期は崩壊定数に反比例しています。
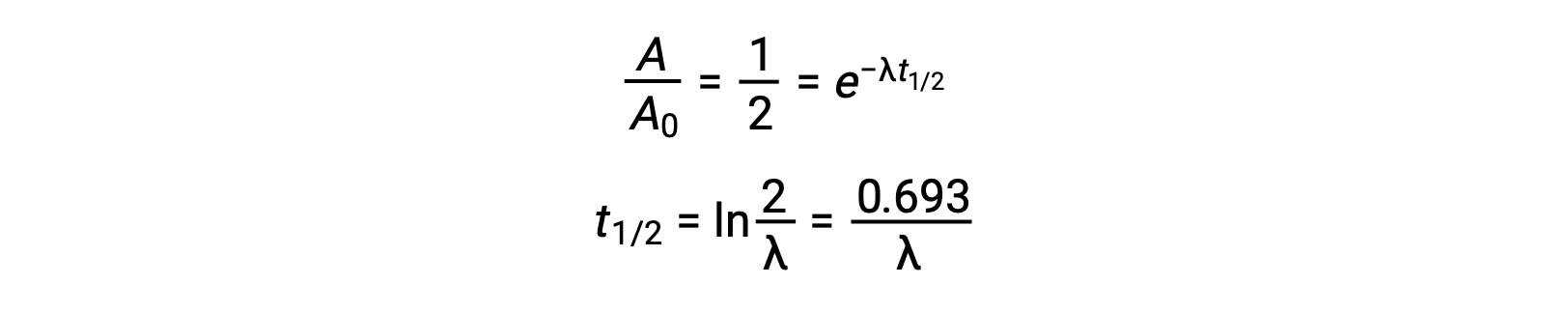
半減期は放射性核種に固有の性質であり、不安定な核種の原子は、完全に孤立した真空中にあっても、他の多くの核種の原子が存在する試料中にあっても、同一の半減期を持ちます。放射性核種の半減期は様々であり、ラドン-220の半減期は1分である(100万個の原子が1分で50万個になり、さらに1分で100万個の4分の1になる)のに対し、トリウム-232の半減期は140億年です。
放射性同位元素は半減期を持つため、考古学的な遺物やかつての生物、地層などの時間的な起源を調べる「年代測定」の目的に適しています。
半減期5730年の放射性核種である炭素-14は、生物の一部を構成していた年代を測定する方法を提供します。この放射性年代測定法は、約3万年前までの炭素を含む物質の年代を正確に測定することができ、最大で約5万年前までの年代を測定することができます。
自然界に存在する炭素は、地球上の炭素の約99%を占める炭素-12、約1%を占める炭素-13、そして微量の炭素-14の3つの同位体で構成されています。炭素-14は、大気上層部で宇宙線による中性子と窒素原子が反応して生成します。
すべての炭素の同位体は、酸素と反応してCO2分子を生成します。したがって、生きている植物や動物は、炭素-14と炭素-12の比率が大気と同一です。しかし、生きている植物や動物が死ぬと、炭素の補給が止まり、放射性の炭素-14が継続的に崩壊することで、炭素-14と炭素-12の比率が減少し始めます。例えば、考古学的に発見された木製品の炭素-14と炭素-12の比が生きている木の半分であれば、その木製品は5730年前に伐採された木から作られたことになります。炭素-14と炭素-12の比率は、質量分析計を使うことで、1ミリグラムという非常に小さなサンプルであっても高精度に測定することができます。
放射性年代測定では、半減期の長い他の放射性核種を使って、より古い年代についても測定することもできます。例えば、ウラン-238は一連の過程を経て鉛-206に崩壊するので、岩石の年代(地球上で最も古い岩石のおおよその年代)を確定するのに利用できます。ウラン-238の半減期は45億年なので、元々あったウラン-238の半分が崩壊して鉛-206になるには、それだけの時間がかかます。鉛の同位体である鉛-208がほとんど含まれていない岩石では、その岩石が形成されたときに鉛は存在しなかったと考えることができます。したがって、U-238:Pb-206の比率を測定・分析することで、岩石の年代を決定することができます。これは、存在するすべての鉛-206がウラン238の崩壊によって生じたと仮定しています。もし、鉛-206がさらに存在する場合、それは試料中に他の鉛同位体が存在する可能性を意味するため、それに応じた調整が必要です。カリウム・アルゴン年代測定も同様の方法で行われます。カリウム-40は陽電子放出と電子捕獲によって崩壊し、半減期12.5億年のアルゴン-40になります。岩石を砕いて出てくるアルゴン-40ガスの量を測定し、Ar-40:K-40の比を求めれば、岩石の年代がわかります。
上記の文章は以下から引用しました。 Openstax, Chemistry 2e, Section 21.3: Radioactive Decay.
