9.5:
Decaimento Radioativo e Datação Radiométrica
9.5:
Decaimento Radioativo e Datação Radiométrica
A radioatividade é uma desintegração espontânea de um nuclídeo instável e é um processo aleatório, uma vez que todos os núcleos da amostra não decaem simultaneamente. O número de desintegrações por unidade de tempo é chamado de atividade (A), que é diretamente proporcional ao número de núcleos na amostra. A constante de decaimento (λ) é uma probabilidade média de decaimento por núcleo em tempo unitário.
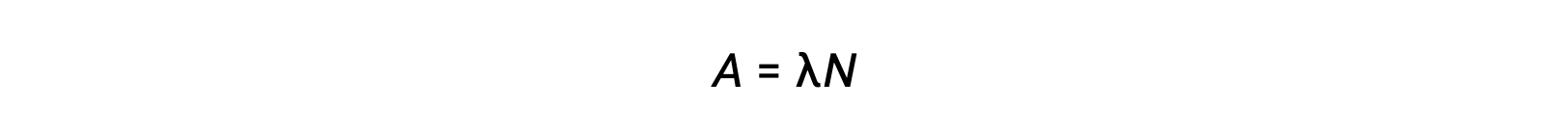
A unidade SI para a atividade é o becquerel, que é uma desintegração por segundo. Outra unidade de atividade é o curie, que equivale a 37 mil milhões de becquerels. O gráfico da atividade vs tempo para diferentes radionuclídeos indica diferentes velocidades de decaimento. O tempo necessário para que a atividade caia de qualquer valor para metade desse valor é uma meia-vida, indicada como t1/2.
Como a atividade é proporcional ao número de átomos radioativos, ela diminui com o tempo à medida que a quantidade de amostra diminui. Matematicamente, a atividade de um radionuclídeo é indicada por uma equação exponencial:
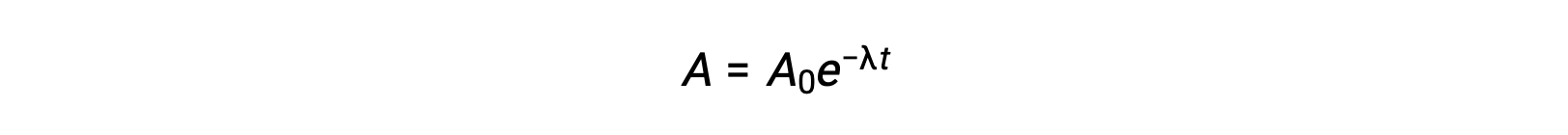
Assim, quando a atividade é reduzida para metade, rearranjar a equação fornece uma maneira de calcular a meia-vida, que é inversamente proporcional à constante de decaimento.
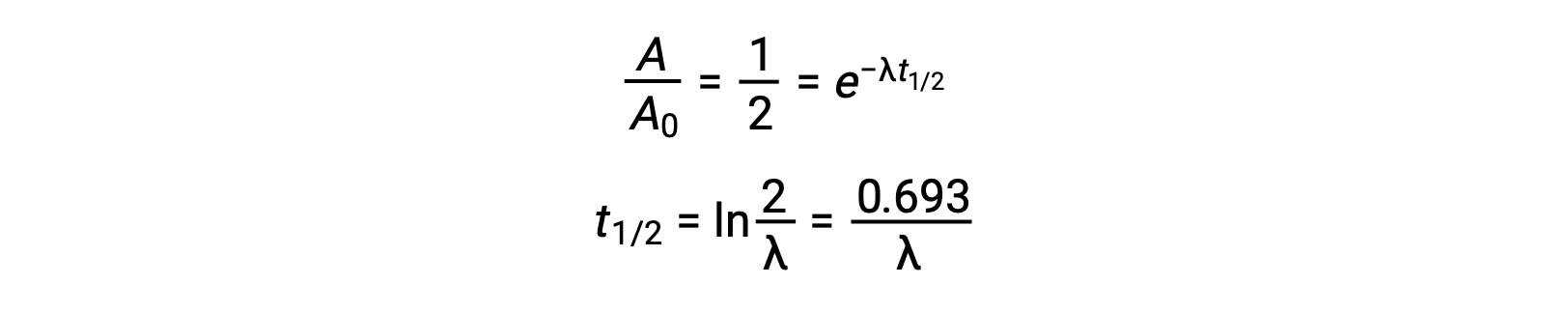
Uma meia-vida é uma propriedade intrínseca de um radionuclídeo, e qualquer átomo único de um nuclídeo instável tem a mesma meia-vida independentemente de estar completamente sozinho em um vácuo ou em uma amostra com muitos outros átomos desse nuclídeo. A meia-vida dos radionuclídeos varia amplamente: o rádon-220 tem uma meia-vida de 1 minuto: um milhão de núcleos decaem para meio milhão em um minuto e decaem mais até um quarto de milhão em outro minuto. No entanto, o tório-232 tem uma meia-vida de 14 mil milhões de anos.
Vários radioisótopos têm meias-vidas e outras propriedades que os tornam úteis para fins de “datar” a origem temporal de objectos como artefactos arqueológicos, organismos anteriormente vivos, ou formações geológicas.
O carbono-14, um radionuclídeo com meia-vida de 5730 anos, fornece um método de datação de objectos que faziam parte de um organismo vivo. Este método de datação radiométrica é preciso para datar substâncias contendo carbono que têm até cerca de 30.000 anos de idade e pode fornecer datas razoavelmente precisas até um máximo de cerca de 50,000 anos de idade.
O carbono que ocorre naturalmente é composto por três isótopos: O carbono-12, que constitui cerca de 99% do carbono na terra; o carbono-13, cerca de 1% do total; e quantidades residuais de carbono-14. O carbono-14 forma-se na atmosfera superior pela reação de átomos de azoto com neutrões a partir de raios cósmicos no espaço.
Todos os isótopos de carbono reagem com oxigénio para produzir moléculas de CO2. Assim, plantas e animais vivos têm uma razão de carbono-14 para carbono-12 idêntica à atmosfera. Mas quando a planta ou o animal morre, o reabastecimento de carbono pára, e a razão de carbono-14 para 12 começa a diminuir à medida que o carbono-14 radioativo decai continuamente. Por exemplo, se a razão de carbono-14 para carbono-12 em um objeto de madeira encontrado em uma escavação arqueológica for metade do de uma árvore viva, isso sugere que o objeto foi feito a partir de madeira cortada há 5730 anos. Determinações de razões de carbono-14 para carbono-12 altamente precisas podem ser obtidas a partir de amostras muito pequenas (tão pouco como um miligrama) utilizando um espectrómetro de massa.
A datação radioativa também pode utilizar outros nuclídeos radioativos com meias-vidas mais longas para datar eventos mais antigos. Por exemplo, o urânio-238, que decai em uma série de passos até chumbo-206, pode ser utilizado para determinar a idade de rochas (e a idade aproximada das rochas mais antigas na terra). Uma vez que o urânio 238-tem uma meia-vida de 4,5 mil milhões de anos, é necessário esse período de tempo para metade do urânio-238 original decair para chumbo-206. Em uma amostra de rocha que não contém quantidades apreciáveis de chumbo-208, o isótopo mais abundante de chumbo, podemos supor que o chumbo não estava presente quando a rocha foi formada. Portanto, medindo e analisando a razão de U-238:Pb-206, podemos determinar a idade da rocha. Isto pressupõe que todo o chumbo-206 presente provém da deterioração do urânio-238. Se existir chumbo-206 adicional, indicado pela presença de outros isótopos de chumbo na amostra, é necessário proceder a um ajuste. A datação potássio–árgon usa um método semelhante. O potássio-40 dacai por emissão de positrões e captura de eletrões para formar árgon-40 com uma meia-vida de 1,25 mil milhões de anos. Se uma amostra de rocha for esmagada e a quantidade de gás árgon-40 que escapa for medida, a determinação da razão Ar-40:K-40 produz a idade da rocha.
Este texto é adaptado de Openstax, Chemistry 2e, Section 21.3: Radioactive Decay.
