9.5:
Desintegración Radiactiva y Datación Radiométrica
9.5:
Desintegración Radiactiva y Datación Radiométrica
La radiactividad es la desintegración espontánea de un nucleido inestable y es un proceso aleatorio, ya que todos los núcleos de la muestra no decaen simultáneamente. El número de desintegraciones por unidad de tiempo se denomina actividad (A), que es directamente proporcional al número de núcleos de la muestra. La constante de desintegración (λ) es una probabilidad media de desintegración por núcleo en unidad de tiempo.
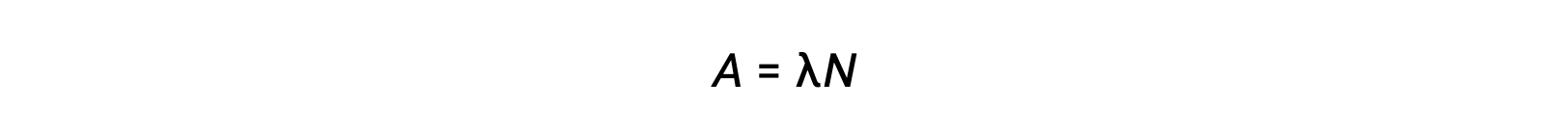
La unidad SI para la actividad es el becquerel, que es una desintegración por segundo. Otra unidad de actividad es la curie, que equivale a 37 mil millones de becquereles. El gráfico de la actividad frente al tiempo para diferentes radionucleidos indica diferentes velocidades de desintegración. El tiempo requerido para que la actividad caiga desde cualquier valor a la mitad de ese valor es una vida media, indicada como T1/2.
Como la actividad es proporcional al número de átomos radiactivos, esta disminuye con el tiempo a medida que disminuye la cantidad de muestra. Matemáticamente, la actividad de un radionucleido se indica mediante una ecuación exponencial:
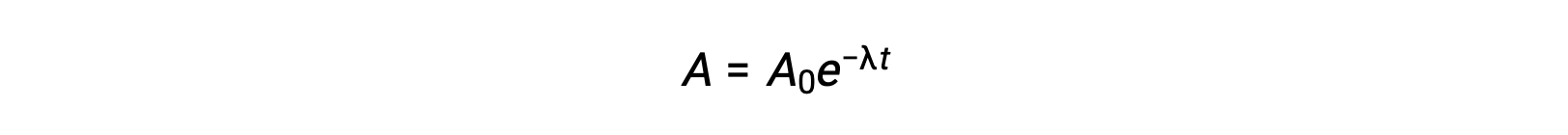
Por lo tanto, cuando la actividad se reduce a la mitad, la reorganización de la ecuación proporciona una manera de calcular la vida media, que es inversamente proporcional a la constante de desintegración.
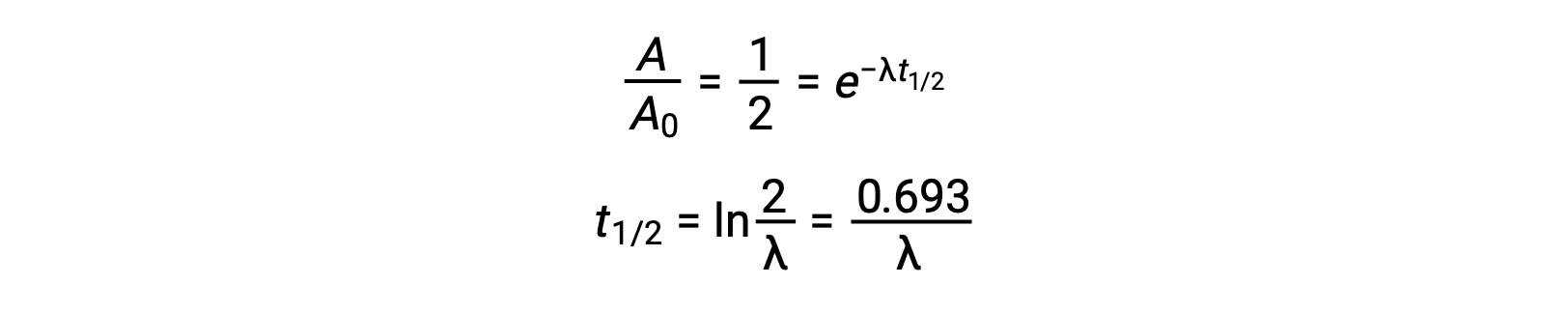
Una vida media es una propiedad intrínseca de un radionucleido, y cualquier átomo único de un nucleido inestable tiene la misma vida media, independientemente de si está completamente solo en un vacío o en una muestra con muchos otros átomos de ese nucleido. Las semividas de los radionucleidos varían ampliamente: El radón-220 tiene una semivida de 1 minuto: Un millón de núcleos se desintegran hasta medio millón en un minuto y se desintegran aún más hasta un cuarto de millón en otro minuto. Sin embargo, el torio-232 tiene una vida media de 14 millones de años.
Varios radioisótopos tienen semividas y otras propiedades que los hacen útiles para “datar” el origen temporal de objetos tales como artefactos arqueológicos, antiguos organismos vivos o formaciones geológicas.
El carbono-14, un radionucleido con una vida media de 5730 años, proporciona un método para datar objetos que eran parte de un organismo vivo. Este método de datación radiométrica es preciso para datar sustancias que contienen carbono de hasta unos 30.000 años de antigüedad y pueden proporcionar fechas razonablemente precisas en hasta un máximo de unos 50.000 años de antigüedad.
El carbono natural consiste en tres isótopos: Carbono-12, que constituye aproximadamente el 99% del carbono en la tierra; carbono-13, alrededor del 1% del total; y trazas de carbono-14. El carbono-14 se forma en la atmósfera superior por la reacción de los átomos de nitrógeno con neutrones de los rayos cósmicos en el espacio.
Todos los isótopos de carbono reaccionan con oxígeno para producir moléculas de CO2. Así, las plantas y animales vivos tienen una proporción de carbono-14 y carbono-12 idéntica a la atmósfera. Pero cuando la planta o el animal vivo mueren, la reposición de carbono se detiene y la relación carbono-14 a 12 comienza a disminuir a medida que el carbono radiactivo-14 decae continuamente. Por ejemplo, si la relación carbono-14 a carbono-12 en un objeto de madera encontrado en una excavación arqueológica es la mitad de lo que es en un árbol vivo, esto sugiere que el objeto fue hecho de madera cortada hace 5730 años. Se pueden obtener determinaciones muy precisas de las relaciones carbono-14 a carbono-12 a partir de muestras muy pequeñas (tan sólo un miligramo) utilizando un espectrómetro de masas.
La datación radiactiva también puede utilizar otros nucleidos radiactivos con semividas más largas para datar eventos más antiguos. Por ejemplo, el uranio-238, que se desintegra en una serie de pasos en plomo-206, puede utilizarse para establecer la edad de las rocas (y la edad aproximada de las rocas más antiguas de la tierra). Dado que el uranio-238 tiene una vida media de 4,5 millones de años, se necesita esa cantidad de tiempo para que la mitad del uranio-238 original se convierta en plomo-206. En una muestra de roca que no contiene cantidades apreciables de plomo-208, el isótopo más abundante de plomo, podemos suponer que el plomo no estaba presente cuando se formó la roca. Por lo tanto, midiendo y analizando la proporción de U-238:Pb-206, podemos determinar la edad de la roca. Esto supone que todo el plomo-206 presente vino de la desintegración del uranio-238. Si hay plomo-206 adicional presente, que se indica por la presencia de otros isótopos de plomo en la muestra, es necesario realizar un ajuste. La datación de potasio-argón utiliza un método similar. El potasio-40 decae por emisión de positrones y captura de electrones para formar argón-40 con una vida media de 1,25 mil millones de años. Si una muestra de roca es triturada y se mide la cantidad de gas argón-40 que escapa, la determinación de la relación Ar-40:K-40 produce la edad de la roca.
Este texto es adaptado de Openstax, Química 2e, Sección 21.3: Desintegración Radiactiva.
