5.3:
이상기체 법칙의 응용: 몰질량, 밀도, 부피
5.3:
이상기체 법칙의 응용: 몰질량, 밀도, 부피
물질의 한 두더지가 차지하는 볼륨은 어금니 볼륨입니다. 이상적인 가스 법인 PV = nRT는주어진 양의 가스의 양과 지정된 가스 부피의 두더지 수가 압력과 온도의 변화에 따라 달라지는 것을 시사합니다. 표준 온도 및 압력 또는 STP(273.15 K 및 1 atm)에서 이상적인 가스의 두더지 1개(정체성에 관계없이)의 두더지는 약 22.4L의 부피를 가지며 이는 표준 어금니 부피라고 합니다.
예를 들어, 수소, 산소, 아르곤 또는 이산화탄소각각의 두더지 1개가 STP에서 22.4리터를 차지합니다. 이는 STP의 가스 0.5두더지가 11.2L의 부피를 차지하고 있으며, 이와 유사하게 STP의 모든 가스 의 2두더지가 44.8L의 부피를 차지한다는 것을 의미합니다.
이상적인 가스 법은 가스의 화학적 정체성에 관계없이 압력, 부피, 두더지 수 및 가스 온도와 관련된 보편적입니다.
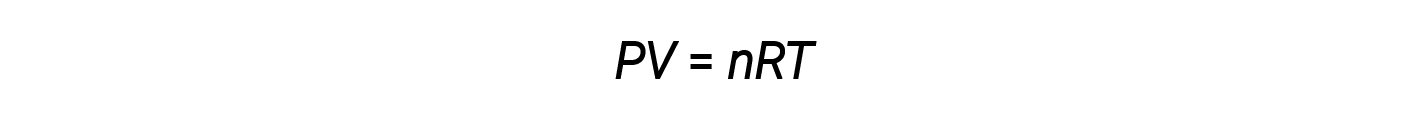
반면에 가스의 밀도 D는 그 정체성에 의해 결정됩니다. 밀도는 볼륨보다 질량의 비율입니다. 이상적인 가스 방정식을 재배치하여 V를 분리하고 밀도 방정식 수율로 대체합니다.
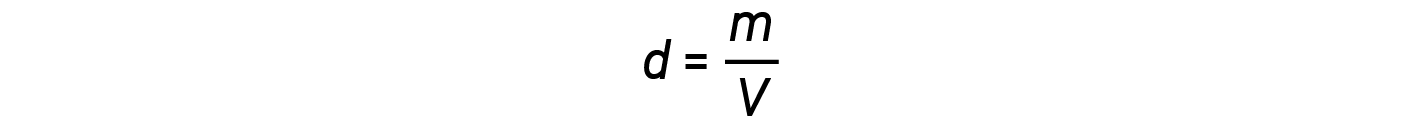
비율 m/n 즉, 두더지 위에 질량, 어금니 질량의 정의입니다, M:
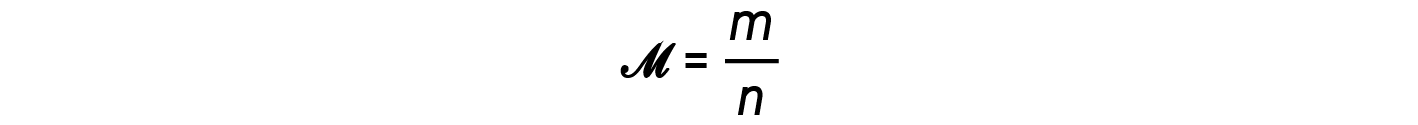
그런 다음 밀도 방정식을
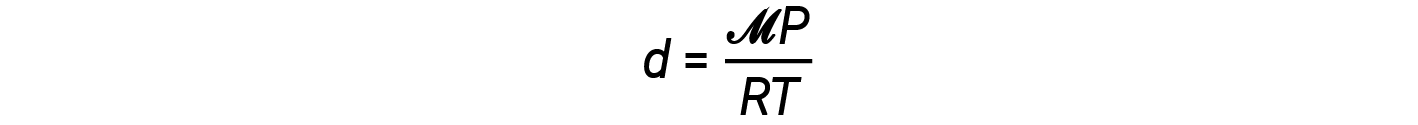
이 방정식은 가스 밀도가 압력 및 어금니 질량에 직접 비례하며 온도에 반비례한다는 것을 알려줍니다. 예를 들어, CO 2(어퍼 질량 = 44 g/mol)는 N2(어퍼 질량 = 28 g/mol) 또는 O2(어퍼 질량 = 32 g/mol)보다 무겁고, 따라서 공기보다 밀도가 높습니다. 이러한 이유로CO2는 CO2 소화기에서 화재를 진압하여O2가 가연성 물질에 도달하지 못하도록 합니다. 열기구의 리프팅 현상은 동등한 어금니 덩어리(예: 공기)의 가스가 더 높은 온도에서 밀도가 낮기 때문에 열기구가 떠있을 수 있다는 관계에 달려 있습니다.
이 텍스트는 Openstax, 화학 2e, 섹션 9.3: 기체 물질의 스토이치오메트리, 혼합물 및 반응에서 채택됩니다.
