5.4:
气体混合物-道尔顿分压定律
A subscription to JoVE is required to view this content. Sign in or start your free trial.
JoVE Core
Chemistry
Mixtures of Gases: Dalton’s Law of Partial Pressures and Mole Fractions
纯气体的压力是它的 粒子和周围表面之间分 子碰撞的总和。一个在给定体积中有较少粒子的气体样本 在相同体积中,会施加比较多粒子 的样本较低的压力。但是不同气体的混合物压力是多少?对于多组成的混合气体,压力就是来自所有气体分 子碰撞的总和。假定混合物里的每个成分 会施加自己的压力,这个压力是独立于其 他存在的气体的。这个来自任何单一成分的压力 叫做它的分压。理想气体混合物的总压 等于它的组成物分压的总和。这个观察是道尔顿分压定律。透过应用理想气体定律,各个气体 组成成分的分压将被 可测量的变数替代。由于混合物中的气体占据相同的体积 且在同样的温度下,可以简化方程式。各个组成物的莫耳数和 等于所有气体组成物的莫耳数,n-总数。因此,混合气体的总压力 等于n总数乘以常数R-T/V 化合物的莫耳数除以 混合物的总莫耳数是莫耳分数。重新排列总莫耳数的莫耳分数,并代换道尔顿分压定律 中的n总数,得出 总压的表达式。再重新排列,混合气体中的分压 是它的莫耳分压 和混合物的总压的乘积。所以,在混合气体中,任何化合物 的分压,i,等于i的莫耳分数 乘以总压。作为范例计算,假设一个容器装有 两种气体,氦气和氩气,40%的体积是氩气。这意味着氩气的穆尔分压是 0.4。如果总压是 4atm,氦气的分压式多少?使用气体分压方程式,氩气的分压等于它的莫耳分数 乘以总压。因此,0.4 乘以 4atm 可得出氩的分压 是 1.6 atm 因为分压的总和 等于总压,方程式 可以被重新排列使得氩的分压 从总压当中被减去。因此,氦的分压是 2.4atm。
5.4:
气体混合物-道尔顿分压定律
除非个别气体彼此发生化学反应,否则混合气体中的个别气体不会相互影响压力。混合物中的每种气体所施加的压力与单独存在于容器中时所施加的压力相同。每种气体在混合物中施加的压力称为其分压。
这意味着在包含三种不同气体A,B和C的混合物中,如果 P A 是气体A的分压; P B 是气体B的分压; P C 是气体C的分压;则总压力由公式1给出:
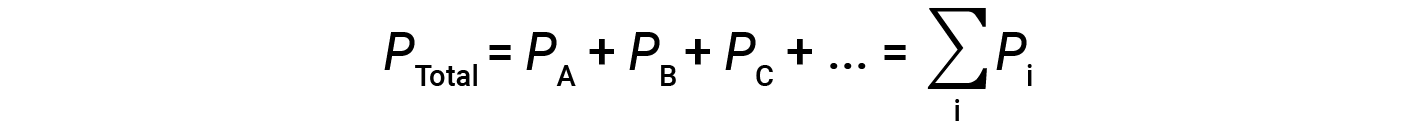
这是道尔顿分压定律:理想气体混合物的总压力等于组成气体分压的总和。
让 n A , n B 和 n C 是混合物中每种气体的摩尔数。如果每种气体都遵循理想气体方程,则分压可以写为:
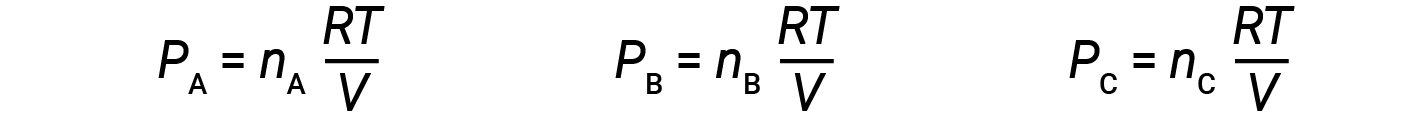
由于所有气体处于相同的温度且占据相同的体积,因此代入等式1可得出:
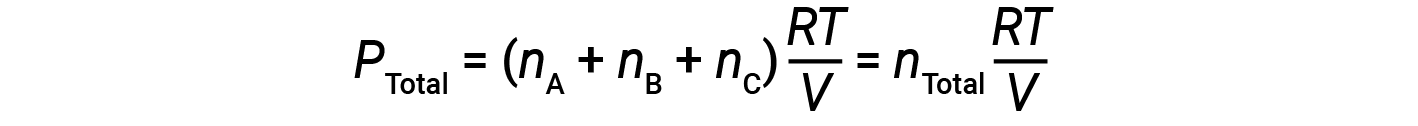
该方程式表明,在恒定温度和恒定体积下,气体样品的总压力取决于存在的气体的总摩尔数。
对于气体混合物,引入一个称为摩尔分数的量是很方便的,它的定义是混合物中特定物质的摩尔数除以存在的所有物质的摩尔数。数学上,物质A与B和C的混合物中的摩尔分数表示为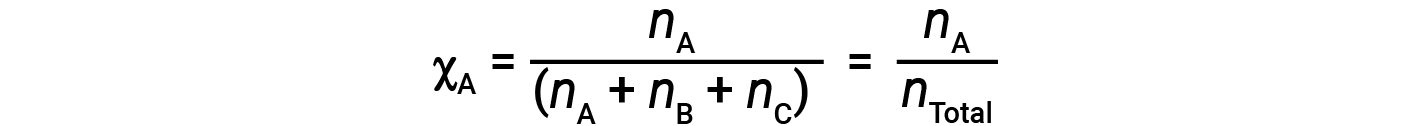
类似地,B和C的摩尔分数是;
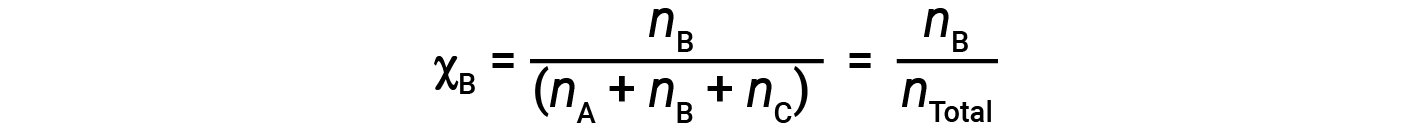
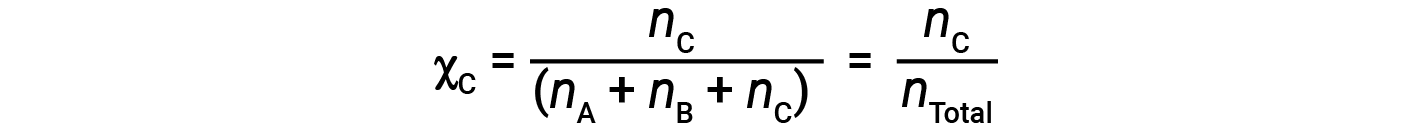
结合A的摩尔分数方程和分压方程得出:
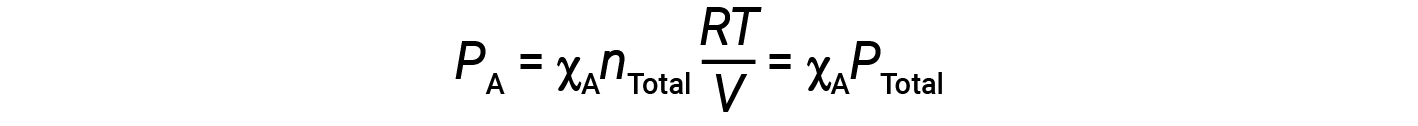
气体A的分压通过其摩尔分数与混合气体的总压力相关。
换句话说,气体在气体混合物中的压力是其摩尔分数与混合物总压力的乘积。
Tags
Mixtures Of GasesDalton’s Law Of Partial PressuresMole FractionsPressure Of A Pure GasMolecular CollisionsGas SampleParticlesVolumeMulticomponent Gas MixtureCollisions From All Gas MoleculesPartial PressureTotal PressureIdeal Gas MixtureDalton’s Law Of Partial PressuresIdeal Gas LawMeasurable VariablesMoles Of The Individual ComponentsTotal Number Of MolesGas ComponentsConstant RT Over VMole Fraction
