11.12:
加热和冷却曲线
A subscription to JoVE is required to view this content. Sign in or start your free trial.
JoVE Core
Chemistry
Heating and Cooling Curves
加热或冷却物质会导致温度变化,然后发生相变。加热某物质会增加其分子的热能,这反映为温度的升高,直到达到转变点为止。当物质吸收了足够的热量时,其分子之间的吸引力便被克服,导致在恒定温度下 发生相变。一旦转变完成,加热 将导致温度再次升高。当热量从物质中去除时,其分子的热能下降,对应温度会下降,直到达到转变点为止。然后,在相变过程中会重新建立 更强的分子间力,同时温度保持恒定。可以使用加热曲线或冷却曲线对物质响应温度变化的行为 进行建模,其中对温度变化与所添加热量或所去除热量的函数关系 进行绘图。来看一下一个装满冰块的烧杯,初始温度为 20°C。随着热量的流入,冰的温度 稳步上升。在使冰变暖过程中吸收的热量 取决于冰的比热容。一旦达到冰的熔点,尽管热量不断流动,温度 会停止升高。吸收的热量会减弱分子间作用力,直到冰完全 融化成液态水。有一个固液平衡平台是 恒温下相变的特征。平台的开始点和结束点之间的焓变 指示融化过程所需的热量,或者换句话说,是水的熔化焓。融化过程结束后,吸收的热量会导致温度 相应地线性上升。水的比热容 决定了所吸收的热的量。达到沸点时,温度停止上升。吸收的热量反而 有助于克服水分子之间的吸引力,直到水完全蒸发为止。液-气平衡平台代表 恒定温度下的相变。平台开始点和结束点之间 的焓变是 水的蒸发焓。在所有液体转化为蒸气之后,额外的热量会导致温度再次升高。
11.12:
加热和冷却曲线
当与环境隔离的物质发生热变化时,会观察到该物质的温度和相位的相应变化;这通过加热和冷却曲线以图形方式表示。
例如,加热会升高固体的温度;吸收的热量取决于固体的热容量 (q = mcsolidΔT)。根据热化学,物质吸收或释放的热量q及其伴随的温度变化ΔT之间的关系是:
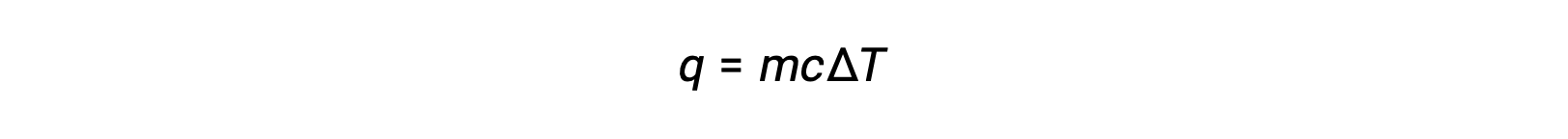
其中 m 是物质的质量, c 是物质的特定热量。 关系适用于正在加热或冷却的物质,但不会改变状态。
当温度足够高时,固体开始熔化 (图 1 , A 点)。 吸收的热量取决于固体的热容量 (q = mcsolidΔT),在熔点上观察到一个高原。 高原表示状态从固体变为液体,在此期间温度不会因熔化热(q = mΔHfusion) 而升高。 换言之,进一步热增益是分子间吸引力减少而不是分子动能增加的结果。 因此,当物质的状态发生变化时,其温度保持不变。
一旦固体完全熔化 (图 1 , B 点) ,液体就会开始升温,温度会升高。 吸收的热量取决于液体的热容量(q = mcliquidΔT)。 当液体到达沸点时,液体开始汽化 (图 1 ,点 C) ,尽管持续加热,温度仍保持不变。由于汽化热 (q = mΔHvap),在液体向气体过渡期间,在液体的沸点处观察到另一个平稳度 (恒定温度)。 只要是沸腾,液体就会保持同样的温度。 如果以更高的速度加热,液体温度不会升高,而是沸腾会变得更强 (快速)。 所有液体汽化后 (图 1 ,点 D) ,气体温度会升高。
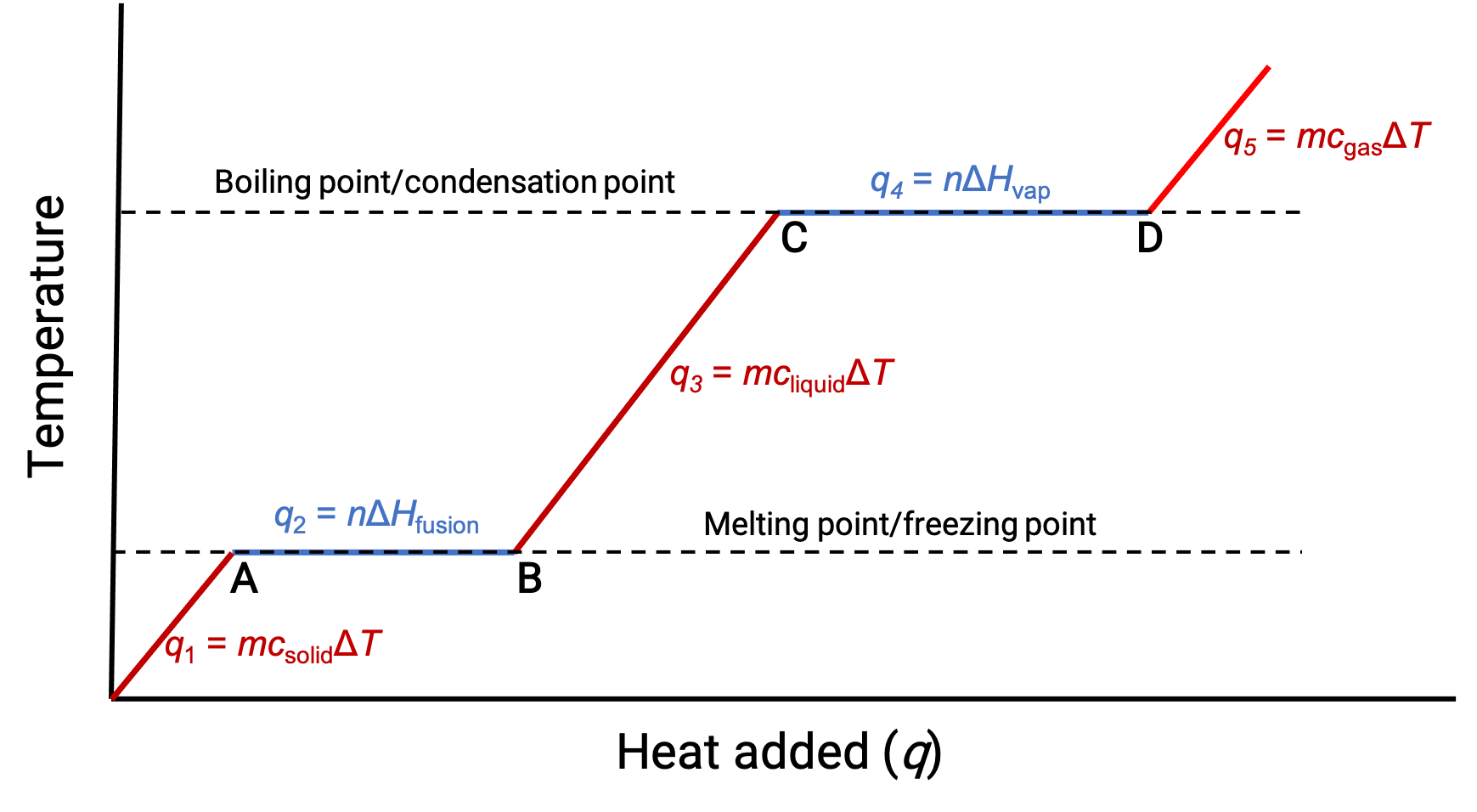
图 1. 物质的典型加热曲线描述了随着物质吸收越来越多的热量而导致的温度变化。 当物质低于相变时,曲线中的平台 (恒定温度的区域) 会显示出来。
本文改编自 Openstax, 化学 2e, 第10.3节:相变。
