16.8:
指示薬
16.8:
指示薬
ある種の有機物質は、ヒドロニウムイオン濃度が特定の値に達すると、希薄な溶液中で色を変えます。例えば、フェノールフタレインは、ヒドロニウムイオン濃度が5.0 × 10−9 M (pH < 8.3)以上の水溶液中では無色の物質です。ヒドロニウムイオン濃度が5.0 × 10−9 M (pH > 8.3)以下の塩基性の溶液では、赤色やピンク色です。フェノールフタレインのように、溶液のpHを測定することができる物質を酸塩基指示薬といいます。酸塩基指示薬には、弱有機酸または弱有機塩基があります。
弱酸性である酸塩基指示薬メチルオレンジの溶液の化学平衡は、複雑なメチルオレンジ分子を単純に表現したHInを用いた式で表すことができます。
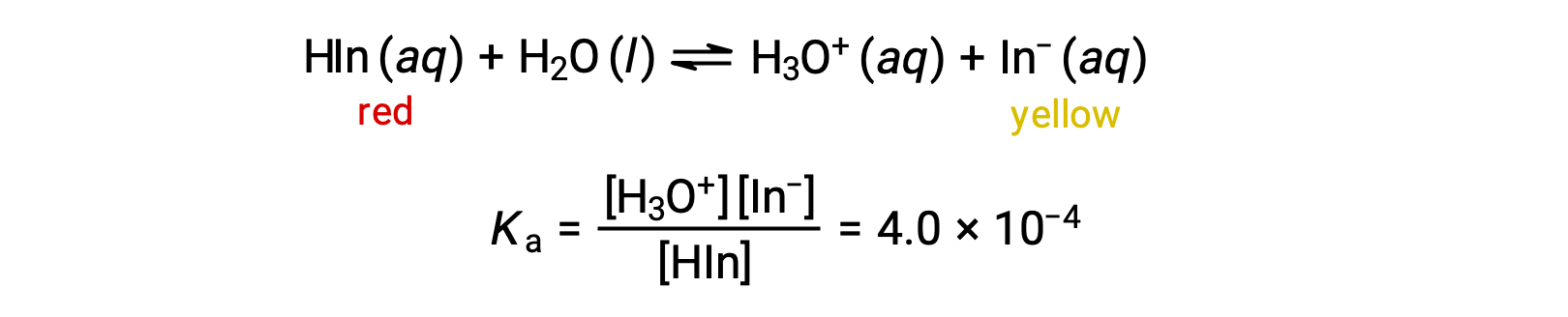
メチルオレンジの陰イオンであるIn−は黄色で、非電離体であるHInは赤色です。メチルオレンジの溶液に酸を加えると、ヒドロニウムイオンの濃度が上昇し、ルシャトリエの原理によって赤色の非電離体に平衡がシフトします。塩基を加えると、平衡は黄色側にシフトします。この挙動は緩衝剤の作用と類似しています。
指示薬の色は、In−とIn−の濃度比によって決まり、指示薬の大部分(約60%以上)がIn−として存在する場合、溶液の色は黄色になります。大部分がHInとして存在する場合は、溶液の色は赤色に見えます。ヘンダーソン・ハッセルバルヒ式は、指示薬溶液のpHとその組成(したがって、知覚される色)の関係を理解するのに役立ちます。
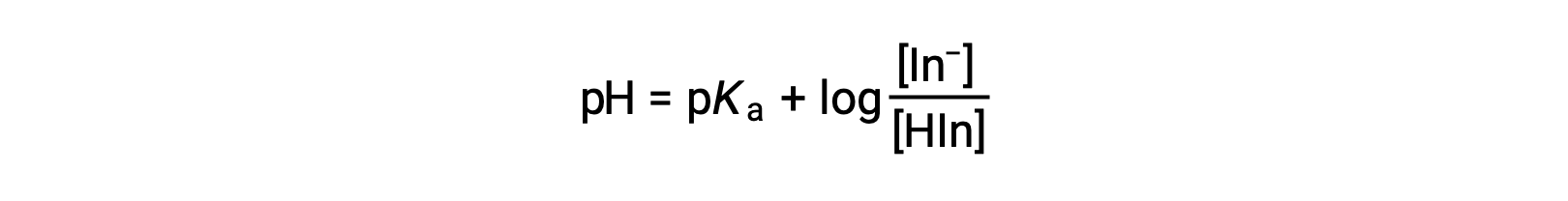
pH > pKaの溶液では、対数項は正のため、指示薬の共役塩基形が過剰(黄色の溶液)であることを示しています。pH > pKaの場合、対数項は負のため、共役酸が過剰(赤色の溶液)であることを示します。溶液のpHが指示薬のpKaに近いときは、共役塩基と共役酸が同程度存在するため、溶液の色はそれぞれの足し合わせとなる(黄色と赤色でオレンジになる)。酸塩基指示薬の変色区間(またはpH区間)は、色の変化が観察されるpH値の範囲として定義され、ほとんどの指示薬では、この範囲はおよそpKa ±1となっています。
酸塩基指示薬には、幅広いpH値をカバーする多くの種類があるため、未知の溶液であってもおおよそのpHを決定することができます。万能指示薬やpH紙は、pHによって異なる色を示す複数の指示薬から構成されます。
上記の文章は以下から引用しました。Openstax, Chemistry 2e, Section 14.7: Acid-Base Titrations
Suggested Reading
Coleman, William F. "Molecular models of indicators." Journal of Chemical Education 87 no.1, (2008):1152 https://pubs.acs.org/doi/pdf/10.1021/ed800038w.
