Summary
双水相系统,用于同时图案多个的细胞群体。此快速和容易的方法,细胞图案利用葡聚糖和聚乙二醇的水溶液,和两者之间的聚合物溶液中存在的界面张力的相分离。
Abstract
细胞图案化技术,速度快,易于使用,价格合理的高通量细胞分析平台的未来发展将需要研究细胞间的相互作用和组织工程化系统。此详细的协议描述了一种用于产生的细胞的共培养物,使用生物相容的解决方案的葡聚糖(DEX)和聚乙二醇(PEG),发生相分离时,在阈值以上的浓度相结合的方法。细胞可以使用此方法的配置的各种图案。可以通过印刷在基板上的液滴的DEX和覆盖它们的PEG含有细胞的溶液进行细胞排斥构图。两者之间的聚合物溶液形成的界面张力,使细胞落在对DEX液滴周围的外侧,并形成了一个环形的结算可以用于迁移实验。细胞岛可以分配到的PEG溶液的细胞丰富的DEX阶段,或图案覆盖的DEX液滴与PEG的溶液。共培养物,可形成直接与地塞米松岛屿构图通过结合细胞排斥。这些方法兼容的各种液体处理方法,包括手动微穿刺,可用于几乎任何粘附的细胞类型。
Introduction
双水相的系统(ATPSs)形式时,两种不相容的聚合物的溶液混合在一起,在足够高的浓度。相分离的影响,由多种因素,其中包括的聚合物的分子量和极性,温度下的溶液,pH值和离子含量的水性溶剂1,2。在该点的两种聚合物溶液单独确定由所选择的三相系统的理化性质,但一般发生在低聚合物的浓度(小于20%重量/重量),在非变性条件下,允许将用于生物技术的ATPSs应用程序3-9。
到目前为止研究得最广泛的ATPS是聚乙二醇(PEG)/葡聚糖(DEX)系统。由这些廉价的和生物相容的聚合物形成的ATPS最初被描述为纯化的生物分子的分子的分区2,10的方式。分区没有贡献的相位系统的额外的分子或颗粒时,会发生混合与PEG和DEX。基于它们的相对亲和力地塞米松或PEG,分子或颗粒内的两个阶段中的一个或界面处将优先驻留。另一个特性PEG / DEX ATPS的是两种聚合物相之间的界面张力的存在。由PEG和DEX ATPSs形成一般显示是低得多的比其他如油和水的液-液两相体系的界面张力;然而,界面张力仍然发挥效果的小颗粒,如病毒,细胞和蛋白质总量2 11-13。最后,因为较高分子量的PEG和DEX单独的生理浓度的盐的存在下,在低浓度(小于5%的高分子量的聚合物品种的重量/重量),有一些对哺乳动物细胞的任何有害的影响,如果在这些注册成立系统14-16。
近日,界面性质和分区的ATPSs已被应用于本实验室的细胞图案14,16-20。这是通过缩微更密集地塞米松溶液对PEG的存在下,在细胞培养基材。当细胞被纳入PEG相,他们被排除进入对DEX由于PEG / DEX界面张力20的液滴。当细胞被图案化中的DEX相,它们被保持在通过界面张力和分区16,17,19的细胞培养基材的表面上。
在对比等方法进行细胞图案,ATPS的细胞图案是简单易学,只需要基本的知识有关的聚合物,并能进行细胞培养和使用微量移液器。细胞图案的其他方法往往涉及专门的设备和培训,不容易被转换为日e生活科学。例如,一些方法(微接触印刷或喷墨印刷)图案细胞间接通过施加模式的细胞粘附的生物分子到培养基材,随后作为电池附件21,22的网站。尽管间接方法对于某些类型的细胞是有用的,它们需要用户的技能和专门的设备来制造图案形成工具的高度的,并且可以取决于对特定类型的细胞/生物分子图案缺乏特异性。此外,细胞可以沉积模式特异性高的方式直接图形的方法,包括层流图案,制版和喷墨印刷23日至26日 。然而,这些技术也需要用户的专业知识和专门的设备,在印刷过程中,可能会损坏细胞。尽管这些方法通常会产生的细胞,细胞图案的精确模式是一个有用的工具,在生命科学领域,它必须是符合成本效益的一个实现ND简单。
在这里,我们报告的详细描述在我们之前发布的应用程序使用ATPSs产生图案的细胞培养协议。只使用微量移液器,用户可以生成细胞的禁区或细胞的岛屿迁移实验。这是通过PEG / DEX的界面张力,可以保持细胞在对DEX相中或排除细胞沉积在从DEX PEG相方式。通过梳理上述两个基本图案形成技术,它是可能的,以迅速产生如肝成纤维细胞共培养的细胞的共培养。图案形成方法,ATPS参数和预期结果进行详细说明。
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1。相体系相分离的特性:确定阈值
- 准备含有PEG和DEX的解决方案中所需的缓冲区或细胞培养基中所示,在图1(紫色的点)在15毫升或50毫升锥形管。在下文中,PEG和DEX将参考35 kDa的PEG和500 kDa的DEX;然而,临界浓度会改变,这取决于所用的两种聚合物。记录每个解决方案中的质量PEG和DEX。高浓度聚合物解决方案可能需要几个小时才能溶解。无血清的解决方案可用于涡旋。含有蛋白或血清,把试管放在两种聚合物的摇摆阶段,直到完全溶解。记录的重量,所使用的介质的初始浓度溶解的聚合物和注意到。
- 一旦聚合物充分溶解,解决方案应该会出现混浊。这是第一个迹象表明已发生相分离。为了证实这一点,让聚合物溶液在一个垂直的位置,在室温下20分钟的休息。离心以1,000 xg离心可以用于加速的相分离过程。密集的底部阶段将DEX丰富,顶部阶段将PEG丰富。
- 慢慢地添加额外的缓冲或媒体的管。应使用小的增量,以便不进行过冲的相分离点。
- 当该溶液变得清晰和不再相离心后分离,相分离的阈值已被达到。记录管的最终重量。
- 使用以前的记录的权重的聚合物,随着添加媒体后的最终重量,确定%wt / wt的每两个在该相分离的聚合物中不再出现。
- 绘制这些值作为%wt / wt的PEG对y轴和%wt / wt的DEX在x-轴。称为双结点曲线,此图中,可以用来确定的阈值浓度的相分离为不同的concentrati在一个特定的细胞培养基中的PEG / DEX附加。
2。配置1:排除图案(96孔板格式)
- 准备单独的解决方案,为5.0%wt / wt的PEG和12.8%wt / wt的DEX细胞培养液中。使用双水相的至少两倍的临界点的解决方案,以确保保持ATPS后的聚合物相对于彼此平衡。有一个小的量的磁通的DEX到的富含PEG的相,反之亦然,因此,工作太附近的临界浓度,可导致损失的浓度下降到低于临界点的相位系统。同样地,将细胞培养皿中的湿度和温度控制培养箱可以改变两相性能,使两种溶液混溶的。注:某些细胞可能有更好的表现与其他ATPS配方。上可接受的制剂,可以选择是根据从第1部分上的双结点曲线确定。
- 收获细胞,用于排斥patterning。确定可用的细胞的总数目/浓度。可选:标记的细胞与CellTracker或其他的非细胞毒性的标签为荧光显微镜。
- 沉淀细胞,将沉淀重悬于5.0%的适当体积的PEG排除,以达到所需的细胞数。例如,一个96孔板需要37,500成纤维细胞重新悬浮在200μl的PEG产生合流翌日。适用于其他类型的细胞和文化基板尺寸缩放这些数字。
- 使用微量移液器,免除0.5微升滴的DEX到干细胞培养基质。较大的体积的液滴产生较大的禁区。液滴大小不等,从0.1到1微升建议排除缩微。可选:DEX液滴可以沉积提前24小时的时间,并允许在室温下进行脱水。这可能会产生更清洁的模式。
- 分配的200μl的PEG细胞悬液到吨他很好地掩饰的DEX液滴。
- 在加湿培养箱中培养12小时,在37℃下,5%CO 2的地点。确保菜不倾斜,在处理过程中,它被放置在一个水平的培养箱搁板,以避免破坏模式。
- 取出的PEG溶液,用200μl的培养基中洗涤三次。
- 加入新鲜的培养基中,并返回到培养箱。
- 定期监测的文化隔离区观察到细胞的运动。
3。配置2:岛图案(96孔板格式)
- 准备5.0%wt / wt的PEG和12.8%wt / wt的DEX在细胞培养基中,如上述的解决方案。
- 收获细胞用于岛屿构图。确定可用的细胞的总数目/浓度。
- 颗粒和重悬的细胞在适当体积的12.8%DEX岛屿构图以达到所需浓度的细胞。 5000行政长官的浓度LLS /μl以下建议强粘附性的细胞类型。对于细胞,具有难以附着或松散附着的细胞,最多至10,000个细胞/微升的浓度也可以考虑。
- 工作迅速,以避免干燥,移液管加入0.5μl的DEX液滴到干细胞培养基材中,如上所述。不要让水滴干。可选:可以向孔中加入200μl的PEG溶液的时间提前。 DEX液滴,然后可以存入PEG的解决方案,在那里他们将沉入水底的文化联系面。这可能会产生更清洁的岛模式。
- 量的DEX液滴用200μl的PEG。
- 在加湿培养箱中培养12小时,在37℃下,5%CO 2的地点。确保菜不倾斜,在处理过程中,它被放置在一个水平的培养箱搁板,以避免破坏模式。
- 取出的PEG溶液,用200μl的培养基中洗涤三次。
- 添加新的培养介质和返回培养箱。
- 定期监测的文化观察细胞运动和增殖向外的岛屿。
4。配置3:排除文化(96孔板格式)
- 准备5.0%wt / wt的PEG和12.8%wt / wt的DEX在细胞培养基中,如上述的解决方案。
- 收获细胞用于排斥和岛屿构图。确定的总的数目/浓度的细胞,可用于不同的细胞类型。可选:有些细胞配对可能会显示增殖指数显着不同。为了防止被排除在外的的细胞overpopulating岛图案的细胞(尤其是长期文化),2小时排除与丝裂霉素C用于治疗的细胞,他们收获前或照射。这将防止扩散。来区分两种细胞群,如果必要,可以使用荧光CellTracker染料。
- 颗粒细胞和悬浮颗粒exclusioŇ图案形成在适当体积的10.0%的PEG,以达到所需的细胞数,如上述。将沉淀重悬于岛图案形成在适当体积的12.8%DEX,以达到所需的浓度的细胞,如上述。
- 使用微量移液器,免除0.5微升滴DEX细胞悬液到干细胞培养基质。不要让水滴干。
- 量对DEX用200μl的PEG细胞悬浮液的液滴。
- 在加湿培养箱中培养12小时,在37℃下,5%CO 2的地点。确保菜不倾斜,在处理过程中,它被放置在一个水平的培养箱搁板,以避免破坏模式。
- 删除的PEG溶液,并在200μl的培养基中洗涤三次。
- 加入新鲜的培养基中,并返回到培养箱。
- 监视共培养,观察细胞群之间的相互作用。可选:可以控制排斥或岛屿的图案逐张进行准备idually,通过共培养细胞不发生相互作用,或通过阻断利益途径之前或之后,图案形成在一个或两个细胞群。
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
要选择PEG和DEX细胞图案的适当组合,重要的是要确定的双结点曲线。这条曲线描绘的点,可以形成一个ATPS可以改变为一组给定的基础上的温度,pH值和离子含量的聚合物。用于培养细胞的需要定制的培养基配方中,可能有必要通过实验确定的双结点曲线。这是通过产生一系列ATPSs是远离的双结点和在他们的PEG和DEX内容变化( 图1,紫色圆圈)。 ATPS是本时,聚合物溶液出现混浊混合时,将到单独的相,如果平衡左不受干扰。通过加入额外的溶剂的聚合物混合物,ATPS将接近0%的PEG / 0%DEX。在某些时候,该混合物将不再相分离。在发生这种情况的PEG / DEX浓度表示的双结点曲线上的一个点;那点之上一个AT,PS可以形成和下面这一点上它不能。在图1中的曲线代表binodals三种常见的与不加10%牛胎儿血清(FBS)的细胞培养介质。 ATPS形成在其中的浓度稍高的胎牛血清(FBS)的存在。
在我们以前的报告中,我们使用的基础上的临界点(在该点上的双节相等体积的PEG和DEX平衡后的形式)的2.5%的PEG 35 kDa/3.2%DEX 500 kDa的。ATPSs我们的双节数据的结果是在接近这个临界点值。我们测试了九个相系统的图案化的组合,如表1中所示。因为纯PEG和DEX的解决方案相对于他们的聚合物浓度达到平衡后,它们被组合,一些这些解决方案没有形成稳定ATPSs的,并且,对于用于图案化( 表1a中,x标记),因此没有用处。其他聚合物组合识别的模式,但没有足够均匀实验( 表1a X /“✓”商标“)。有用的聚合物的配方形成的禁区或在非图案化区域( 表1a,✓标记的)几乎没有细胞的岛屿。
10%PEG,我们发现,细胞形态异常轮和纺锤状24小时后,细胞显示一个附加的文化面( 表1b,X标记)的能力降低。形态和附件分别为2.5%和5%PEG( 表1b,✓标记的)的正常现象。我们观察到,血清在高浓度PEG( 表1c中,x标记)从培养基中析出,这表明在10%PEG的异常细胞的形态和附件可与血清的访问的问题有关。此外,PEG是已知扰乱质膜27。虽然只观察到这些效果在高浓度的低摩尔ecular量的PEG,它是最好,,使用PEG浓度最低,提供了可靠的图案。
我们以前的报告相一致,我们得出结论,5%PEG/6.4%地塞米松和5%PEG/12.8%DEX非常适合的细胞图案,12.8%DEX统一模式。预期结果的三个图案化格式,使用Cell跟踪标记的HeLa细胞在图2中所示。通过以下每个图案的方法,它是可能的每种类型创建统一的图案以外的图案化的区域,具有非常少的细胞。
使用排除和岛屿图案,它是可以评估的图案细胞的增殖和迁移( 图3)。在为期三天的HeLa细胞充满了禁区( 图3A-C)。岛图案化的细胞从最初的模式( 图3d-f)的向外扩大。这些变化可以定量标准ImageJ的测量工具( 图3 C,F)。重要的是要注意,当多个细胞群共培养( 图2,格式3),一个细胞群体可能出增殖和更换其他。排除图案和岛屿的图案可以是非常有用的工具,以评估是否这将是一个问题。在增殖指数发生戏剧性的差异的情况下,它是建议一个细胞群体被处理的照射或化学因素,以限制其增殖。使用一种细胞类型作为支持细胞的生长较慢的更敏感的细胞类型中的情况下,这是特别有用的。
我们证明了这一原则,培养HepG2细胞,肝癌细胞株,常用于肝细胞生物学模型,与NIH 3T3成纤维细胞用丝裂霉素C( 图4),被逮捕的。随着时间的推移,HepG2细胞保持其国产化ð的菌落形状( 图4a)。在相同的板,并通过将许多液滴他们周围与成纤维细胞,它是可以用于多路复用的研究( 图4b)是潜在有用的格式,这些细胞在增长。用这种格式作为旁分泌因子的影响( 图4c)的控制,可以使用细胞岛单作物。
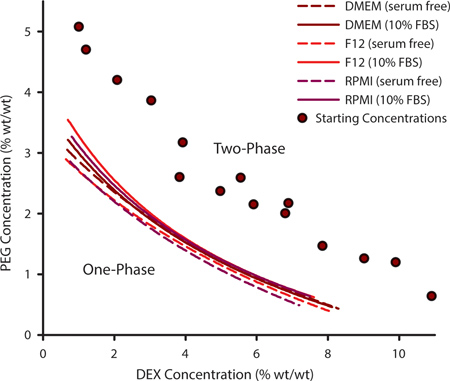
图1。其中ATPS可形成的聚合物浓度可以从实验确定的双结点曲线外推,这双结点曲线构建使用的浊点的方法,通过添加额外的溶剂来测量的点,不同的PEG / DEX浓度的两相混合物(紫色圆)不再有能力的阶段separatiNG。 Binodals被确定为无血清DMEM,F12和RPMI。的数据点进行拟合三参数有理函数。 N = 3,为每个数据点。

图2。通过配药ATPS到聚苯乙烯板的解决方案,可以产生用于细胞构图三种格式,该过程开始DEX液滴通过移液),再涂上与PEG b)。一旦细胞附着,的ATPS解决方案可以被冲走替换培养基(C,D)。荧光图像为单一种植染色后图案的CellTracker染料。共培养,细胞染色,之前图案CellTracker染料。 HeLa细胞被用来生成所有三个文化格式。 
图3。排除图案和岛屿的图案,可以用来评估细胞迁移和增殖。一)排除图案的HeLa细胞后第1天的图案。 二)排除图案的HeLa细胞后第3天的图案。 三)细胞增殖和迁移,显着减少的大小禁区四)岛图案的HeLa细胞后第1天的图案。 五)岛图案的HeLa细胞后第3天的图案,F)细胞增殖和迁移的向外,显着扩大的大小岛屿。使用ImageJ软件,可以衡量的细胞结算和细胞岛区的前,后迁移图像进行量化。酒吧代表的意思±SEM至少三名独立意见的。

图4。肝细胞/成纤维细胞培养,可以使用的ATPS排除合作的文化图案。)这些殖民地保持他们的组织至少4天的文化。b)多岛可以排列在一个单一的菜有潜力的复用或高通量测定三)与非共培养的岛屿模式相比,共培养的细胞显示白蛋白生产水平略高(褐色染色)显而易见的,从定性比较白蛋白染色的共培养物对单作物。白蛋白是由肝细胞产生的一种蛋白质。因此,这样的结果表明,肝细胞的功能被增强时使用ATPS与成纤维细胞共培养。
| A)格局形成 | DEX 3.2% | DEX 6.4% | DEX 12.8% |
| PEG 2.5% | x | x | x |
| PEG 5.0% | X /✓ | ✓ | ✓ |
| PEG 10.0% | X /✓ | ✓ | ✓ |
| B)形态 | DEX 3.2% | DEX 6.4% | DEX 12.8% |
| PEG 2.5% | ✓ | ✓ | ✓ |
| PEG 5.0% | ✓ | ✓ | ✓ |
| PEG 10.0% | x | x | x |
| C)血清降水 | DEX 3.2% | DEX 6.4% | DEX 12.8% |
| PEG 2.5% | ✓ | ✓ | ✓ |
| PEG 5.0% | ✓ | ✓ | ✓ |
| PEG 10.0% | x | x | x |
表1中。)ATPS配方,可用于形成图案表示的复选标记,那些不能由x标记表示)表示保留细胞的正常形态和附件属性的配方by检查标记,那些不能由x标记表示。)配方在血清蛋白的沉淀,导致由x标记表示。
Subscription Required. Please recommend JoVE to your librarian.
Discussion
的ATPS细胞缩微方法只需要很少的细胞培养技术熟练的专业知识之外,可以很快掌握。这种方法的优点是,它是廉价的,快速的和具有多种类型的细胞和文化格式兼容。由于这些原因,我们的协议应该很容易通过生命科学家,特别是研究细胞的增殖,迁移和趋化性,近分泌和旁分泌的细胞群之间的相互作用的影响。这里介绍的分析,可以很容易地使用标准的图像分析程序,可用的软件,如ImageJ的细胞群体的量化。
为了产生一致的模式,我们建议以下注意事项。首先,应使用的移液管尖,以免除对DEX溶液后,每个的DEX液滴沉积到提供更一致的液滴体积改变。由于对DEX溶液是比较粘稠,这也是很重要的,以避免沉积过剩DEX,可能会对本的移液管尖端部的外表面上,以确保的整个体积为DEX退出的前端。二,液滴可以将,如果PEG加入太大力,如果菜倾斜。保持一个水平的表面上,并允许PEG解决方案,逐步未经允许从PEG半月板的大部队赶走的液滴覆盖的液滴从上面的菜,DEX可以尽量减少中断。大DEX液滴液滴更频繁地发生中断,所以如果可能的话,应使用滴的0.5μl以下。除了从配药的解决方案所涉及的这些技术问题,很少有与此技术相关联的缺陷,提供适当的聚合物的分子量和浓度使用。
虽然ATPS构图可以容易地进行使用微量吸移管(如这里介绍的),也有各种更多sophisticated,可用于更复杂的几何阵列( 例如,液体处理机器人和声学液滴喷射),以迅速产生图案的方法,如在我们以前的研究14,15,20。另外,也可以生成DEX的液滴,在体积小得多由气动喷射DEX通过毛细管孔,或通过致动微通道中的孔,以产生流动DEX液滴护套,用PEG 19。这些方法可能是为那些寻求产生高通量或复合作培养或迁移实验的兴趣。此外,使用微流体的方法,它能够与一个小数量的细胞进行实验,或与细胞中的微通道的流体流的影响,和纯粹可以检查。然而,这些先进的方法不需要用于大多数应用。
双水相的细胞构图是简单和容易地适用于一个典型的细胞文化背景。此方法允许的任何研究人员访问一个典型的细胞培养实验室(进入机罩,CO 2培养箱中,和微量)和上述聚合物的重复图案在单作和共培养细胞。我们的实验室已经证明了这一点印刷阵列功能的细胞在伤口愈合实验研究细胞迁移和分化的胚胎干细胞16,17,20在检查的影响,近分泌和旁分泌信号。的其它方法,包括细胞外基质28,喷墨印刷29,和图案化,通过在微流体装置25中的层流的图案化,26也被用于本地化细胞。这些其他的方法都是有效的方法来实现定义的模式细胞,往往能达到单细胞的精度。然而,这些方法也需要高度专业化的设备和/或进入洁净室设备制作的邮票公关诠释细胞外基质蛋白或产生微流体设备。它们连接到电源供应器,注射泵和其他外部元件也阻碍了其实现的成本与操作所需的设备和用户的技术。
在未来的应用中,我们希望,我们的方法将用于发展文化系统,使细胞运动和增殖的高通量分析,以及研究多个细胞群的细胞与细胞之间的相互作用。在这一点上,我们的报告把重点放在检查,只有极少数类型的图案的细胞在一次互动。然而,可以想象的是,可以一起成长在一个单一的细胞培养设置的许多类型的细胞进行调查的影响的旁分泌和近分泌信令与一个共同的饲养层培养许多细胞亚群的。最后,组织工程的应用经常需要的空间定位一种或多种类型的细胞。它可能会适应我们在图案形成细胞中使用的技术,以产生多种生理上有关的组织工程疾病模型或为临床应用的植入材料上的图案格。
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
作者没有竞争的金融利益。
Acknowledgments
这项工作是支持由库尔特基金会,Beyster基金会,ATA和美国国家科学基金会研究生研究奖学金(批准号DGE 0718128;编号:2010101926)JBW暑期班的本科生研究机会(UROP)。
Materials
| Name | Company | Catalog Number | Comments |
| Dextran 500,000 kDa | Pharmacosmos, Denmark | ||
| Polyethylene Glycol 35,000 kDa | Sigma-Aldrich, St. Louis, MO | ||
| Hela | ATCC, Manassas, VA | ||
| HepG2 C3A | ATCC, Manassas, VA | ||
| NIH 3T3 | ATCC, Manassas, VA | ||
| Cell Tracker | Invitrogen, Carlsbad, CA | ||
| DMEM | Gibco, Carlsbad, CA | ||
| RPMI | Gibco, Carlsbad, CA | ||
| F12 | Gibco, Carlsbad, CA | ||
| Fetal Bovine Serum | Gibco, Carlsbad, CA |
References
- Hatti-Kaul, R. Aqueous two-phase systems : methods and protocols. Methods in biotechnology. xiii, Humana Press. 440 (2000).
- Albertsson, P. A. k Partition of cell particles and macromolecules: separation and purification of biomolecules, cell organelles, membranes, and cells in aqueous polymer two-phase systems and their use in biochemical analysis and biotechnology. , 3rd ed, Wiley. 346 (1986).
- Yamada, M., et al. Continuous cell partitioning using an aqueous two-phase flow system in microfluidic devices. Biotechnol. Bioeng. 88 (4), 489-494 (2004).
- Soohoo, J. R., Walker, G. M. Microfluidic aqueous two phase system for leukocyte concentration from whole blood. Biomed. Microdevices. 11 (2), 323-329 (2009).
- Hahn, T., Hardt, S. Concentration and size separation of DNA samples at liquid-liquid interfaces. Anal. Chem. 83 (14), 5476-5479 (2011).
- Hatti-Kaul, R. Aqueous two-phase systems. A general overview. Mol. Biotechnol. 19 (3), 269-277 (2001).
- Hustedt, H., Kroner, K. H., Menge, U., Kula, M. -R. Protein recovery using two-phase systems. Trends in Biotechnology. 3 (6), 139-144 (1985).
- Keating, C. D. Aqueous Phase Separation as a Possible Route to Compartmentalization of Biological Molecules. Acc Chem. Res. 45 (12), 2114-2124 (2012).
- Helfrich, M. R., et al. Partitioning and assembly of metal particles and their bioconjugates in aqueous two-phase systems. Langmuir. 21 (18), 8478-8486 (2005).
- Diamond, A. D., Hsu, J. T. Prote. Partitioning in PEG/Dextran Aqueous Two-Phase Systems. AIChE Journal. 36 (7), 1017-1024 (1990).
- Y-T,, Zhu, Z. -Q. Modeling of interfacial tension of aqueous two-phase systems. Chemical Engineering Science. 54 (4), 433-440 (1999).
- Liu, Y., Lipowsky, R., Dimova, R. Concentration dependence of the interfacial tension for aqueous two-phase polymer solutions of dextran and polyethylene glycol. Langmuir. 28 (8), 3831-3839 (2012).
- Rha, C. Interfacial Tension of Polyethylene Glycol/Potassium Phosphate Aqueous Two-Phase Systems. Physics and Chemistry of Liquids: An International Journal. 38 (1), 25-34 (2000).
- Fang, Y., et al. Rapid Generation of Multiplexed Cell Cocultures Using Acoustic Droplet Ejection Followed by Aqueous Two-Phase Exclusion Patterning. Tissue Eng. Part C. Methods. 18 (9), 647-657 (2012).
- Tavana, H., et al. Nanolitre liquid patterning in aqueous environments for spatially defined reagent delivery to mammalian cells. Nat. Mater. 8 (9), 736-741 (2009).
- Tavana, H., Mosadegh, B., Takayama, S. Polymeric aqueous biphasic systems for non-contact cell printing on cells: engineering heterocellular embryonic stem cell niches. Adv. Mater. 22 (24), 2628-2631 (2010).
- Tavana, H., et al. Microprinted feeder cells guide embryonic stem cell fate. Biotechnol. Bioeng. , (2011).
- Tavana, H., Takayama, S. Aqueous biphasic microprinting approach to tissue engineering. Biomicrofluidics. 5 (1), 13404 (2011).
- Frampton, J. P., et al. Precisely targeted delivery of cells and biomolecules within microchannels using aqueous two-phase systems. Biomed. Microdevices. 13 (6), 1043-1051 (2011).
- Hossein Tavana, K. K., Bersano-Begey, T., Luker, K. E., Luker, G. D., Takayama, S. Rehydration of Polymeric, Aqueous, Biphasic System Facilitates High Throughput Cell Exclusion Patterning for Cell Migration Studies. Advanced Functional Materials. 21 (15), 2920-2926 (2011).
- Falconnet, D., et al. Surface engineering approaches to micropattern surfaces for cell-based assays. Biomaterials. 27 (16), 3044-3063 (2006).
- Lim, J. Y., Donahue, H. J. Cell sensing and response to micro- and nanostructured surfaces produced by chemical and topographic patterning. Tissue Eng. 13 (8), 1879-1891 (2007).
- Ringeisen, B. R., et al. Jet-based methods to print living cells. Biotechnol. J. 1 (9), 930-948 (2006).
- Wright, D., et al. Generation of static and dynamic patterned co-cultures using microfabricated parylene-C stencils. Lab Chip. 7 (10), 1272-1279 (2007).
- Takayama, S., et al. Patterning cells and their environments using multiple laminar fluid flows in capillary networks. Proc. Natl. Acad. Sci. U.S.A. 96 (10), 5545-5548 (1999).
- Berthier, E., et al. Pipette-friendly laminar flow patterning for cell-based assays. Lab Chip. 11 (12), 2060-2065 (2011).
- Davidson, R. L., O'Malley, K. A., Wheeler, T. B. Polyethylene glycol-induced mammalian cell hybridization: effect of polyethylene glycol molecular weight and concentration. Somatic Cell Genet. 2 (3), 271-280 (1976).
- Johnson, D. M., LaFranzo, N. A., Maurer, J. A. Creating Two-Dimensional Patterned Substrates for Protein and Cell Confinement. J. Vis. Exp. (55), e3164 (2011).
- Moon, S., Lin, P., Keles, H. O., Yoo, S., Demirci, U. Title Cell Encapsulation by Droplets. J. Vis. Exp. (8), e316 (2007).



