Overview
Fonte: Laboratório do Dr. Henrik Sundén – Universidade de Tecnologia Chalmers
A espectroscopia de ressonância magnética nuclear (NMR) é uma técnica de análise vital para químicos orgânicos. Com a ajuda da RMN, o trabalho no laboratório orgânico foi facilitado tremendamente. Não só pode fornecer informações sobre a estrutura de uma molécula, mas também determinar o conteúdo e a pureza de uma amostra. Em comparação com outras técnicas comumente encontradas para químicos orgânicos — como análise térmica e espectrometria de massa (MS) — a NMR é um método não destrutivo que é valioso quando a recuperação da amostra é importante.
Uma das técnicas de RMN mais utilizadas para um químico orgânico é o próton (1H) NMR. Os prótons presentes em uma molécula se comportarão de forma diferente dependendo de seu ambiente químico circundante, possibilitando elucidar sua estrutura. Além disso, é possível monitorar a conclusão de uma reação comparando os espectros de RMR do material inicial com o do produto final.
Este vídeo exemplifica como a espectroscopia de NMR pode ser usada no trabalho cotidiano de um químico orgânico. O seguinte será mostrado: i) preparação de uma amostra de RMN. ii) Utilização de 1H NMR para monitorar uma reação. iii) Identificação do produto obtido a partir de uma reação com 1H NMR. A reação que será mostrada é a síntese de um E-chalcone (3) de um aldeído (1) e uma cetona (2)(Esquema 1). 1
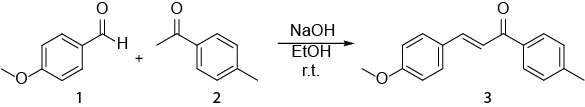
Esquema 1. Síntese de (2E)-3-(4-metoxifenil)-1-(4-metilfenil)-2-propen-1-one.
Principles
Núcleos com massa ímpar ou número atômico terão uma propriedade chamada spin, possibilitando o uso de RMN para detectar elementos como hidrogênio(1H), carbono(13C) e fósforo(31P). As voltas são aleatórias e giram em direções aleatórias; no entanto, aplicando um campo magnético externo, esses núcleos se alinharão com ou contra o campo magnético aplicado. Esses dois estados têm diferentes níveis de energia: um estado de baixa energia e um estado de alta energia. Irradiação com radiação eletromagnética fará com que o estado de baixa energia vire para o estado de alta energia. Quando a radiação é cessada, os núcleos sofrerão relaxamento e uma decadência indutiva livre (FID) é obtida. O FID é Fourier transformado para dar os picos do espectro NMR. Diferentes elementos terão frequências diferentes levando a diferentes mudanças químicas(Tabela 1). O espectro NMR pode fornecer diferentes tipos de informações sobre um composto; a integral de um pico fornece o número de prótons representados por ele, a constante de acoplamento (J-acoplamento) dá a correlação dos prótons, e o padrão de divisão de um pico diz quantos outros núcleos ativos de RN estão por perto (muitas vezes chamados de "vizinhos").
Uma vez que 1H NMR mede 1H núcleos é importante usar solventes deuterados; caso contrário, o sinal de interesse será perdido no ruído do sinal de solvente.
| Tipo de próton | Shift (δ, ppm) | Tipo de carbono | Shift (δ, ppm) |
| 1° Alkyl, RCH3 | 0.8–1.2 | 1° Alkyl, RCH3 | 0–40 |
| 2° Alkyl, R2CH2R | 1.2–1.5 | 2° Alkyl, R2CH2R | 10–50 |
| 3° Alkyl, RCHR2 | 1.4–1.8 | 3° Alkyl, RCHR2 | 15–50 |
| Aliado, R2C=CRCH3 | 1.6–1.9 | Alkene, C=C | 100–170 |
| Cetona, RC(=O)CH3 | 2.1–2.6 | Aryl, C em anel aromático | 100–170 |
| Éter, ROCH2R | 3.3–3.9 | Álcool ou éter, R3COR | 50–90 |
| Álcool, HOCH2R | 3.3–4.0 | Ácido carboxílico ou éster, RC(=O)OR |
160–185 |
| Vinilic, R2C=CH2 | 4.6–5.0 | Aldeído ou cetona, RC(=O)R |
182–215 |
| Vinilic, R2C=CRH | 5.2–5.7 | ||
| Aromático, ArH | 6.0–8.5 | ||
| Aldeído RC(=O)H | 9.5–10.5 | ||
| Hidroxílado alcoólica, ROH | 0.5–6.0 | ||
| Carboxílico, RC(=O)OH | 10–13 |
Mesa 1. Mudanças químicas comuns de prótons e NMR de carbono. 2
Subscription Required. Please recommend JoVE to your librarian.
Procedure
1. Preparação do material de partida nmr
- Adicione ~10 mg de material inicial a um tubo NMR limpo.
- Dissolva o material de partida em solvente deuterado de ~0,7 mL (exemplo dado CDCl3). Uma altura adequada do solvente para um bom espectro é de 4,5-5 cm.
- Cape o tubo NMR cuidadosamente e escreva o nome da amostra na tampa.
- Agite a amostra suavemente para garantir que todo o material tenha dissolvido. Tome cuidado para evitar o contato entre o solvente e a tampa, o que pode levar a uma possível contaminação da amostra.
- Insira o tubo NMR cuidadosamente em um spinner. O rotador irá girar uma vez inserido no ímã para garantir que toda a amostra experimente um campo magnético homogêneo. Limpe a parte externa do tubo NMR e o rotador com tecidos de 2 propanol e laboratório, a fim de remover impressões digitais e sujeira.
- Coloque o rotador em um medidor de profundidade de amostra para garantir que a parte inferior do tubo NMR não seja inserida muito longe na sonda NMR, pois isso poderia possivelmente danificar o espectrômetro. Diferentes sondas têm diferentes profundidades de amostra e o usuário deve estar ciente do medidor de profundidade específico.
- Coloque a amostra no espectrômetro NMR. Aqui foi utilizado um espectrômetro Varian de 400 MHz, equipado com um autosampler.
- Após a conclusão da medição do NMR, processe o espectro e atribua os picos no espectro.
2. Preparação de 3 M NaOH e Chalcone Synthesis
- Adicione 60 mg NaOH a um frasco volumoso de 50 mL.
- Dissolva o NaOH adicionando água deionizada à metade do frasco. Diluir ainda mais a solução adicionando mais água até que a marca seja atingida.
- Adicione 10 mL de etanol a um frasco de fundo redondo de 50 mL equipado com uma barra de agitação magnética.
- Depois disso, adicione 680,5 mg 4-metoxibenzaldeído e 5 mL naoh solução preparada na etapa 2.1 para o mesmo frasco.
- Adicione 671 mg 4-metilacetofenona posteriormente à solução agitada e tampa o frasco e mexa à temperatura ambiente.
- Monitore o progresso da reação por 1H NMR em intervalos de 30 minutos (ver passo 3) até o consumo total de materiais iniciais.
- Adicione 5 mL de água quando a reação chegar à conclusão (~3 h). Filtre o precipitado resultante e lave-o com 20 mL 1:2 etanol/água. Deixe o ar precipitado secar.
- Calcule o rendimento do produto obtido. Prepare uma amostra de RMN de acordo com a etapa 1.2.2.7. Verifique a pureza com 1H NMR. Se não for puro, purifique o produto via recrimistificação com etanol.
- Adicione aproximadamente 3 gotas de mistura de reação a um tubo NMR usando uma pipeta Pasteur e enxágue a pipeta com solvente deuterado.
- Repetir as etapas 1.2-1.8.
3. Breve Interpretação de um Espectro NMR
- Processe o espectro com um programa adequado (exemplo dado MestReNova).
- Correlacionar os diferentes picos aos turnos da RMN na Tabela 1. As mudanças químicas dão uma dica de que tipo de ambiente os prótons existem.
- Integre os picos para dar o número de hidrogênios correspondentes a cada pico. A integração de todos os picos dá um número relativo de prótons totais.
- Avalie a divisão dos picos de prótons, que indicam o número de vizinhos.
- Meça o acoplamento J para ver como os prótons estão conectados entre si.
Ressonância magnética nuclear, ou NMR, espectroscopia é um método importante para determinar a estrutura molecular e a pureza das amostras em química orgânica.
Na espectroscopia NMR, as amostras são expostas a um forte campo magnético. Após a exposição, certos núcleos transitam, ou ressoam, entre níveis discretos de energia. A lacuna de energia entre esses níveis pode ser medida e visualizada como espectro. Esses dados podem ser usados para elucidar a estrutura química da amostra.
Nem todos os núcleos têm as propriedades necessárias para serem ativos em RMN. Os isótopos comuns estudados são 1H, 2H, 13C, 19F e 31P.
Este vídeo introduzirá os princípios por trás da NMR, passará por preparações de exemplo de amostras de NMR de diferentes estágios de uma reação química e discutirá várias aplicações.
No instrumento NMR, nitrogênio líquido e hélio são usados para resfriar um ímã super condutor. O ímã aplica um campo magnético constante a uma amostra. Dentro da amostra, núcleos atômicos com um número ímpar de prótons e/ou nêutrons se alinharão tanto com o campo, adotando um estado de baixa energia, ou contra ele, adotando um estado de alta energia.
A diferença de energia entre os dois níveis é a frequência ressonante, que depende da força do campo aplicado e do tipo de núcleo. Para os ímãs usados em NMR, o valor está na frequência de rádio, ou RF, alcance.
Uma bobina RF excita a amostra com um pulso de radiofrequência, movendo os núcleos de baixa energia para o estado mais alto, antes de reverter. A bobina detecta essas mudanças na magnetização, que são exibidas como picos.
A força da RMN está em sua capacidade de distinguir núcleos, neste caso hidrogênio, por seu ambiente químico. Elétrons em átomos vizinhos bloquearão, ou "escudo", os núcleos de alguns dos campos magnéticos. Este campo eficaz altera a frequência ressonante para os núcleos particulares, chamado de mudança química. No etanol, o metileno, hidroxil e prótons de metila têm frequências de ressonância únicas. Determinar a área sob cada pico elucida o número de cada tipo de próton.
Uma vez que instrumentos com diferentes forças magnéticas mudarão as frequências ressonantes, eles são referenciados a uma molécula padrão adicionada à amostra, muitas vezes tetrametilosiltano, ou TMS. A mudança química das frequências é muito pequena, frequentemente relatada em partes por milhão, ou ppm.
Ao usar um ímã forte com alta resolução, picos às vezes se dividem em subpeaks. Isso é causado pelos núcleos vizinhos, alguns dos quais estão alinhados com o campo magnético, alguns contra; mudando ainda mais o campo efetivo aplicado aos núcleos. No etanol, os 2 prótons de metileno dividem o pico de metila duas vezes em um trigêmeo, e os 3 prótons de metila dividiram o pico de metileno três vezes em um quarteto. A distância da divisão, ou Acoplamento J, está relacionada à distância dos núcleos, auxiliando na descoberta qualitativa.
Agora que você entende os princípios básicos por trás da RMN, vamos rever um procedimento de exemplo que usa nMR de prótons para monitorar a síntese de chalcone a partir de um aldeído e cetona.
Comece usando uma pipeta Pasteur para adicionar uma pequena quantidade do material inicial a um béquer. Mova-se para o capô da fumaça e dilua o material inicial com 0,7 mL de solvente deuterado. Solventes deuterados são usados, pois a frequência ressonante do deutério está fora do alcance para prótons.
Use uma pipeta Pasteur para adicionar 0,7 mL do material de partida diluído em um tubo NMR limpo de 5 mm, preenchendo o fundo de 4,5 a 5 cm. Tampe o tubo NMR e rotule-o. Agite suavemente o tubo, tomando cuidado para evitar o contato entre a amostra e a tampa. Em seguida, insira o tubo no rotador.
Limpe o lado de fora do tubo e do rotador usando tecidos de 2 propanol e laboratório. Em seguida, coloque o conjunto da amostra no medidor de profundidade e calibrar a profundidade de inserção.
Após a calibração, carregue o conjunto da amostra no espectrômetro NMR manualmente ou usando um amostrador automático. Finalmente, use uma estação de trabalho de computador para adquirir o espectro NMR.
Gerar espectros de RMN usando este procedimento para cada um dos materiais de partida da reação. Para a síntese de chalcone, espectros devem ser gerados tanto para metoxibenzaldeído quanto para metilacetofenona.
Em seguida, realize a síntese da amostra combinando os materiais de partida e os reagentes em um frasco para começar a reação.
Em intervalos de 30 minutos, remova uma pequena alíquota da mistura de reação usando uma pipeta Pasteur e adicione 3 gotas a um tubo NMR limpo.
Diluir este produto de reação bruta com solvente deuterado e preparar-se para A RMN usando o procedimento descrito anteriormente.
À medida que a reação progride, um precipitado amarelo se formará. Quando a reação estiver completa, lave e filtre o precipitado e gere espectros de RMR para o produto de reação purificado.
Agora que geramos espectros de NMR em cada fase da reação química, vamos analisá-los.
Os picos do espectro NMR para cada um dos materiais iniciais são atribuídos a diferentes grupos de prótons dentro da molécula de acordo com suas mudanças químicas e o número de prótons contribuindo para cada pico. Aqui, atribuímos os 4 principais grupos de prótons para metilacetofenona e metoxibenzaldeído, observando o pico de aldeído entre 9,5 e 10,5 ppm. Comparando o espectro de RMR dos produtos de reação bruta em diferentes pontos de tempo, a evolução da reação química que sintetiza o chalcone é elucidada. Por exemplo, o pico de aldeído do material inicial metoxibenzaldeído ainda está presente após 30 minutos de reação, mas está completamente desaparecido após 3h, significando a conclusão da reação.
Examinando o espectro do produto purificado podemos atribuir cada pico a um grupo de prótons na estrutura do Chalcone. Por exemplo, examinando os picos 3 e 4 vemos que suas integrais são ambas uma, correspondendo a grupos que contêm apenas um próton.
Os picos 3 e 4 são os chamados doublets indicando um próton vizinho. Ambos têm constantes de acoplamento J de 16 Hz, sugerindo que os prótons estão situados em um vínculo E-duplo. Ao atribuir todos os picos de RMN do produto de reação purificada, confirmamos a síntese de um chalcone puro.
A espectroscopia NMR tem uma ampla gama de aplicações e é usada em muitas áreas científicas e médicas.
Nesta aplicação, o Próton NMR é usado para verificar a síntese e estrutura tanto da diamidocarbene quanto da mononoamidocarbina, cujos espectros NMR têm padrões diferentes de divisão de picos. Essas carbenas também geraram produtos de reação aparentemente diferentes quando combinados com fósforo branco; O DAC1 gerou um produto de reação vermelha brilhante, enquanto o MAAC2 produziu um produto laranja brilhante. Essas diferenças nos produtos de reação foram confirmadas utilizando-se uma segunda aplicação de NMR, 31P NMR, que gera espectros baseados em diferenças na frequência ressonante dos núcleos de fósforo.
Aqui, a ressonância magnética nuclear, ou ressonância magnética, foi usada para gerar um mapa anatômico do cérebro e selecionar as regiões de interesse do cérebro. Em seguida, a espectroscopia NMR foi usada para gerar espectros de metabólitos-chave. Finalmente, foram avaliadas alterações de ressonância magnética no metabolismo cerebral em diferentes condições experimentais.
Nesta aplicação, a RMR foi utilizada para analisar as propriedades de ligação e propor uma estrutura 3D de um peptídeo de ligação de cobre. Primeiro, os espectros de NMR foram comparados para os estados desvinculados do peptídeo e do cobre. Em seguida, utilizando técnicas de RMN bidimensionais mais avançadas, foram avaliadas diferentes conformações potenciais da estrutura do peptídeo. Finalmente, essas restrições estruturais derivadas da RMM foram utilizadas para desenvolver uma estrutura 3-Dimensional proposta para o peptídeo não vinculado.
Você acabou de assistir a introdução de JoVE à Análise NMR. Agora você deve entender os princípios subjacentes por trás da geração e análise de espectros NMR, bem como um procedimento para a preparação da amostra de RMN.
Obrigado por assistir!
Subscription Required. Please recommend JoVE to your librarian.
Results
Comparando-se os espectros dos materiais iniciais (Figuras 1 e 2) com o do produto final (Figura 5) pode-se observar uma clara diferença entre os espectros, indicando a formação do chalcone. O ponto final da reação pode ser determinado mediante a coleta de amostras de RMM em diferentes intervalos de tempo; por exemplo, o pico de próton de aldeído (C(=O)H) (1) pode ser visto na Figura 3, mas não na Figura 4, significando a conclusão da reação após 3h. Olhando para as integrais, padrões de divisão e acoplamentos J dos picos, é possível validar a estrutura do chalcone. As integrais dos picos (números abaixo do pico, Figura 5) mostram a quantidade relativa de hidrogênios presentes que devem se correlacionar com a quantidade de hidrogênios encontrada no produto. Além disso, o padrão de divisão dá uma indicação do número de vizinhos; por exemplo, o pico (5) e (1) — ambos singlets — não indicam vizinhos próximos com integrais de 3 correlações com o MeO e o grupo Me, respectivamente. Comparando as mudanças químicas no espectro com a Tabela 1 é possível elucidar que o grupo MeO corresponde ao singlet a 3,80 ppm e ao grupo Me a 2,45 ppm. Além disso, a formação do vínculo duplo pode ser vista como dois doublets(Figura 5),7,80 e 7,44 ppm. Olhar para o acoplamento J de 16 Hz indica a formação de um E-alkene; o Z-alkene normalmente tem um valor menor de 10-12 Hz.3 Atribuindo os picos aromáticos verifica a estrutura (Figura 5). 4

Figura 1. Especificação NMR atribuída 1H de 4-metilacetofenona Clique aqui para ver uma versão maior desta figura.

Figura 2. Especificação NMR atribuída 1H de 4-metoxibenzaldeído. Clique aqui para ver uma versão maior desta figura.

Figura 3. Espectros brutos de 1HNMR após 30 min mostrando o pico de aldeído residual. Por favor, clique aqui para ver uma versão maior desta figura.

Figura 4. Espectro de NMR bruto de 1H após 3h não mostrando nenhum pico residual de aldeído. Por favor, clique aqui para ver uma versão maior desta figura.

Figura 5. 1H NMR espectros do produto obtido após o trabalho. A imagem inserida mostra os acoplamentos J do alkene. Clique aqui para ver uma versão maior desta figura.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
A RN pode, por exemplo, ser usada para detectar intermediários de reação, facilitando o trabalho de elucidação de um mecanismo de reação. Com a ajuda da RMN também é possível observar movimentos moleculares e interações importantes para o desenvolvimento de medicamentos. Além disso, a RMN pode dar informações estruturais sobre materiais sólidos; por exemplo, para fornecer uma lógica para propriedades materiais observadas. Outras aplicações de RMN podem ser encontradas no campo da medicina, onde a ressonância magnética (RM) é frequentemente utilizada para diagnóstico médico. A RN também tem sido usada em metabolômica para detectar diferentes metabólitos excretados por um organismo, fornecendo assim uma impressão digital metabólica. Os usos de RMN são amplos; desde determinar a estrutura de uma única molécula até a imagem do cérebro humano.
Subscription Required. Please recommend JoVE to your librarian.
References
- Ta, L., Axelsson, A., Bijl, J., Haukka, M., Sundén, H., Ionic Liquids as Precatalysts in the Highly Stereoselective Conjugate Addition of α,β-Unsaturated Aldehydes to Chalcones. Chem. Eur. J. 20 (43), 13889-13893 (2014).
- Table adapted from Graham Solomons, T. W. Fryhle, C. B., Organic Chemistry, 10th edition, Wiley, p. 387, 418 (2011).
- Clayden, J., Greeves, N., Warren, S., Wothers, P. Proton nuclear magnetic resonance. Organic Chemistry, Chapter 11, Oxford University Press, 269 (2001).
- Wu, X.-F., Neumann, H., Spannenberg, A., Schulz, T., Jiao, H., Beller, M.,Development of a General Palladium-Catalyzed Carbonylative Heck Reaction of Aryl Halides. J. Am. Chem. Soc. 132 (41), 14596-14602 (2010).




