10.1:
价层电子对互斥理论(VSEPR) 和基本形状
A subscription to JoVE is required to view this content. Sign in or start your free trial.
JoVE Core
Chemistry
VSEPR Theory and the Basic Shapes
价层电子对互斥理论或 VSEPR 理论 用作预测分子结构的工具。它假定带负电的电子基团相互排斥,并尽力保持彼此之间有最大可能的距离,从而使排斥达到最小,这些电子基团可能涉及 单键、多重键或孤对电子。想象一下一组绑在一起的气球。每个气球都尽可能地使自己远离 另一个。分子的几何形状由中心原子周围 各种电子基团的排列决定。氟化铍在中心原子周围 有两个电子基团。根据 VSEPR 理论,这些电子 基团之间的最小斥力 是通过最大分离实现的。因此,键角为 180 度,并且分子形状为线性。三氟化硼在中心硼原子周围 具有三个电子基团。通过假定 120 度的键角,可以使这些基团之间的排斥 达到最小。VSEPR 理论预测该分子表现出 平面三角几何形状。就甲烷而言,中心碳原子周围 有四个电子基团。当键角为 109.5 度 且分子呈三维正四面体几何形状时,电子基团距离最远。如果将五个气球绑在一起,则当三个气球在一个平面上 并且其余两个放在该平面的两侧时,可以实现最大的分隔。五氯化磷在中心原子周围 有五个电子基团。三个赤道氯原子彼此分离,之间的键角为 120 度,并且呈平面三角形排列。平面上下各有一个氯原子。赤道氯和轴向氯之间的夹角 为 90 度。该分子的几何形状是三角双锥。在六氟化硫中,硫原子周围 有六个电子基团。四个基团占据一个平面。另外两个基团位于该平面的两侧。分子的几何形状为正八面体。所有的键都是等价的,键角是 90 度。这些例子表明,中心原子周围有 2 到 6 个键合的电子基团,形成了线性、平面三角形、正四面体、三角双锥和正八面体 五种基本的分子形状。
10.1:
价层电子对互斥理论(VSEPR) 和基本形状
价层电子对互斥理论(VSEPR) 概述
价壳层电子对互斥理论 (价层电子对互斥理论(VSEPR)) 使我们能够通过检查路易斯结构中的键和单电子对数来预测分子的分子结构,包括围绕中心原子的近似键角度。 价层电子对互斥理论(VSEPR) 模型假设中央原子的价壳层中的电子对将采用一种排列方式,通过最大化电子对之间的距离来最大程度地减少电子对之间的脉冲。 中央原子的价壳层中的电子形成主要位于键合原子或孤对之间的键对电子。 当高电子密度的不同区域假设位置尽可能彼此间距离时,这些电子的静电互斥会降低。
价层电子对互斥理论(VSEPR) 预测每个中心原子周围的电子对排列,通常是分子中原子的正确排列。 但是,我们应该理解,理论只考虑电子对脉冲。 其他相互作用,如核核粉碎和核电子景点,也涉及原子在特定分子结构中采用的最终安排。
价层电子对互斥理论(VSEPR) 的应用
价层电子对互斥理论(VSEPR) 可用于预测分子的结构。 例如,让我们预测气态二氧化碳分子的结构。 二氧化碳的路易斯结构 (图 1) 仅显示围绕中央碳原子的两个电子组。 由于中央原子上有两个键组且没有孤对电子,键尽可能地分离,当这些高电子密度区域位于中央原子的另一侧时,它们之间的静电互斥将降至最低。 键角度为 180°。
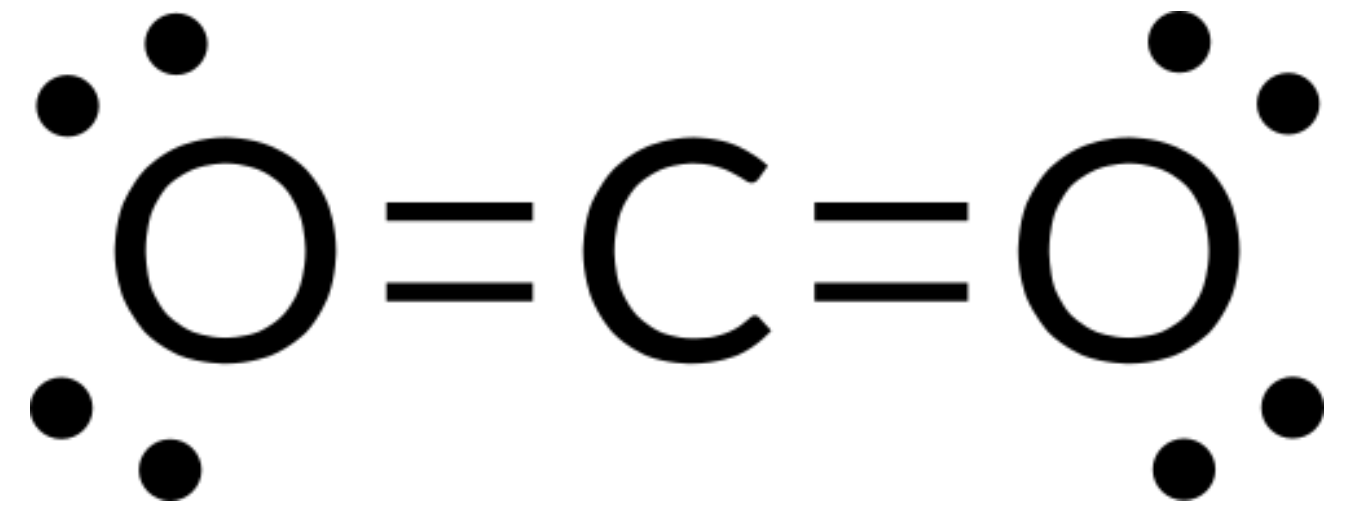
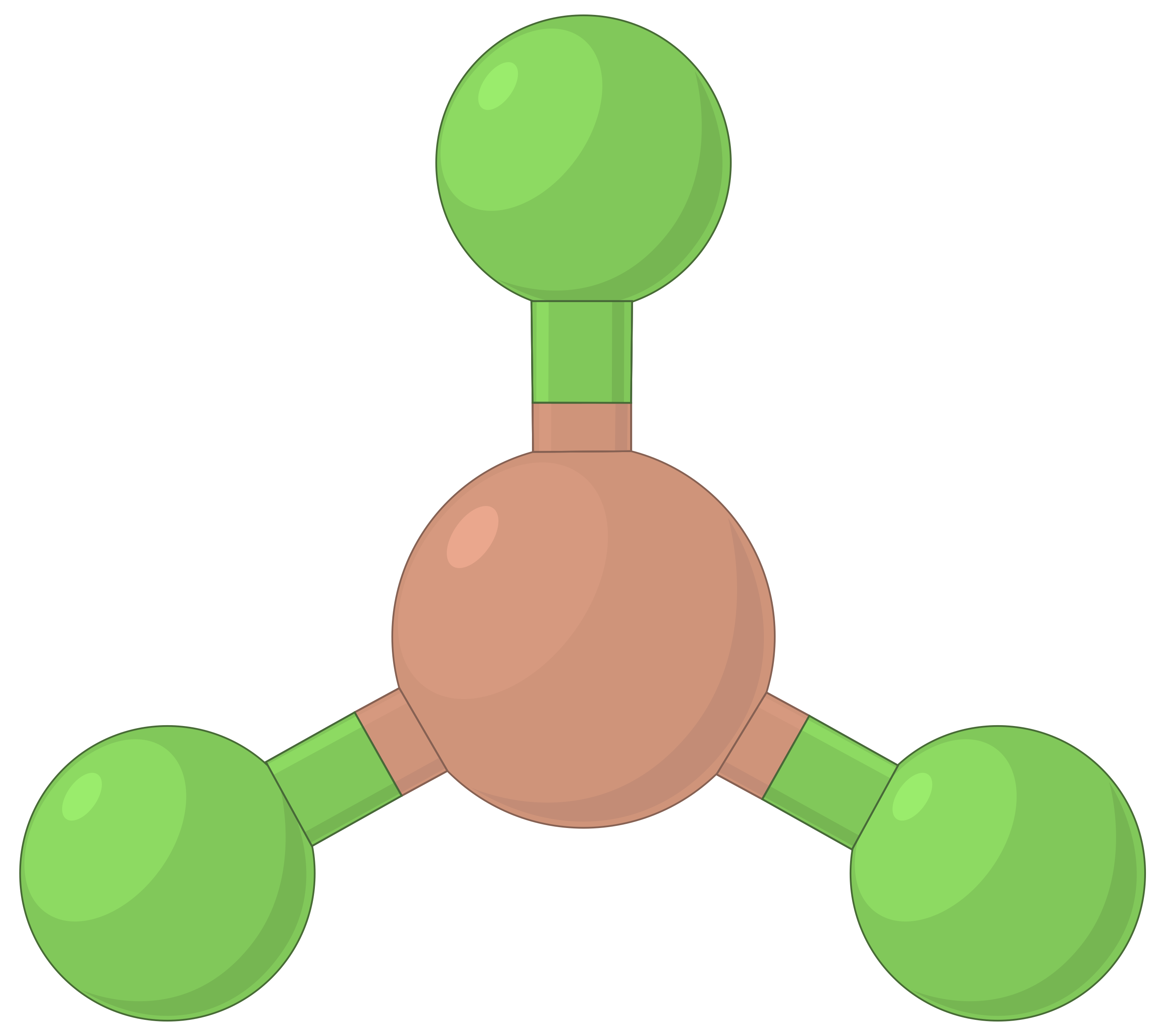
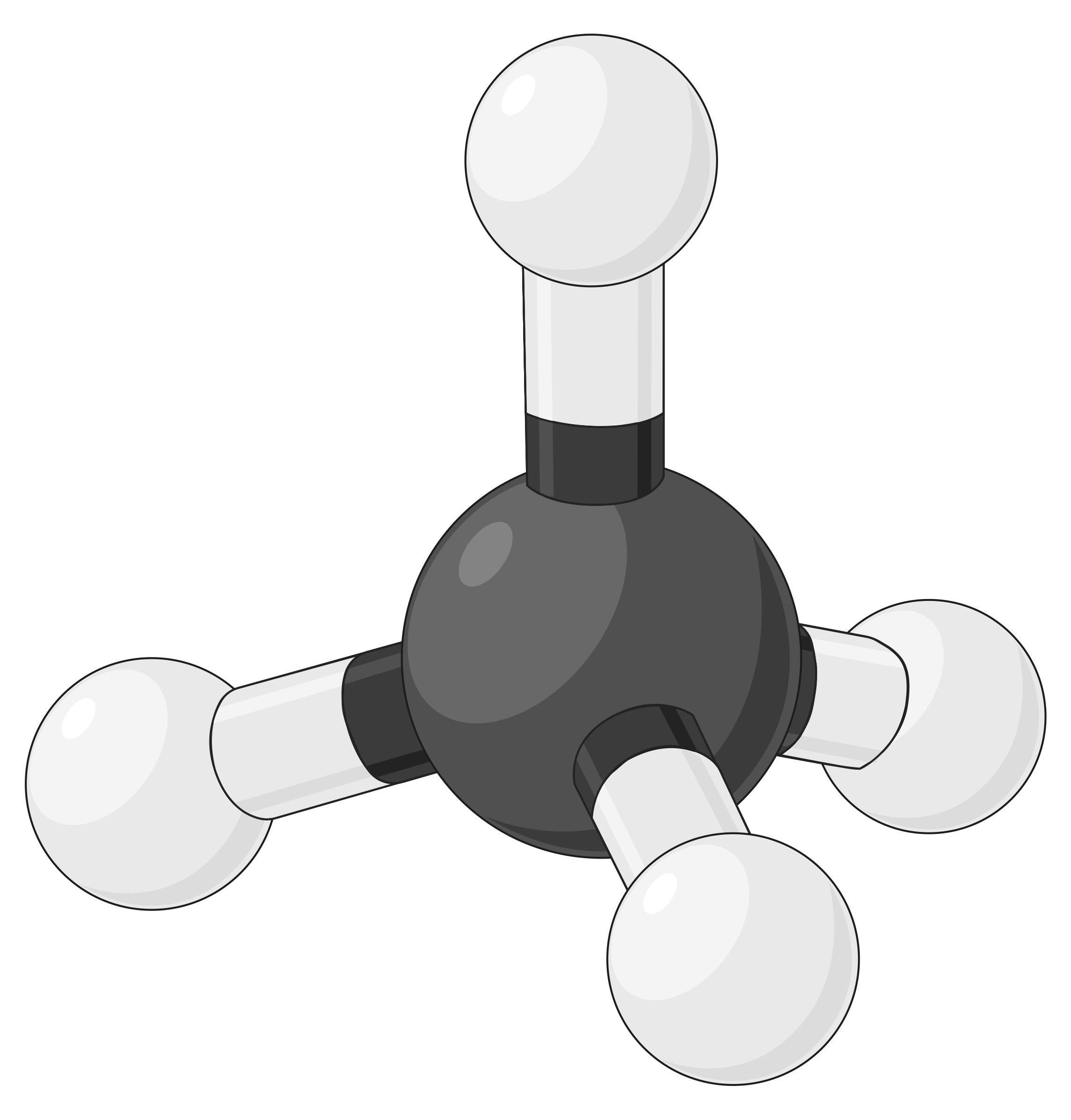
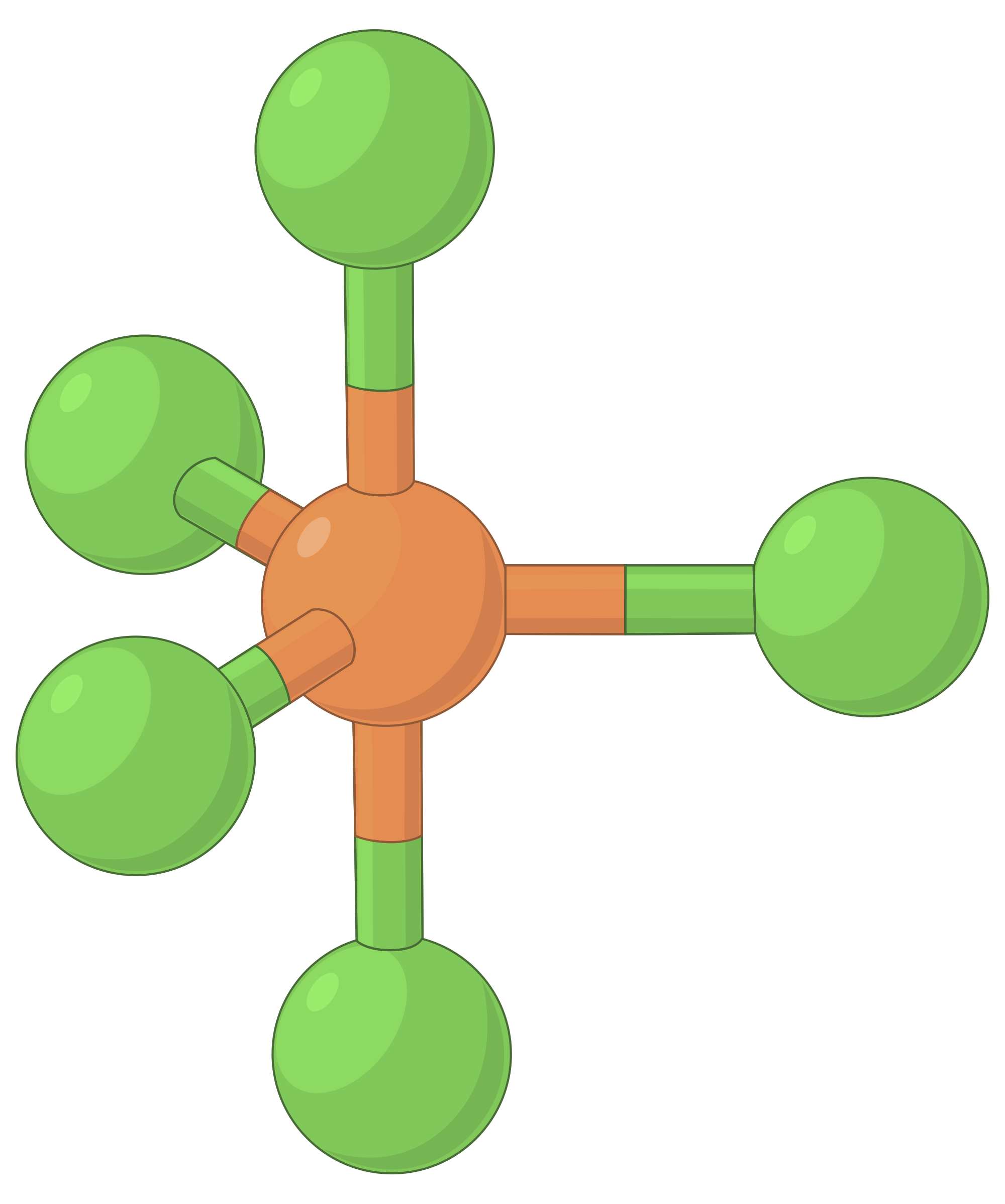
下表说明了电子对几何形状,这些几何形状可以最大程度地减少高电子密度区域 (键和 / 或孤对) 之间的脉冲。 分子中一个中心原子周围的两个电子密度区域形成线性几何体;三个区域形成三角平面几何体;四个区域形成四面几何体;五个区域形成三角斜向几何体,六个区域形成八面体几何体。
| 错误 2 | BF3 | 甲烷 | PCL5 | SF6 | |
| 电子区域数 | 2.3. | 4. | 5. | 6. | |
| 电子区域几何体 | 线性; 180° 角 | 三角平面;所有角度为 120° | 四面;所有角度 109.5° | 三角双相,角度为 90° 或 120°。 | 八面体;所有角度 90° 或 180°。 |
| 空间安排 | 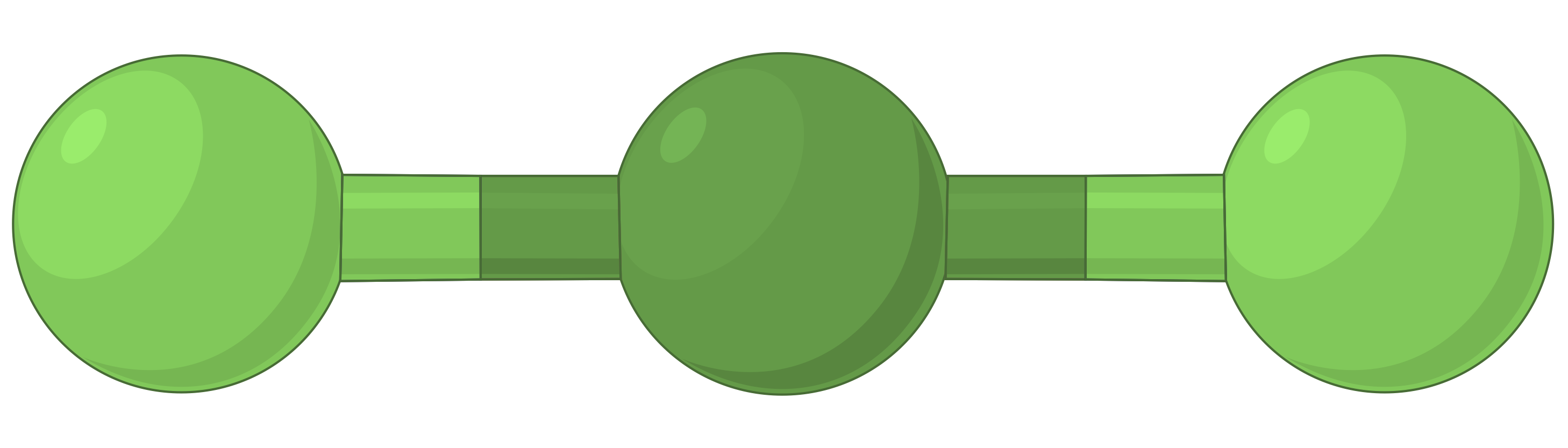 |
 |
 |
 |
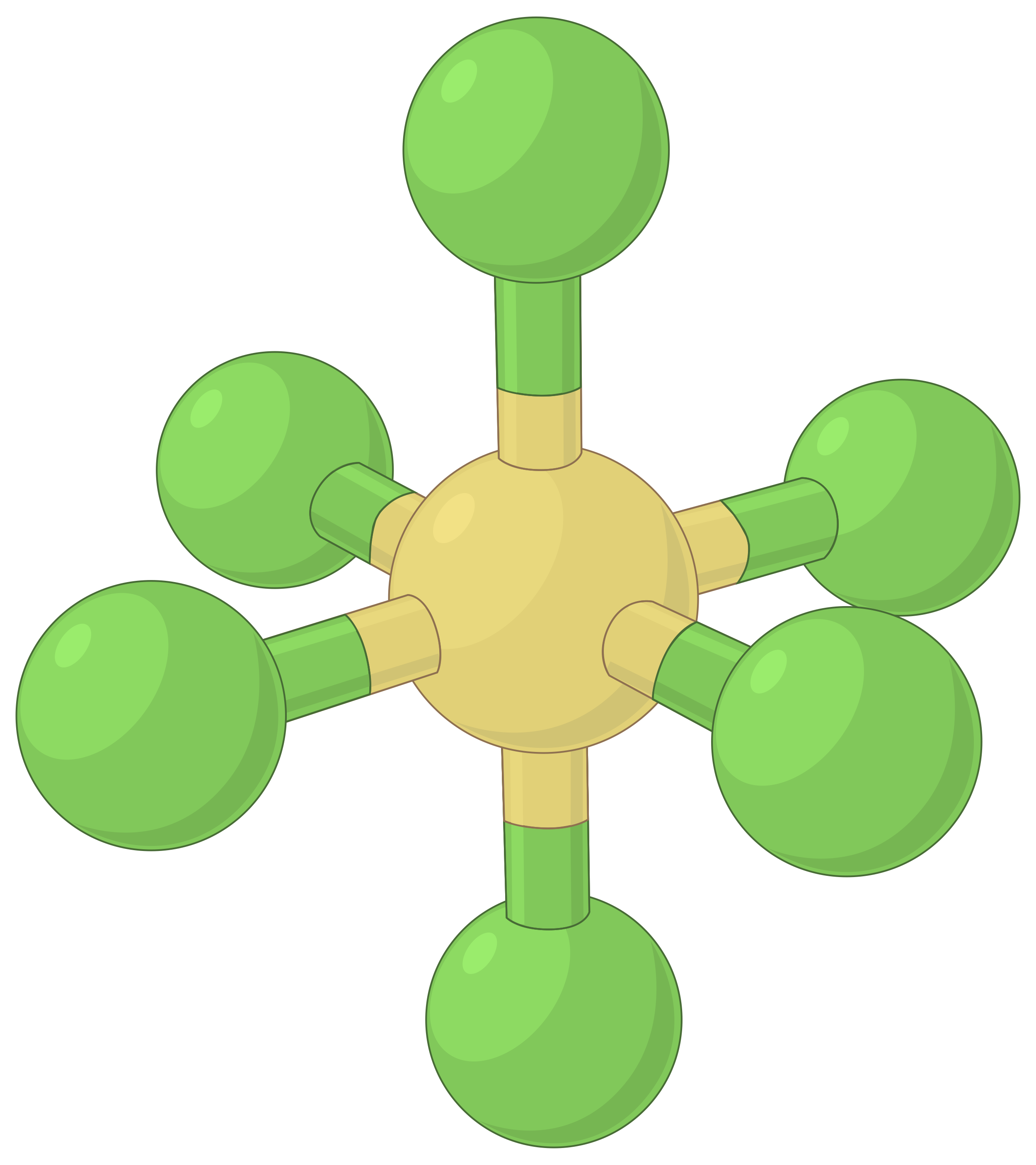 |
表 1. 价层电子对互斥理论(VSEPR) 预测的基本电子对几何形状可最大化电子密度任何区域 (键或孤对) 周围的空间。
