11.11:
相变:升华和气相沉积
A subscription to JoVE is required to view this content. Sign in or start your free trial.
JoVE Core
Chemistry
Phase Transitions: Sublimation and Deposition
人们经常观察到,在环境条件下,常规冰会融化,但干冰则不会融化;相反,干冰会直接转化为气相。从固体到气体的转变,没有经过液相,被称为升华。一般来说,升华的化合物 在固态时表现出微弱的分子间作用力。在干冰或固体二氧化碳中,二氧化碳分子之间存在微弱的色散力。在大气压力下,干冰 在 78.5°C 以下仍为固体。然而,在 78.5°C 时,表面分子 获得足够的热能可完全克服 吸引力,并直接转化为 蒸气相。这就是干冰的升华点。升华一摩尔固体所需的能量 称为摩尔升华热 或摩尔升华焓。由于升华是一个吸热过程,因此其焓值始终为正。升华的逆过程,也就是 从蒸气到固体的直接转变,被称为凝华。当气体分子与较冷的固体表面碰撞时,它们会失去热量。多次碰撞导致大量的热量流失,分子最终凝华。由于凝华涉及能量损失,它是一种放热相变,焓值为负。尽管凝华焓为负,但其大小与升华焓相同。当在开放系统中发生升华时,大多数升华的分子会分散在空气中,再也不会回来。因此,升华速率 大于凝华速率。然而,在封闭系统中,在固体的升华点处 建立了固体-蒸气平衡。气体与其固体动态平衡时所施加的分压 称为蒸气压。升华的固体具有较高的蒸气压。例如,干冰在 20°C 时的 蒸气压高达 56.5 atm。但是,由于大多数固体在容易接近的温度下 具有较低的蒸气压,因此升华并不常见。
11.11:
相变:升华和气相沉积
某些固体可以通过称为升华的过程绕过液体状态直接过渡到气体状态。 在室温和标准压力下,一块干冰 (固体二氧化碳) 会升华,似乎逐渐消失,而不会形成任何液体。 雪和冰在低于水熔点的温度下升华,这是一个缓慢的过程,风速可能会加速,在高海拔地区,大气压力会降低。 固体碘加热后,固体会变子并形成鲜艳的紫色蒸汽。 升华的反向称为气相沉积,在该过程中,气体物质直接凝结为固态,绕过液体状态。 结霜是气相沉积的一个例子。
与汽化一样,升华的过程需要输入能量以克服分子间吸引力。 因此,升华是一个内置式相变。 升华焓, ΔHsub ,是将一摩尔物质从固体状态转换为气体状态所需的能量。 例如,二氧化碳的升华表示为:

同样,气相沉积反向过程的焓变化幅度相等,但与升华相反。 由于气相沉积涉及到分子间作用力的形成,因此它是一种外发性相变。

考虑实现给定相变必须克服分子间吸引力的程度。 将固体转化为液体需要只能部分克服这些吸引力;向气体状态过渡需要完全克服它们。 因此,物质的熔化焓小于其汽化焓。 同一逻辑可用于在给定物质的所有相变的焓之间得出近似关系。 尽管描述不完全准确,但为了应用赫斯定律,可以方便地将升华建模为熔化的连续两步流程,然后是汽化。 从这种角度看,一种物质的升华焓可能被估计为其熔化与汽化焓的总和。
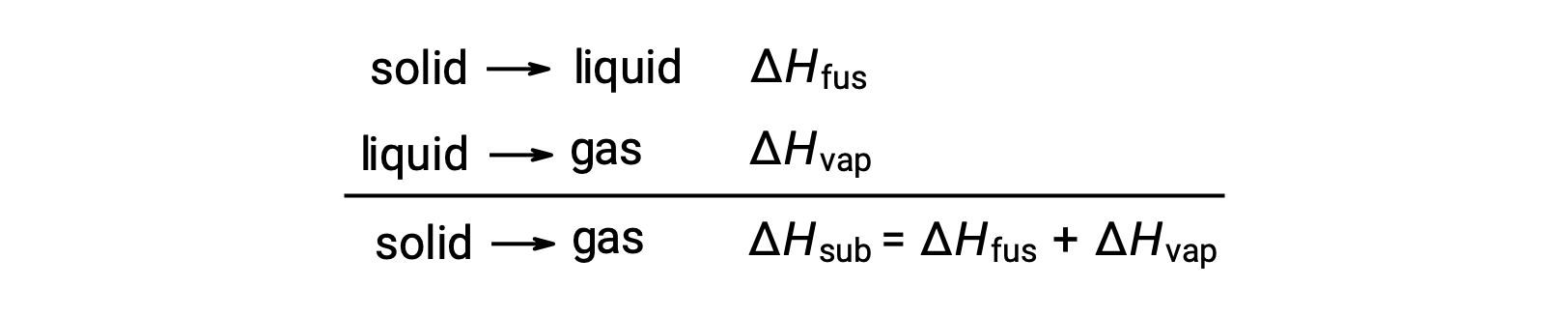
本文改编自 Openstax, 化学 2e, 第10.3节:相变。
