14.6:
Расчет равновесных концентраций
14.6:
Расчет равновесных концентраций
Способность рассчитать равновесные концентрации имеет важное значение для многих областей науки и техники, например, при разработке и дозировании фармацевтических продуктов. После проглатывания или введения препарата он обычно участвует в нескольких химических равновесии, которые влияют на его конечную концентрацию в системе интереса. Знание количественных аспектов этих равновесий необходимо для расчета дозы, которая будет добиваться желаемого терапевтического эффекта.
Более сложным типом расчета равновесия может быть расчет равновесных концентраций, производных от начальных концентраций и константы равновесия. Для этих расчетов обычно используется четырехэтапный подход:
- Определите направление, в котором реакция будет двигаться к равновесию.
- Разработайте ледяной стол.
- Рассчитайте изменения концентрации и затем равновесные концентрации.
- Подтвердите расчетные концентрации равновесия.
Расчет равновесных концентраций
При определенных условиях равновесная константа Kc разложения PCL5(g) на PCl3(g) и Cl2(g) составляет 0.0211. Описанная выше процедура может использоваться для определения равновесных концентраций PCL5, PCl3 и Cl2 в смеси, которая изначально содержала только PCL5 в концентрации 1.00 M.
Шаг 1. Определите направление, в котором идет реакция.
Сбалансированное уравнение разложения PCL5 составляет
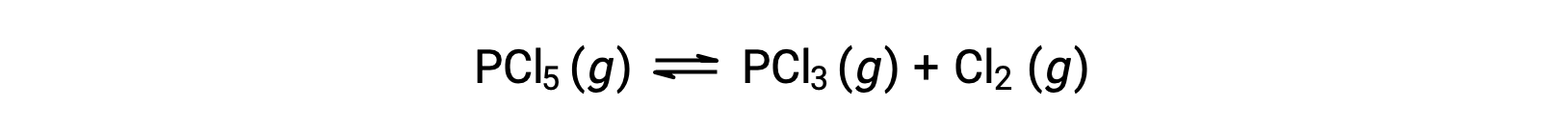
Поскольку изначально присутствует только реагент, QC = 0, и реакция будет идти вправо.
Шаг 2. Разработайте ледяной стол.
| PCl5 (g) | PCl3 (g) | Cl2 (g) | |
| Начальная концентрация (M) | 1.00 | 0 | 0 |
| Изменение (M) | x | +x. | +x. |
| Равновесная концентрация (M) | 1.00 – x. | x | x |
Шаг 3. Решите для изменения и равновесных концентраций.
Подстановка равновесных концентраций в уравнение равновесной константы дает
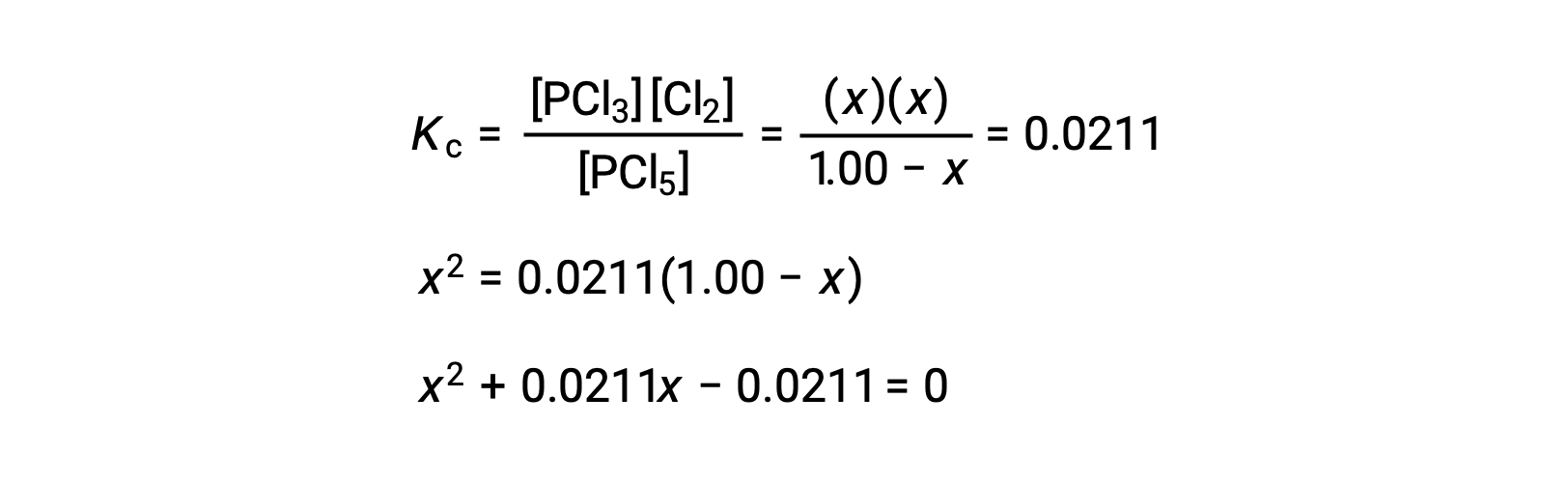
Уравнение формы ax2 + bx + c = 0 можно изменить для решения для x:
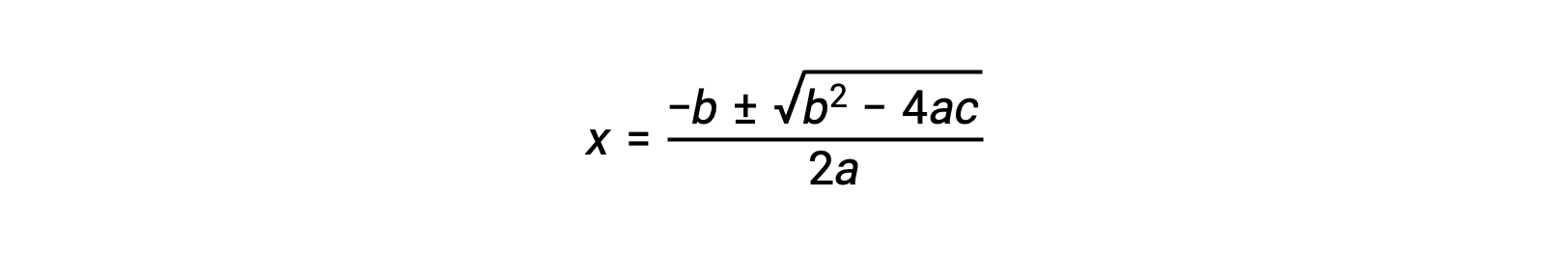
В этом случае a = 1, b = 0.0211 и c = -0.0211. Подстановка соответствующих значений для a, b и c дает:
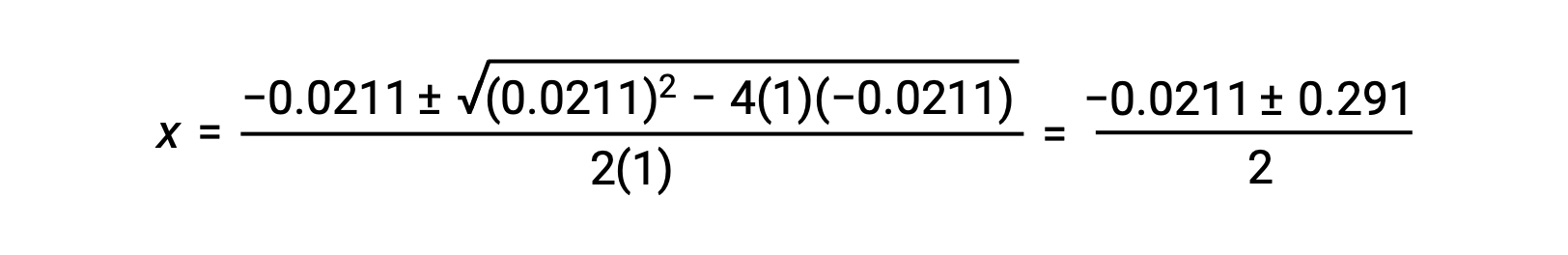
Таким образом, два корня квадрата являются
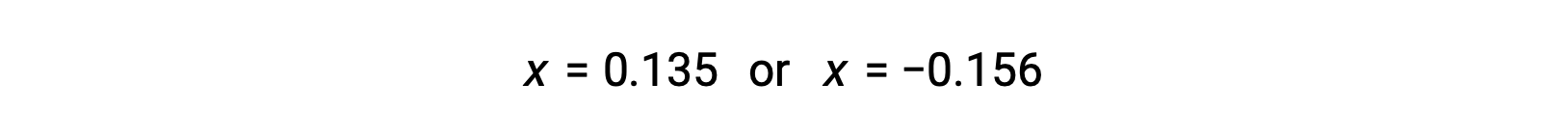
Для этого сценария физически значимым является только положительный корень (концентрации равны нулю или положительны), и поэтому x = 0.135 M. равновесные концентрации являются
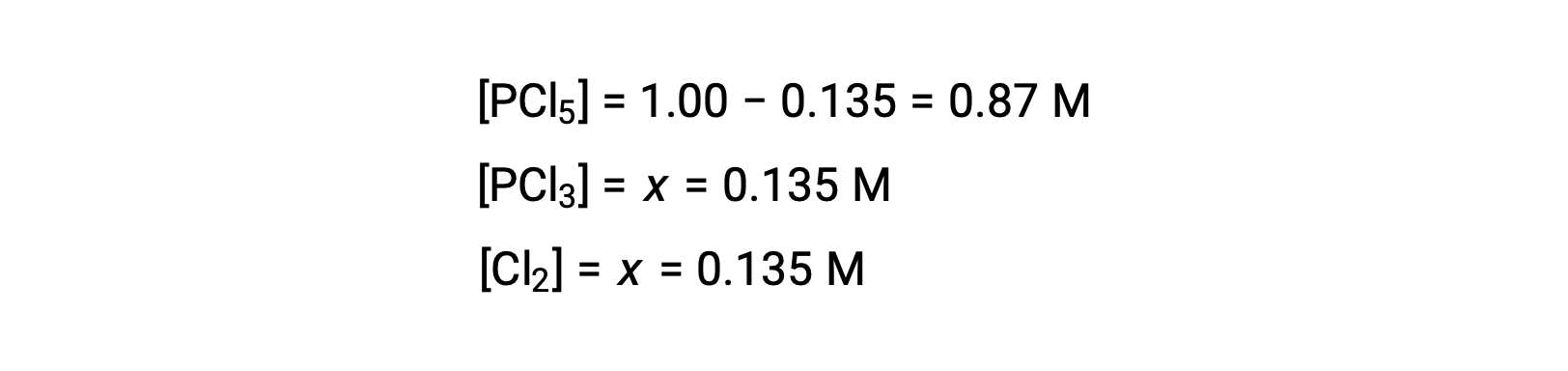
Шаг 4. Подтвердите расчетные концентрации равновесия.
Подстановка в выражение для Kc (для проверки вычисления) дает
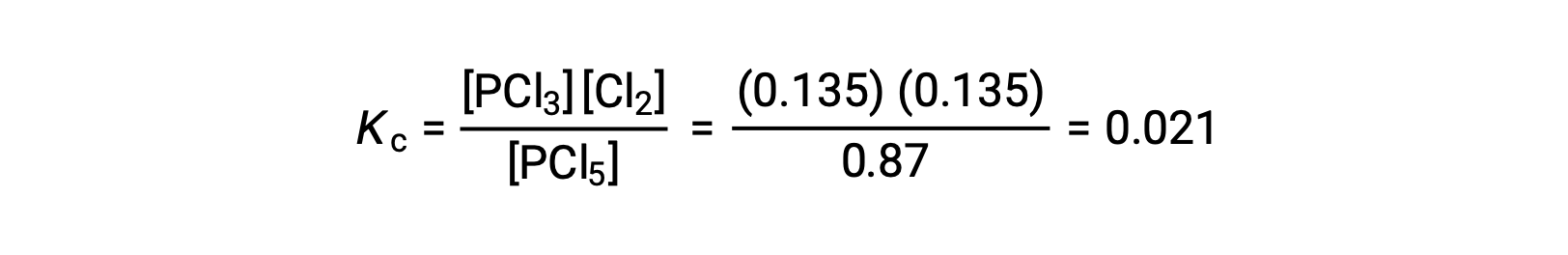
Константа равновесия, рассчитанная на основе равновесных концентраций, равна значению Kc, данному в задаче (округляется до правильного количества значительных цифр).
Этот текст был адаптирован к расчетам равновесия Openstax, Химия 2е изд., раздел 13.4.
Suggested Reading
- Lim, Kieran F. "Using graphics calculators and spreadsheets in chemistry: Solving equilibrium problems." Journal of Chemical Education 85, no. 10 (2008): 1347. https://pubs.acs.org/doi/pdf/10.1021/ed085p1347
