Summary
Se describe una técnica para la preparación de aclarar homogeneizados humanos cortical, la separación de proteínas por SDS-PAGE, la recuperación de antígeno y la inmunotransferencia con un anticuerpo para el péptido Aß. El uso de este protocolo, estamos constantemente detectar Aß monoméricos y multimérica en el tejido cortical de los seres humanos con la patología de Alzheimer.
Abstract
El plegamiento anómalo y la polimerización de la β-amiloide (Aß) péptido se cree que inician la cascada neurodegenerativa en la patogénesis de la enfermedad de Alzheimer
Protocol
Parte 1: Preparación de tejido homogeneizado aclaró
- Dounce homogeneizar el tejido cortical no fijadas en 4 veces el volumen de helado de amortiguación (0,1 M de buffer fosfato salino [Ca + + - y Mg + +-libre] proteasa más 2x cóctel de inhibidores de [Santa Cruz]), con aproximadamente 30 golpes, incluso mortero (es decir, buffer añadir 400μl a 100 mg de tejido).
- Homogeneizado de giro durante 5 minutos a 3.000 g (4 ° C). Retire con cuidado el sobrenadante clarificado y almacenar alícuotas de estos extractos a -80 ° C hasta su uso.
- Determinar la concentración de proteínas totales (mg / l) para aclarar homogeneizados utilizando un ácido bicinchoninic (BCA) de ensayo, de acuerdo con las instrucciones del fabricante (ThermoFisher).
Parte 2: SDS-PAGE preparación de la muestra
- Con un 10, así, el 10-20% Tricina gel (Invitrogen), el volumen máximo que se puede cargar por pozo es de ~ 25μl. El volumen total incluye buffer 2x SDS muestra y el agente 10x reduce, por lo que el volumen máximo de homogeneizado aclaró que se puede cargar por pozo es 10μl. Aclaró el 20% (w / v) homogeneizados corticales debe tener una concentración de proteínas totales de más de 5 mg / l, lo que permite 50 microgramos de proteínas totales por pozo. Las muestras con menos de 5mg/ml proteína se requieren menos carga de proteínas totales por pozo. Sin embargo, los altos niveles de proteínas son las más adecuadas para la detección de Aß monoméricos y agregados (50-60μg de proteínas totales es óptimo).
Cargue siempre la misma cantidad de proteínas totales por pozo. - Para cada gel, la carga de al menos un pozo con 10μl de un marcador de peso molecular tales como SeeBlue Plus2 (Invitrogen). Como control positivo, carrera de 10 100 ng de sintético Aβ40 o Aß42 péptido (diluida en 1XPBS) en otro pozo.
- Preparar las mezclas de reacción sobre hielo, con recién descongelada, homogenizados aclaró. Tubos de vórtice de 5-10 segundos, el calor en un baño seco a 100 º C durante 5 minutos, luego empieza a estar todas las muestras para eliminar la condensación en la tapa.
Parte 3: SDS-PAGE electroforesis en gel
- Cargar las muestras en un gel de vortex Tricina 10-20% en el XCell Sure Lock Mini-Celular Gelbox, utilizando Tricina buffer SDS funcionamiento, de acuerdo con las instrucciones del fabricante (Invitrogen),
- Corra el gel a un voltaje constante de 125V durante unos 90 minutos. Deje que las muestras de funcionar hasta que el marcador 4KDa banda es de aproximadamente 1 cm de la parte inferior del gel.
Parte 4: Las proteínas de transferencia de geles a membranas
- Retire con cuidado el gel de caja de plástico y montar el sandwich de transferencia en el interior del módulo XCell II Blot, de acuerdo con las instrucciones del fabricante (Invitrogen). Pre-húmedo secante almohadillas y membranas de nitrocelulosa 0.2μm con Tris-Glicina transferencia de buffer (20% de metanol), y eliminar las burbujas de pastillas de secado o el sándwich de papel de filtro / membrana.
- En el Gelbox XCell, llena la cámara interior con tampón de transferencia y llenar la cámara exterior con DIH 2 O (exposición metanol pueden desgastar el plástico gelbox lo largo del tiempo).
- Ejecutar la transferencia de 03.02 horas a un amperaje constante de 25 mA.
- Cuando se complete la transferencia, deconstruir el bocadillo y el lugar de los geles en DIH 2 O y las membranas en 1XPBS, tanto en la plaza de placas Petri de plástico (u otro recipiente apropiado).
- Para visualizar la eficiencia de la transferencia de las proteínas, los geles se pueden teñir con Simply Blue SafeStain (Invitrogen), y las membranas con mancha roja Ponceau S (Sigma Aldrich), ambos de acuerdo a las instrucciones del fabricante. Esta coloración no interfiere con inmunotransferencia. Si la tinción revela la transferencia de las proteínas ineficiente, modificar el tiempo de transferencia en el paso 3.
Parte 5. Antígeno de recuperación del epítopo y Immunoblotting
- La recuperación de antígeno es un paso importante en la revelación de los epítopos Aß en la membrana de unión de los anticuerpos durante inmunotransferencia. Baño de vapor cualquiera, microondas, o que el agua mantiene una temperatura constante de 100 º C es suficiente. Para la recuperación de antígeno en un barco de vapor, de sellado de la membrana en una bolsa de plástico resistente Kapak lleno de 1XPBS, a temperatura ambiente. Coloque la bolsa plana en un barco de vapor precalentadas, una vez que la bolsa comienza a expandirse, se incuba durante 15 minutos adicionales. Permitir que la membrana que se enfríe lentamente antes de sacarlo de la bolsa, para evitar las arrugas excesivas.
- A temperatura ambiente, retire con cuidado la membrana de la bolsa de vapor y lavado de la membrana durante 5 minutos en 1XPBS, seguido por un enjuague de 5 minutos en TBS-T (Tris-Buffered Saline pH, 8,0 con 0,05% de Tween-20 [Sigma] ), en un agitador orbital. Incube la membrana en solución de bloqueo (2,5% de leche descremada en TBS-T) durante una hora, temblando. Sin aclarar, la transferencia de la membrana de un plato o una bolsa de plástico que contiene el anticuerpo primario diluido en solución de bloqueo (6E10 a 1:1000 [1μg/ml] 1:5.000 [0.2μg/ml] dilución, Covance), evitando la burbujas. Incubar en un agitador orbital a temperatura ambiente durante una hora y después de 24-48 horas con agitación a 4 ° C (más de incubación puede dar una mejor señal).
- Enjuague la membrana durante 30 minutos en TBS-T (un enjuague rápido seguido de tres enjuagues minutos x 10).
- Incube la membrana en el HRP-anticuerpo secundario conjugado (Amersham ECL de oveja anti-ratón, GE Healthcare), diluidos en 1:10.000 en solución de bloqueo, durante 90 minutos en el agitador a temperatura ambiente.
- Enjuague la membrana durante 30 minutos en TBS-T (un enjuague rápido seguido de tres enjuagues minutos x 10).
- En la coctelera, se incuba la membrana en el recién hechas SuperSignal reactivo electroquimioluminiscencia West Pico (ThermoFisher) durante 5 minutos, seque fuera de reactivo en exceso en que no suelte pelusa de papel de filtro y colocar la membrana en un cassette de la película, entre los protectores de plástico. Mancha de más reactivo SuperSignal con polvo Kimwipes si es necesario.
- Exponerlo a la película Kodak Biomax MR para intervalos de 30 segundos hasta 30 minutos y se desarrollan en un desarrollador de la película. Después de 5 minutos, las bandas de monómero de Aß será probablemente saturada.
- Las membranas pueden ser despojado (después de lavado en TBS-T) por agitación en Restore Plus stripping buffer durante 30 minutos a temperatura ambiente y reprobed con anticuerpos adicionales si así lo desea.
Parte 6: Representante Inmunoblot:
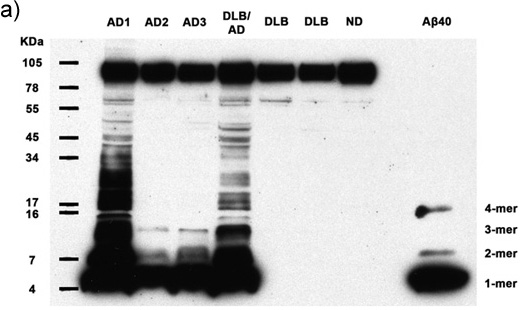


Figuras 1a-c. Homogeneizados aclaró que contienen 50 microgramos de proteína total de 7 sujetos humanos se analizó la presencia de Aß multimérica y APP. Inmunotransferencia con anticuerpos 6E10 revela monómeros Aß, dímeros, trímeros, tetrámeros y APP (banda superior) en todos los casos de Alzheimer, así como abundante mayor multímeros molecular Aß peso en 2 casos de EA. Sintético Aβ40 confirma la identidad de las bandas de menor peso molecular. AD: la enfermedad de Alzheimer, la DCL: demencia con cuerpos de Lewy, ND: humana no dementes (a) exposición de 30 minutos de duración, (b) la exposición 5 minutos de cine, (c) 30 exposición de la película segundos..
Subscription Required. Please recommend JoVE to your librarian.
Discussion
A pesar de la importancia de la agregación de Aß en la patogénesis de la enfermedad de Alzheimer 1,4,5, pocos estudios han descrito o cuantificar la distribución de los diversos multímeros Aß en muestras de tejido cortical 2. Comúnmente utilizado las técnicas de inmunohistoquímica no permiten la discriminación de las distintas especies de Aß multimérica en el tejido cortical fijo. En fijadas homogeneizados de tejido cortical, multímeros Aß se pueden separar y bioquímicamente evaluó mediante electroforesis en gel a base de anticuerpos y los métodos de detección. Sin embargo, los epítopos Aß que están dirigidos pueden estar ocultos dentro de las estructuras de péptidos modificados y agregados posteriormente a la traducción, la prevención de la detección y cuantificación precisa de Aß agregado. El uso de calor inducido por antígenos de recuperación del epítopo combinado con SDS-PAGE e inmunotransferencia con un anticuerpo contra la región N-terminal de Aß 6,7, somos capaces de separar y detectar natural multímeros Aß aislado de cerebros humanos. Distintas poblaciones multímero Aß en homogeneizados de tejido aclaró entonces puede ser cuantificada por densitometría. Además, la combinación de gel o de la membrana de extracción con Aß inmunotransferencia permitirá una mayor caracterización estructural de origen natural, posteriormente a la traducción modificada multímeros Aß a partir de tejido humano. Será importante determinar si multímeros Aß en el cerebro humano son SDS-resistente, o si son SDS-sensible y por lo tanto, divididos en pequeños agregados de desnaturalización SDS en condiciones definidas. La caracterización de las diversas formas de Aß agregado en el cerebro humano facilita la búsqueda de terapias y biomarcadores para la enfermedad de Alzheimer.
Subscription Required. Please recommend JoVE to your librarian.
Acknowledgments
Muchas gracias a Elaine Pranski y Carolyn Suwyn por su excelente asistencia técnica y Harry Levine III, M. Paul Murphy, y Transmisiones para conversaciones importantes Marla. El financiamiento fue proporcionado por el RR-00165, PO1AG026423, P50AG025688, AG030539, la Fundación Woodruff y la Universidad de Emory Comité de Investigación.
Materials
| Name | Company | Catalog Number | Comments |
| Complete Protease Inhibitor Cocktail Tablets | Santa Cruz Biotechnology, Inc. | Sc-29130 | 1 tablet in 25ml buffer |
| BCA Protein Assay kit | Thermo Fisher Scientific, Inc. | 23225 | |
| XCell SureLock Mini-Cell and XCell II Blot Module Kit CE Mark | Invitrogen | EI0002 | |
| Novex Tricine SDS Sample Buffer (2X) | Invitrogen | LC1676 | |
| NuPAGE Sample Reducing Agent (10X) | Invitrogen | NP0004 | |
| SeeBlue Plus2 Pre-Stained Standard | Invitrogen | LC5925 | |
| Novex 10-20% Tricine Gel 1.0 mm, 10 well | Invitrogen | EC6625BOX | |
| Nitrocellulose membranes, 0.2 μm pore size | Invitrogen | LC2000 | |
| Novex Tricine SDS Running Buffer (10X) | Invitrogen | LC1675 | |
| Novex Tris-Glycine Transfer Buffer (25X) | Invitrogen | LC3675 | |
| SimplyBlue SafeStain | Invitrogen | LC6060 | Will not interfere with immunostaining |
| ATX Ponceau S Red staining solution | Sigma-Aldrich | 09276 | Will not interfere with immunostaining |
| Kapak heat sealable plastic sample pouches | Fisher Scientific | 0181225AA | |
| 6E10 mouse monoclonal antibody to Aβ(1-16) | Covance | SIG-39320 | Dilute 1:1,000 up to 1:5,000 for WB |
| Tween 20 | Sigma-Aldrich | P2287 | |
| ECL Mouse IgG, HRP-Linked Whole Aβ (from sheep) | GE Healthcare | NA931-1ML | Dilute at 1:10,000 |
| SuperSignal West Pico Chemiluminescent Substrate | Thermo Fisher Scientific, Inc. | 34077 | |
| Kodak Biomax MR Film | Carestream Health | 870 1302 |
References
- Hardy, J., Selkoe, D. J. The amyloid hypothesis of Alzheimer's disease: progress and problems on the road to therapeutics. Science. 297, 353-356 (2002).
- Haass, C., Selkoe, D. J. Soluble protein oligomers in neurodegeneration: lessons from the Alzheimer's amyloid beta-peptide. Nat. Rev. Mol. Cell. Biol. 8, 101-112 (2007).
- Walker, L. C., LeVine, H. The cerebral proteopathies. Neurobiol. Aging. 21, 559-561 (2000).
- Selkoe, D. J. Aging, amyloid, and Alzheimer's disease: a perspective in honor. of Carl Cotman. Neurochem. Res. 28, 1705-1713 (2003).
- Walsh, D. M., Selkoe, D. J. Abeta oligomers - a decade of discovery. J. Neurochem. 101, 1172-1184 (2007).
- Swerdlow, P. S., Finley, D., Varshavsky, A. Enhancement of immunoblot sensitivity by heating of hydrated filters. Anal. Biochem. 156, 147-153 (1986).
- Ida, N., Hartmann, T., Pantel, J., Schröder, J., Zerfass, R., Förstl, H., Sandbrink, R., Masters, C. L., Beyreuther, K. Analysis of hetergeneous A4 peptides in human cerebrospinal fuid and blood by a newly developed sensitive Western blot assay. J. Biol. Chem. 271, 22908-22914 (1996).



