Summary
Total Vaporization Solid Phase Microextraction (TV-SPME) verdampft eine flüssige Probe vollständig, während Analyten an eine SPME-Faser sorbiert werden. Dies ermöglicht die Aufteilung des Analyten zwischen nur dem Lösungsmitteldampf und der SPME-Faserbeschichtung.
Abstract
Gaschromatographie – Massenspektrometrie (GC-MS) ist eine häufig verwendete Technik zur Analyse zahlreicher Analyten von forensischem Interesse, einschließlich kontrollierter Substanzen, entzündbarer Flüssigkeiten und Sprengstoffe. GC-MS kann mit der Festphasen-Mikroextraktion (SPME) gekoppelt werden, bei der eine Faser mit einer sorptiven Beschichtung in den Kopfraum über einer Probe gelegt oder in eine flüssige Probe eingetaucht wird. Analyten werden an die Faser sorbiert, die dann zur Desorption in den beheizten GC-Einlass gelegt wird. Total Vaporization Solid-Phase Microextraction (TV-SPME) verwendet die gleiche Technik wie Immersion SPME, taucht die Faser jedoch in einen vollständig verdampften Probenextrakt ein. Diese vollständige Verdampfung führt zu einer Trennung zwischen nur der Dampfphase und der SPME-Faser ohne Interferenz durch eine flüssige Phase oder unlösliche Materialien. Je nach Siedepunkt des verwendeten Lösungsmittels ermöglicht TV-SPME große Probenvolumina (z.B. bis zu Hunderte von Mikrolitern). Die On-Fiber-Derivatisierung kann auch mit TV-SPME durchgeführt werden. TV-SPME wurde verwendet, um Medikamente und ihre Metaboliten in Haaren, Urin und Speichel zu analysieren. Diese einfache Technik wurde auch auf Straßendrogen, Lipide, Kraftstoffproben, explosive Rückstände nach der Explosion und Schadstoffe im Wasser angewendet. Dieses Papier hebt die Verwendung von TV-SPME zur Identifizierung illegaler Verfälschungsmittel in sehr kleinen Proben (Mikrolitermengen) alkoholischer Getränke hervor. Sowohl Gamma-Hydroxybutyrat (GHB) als auch Gamma-Butyrolacton (GBL) wurden in Konzentrationen identifiziert, die in Spitzengetränken gefunden werden würden. Die Derivatisierung durch ein Trimethylsilylmittel ermöglichte die Umwandlung der wässrigen Matrix und GHB in ihre TMS-Derivate. Insgesamt ist TV-SPME schnell, einfach und erfordert keine Probenvorbereitung, abgesehen davon, dass die Probe in eine Headspace-Durchstechflasche gelegt wird.
Introduction
Festphasen-Mikroextraktion (SPME) ist eine Probenahmetechnik, bei der eine flüssige oder feste Probe in eine Headspace-Durchstechflasche gelegt wird und eine SPME-Faser, die mit einem polymeren Material beschichtet ist, dann in den Probenkopfraum eingeführt (oder in eine flüssige Probe eingetaucht) wird. Der Analyt wird an der Faser sorbiert und dann wird die Faser zur Desorption1,2in den GC-Einlass gelegt. Total Vaporization Solid-Phase Microextraction (TV-SPME) ist eine ähnliche Technik wie Immersion SPME, verdampft jedoch vollständig eine flüssige Probe, bevor Analyten an die Faser adsorbiert werden. Dies ermöglicht die Aufteilung des Analyten zwischen nur dem Lösungsmitteldampf und der Beschichtung der Faser, so dass mehr analyt an die Faser adsorbiert werden kann und eine guteEmpfindlichkeit entsteht 3. Es stehen verschiedene SPME-Fasern zur Verfügung und die Faser sollte basierend auf dem interessierenden Analyten, Lösungsmittel / Matrix und Derivatisierungsmittel ausgewählt werden. Siehe Tabelle 1 für etablierte TV-SPME-Analyten.
| Probe | Analyt(en) | Empfohlene SPME-Faser | Referenz(en) |
| Menschliches Haar | Nikotin, Cotinin | Polydimethylsiloxan/Divinylbenzol (PDMS/DVB), Polyacrylat (PA) | 3 |
| Rauchfreies Pulver | Nitroglycerin, Diphenylamin | Polydimethylsiloxan (PDMS), Polyethylenglykol (PEG) | 7, 8 |
| Rennkraftstoff | Methanol, Nitromethan | Pflock | 9 |
| Wasser | Polyzyklische aromatische Kohlenwasserstoffe | PDMS | 10 |
| Getränke | ɣ-Hydroxybuttersäure, ɣ-Butyrolacton | PDMS | Dieses Werk |
| Festes Pulver | Methamphetamin, Amphetamin | PDMS/DVB | unveröffentlicht |
Tabelle 1. Empfohlene SPME-Fasern mit etablierten TV-SPME-Analyten.
Um TV-SPME durchzuführen, werden Analyten in einem Lösungsmittel gelöst und ein Aliquot dieser Mischung in eine Kopfraumfläschchen gegeben. Proben müssen nicht gefiltert werden, da nur das Lösungsmittel und flüchtige Analyten verdampfen. Bestimmte Mengen flüssiger Proben müssen verwendet werden, um eine vollständige Verdampfung der Probe zu gewährleisten. Diese Volumina werden mit Dem Idealen Gasgesetz bestimmt, um die Anzahl der Mole eines Lösungsmittels multipliziert mit dem molaren Volumen der Flüssigkeit zu berechnen (Gleichung 1). Gleichung 1
Gleichung 1
wobei Vo das Volumen der Probe (ml), P der Dampfdruck des Lösungsmittels (bar), Vv das Volumen der Durchstechflasche (L), R die ideale Gaskonstante (0,083145),  M die molare Masse des Lösungsmittels (g/mol), T die Temperatur (K) und die Dichte des
M die molare Masse des Lösungsmittels (g/mol), T die Temperatur (K) und die Dichte des  Lösungsmittels (g/ml) ist. 3
Lösungsmittels (g/ml) ist. 3
Um den richtigen Dampfdruck zu verwenden, wird die Antoine-Gleichung (Gleichung 2) verwendet, um den Einfluss der Temperatur zu berücksichtigen:4 Gleichung 2
Gleichung 2
wobei T die Temperatur ist und A, B und C die Antoine-Konstanten für das Lösungsmittel sind. Gleichung 2 kann durch Gleichung 1 ersetzt werden, was ergibt: Gleichung 3
Gleichung 3
Gleichung 3 gibt das Volumen der Probe (Vo) an, das in Abhängigkeit von der Temperatur und dem verwendeten Lösungsmittel vollständig verdampft werden kann.
Um die Derivatisierung mit TV-SPME durchzuführen, wird die SPME-Faser zunächst einer Durchstechflasche ausgesetzt, die das Derivatisierungsmittel für eine bestimmte Zeit, abhängig vom Analyten, enthält. Die SPME-Faser wird dann einer neuen Durchstechflasche ausgesetzt, die den interessierenden Analyten enthält. Diese Durchstechflasche wird in einem beheizten Rührwerk erhitzt. Der Analyt wird dann mit dem Derivatisierungsmittel an die Faser adsorbiert. Die Derivatisierung des Analyten und/oder der Matrix erfolgt auf der Faser, bevor sie zur Desorption in den GC-Einlass eingeführt wird. Abbildung 1 zeigt eine Darstellung des TV-SPME-Prozesses mit Derivatisierung.

Abbildung 1: Darstellung des TV-SPME-Prozesses mit Derivatisierung. Die SPME-Faser gelangt zuerst in die Derivatisierungsfläschchen, wo das Derivatisierungsmittel (gelbe Kreise) an der Faser sorbiert. Die Faser wird dann in die Probe eingeführt (blaue Kreise) und erhitzt. Die Bildung des Derivats (grüne Kreise) findet während der Extraktionszeit auf der Faser statt. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
TV-SPME ist vorteilhaft, da es ermöglicht, den Analyten während des Extraktionsprozesses zu derivatieren, was die Analysezeit verkürzt. Andere Methoden, wie die Flüssigkeitsinjektion, erfordern, dass der Analyt mit dem Derivatisierungsmittel in Lösung reagiert, bevor er in den GC injiziert wird. TV-SPME erfordert auch wenig bis gar keine Probenvorbereitung. Eine Matrix, die einen Analyten enthält, kann direkt in die Kopfraumfläschchen gelegt und analysiert werden. Viele interessante Compounds sind mit TV-SPME kompatibel. Verbindungen müssen in einem Lösungsmittel löslich und ausreichend flüchtig sein, um eine Verdampfung zu ermöglichen. Darüber hinaus müssen Verbindungen thermisch stabil sein, um mit GC-MS analysiert zu werden. TV-SPME wurde verwendet, um Drogen und Arzneimittelmetaboliten, Rennkraftstoffe, polyzyklische aromatische Kohlenwasserstoffe und explosive Materialien3,5,6, 7,8,9,10zu analysieren.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1. Allgemeine TV-SPME Probenvorbereitung und GC-MS Analyse
HINWEIS: Wenn die Probe bereits in einer Matrix gelöst ist, fahren Sie mit Schritt 1.2 fort.
- Extrahieren oder lösen Sie die feste Probe in genügend Lösungsmittel (Wasser, Methanol, Aceton usw.), um die gewünschte Konzentration zu erreichen. Flüssige Proben können "wie besehen" verwendet werden.
HINWEIS: Die Menge der verwendeten festen Probe hängt von der gewünschten Konzentration der Probe ab. Konzentrationen unter 1 ppm (w/v) werden empfohlen, um eine Überlastung der GC-Säule zu vermeiden. Analyt sollte in ausgewählten organischen Lösungsmitteln löslich sein.- Stellen Sie sicher, dass sich die Probe vollständig aufgelöst hat.
- Berechnen Sie das Volumen, das erforderlich ist, um die Probe vollständig zu verdampfen, indem Sie Gleichung 3 bei der gewählten Temperatur verwenden. Wenn das Experiment beispielsweise bei 60 °C durchgeführt werden soll, berechnen Sie das Volumen, das benötigt wird, um das Lösungsmittel bei 60 °C vollständig zu verdampfen.
- Übertragen Sie dieses Probenvolumen in eine Headspace-Durchstechflasche und befestigen Sie die Kappe. Akzeptable Methoden zum Übertragen flüssiger Proben im Mikroliterbereich umfassen die manuelle Übertragung über eine Glasspritze, eine elektronische Glasspritze oder einen Autosampler-Roboter, der Flüssigkeitstransfers zur Probenvorbereitung ermöglicht.
- Wenn Sie die Probe derivatisieren, bereiten Sie das richtige Derivatisierungsmittel vor, indem Sie ~ 1 ml des Mittels in eine Kopfraumdurchstechflasche geben.
- Wählen Sie das Derivatisierungsmittel basierend auf der Art der erforderlichen Derivatisierung: Alkylierung, Acylation oder Silyation. In diesem Fall ist das empfohlene Derivatisierungsmittel für die auf GHB gefundenen funktionellen Gruppen von Carbonsäure und Alkohol O-Bis(trimethylsilyl)trifluoracetamid (BSTFA). Das Derivatisierungsmittel kann "wie besehen" verwendet werden und erfordert keine Verdünnung. Ein ml Derivatisierungsmittel reicht aus, um eine vollständige Sättigung der SPME-Faser zu gewährleisten.
ACHTUNG: Derivatisierungsmittel sind giftig und sollten in einem Abzug gehandhabt werden.
- Wählen Sie das Derivatisierungsmittel basierend auf der Art der erforderlichen Derivatisierung: Alkylierung, Acylation oder Silyation. In diesem Fall ist das empfohlene Derivatisierungsmittel für die auf GHB gefundenen funktionellen Gruppen von Carbonsäure und Alkohol O-Bis(trimethylsilyl)trifluoracetamid (BSTFA). Das Derivatisierungsmittel kann "wie besehen" verwendet werden und erfordert keine Verdünnung. Ein ml Derivatisierungsmittel reicht aus, um eine vollständige Sättigung der SPME-Faser zu gewährleisten.
- Stellen Sie die richtige Inkubations-/Extraktionstemperatur basierend auf der Berechnung in Schritt 1.2 ein. Diese Temperatur gewährleistet eine vollständige Verdampfung, eine ausreichende Probenextraktion und eine vollständige Derivatisierung (falls erforderlich).
- Wählen Sie GC-MS-Parameter (Ofentemperaturprogramm, Durchflussrate, Eingangstemperatur usw.) basierend auf der Klasse der interessierenden Verbindung(en). Einen Beispielparametersatz finden Sie in Schritt 3.
- Stellen Sie sicher, dass sich die richtige Einlassfolie (z. B. 2 mm Innendurchmesser oder weniger) im GC-Einlass befindet.
- Stellen Sie sicher, dass die SPME-Faser ordnungsgemäß konditioniert wurde und sich in einem guten Betriebszustand befindet, bevor Sie mit der Analyse beginnen.
- Variieren Sie die Konditionierungsparameter basierend auf der Art der verwendeten SPME-Faser. Bitte beachten Sie die SPME-Faseranweisungen für die richtige Konditionierungstemperatur und -zeit. Im Allgemeinen reicht die Analyse mehrerer SPME-Faserrohlinge aus, bis sie reproduzierbar sind, um eine SPME-Faser als vollständig konditioniert zu charakterisieren.
2. Gamma-Hydroxybutyrat (GHB) und Gamma-Butyrolacton (GBL) Probenvorbereitung
- Bereiten Sie eine Probe von GHB und/oder GBL in Wasser mit einer Konzentration von weniger als 1 ppm vor.
- 1 μL dieser Probe wird mit einem der in 1.2.1 beschriebenen Verfahren in eine Durchstechflasche mit 20 ml Headspace überführen.
- Beachten Sie, dass die Analyse wässriger Proben die geringsten Probenvolumina erfordert. Zum Beispiel verdampft ein μL Wasser vollständig in eine 20 ml Headspace-Durchstechflasche bei 60 °C.
- Die Durchstechflasche sofort verschließen.
- Legen Sie ~1 ml BSTFA + 1% Trimethylchlorsilan (TMCS) in eine separate 20 ml Headspace-Durchstechflasche und -Kappe.
HINWEIS: GBL derivatisiert nicht. Ein Derivatisierungsschritt ist jedoch weiterhin erforderlich, um sicherzustellen, dass das Wasserlösungsmittel derivatisiert und die Probe nicht stört.
ACHTUNG: BSTFA ist giftig und sollte in einem Abzug gehandhabt werden.
3. GC-MS Parameter und Setup für GHB und GBL im Wasser
- Erstellen Sie eine Methode mit den folgenden GC-MS-Parametern:
Anfängliche Ofentemperatur: 60 °C für 1 Minute gehalten.
Ofenprogramm: 15 °C/Minute.
Endtemperatur des Ofens: 280 °C, 1 Minute gehalten.
Durchfluss: 2,5 ml/Minute (drehzahloptimierter Durchfluss für eine 0,25 mm i.d. Säule).
Eingangstemperatur: 250 °C.
Temperatur der Transferleitung: 280 °C. - Stellen Sie sicher, dass ein schmaler (2 mm i.d. oder weniger) SPME-Einlassliner im GC-Einlass platziert wurde.
- Stellen Sie vor der Analyse sicher, dass die PDMS/DVB SPME-Faser ordnungsgemäß konditioniert wurde und in gutem Zustand ist.
HINWEIS: PDMS/DVB SPME-Fasern sollten im GC-Einlass bei 250 °C für 30 Minuten konditioniert werden. PDMS/DVB SPME-Fasern sollten eine cremefarbene Farbe haben. - Führen Sie gc-MS für das Beispiel aus.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
Eine GBL-Volumenstudie wurde durchgeführt, um die Empfindlichkeit von TV-SPME im Vergleich zu Headspace und Immersion SPME zu demonstrieren. Eine 100ppmv-Probe von GBL in Wasser wurde vorbereitet und in 20 ml Headspace-Fläschchen mit Volumina von 1, 3, 10, 30, 100, 300, 1000, 3000 und 10.000 μL gelegt. Das Phasenverhältnis der Proben erlaubte TV-SPME (1-3 μL), Headspace SPME (10 – 3.000 μL) und Immersion SPME (10.000 μL). Alle Proben wurden in dreifacher Ausfertigung analysiert und die durchschnittliche Peakfläche wurde gegen das Probenvolumen aufgeschrieben. Insgesamt zeigten Probenvolumina, die TV-SPME ermöglichten, eine mehr Empfindlichkeit als Headspace oder Immersion SPME für GBL in Wasser, wie in Abbildung 2 gezeigt. Ein Vergleich der Chromatogramme für jede Methode ist in Abbildung 3 dargestellt.

Abbildung 2: Diagramm der durchschnittlichen Spitzenfläche im Vergleich zum Probenvolumen für GBL in Wasser. Eine GBL-Volumenstudie wurde durchgeführt, um die Wirksamkeit von TV-SPME im Vergleich zu Headspace und Immersion SPME zu demonstrieren. Eine 100ppmv-Probe von GBL in Wasser wurde vorbereitet und in 20-ml-Headspace-Fläschchen mit Volumina von 1, 3, 10, 30, 100, 300, 1000, 3000 und 10000 μL gelegt. Alle Proben wurden dreifach analysiert und Fehlerbalken entsprechen der Standardabweichung des Mittelwerts. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 3: Gesamtionenchromatogramme für GBL in Wasser. (100 ppm) für 3 μL (blau), 300 μL (rot) und 10.000 μL (grün). Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Realistische Proben von Wein mit einer effektiven Dosis von GHB und GBL sind in Abbildung 4 bzw. Abbildung 5dargestellt. Diese Proben zeigen auch die Interkonversion von GBL und GHB. Wenn TV-SPME ordnungsgemäß ausgeführt wird, ergibt sich ein scharfer, reichlich vorhandener Peak, wie in Abbildung 6 dargestellt. TV-SPME hat eine gute Empfindlichkeit und daher sollten geeignete Konzentrationen verwendet werden, um die Säule nicht zu überlasten. Wenn hohe Konzentrationen vorhanden sind, ergibt sich eine Peak-Asymmetrie, wie in Abbildung 5 und Abbildung 7 dargestellt. In diesen Fällen kann die Verdünnung der Probe oder die Verwendung einer geteilten Injektion die Spitzenform verbessern.

Abbildung 4: Realistische GHB-Probe in Wein mit einer Konzentration von 8 mg/ml. Peaks: 1) GBL, 2) Hexansäure-TMS, 3) GHB-TMS2,4) Benzoesäure-TMS, 5) Octansäure-TMS, 6) Glycerin-TMS3,* bezeichnet ein cyclisches Siloxan (Faser-/Säulenblutung). Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 5: Realistische GBL-Probe in Wein mit einer Konzentration von 10 mg/ml. Peaks: 1) GBL, 2) Hexansäure-TMS, 3) Siloxan, 4) Trimethyl(2-phenylethoxy)silan, 5) GHB-TMS2. TIC zeigt die GBL-Konvertierung in GHB. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 6: Gesamtionenchromatogramm für GBL in Wasser mit einer Konzentration von 0,1 ppm. Ergebnisse nach der zuvor beschriebenen TV-SPME-Methode für GBL in Wasser. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 7: Gesamtionenchromatogramm für GBL in Wasser mit einer Konzentration von 10 ppm. Ergebnisse nach der zuvor beschriebenen TV-SPME-Methode für GBL in Wasser. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Bei der Derivatisierung sollte der Analytiker sicherstellen, dass die Methode es ermöglicht, dass der/die Analyt(en) vollständig derivatisiert werden kann,bevor er in den GC desorgiert wird. Eine partielle Derivatisierung kann zu einem Peak führen, der den derivatisierten Analyten darstellt, und zu einem Peak, der den nicht derivatisierten Analyten darstellt. Eine partielle Derivatisierung führt auch zu einer geringeren Empfindlichkeit für den Analyten, da weniger davon an der Faser adsorbieren kann.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
TV-SPME hat einige Vorteile gegenüber der Flüssigkeitsinjektion GC, da große Probengrößen (z. B. 100 μL) ohne Gerätemodifikationen verwendet werden können. TV-SPME hat auch einige der gleichen Vorteile wie Headspace SPME. Headspace SPME erfordert keine Extraktion oder Filtration, da nichtflüchtige Verbindungen in der Headspace-Durchstechflasche verbleiben und nicht an die Faser adsorbiert werden, was zu einer sauberen Probe führt. Diese Methode hilft auch, Matrixeffekte zu eliminieren, da es sich um ein zweiphasiges System (Headspace und Faser) im Gegensatz zu einem dreiphasigen System (Probe, Headspace und Faser) wie Standard-Headspace SPME handelt. TV-SPME ist wie Immersion SPME, da Immersion SPME auch ein zweiphasiges System ist. Beim Eintauchen von SPME wird eine Faser in eine flüssige (typischerweise wässrige) Probe getaucht, die den Analyten enthält, anstatt den Analyten aus seinem Dampf zu extrahieren. TV-SPME unterscheidet sich von Immersions-SPME, da Immersions-SPME eine polare/wässrige Matrix benötigt, um genügend Antriebskraft für Analyten zu erzeugen, die die Lösungsphase verlassen und an der Faserbeschichtung sorbieren können. Darüber hinaus erfordert Immersions-SPME viel größere Probenvolumina (z. B. ml).
Viele Lösungsmittel können mit TV-SPME verwendet werden, einschließlich Methanol, Aceton, Wasser und Acetonitril. SPME-Fasern sollten chloroform nicht ausgesetzt oder in chloroform eingetaucht werden, da diese Lösungsmittel die Faserbeschichtung beschädigen können. Zwanzig ml Schraubverschluss Glas Headspace Fläschchen haben die beste Leistung mit TV-SPME-Methoden. Es wird empfohlen, einen Autosampler mit TV-SPME zu verwenden. Während viele Parameter der TV-SPME-Methode nach Belieben eingestellt werden können, muss für jedes Lösungsmittel das richtige Volumen und die richtige Extraktionstemperatur verwendet werden. Probenvolumen und Extraktionstemperatur sind proportional zueinander und müssen entsprechend angepasst werden. Beispielsweise kann die Extraktionstemperatur eines Verfahrens reduziert werden, aber auch das Probenvolumen muss reduziert werden. Dieses Volumen kann durch Anpassen von Gleichung 3 gefunden werden.
Änderungen am Derivatisierungsverfahren können vorgenommen werden. Die Derivatisierung kann vor oder nach der Extraktion bei Raumtemperatur oder im Rührwerk erhitzt werden, indem die Faser dem Dampf des Derivatisierungsmittels ausgesetzt oder die Faser direkt in das Derivatisierungsmittel eingetaucht wird.
Es gibt Einschränkungen für die TV-SPME-Methode, einschließlich der Notwendigkeit, dass Verbindungen löslich, thermisch stabil und flüchtig sind. TV-SPME benötigt teure SPME-Fasern, deren Beschichtung während der Analyse abgestreift oder gebrochen werden kann. Diese Einschränkungen werden durch Vorteile wie große Probenvolumina im Vergleich zu typischen GC-Injektionsvolumina, hohe Empfindlichkeit und keine Notwendigkeit einer Filtration aufgewogen. TV-SPME wird Headspace SPME vorgezogen, da mehr von der Probe auf die Faser extrahiert wird und Matrixeffekte reduziert werden. TV-SPME wird auch dem Immersions-SPME vorgezogen, da Immersions-SPME viel mehr Samples verbraucht als TV-SPME. TV-SPME ermöglicht eine Derivatisierung während des Extraktionsprozesses, was die Analysezeit im Vergleich zu Methoden wie der Flüssigkeitsinjektion reduziert, bei denen der Analyt vor der Injektion derivatisiert werden muss. TV-SPME erfordert auch wenig bis gar keine Probenvorbereitung. TV-SPME ist einfach, effizient und empfindlich für die Analyse einer Vielzahl von Proben, einschließlich Drogen, explosiven Materialien und Rennkraftstoffen.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Die Autoren haben nichts preiszugeben.
Acknowledgments
Diese Forschung wurde vom National Institute of Justice unterstützt (Award No. 2015-DN-BX-K058 & 2018-75-CX-0035). Die hier geäußerten Meinungen, Erkenntnisse und Schlussfolgerungen sind die des Autors und spiegeln nicht unbedingt die der Förderorganisationen wider.
Materials
| Name | Company | Catalog Number | Comments |
| 10 µL Syringe | Gerstel | 100111-014-00 | |
| BSTFA + 1% TMCS (10 x 1 GM) | Regis Technologies Inc. | 50442882 | |
| eVol XR Sample Dispensing System Kit | ThermoFisher Scientific | 66002-024 | |
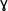 -Butyrolactone (GBL) -Butyrolactone (GBL) |
Sigma-Aldrich | B103608-26G | |
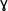 -Hydroxy Butyric Acid (GHB) -Hydroxy Butyric Acid (GHB) |
Cayman Chemicals | 9002506 | |
| Headspace Screw-Thread Vials, 18 mm | Restek | 23083 | |
| Magnetic Screw-Thread Caps, 18 mm | Restek | 23091 | |
| Optima water for HPLC | Fisher Chemical | W71 | |
| SPME Fiber Assembly Polydimethylsiloxane (PDMS) | Supelco | 57341-U | |
| SPME Fiber Assembly Polydimethylsiloxane/Divinylbenzene (PDMS/DVB) | Supelco | 57293-U | |
| Topaz 2.0 mm ID Straight Inlet Liner | Restek | 23313 |
References
- Pawliszyn, J. B. Method and Device for Solid Phase Microextraction and Desorption. United States patent. , (2005).
- Pawliszyn, J. Solid phase microextraction: theory and practice. , John Wiley & Sons. (1997).
- Rainey, C. L., Bors, D. E., Goodpaster, J. V. Design and optimization of a total vaporization technique coupled to solid-phase microextraction. Analytical Chemistry. 86 (22), 11319-11325 (2014).
- Sinnott, R. Chemical Engineering Design: Chemical Engineering. 6, Elsevier. (2005).
- Davis, K. Detection of Illicit Drugs in Various Matrices Via Total Vaporization Solid-Phase Microextraction (TV-SPME). , Indiana University - Purdue University Indianapolis. Master of Science thesis (2019).
- Ash, J., Hickey, L., Goodpaster, J. Formation and identification of novel derivatives of primary amine and zwitterionic drugs. Forensic Chemistry. 10, 37-47 (2018).
- Sauzier, G., Bors, D., Ash, J., Goodpaster, J. V., Lewis, S. W. Optimisation of recovery protocols for double-base smokeless powder residues analysed by total vaporisation (TV) SPME/GC-MS. Talanta. 158, 368-374 (2016).
- Bors, D., Goodpaster, J. Mapping smokeless powder residue on PVC pipe bomb fragments using total vaporization solid phase microextraction. Forensic science international. 276, 71-76 (2017).
- Bors, D., Goodpaster, J. Chemical analysis of racing fuels using total vaporization and gas chromatography mass spectrometry (GC/MS). Analytical Methods. 8 (19), 3899-3902 (2016).
- Beiranvand, M., Ghiasvand, A. Design and optimization of the VA-TV-SPME method for ultrasensitive determination of the PAHs in polluted water. Talanta. 212, 120809 (2020).



