Overview
Fonte: Tamara M. Powers, Dipartimento di Chimica, Texas A & M University
I complessi carbonilici metallici sono utilizzati come precursori metallici per la sintesi di complessi organometallici e catalizzatori. La spettroscopia infrarossa (IR) è uno dei metodi di caratterizzazione più utilizzati e informativi dei composti contenenti CO. La teoria dei gruppi, o l'uso della matematica per descrivere la simmetria di una molecola, fornisce un metodo per prevedere il numero di modalità vibrazionali C-O attive IR all'interno di una molecola. Osservare sperimentalmente il numero di allungamenti C-O nell'IR è un metodo diretto per stabilire la geometria e la struttura del complesso carbonilico metallico.
In questo video, sintetizzaremo il complesso carbonilico di molibdeno Mo(CO)4[P(OPh)3]2, che può esistere nelle forme cis- e trans-(Figura 1). Useremo la teoria dei gruppi e la spettroscopia IR per determinare quale isomero è isolato.
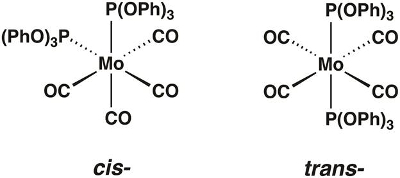
Figura 1. Gli isomeri cis- e trans-isomeri di Mo(CO)4[P(OPh)3]2.
Principles
Regole di selezione:
Le regole di selezione dettano il numero di transizioni elettroniche, da uno stato quantistico all'altro, che sono possibili per una data molecola. La spettroscopia IR sonda le transizioni vibrazionali dallo stato fondamentale della molecola, v = 0, al primo stato eccitato, v = 1. Il numero di gradi di libertà vibrazionale (normali modi di vibrazione) per molecole lineari e non lineari può essere calcolato utilizzando rispettivamente l'equazione 1 e l'equazione 2.
3N - 5 (1)
3N - 6 (2)
dove N = il numero di atomi nella molecola
Affinché una normale modalità di vibrazione sia attiva IR, il dipolo della molecola deve cambiare. Pertanto, tutte le normali modalità di vibrazione in cui non si verifica un cambiamento nel dipolo sono IR inattive. Il numero di modalità IR attive può essere determinato utilizzando la teoria dei gruppi.
Teoria deigruppi :
I chimici usano la teoria dei gruppi per comprendere la relazione tra la simmetria e le proprietà fisiche di una molecola. Mentre l'ambito della teoria dei gruppi è troppo ampio per essere rigorosamente coperto in questo video, forniremo gli strumenti necessari per applicare la teoria dei gruppi a semplici complessi di coordinazione e mostrare come può essere utilizzata per prevedere il numero di modalità vibrazionali attive IR. Per dimostrare, cammineremo attraverso l'applicazione della teoria dei gruppi alla molecola cis-Mo(CO)4[P(OPh)3]2.
In primo luogo, dobbiamo determinare il gruppo di punti della molecola. I gruppi di punti sono usati per descrivere gli elementi di simmetria presenti in una data molecola. Per determinare il gruppo puntiare di cis-Mo(CO)4[P(OPh)3]2, possiamo usare un diagramma di flusso chiamato albero di simmetria, che pone una serie di domande sugli elementi di simmetria presenti nella molecola ( Figura2). La Tabella 1 riassume tutti gli elementi di simmetria inclusi nell'albero di simmetria. Usando l'albero di simmetria, e assumendo che i ligandi P(OPh)3 siano ligandi punti (ignorando la simmetria di quei ligandi), troviamo che cis-Mo(CO)4[P(OPh)3]2 è nel gruppo di punti C2v.

Figura 2. Albero di simmetria utilizzato per la determinazione del gruppo di punti.
Tabella 1. Elementi di simmetria utilizzati nella determinazione del gruppo di punti.
| Elemento di simmetria | Simbolo utilizzato | Esempio* |
| Identità | E |  |
| Asse di rotazione (rotazione di 360°/n) |
Cn |  |
| Piano speculare orizzontale (riflessione sul piano xy) |
σh |  |
| Piano dello specchio verticale (riflessione sul piano xz o yz) |
σv |  |
| Piano diagonale dello specchio (riflessione tra i piani xz e yz) |
σd |  |
| Centro inversione | io |  |
| Asse di rotazione improprio (rotazione di 360°/n seguita da riflessione perpendicolare all'asse di rotazione) |
Sn |  |
| *Esempi sono per un complesso ottaedrico, dove i ligandi 1–6 sono equivalenti. Dopo aver eseguito l'operazione, la molecola risultante dovrebbe essere indistinguibile dalla sua configurazione originale. | ||
Per il passaggio successivo, dobbiamo introdurre tabelle di caratteri, che descrivono tutta la simmetria presente all'interno di un determinato gruppo di punti. La tabella dei caratteri per il gruppo di punti C2v è mostrata di seguito.
| C2v | E | C2 | σv(xz) | σv'(yz) | ||
| A1 | 1 | 1 | 1 | 1 | z | x2, y2, z2 |
| A2 | 1 | 1 | −1 | −1 | Rz | xy |
| B1 | 1 | −1 | 1 | −1 | x, Ry | xz |
| B2 | 1 | −1 | −1 | 1 | y, Rx | yz |
Il gruppo di punti è indicato nell'angolo in alto a sinistra della tabella dei caratteri. A destra del gruppo di punti sono elencate tutte le operazioni di simmetria inerenti a tale gruppo di punti. Le righe successive elencano tutte le rappresentazioni di simmetria (rappresentazioni irriducibili, rappresentate dai simboli di Mulliken, cioè A1) contenute in quel gruppo di punti, insieme alla simmetria delle funzioni, che possono dirci della simmetria degli orbitali atomici e del movimento lineare lungo gli assi x, y e z.
Utilizzando la tabella dei caratteri per il gruppo di punti C2v,generiamo una rappresentazione riducibile (Γrosso)dei modi di allungamento C-O nella molecola cis-Mo(CO)4[P(OPh)3]2 (Figura 3). La rappresentazione riducibile, o la combinazione lineare di rappresentazioni irriducibili, può essere generata applicando ciascuna delle operazioni di simmetria all'interno della tabella dei caratteri alle vibrazioni all'interno della molecola e registrando il numero di vibrazioni C-O che rimangono invariate (nella stessa posizione nello spazio). Ad esempio, applicando l'elemento di simmetria dell'identità alle vibrazioni C-O in cis-Mo(CO)4 [P(OPh)3]2, tutte e quattro le frecce vibrazionali rimangono nellastessaposizione. Pertanto, il primo valore nella nostra rappresentazione riducibile è 4. Se continuiamo questo esercizio, generiamo la rappresentazione riducibile mostrata di seguito.
| C2v | E | C2 | σv(xz) | σv'(yz) |
| Γrosso | 4 | 0 | 2 | 2 |
Successivamente, usiamo la tabella dei caratteri C2v per trovare la combinazione lineare di rappresentazioni irriducibili che genera Γrosso per le vibrazioni C-O all'interno di cis-Mo(CO)4[P(OPh)3]2. La riduzione della rappresentazione riducibile può essere ottenuta utilizzando la formula di riduzione mostrata nell'equazione 3.
 (3)
(3)
dove:
ni = numero di volte in cui la rappresentazione irriducibile i si verifica nella rappresentazione riducibile
h = ordine del gruppo (numero totale di operazioni di simmetria)
c = la classe di funzionamento
gc = numero di operazioni nella classe
χi = carattere della rappresentazione irriducibile per le operazioni della classe
χr = carattere della rappresentazione riducibile per le operazioni della classe
Usando l'equazione 3 per ciascuna delle rappresentazioni irriducibili nella tabella dei caratteri C2v, troviamo che Γrosso = 2A1 + B1 + B2. Tutte e tre le rappresentazioni irriducibili che contribuiscono, A1, B1e B2, sono attive IR perché si trasformano come asse x, y o z (vedere la simmetria delle funzioni nella tabella dei caratteri). Pertanto, prevediamo che cis-Mo(CO)4[P(OPh)3]2 mostrerà 4 modalità di allungamento C-O nel suo spettro IR.
Per riassumere, sono necessari i seguenti passaggi per determinare il numero di modalità vibrazionali attive IR in una molecola:
1. Determinare il gruppo di punti della molecola.
2. Generare una rappresentazione riducibile delle vibrazioni di allungamento C-O all'interno della molecola.
3. Ridurre la rappresentazione riducibile usando l'equazione 3.
4. Identificare il numero di rappresentazioni irriducibili traslazionali presenti nella rappresentazione ridotta dal passaggio 3.
Se seguiamo questi 4 passaggi con trans-Mo(CO)4[P(OPh)3]2, scopriamo che la molecola possiede solo 1 modalità vibrazionale C-O attiva.

Figura 3. CO si estende vibrazionale in cis-Mo(CO)4[P(OPh)3]2.
Subscription Required. Please recommend JoVE to your librarian.
Procedure
1. Configurazione della linea Schlenk (per una procedura più dettagliata, consultare il video "Schlenk Lines Transfer of Solvent" nella serie Essentials of Organic Chemistry). La sicurezza della linea Schlenk deve essere rivista prima di condurre questo esperimento. La vetreria deve essere ispezionata per le crepe delle stelle prima dell'uso. Prestare attenzione per assicurarsi che O2 non sia condensato nella trappola della linea di Schlenk se si utilizza N2liquido . A temperatura N2 liquida, O2 condensa ed è esplosivo in presenza di solventi organici. Se si sospetta che O2 sia stato condensato o che si osservi un liquido blu nella trappola fredda, lasciare la trappola fredda sotto vuoto dinamico. NON rimuovere latrappola N 2 liquida o spegnere la pompa pervuoto. Nel tempo il liquido O2 sublima nella pompa; è sicuro rimuovere latrappola N 2 liquida solo una volta che tutto l'O2 è sublimare.
- Chiudere la valvola di rilascio della pressione.
- Accendere il gas N2 e la pompa per vuoto.
- Quando il vuoto della linea Schlenk raggiunge la sua pressione minima, preparare la trappola fredda con N2 liquido o ghiaccio secco/acetone.
- Assemblare la trappola fredda.
2. Sintesi di Mo(CO)4[P(OPh)3]2 (Figura 4)1
Nota: Utilizzare tecniche standard della linea Schlenk per la sintesi di Mo(CO)4[P(OPh)3]2 (vedere il video "Sintesi di un metallocene Ti(III) utilizzando la tecnica della linea Schlenk"). I complessi carbonilici metallici sono una fonte di CO libero, che è altamente tossico. L'avvelenamento da monossido di carbonio si verifica quando il CO si lega all'emoglobina, con conseguente significativa riduzione dell'apporto di ossigeno al corpo. Pertanto, è estremamente importante adottare misure di sicurezza appropriate quando si maneggiano e si lavora con complessi metallici carbonilici. Le reazioni che generano CO libero devono essere condotte in una cappa ben ventilata per prevenire l'esposizione al gas tossico.
- Aggiungere 1,6 g (4,92 mmol) di Mo(CO)4(nbd) (nbd = 2,5-Norbornadiene) e 1,6 mL (9,84 mmol) di trifenilfosfito (P(OPh)3) a un matraccio Schlenk da 100 mL e preparare il matraccio Schlenk per il trasferimento cannula del solvente.
Nota: Mo(CO)4(nbd) ((Bicyclo[2.2.1]hepta-2,5-diene)tetracarbonylmolybdenum(0)) può essere acquistato da Sigma Aldrich o sintetizzato utilizzando metodi di letteratura. 2 - Aggiungere 20 ml di diclorometano degassato al matraccio schlenk tramite trasferimento di cannula.
- Mescolare la miscela di reazione per 4 ore a temperatura ambiente sotto N2.
- Rimuovere i volatili sotto vuoto e lavare il precipitato risultante con esani freddi (due lavaggi ciascuno con 10 ml, -78 °C).
- Asciugare il prodotto solido sotto vuoto per 15 min.
- Misurare lo spettro IR del prodotto in una soluzione di esani.

Figura 4. Sintesi di Mo(CO)4[P(OPh)3]2.
La teoria dei gruppi è un modello matematico che collega la simmetria molecolare a proprietà come i modi vibrazionali IR-attivi.
Ogni molecola può essere classificata con un gruppo puntiare, che descrive ogni elemento di simmetria presente in una molecola rispetto a un punto fisso.
La teoria dei gruppi fornisce tabelle speciali, chiamate tabelle dei caratteri,per prevedere l'effetto della simmetria di una molecola sui suoi modi vibrazionali e altre proprietà importanti.
Questo video discuterà i principi alla base della teoria dei gruppi, illustrerà la procedura per la sintesi e la caratterizzazione di un isomero di Mo(CO)4[P(OPh)3]2e introdurrà alcune applicazioni della teoria dei gruppi in chimica.
La simmetria molecolare descrive le configurazioni indistinguibili di una molecola. Le trasformazioni tra loro sono chiamate operazioni di simmetria, che si verificano rispetto a uno o più elementi di simmetria.
I cinque elementi di simmetria sono assi di rotazione corretti e impropri, piani speculari, centri di inversione e identità. Ogni molecola ha l'elemento identità, o E, in cui non si verifica alcun cambiamento.
Un piano speculare,etichettato σ, è un piano di riflessione con configurazioni iniziali e finali identiche. Le molecole possono avere più di un piano speculare. Un centro di inversione, etichettato i, è un punto attraverso il quale ogni atomo viene riflesso.
Un asse di rotazione corretto è un asse attorno al quale una molecola ruota in una configurazione identica. È etichettato Cn, dove n è 360 diviso per l'angolo di rotazione.
Un asse di rotazione improprio, etichettato Sn, è l'asse attorno al quale una molecola viene ruotata e quindi riflessa attraverso un piano speculare perpendicolare. Le molecole possono avere più di un asse di rotazione. L'asse con il più alto n è l'asse principale.
Le molecole sono assegnate a gruppi di punti utilizzando un albero di simmetria, che identifica le operazioni di simmetria necessarie per classificare la molecola.
Ad esempio, BF3 non è lineare. Non ha almeno due assi con n maggiore di 2. Ha almeno un asse di rotazione; il suo asse principale è C3. Ha tre assi C2 perpendicolari al suo asse principale e un piano speculare perpendicolare al suo asse principale. Pertanto, il trifluoruro di boro appartiene al gruppo di punti D3h.
Ogni gruppo di punti ha una tabella di caratteri che elenca le sue operazioni di simmetria essenziali. Ogni riga contiene una rappresentazione irriducibile delle operazioni, insieme ai corrispondenti orbitali atomici e movimenti lineari.
Le rappresentazioni riducibili vengono generate valutando come queste operazioni di simmetria influenzano le proprietà molecolari. La riduzione di questa rappresentazione dà il contributo di rappresentazioni irriducibili.
Ora che hai compreso i principi della teoria dei gruppi, passiamo attraverso una procedura per sintetizzare un isomero di Mo(CO)4[P(OPh)3]2 e confrontando il suo spettro IR con il numero di modi IR-attivi previsti per ciascun isomero dalla teoria dei gruppi.
Per iniziare la procedura, chiudere lo sfiato della linea Schlenk e avviare il flusso di gas N2. Accendere la pompa per vuoto e con il sistema alla sua pressione minima, raffreddare la trappola per vuoto con ghiaccio secco in acetone.
In una cappa aspirante, misurare 0,5 g di Mo(CO)4(nbd) e posizionare il precursore del molibdeno in un matraccio Schlenk da 200 mL. Equipaggiare il pallone di reazione con una barra di agitazione e tappare il pallone con un tappo di vetro. Collegare il pallone alla linea Schlenk tramite ilbraccio laterale e preparare il matraccio per il trasferimento della cannula evacuando il recipiente per 5 minuti, quindi riempiendo il matraccio con N2. Ripetere questo processo di evacuazione e ricarica per un totale di 3 volte.
Preparare poi un altro matraccio Schlenk munito di un setto di gomma contenente 20 ml di CH2Cl2. Collegare il pallone alla linea Schlenk e fissare il pallone nel cofano. Utilizzando una siringa, prelevare 0,87 mL di trifenilfosfito ed erogarlo nel matraccio schlenk. Assicurarsi che il rubinetto della linea Schlenk sia aperto a N2. Degassare la miscela CH2Cl2/trifenilfosfito facendo gorgogliare N2 attraverso il solvente per 10 minuti. Quindi utilizzare il trasferimento della cannula per aggiungere la soluzione al pallone contenente il solido. Aprire il pallone di reazione al gas N2 e mescolare la miscela a temperatura ambiente per 4 ore.
Una volta terminata la reazione, sostituire il setto di gomma con un tappo di vetro e rimuovere i solventi volatili sotto vuoto.
Aggiungere gli esani al prodotto risultante e raffreddare brevemente in un bagno di ghiaccio secco/ acetone, fino a formare un precipitato. Filtrare il precipitato e lavare il precipitato due volte con 10 ml di esani freddi e raccogliere il solido mediante filtrazione. Asciugare il prodotto solido sotto vuoto per 15 minuti.
Infine, sciogliere una parte del prodotto in esani e caricare la soluzione in una cella IR. Acquisire uno spettro IR del complesso.
Ora, determiniamo se il prodotto è l'isomero cis o trans assegnando gruppi di punti a entrambi gli isomeri e confrontando i modi ir-attivi previsti con lo spettro IR.
Né l'isomero cis né trans è lineare e nessuno dei due assi di rotazione ha ordini superiori a 2. Entrambi hanno almeno un asse di rotazione. Gli assi principali per gli isomeri cis e trans sono rispettivamente C2 e C4.
L'isomero cis non ha due assi C2 perpendicolari al suo asse C2, né ha un piano speculare perpendicolare. Ha due piani speculari contenenti l'asse C2, quindi il suo gruppo di punti è C2v. L'isomero trans ha quattro assi C2 e un piano speculare perpendicolare al suo asse C4, quindi il suo gruppo di punti è D4h.
Successivamente, le rappresentazioni riducibili degli allungamenti di CO vengono generate applicando ogni operazione di simmetria alla molecola e contando gli allungamenti C-O che non cambiano posizione nello spazio.
La tabella C2v ha quattro operazioni: identità, rotazione C2 e riflessioni attraverso due piani speculari contenenti l'asse C2. Nell'operazione di identità, tutti e quattro i momenti di dipolo rimangono al loro posto. Tutti e quattro i momenti di dipolo assumono posizioni diverse dopo una rotazione C2. Due momenti di dipolo rimangono nella stessa posizione per ogni riflessione.
La formula di riduzione calcola il coefficiente di ogni rappresentazione irriducibile nella rappresentazione riducibile. L'ordine dei gruppi di punti è il numero di operazioni di simmetria. Le classi sono tipi di operazioni di simmetria. Qui, il numero di operazioni in ogni classe è 1, che viene tradizionalmente omesso da una tabella di caratteri.
Il carattere è il valore corrispondente a una rappresentazione per una determinata classe. Quando viene applicata la formula di riduzione, si trovano tre rappresentazioni irriducibili, di cui una si verifica due volte. Queste rappresentazioni si trasformano come asse x, yo z, che è coerente con quattro allungamenti C-O IR-attivi.
Usando la stessa tecnica, l'isomero trans ha un tratto C-O IR-attivo. Lo spettro IR del prodotto di molibdeno ha picchi a 2046, 1958 e 1942 cm-1. Con dati a risoluzione più elevata, si può osservare un quarto allungamento C-O. Sulla base dell'IR ottenuto, si può concludere che il complesso isolato Mo(CO)4[P(OPh)3]2 è l'isomero cis.
La teoria dei gruppi è ampiamente utilizzata nella chimica organica e inorganica. Diamo un'occhiata ad alcuni esempi.
La spettroscopia Raman rileva vibrazioni molecolari che comportano cambiamenti nella polarizzabilità nella nube di elettroni. Un allungamento simmetrico in CO2 non cambia il momento di dipolo, e quindi non è IR-attivo. Tuttavia, gli elettroni che si allontanano dai nuclei cambiano la polarizzabilità, rendendo l'allungamento Raman-attivo. La teoria dei gruppi può identificare i modi vibrazionali Raman-attivi seguendo lo stesso metodo generale utilizzato per identificare i modi IR-attivi.
La teoria degli orbitali molecolari, o teoria MO, è un modello usato per descrivere il legame nelle molecole. L'aggiunta e la sottrazione degli orbitali atomici di due atomi porta alla formazione di diagrammi orbitali molecolari di semplice biatomica.
Per generare diagrammi MO di complessi di metalli di transizione, gli scienziati usano la teoria dei gruppi per generare combinazioni lineari adattate alla simmetria di orbitali atomici per rappresentare gli atomi o i ligandi esterni. Ciò si ottiene generando rappresentazioni riducibili degli orbitali atomici del ligando e quindi riducendole a una rappresentazione irriducibile.
Le rappresentazioni di simmetria del centro metallico e le combinazioni lineari adattate alla simmetria sono confrontate nel diagramma. In questo modello, orbitali con la stessa simmetria si sovrappongono per formare due orbitali molecolari.
Hai appena visto l'introduzione di JoVE alla teoria dei gruppi. Ora dovresti avere familiarità con i principi alla base della simmetria molecolare, trovando il gruppo di punti di una molecola e alcuni esempi di come la teoria dei gruppi viene utilizzata nella chimica organica e inorganica. Grazie per l'attenzione!
Subscription Required. Please recommend JoVE to your librarian.
Results

Figura 5. IR di Mo(CO)4[P(OPh)3]2.
Soluzione IR in idrocarburi saturi (cm-1): 2046 (s), 1958 (s), 1942 (vs).
La quarta risonanza può essere vista solo in condizioni ad alta risoluzione. Pertanto, è possibile, come in questo caso, che si osservino solo 3 delle 4 risonanze.
Sulla base dell'IR ottenuto, possiamo concludere che l'isomero cis di Mo(CO)4[P(OPh)3]2 è stato isolato.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
In questo video, abbiamo imparato come usare la teoria dei gruppi per prevedere il numero di modalità vibrazionali attive IR in una molecola. Abbiamo sintetizzato la molecola Mo(CO)4[P(OPh)3]2 e abbiamo usato IR per determinare quale isomero è stato isolato. Abbiamo osservato che il prodotto aveva tre vibrazioni C-O nel suo spettro IR, che è coerente con l'isomero cis.
La teoria dei gruppi è un potente strumento che viene utilizzato dai chimici non solo per prevedere i modi vibrazionali attivi IR, ma anche vibrazionali, rotazionali e altri modi a bassa frequenza osservati nella spettroscopia Raman. Inoltre, la teoria dei gruppi è implementata nella teoria degli orbitali molecolari (MO), che è il modello più utilizzato per descrivere il legame all'interno di complessi di metalli di transizione. I diagrammi MO, utilizzati dai chimici organici e inorganici, possono prevedere e spiegare la reattività osservata di una molecola.
I complessi carbonilici metallici di1a,2ae3a fila sono ampiamente utilizzati nella sintesi inorganica come precursori metallici per composti organometallici più complessi. Alcuni dei tipi più comuni di reazioni con complessi carbonilici metallici includono la sostituzione del ligando CO, il redox al centro del metallo e l'attacco nucleofilo all'unità CO. Gli stessi complessi carbonilici metallici sono ampiamente utilizzati nella catalisi. Ad esempio, l'idroformilazione, la produzione industriale di aldeidi dagli alcheni, è catalizzato dal complesso carbonilico metallico HCo(CO)3 (Figura 6).

Figura 6. Idroformilazione da parte del complesso carbonilico metallico HCo(CO)3.
Subscription Required. Please recommend JoVE to your librarian.
References
- Fukumoto, K., Nakazawa, H. Geometrical isomerization of fac/mer-Mo(CO)3(phosphite)3 and cis/trans-Mo(CO)4(phosphite)2 catalyzed by Me3SiOSO2CF3. J Organomet Chem. 693(11), 1968-1974 (2008).
- Darensbourg, M. Y., Magdalena, P., Houliston, S. A., Kidwell, K. P., Spencer, D., Chojnacki, S. S., Reibenspies, J. H. Stereochemical nonrigidity in heterobimetallic complexes containing the bent metallocene-thiolate fragment. Inorg Chem. 31(8), 1487-1493 (1992).
- Darensbourg, M. Y., Darensbourg, D. J. Infrared Determination of Stereochemistry in Metal Complexes. J Chem Ed. 47(1), 33-35 (1970).




