Overview
출처: 퍼셰 티보1,2,3,뮤니에 실뱅1,2,3,소피 노볼트4,레이첼 골럽1,2,3
1 림프포포에이시스, 면역학학과, 파스퇴르 연구소, 파리, 프랑스
2 INSERM U1223, 파리, 프랑스
3 유니버시테 파리 디드로, 소르본 파리 시테, 셀룰레 파스퇴르, 파리, 프랑스
4 흐름 세포측정플리트에서, 세포측정및 바이오마커 UtechS, 번역 과학 센터, 파스퇴르 연구소, 파리, 프랑스
면역 계통의 전반적인 기능은 전염성 유기체 및 그밖 침략자로부터 바디를 방어하는 것입니다. 백혈구, 또는 백혈구는 면역 계통의 주요 한 선수입니다. 감염시, 그(것)들은 활성화되고 면역 반응을 시작합니다. 백혈구는 생물학적, 물리적 및/또는 기능적(예를 들어, 크기, 세분성 및 분비)이 될 수 있는 상이한 파라미터를 기반으로 다양한 하위 집단(예를 들어, 골수성 세포, 림프구, 수지상 세포)으로 나눌 수 있다. 백혈구를 특성화하는 한 가지 방법은 주로 수용체인 표면 단백질을 통해서입니다. 각 백혈구 인구는 인구 중 하위 집합을 정의할 수 있는 수용체(예를 들어, 세포독성, 활성화, 이주 수용체)의 특정 조합을 표현합니다. 면역 계통은 세포 인구의 넓은 범위를 포괄하기 때문에, 면역 반응에 있는 그들의 참여를 해독하기 위하여 그(것)들을 특성화하는 것이 필수적입니다.
유동 세포측정법(FC 또는 FCM)은 세포 표면 및 세포내 분자의 발현을 분석하여 이종성 세포 혼합물에서 상이한 세포 유형을 특성화하고 정의하는 데 널리 사용되는 방법입니다. 유동 세포계는 유체, 광학 및 전자 의 세 가지 주요 하위 시스템으로 구성됩니다. 유체 시스템은 레이저 앞에서 하나씩 통과할 수 있도록 스트림에서 세포를 수송합니다. 광학 시스템은 입자를 조명하는 광원(레이저), 생성된 빛을 지시하는 광학 필터, 적절한 검출기로 형광 신호로 구성됩니다. 마지막으로 전자 시스템은 감지된 광 신호를 컴퓨터에서 처리할 수 있는 전자 신호로 변환합니다. 개별 셀이 레이저 빔 앞에서 지나갈 때 빛이 흩어져 있습니다. 빔 앞의 검출기는 측면 분산(SC)을 측정하기 위해 전방 산란(FS) 및 여러 검출기를 측정합니다. FS는 세포 크기와 상관 관계가 있으며 SC는 세포의 세분성에 비례합니다. 이러한 방식으로, 세포 인구는 종종 혼자 그들의 크기와 세분성의 차이에 따라 구별 될 수 있습니다.
세포의 크기, 모양 및 복잡성을 분석하는 것 외에도, 유동 세포측정은 세포 표면 수용체(1)의 발현을 검출하는 데 널리 사용된다. 이것은 알려진 세포 특정 수용체에 결합하는 불소 크롬 표시 단클론 항체를 사용하여 달성됩니다. 이 결합된 불소크롬은 방출 파장이라고 불리는 특정 파장의 빛을 방출하여 검출및 득점할 수 있습니다. 형광 측정은 형광으로 표지된 세포 표면 수용체에 대한 정량적 및 정성적 데이터를 제공합니다. 혈액학자는 면역 세포 집단 (2)의 치료 후속을 위해 FC를 사용하기 위해 먼저 사용하였다. 지금, 면역 페노티핑, 세포 생존성, 유전자 발현, 세포 계수 및 GFP 분석과 같은 광범위한 응용 분야에 사용된다.
FACS (형광 활성 세포 선별기)는 형광 라벨링을 사용하여 세포의 인구를 하위 집단으로 분류하는 유동 세포 측정의 전문 유형입니다. 기존의 유동 세포측정과 마찬가지로 최초의 FS, SC 및 형광 데이터가 수집됩니다. 이어서, 기계는 전하(음수 또는 양성)를 적용하고 정전기 편향 시스템(전자석)은 세포를 포함하는 충전된 물방울의 수집을 적절한 튜브로 용이하게 한다.
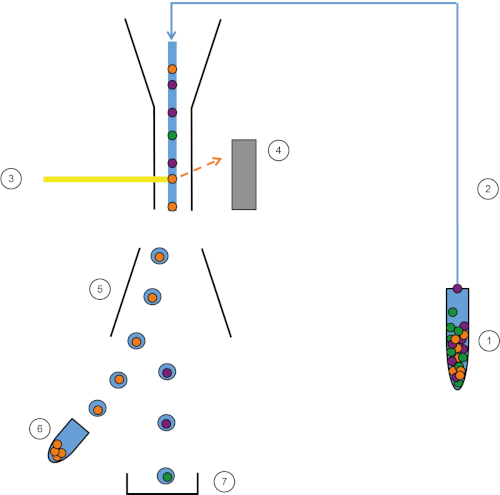
그림 1: FACS의 회로도 표현. 샘플(1)은 FACS(2)에서 흡인되어 레이저(3) 앞에 전달된다. 세포 형광은 형광 검출기 (4)에 의해 감지됩니다. 마지막으로, 세포는 액적에 통합되고 관심 있는 세포는 편향 플레이트(5)에 의해 편향되고 수집 관(6)에서 수집된다. 나머지 세포는 휴지통(7)으로 이동합니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
FACS의 정렬 측면은 많은 장점을 제공합니다. 많은 시험은 RT-qPCR, 세포 주기, 또는 사이토카인 분비와 같은 유전자 발현의 분석과 같은 면역 계통에 있는 특정 세포의 역할을 이해하는 것을 도울 수 있습니다. 그러나 세포는 명확하고 구체적인 결과를 얻으려면 상류에서 정제되어야 합니다. 여기서 FACS는 유용하게 제공되며 원하는 셀은 매우 안정적이고 재현 가능한 결과를 산출하여 매우 순도로 정렬 할 수 있습니다. FACS는 또한 핵 또는 그밖 세포내 염색에 근거하여 그리고 표면 수용체의 존재, 부재 및 밀도에 따라 세포를 분류하기 위하여 이용될 수 있습니다. FACS는 이제 세포의 하위 집단의 정화를 위한 표준 기술이고 동시에 4개의 인구까지 분류하는 능력을 가지고 있습니다.
이 실험실 운동은 비장 백혈구를 분리하는 방법과 FACS를 사용하여 비장 백혈구 세포 혼합물에서 B 림프구 세포를 구체적으로 분류하는 방법을 보여줍니다.
Procedure
1. 준비
- 시작하기 전에 실험실 장갑과 적절한 보호 복을 착용하십시오.
- 먼저 세제로 모든 해부 도구를 살균한 다음 70%의 에탄올로 완전히 건조시하십시오.
- 2% 태아 종아리 혈청(FCS)을 함유한 행크의 균형 잡힌 소금 용액(HBSS)의 50mL를 준비한다.
2. 해부
- 이산화탄소 전달 시스템을 사용하여 저산소증으로 마우스를 안락사시합니다. supine 위치에 있는 해부 판에 안락사 마우스를 고정하고 가위와 집게를 사용하여 세로 복강경을 수행합니다.
- 집게를 사용하여 복부 오른쪽에 내장과 위를 움직여 위와 비장을 노출시십시오. 비장은 위장에 부착됩니다.
- 집게를 사용하여 위에서 비장을 조심스럽게 분리하고 HBSS 2 % FCS의 5mL가 들어있는 페트리 접시에 놓습니다.
3. 면역 세포 격리
- 비장을 같은 페트리 접시 위에 40μm 세포 여과기에 놓습니다. 플런저로 비장을 분쇄하여 동일한 접시에 분리합니다.
- 해리된 비장과 유체를 15mL 원심분리기 튜브로 옮기.
- 10°C에서 7분 동안 370 x g의 튜브를 원심 분리하고 펠릿을 피하여 상체를 버립니다.
- 적혈구를 lyse 칼륨 아세테이트 의 2mL에 펠릿을 다시 중단. 2 분 기다린 다음 HBSS 2 % FCS를 사용하여 최대 15mL의 볼륨을 구성할 수 있습니다.
- 10°C에서 7분 동안 370 x g로 튜브를 다시 원심 분리합니다. 상체를 버리고 HBSS 2 % FCS의 5mL에서 펠릿을 다시 놓습니다.
- 트라이판 블루 염색 분석기를 사용하여 세포를 계산하고 HBSS 2% FCS의 적절한 부피를 사용하여 최종 세포 농도를 107 세포/mL로 조정합니다.
4. 셀 염색
- 세포 현탁액의 200μL을 6개의 FACS 튜브로 전송하여 1에서 6까지 표시합니다.
- 10°C에서 7분 동안 370 x g의 튜브를 원심 분리하고 펠릿을 피하는 상퍼를 폐기하십시오.
- 다음으로, 표 1에 따라 200μL HBSS 2% FCS에 적절한 양의 항체를 추가하여 6개의 새로운 항체 혼합물을 준비한다.
- 이어서, 이러한 항체 믹스를 해당 번호가 매겨진 FACS 튜브로 이송한다.
- 어둠 속에서 얼음에 20 분 동안 항체와 혼합 된 세포 현탁액을 배양합니다.
- 각 튜브에 HBSS 2% FCS 1mL을 추가한 다음 10°C에서 3분 동안 370 x g로 다시 원심분리기를 추가합니다.
- 슈퍼네티드를 버리고 200μL에 펠릿을 2% FCS로 상환한다.
- 재중단된 펠릿을 새로운 FACS 튜브로 전송합니다.

표 1: 항체 혼합 조성. HBSS + 항체의 200μL의 6개의 혼합이 실험을 위해 제조되었다. 믹스 1은 PMT 설정용이며, 혼합 2 ~5는 보상 설정이며, 혼합 6은 셀 정렬용이다.
5. FACS 교정
- 먼저, 선별기를 켜고"Fluidics 시작"을 수행합니다.
- 스트림을 켜고 스트림이 안정화될 때까지 15분 동안 기다립니다.
- 스트림의 진폭을 조정하여 분리된 낙하 형성을 얻습니다. 그런 다음"스위트 스팟"을클릭하여 진폭 조정을 완료합니다.
- 중립 밀도(N.D.) 필터를 넣고 - 1.0을 열고 세포계 설정 및 추적을 의미하는"CST"인터페이스를 엽니다.
- 일일 품질 관리를 수행하기 위해 먼저 제조업체의 지시에 따라 FACS 매체로 CST 구슬을 희석한 다음 CST 제어를 수행합니다.
- CST 제어가 완료되면 N.D. 1.0 필터를 사이토미터의 N.D. 2.0 필터로 바꿉다.
- 다음으로 제조업체의 지시에 따라 FACS 매체의 낙하 지연 구슬을 희석한 다음 FACS에 로드합니다.
- 적절한 정렬이 Drop Delay를수행하도록 하려면 -
- 먼저"전압"을클릭한 다음 "광학 필터"를 클릭합니다. 오른쪽 사분면은 100%와 같아야 합니다. 필요한 경우, 오른쪽 사분면에서 100 %를 얻기 위해 사이토미터 왼쪽 또는 오른쪽에 빨간색 레이저 나사를 조정합니다.
- 그런 다음 스트림이 수집 튜브에 속하는지 확인하기 위해 테스트 정렬을 수행합니다. 이렇게 하려면"폐기물 서랍"을클릭하고"테스트 정렬"을시작합니다. 측면 스트림이 수집 튜브에 속하는지 확인합니다. 그렇지 않으면 전압이 조정될 때까지 조정합니다.
- 실험 템플릿으로 이동합니다. 그런 다음"Accudrop 드롭 지연"실험을 열고"정렬 레이아웃"을 클릭합니다.
- 유량을 변경하여 초당 1000~3000개의 이벤트를 가져옵니다.
- "전압"을클릭한 다음"광학 필터"를 클릭합니다. 왼쪽 사분면은 0과 오른쪽 사분면과 100이어야 합니다.
- "정렬레이아웃"에서" 창을 클릭 "정렬" 다음"취소"를 클릭합니다. 왼쪽 사분면은 100이고 오른쪽 사분면은 0과 같아야 합니다. 왼쪽 사분면이 95미만이면 자동으로 조정하려면"자동 지연"을클릭합니다.
6. 유동 세포및 순도 제어
- 형광의 세포 형태와 음수 피크를 정의하는 튜브 1 (스테인드 셀)로 시작하여 흐름 세포 측정을 시작합니다. 전방 및 측면 분산을 설정하고 각 형광 파라미터의 전압을 정의합니다. 각 점 플롯에 그리드를 사용하여 처음 10년 동안 음수 집단을 배치합니다.
- 다음으로, 사이토미터내의 로드 튜브 2(단일 색상 제어). 음수 및 양수 모집단 중앙값이 정렬될 때까지 스펙트럼 중첩을 조정하거나 자동 계산 소프트웨어를 사용합니다. 신호를 스케일로 유지하는 것이 중요합니다. 보정 컨트롤은 실험용 불소 크롬 및 검출기 설정과 일치해야 합니다. 10,000개의 이벤트를 기록합니다.
- 튜브 3, 4 및 5(다른 단일 색상 컨트롤)로 이 단계를 반복합니다.
- 다음으로, 로드 튜브 6(다중 스테인드 셀)과 특정 게이팅 전략을 사용하여 관심 있는 세포 집단을 정의한다.
- 레이아웃 정렬 창에서 관심 있는 셀 모집단을 선택합니다. "대상이벤트"에서셀 임계값과"정밀도"의정밀도 수준을 선택합니다. 여기서 는 단 하나의 인구만 정렬되고 있지만, 네 개의 다른 인구는 동시에 정렬 할 수 있습니다.
- 일단 준비 클릭 "정렬" 및 "OK", 다음 셀 정렬을 기다립니다.
- 세포 정렬이 완료되면, 먼저 HBSS 2 % FCS의 90 마이크로 리터와 새로운 FACS 튜브에 정렬 된 세포의 10μL을 파이프하여 순도 제어를 수행합니다.
- 그런 다음, 튜브를 사이토미터로 로드합니다. 게이팅 전략이 의도한 대로 작동하는지 확인하기 위해 세포의 표현형을 기록하고 분석합니다.
7. 데이터 분석
- 'FlowJo' 소프트웨어를 열고 각 튜브의 파일을"모든 샘플"창에서 드래그합니다.
- 파일을 두 번 클릭하여 새 창에서 엽니다.
- "다각형"을클릭하고 이전에 사용한 게이팅 전략을 다시 만듭니다.
- 다른 모든 파일로 단계를 반복합니다.
- 점 플롯을 시각화하려면"레이아웃 편집기"를클릭하고 레이아웃 편집기 탭에서 튜브 6 및 순도 제어에서 관심 있는 개체수를 드래그합니다. 셀은 순도 제어에 대한 관심 의 집단에만 나타나야 합니다(그림 2참조).
- 정렬된 셀에서 B 림프구의 순도를 확인하려면"테이블 편집기"를 클릭합니다. 튜브 6에서 B 림프구 모집단을 드래그하고 테이블의 순도 제어.
- "통계"에서메뉴는 CD45+ 셀의 빈도를 선택하여 이 셀 채우기의 순도를 테스트한 다음"테이블 만들기"를 클릭합니다.
- 매개 변수 값이 새 테이블에 나타납니다. 순도 제어 창에서 CD45+ 세포 내에서 B 림프구의 빈도를 확인하여 98 % 이상이어야합니다 (그림 2, 하단 패널 참조).
면역 계통은 백혈구에게 불린 백혈구를 생성해서 병원체를 침략에서 바디를 보호합니다. 병원균이 유기체를 성공적으로 감염시킬 때, 백혈구의 다양한 활성화되고 이 조정된 반응은 면역 반응이라고 합니다.
빈번하게, 연구원이 병원균에 반응하여 활성화된 면역 세포의 특정 모형 그리고 수를 확인할 수 있는 것이 유용합니다. 유동 세포측정은 연구원이 표면에 표현된 특정 전형체에 근거하여 세포를 분리할 수 있는 기술입니다. 이는 알려진 면역 세포 특이적 에피토프에 결합하는 불소 크롬 태그 단일 클론 항체를 사용하여 달성되며, 이러한 결합된 불소크롬은 유동 세포계에 의해 검출되고 득점될 수 있는 빛의 파장을 방출한다.
유동 세포계는 세 가지 시스템으로 구성됩니다. 유체 시스템은 레이저 앞에서 하나씩 통과할 수 있도록 스트림에서 세포를 수송합니다. 광학 시스템은 형광의 존재 또는 부재를 인식하는 레이저및 검출기로 구성됩니다. 마지막으로 전자 시스템은 수집된 광학 데이터를 분석을 위해 전자 파일로 변환합니다.
유동 세포측정의 연장은 형광 활성화 세포 선별기, 또는 FACS로, 특정 세포 집단의 농축을 허용하여 독립적으로 연구할 수 있습니다. 세포 정렬은 마이크로 방울을 형성하는 유체 스트림 내에서 진동 노즐을 사용하여 수행되며, 각각 단일 셀을 함유하고 있습니다. 그런 다음 검출기는 각 액적에서 형광이 방출되는지 여부를 결정하고, 그 정보에 기초하여, 전자석은 각 세포에게 음전또는 양전하를 준다. 다음으로, 강한 전기장은 다른 충전된 액적을 별도의 용기에 정렬합니다. 궁극적으로, 용기 중 하나는 특정 세포 표면 분자의 발현에 기초하여 세포의 균질한 집단을 포함할 것이다.
이 비디오에서는 마우스 비장 조직및 FACS에서 백혈구를 분리하여 B 림프구를 선택하는 유동 세포법을 사용하는 방법을 배웁니다.
시작하려면 실험실 장갑과 적절한 보호 복을 착용하십시오. 다음으로, 해부가위와 집게를 세제로 먼저 씻은 다음 70%에탄올로 씻은 다음 깨끗한 종이 타월로 말리십시오.
그런 다음 행크의 균형 잡힌 소금 용액(HBSS)의 49밀리리터를 50밀리리터 튜브에 추가합니다. 태아 송아지 세럼 또는 FCS의 밀리리터 1밀리리터를 추가하여 HBSS 2% FCS 솔루션을 만들고 약 10회 위아래로 부드럽게 파이펫팅하여 혼합합니다.
다음으로, 해부 판에 안락사 된 마우스를 supine 위치에 놓습니다. 가위와 집게를 사용하여 복강에 접근하기 위해 세로 복강경 절제술을 수행합니다. 집게를 사용하여 복부의 오른쪽에 있는 내장을 한쪽으로 이동하여 위와 비장을 노출시합니다. 비장은 위장에 부착됩니다. 그런 다음 파이펫을 사용하면 HBSS 2% FCS의 5밀리리터를 페트리 접시에 넣습니다. 집게를 사용하여 비장을 위장에서 조심스럽게 분리하고 비장을 페트리 접시에 넣습니다.
면역 세포를 격리하려면 먼저 페트리 접시에 40 미크론 세포 여과기에 비장을 놓습니다. 비장을 플런저로 분쇄하여 접시에 담급됩니다. 그런 다음 페트리 접시에서 분리된 비장과 액체를 15밀리리터 원심분리기 튜브로 피펫합니다. 10도에서 7분 동안 370배 g의 원심분리한 다음 펠릿을 방해하지 않도록 튜브를 조심스럽게 회수합니다.
이제 상체를 제거하고 펠릿을 피하고 적절한 폐기물 용기에 액체를 폐기하십시오. 그런 다음 원심분리기 튜브에 ACK 용해 버퍼 2밀리리터를 추가하여 적혈구를 다시 일시 중단하고 용인합니다. 2분 간 기다린 다음 HBSS 2% FCS를 추가하여 총 15밀리리터를 얻습니다. 원심분리를 반복합니다. 튜브를 조심스럽게 검색하고 상체를 폐기하십시오. HBSS 2% FCS의 5밀리리터에서 펠릿을 다시 중단합니다.
다시 중단 된 세포를 계산하려면 Trypan Blue의 5 마이크로 리터로 셀 서스펜션의 5 마이크로 리터를 희석하십시오. 그런 다음 커버글래스와 말라세즈 슬라이드 사이에 이 희석된 셀 서스펜션의 5개의 마이크로리터 드롭을 부드럽게 증정합니다. 지금, 40X 배율에서 현미경의 밑에, 존재하는 세포의 수를 계산합니다. 이어서, HBSS 2% FCS의 적절한 부피를 추가하여 밀리리터당 7번째 세포로 세포 농도를 10으로 조절한다.
면역 세포를 얼룩지게하려면 6 개의 FACS 튜브를 1에서 6 개의 FACS 튜브로 표시하여 시작합니다. 그런 다음, 세포 용액의 200 마이크로리터를 각각 6개의 튜브로 옮킨다. 원심 분리는 섭씨 10도에서 7 분 동안 370 배 g에서 이 튜브를 제거하고 상체를 제거합니다.
그런 다음 6개의 새로운 FACS 튜브를 1~6개의 튜브로, HBSS 2% FCS의 파이펫 200 마이크로리터를 각각 라벨로 지정합니다. 표 1에 따라 각 튜브에 적절한 양의 항체를 추가하여 6개의 새로운 항체 혼합물을 준비한다. 혼합 하나는 항체를 첨가하지 않은 미염색 된 세포를 위한 것입니다. 2~5개를 혼합하여 보상 설정을 위한 상이한 단일 항체를 함유하고 있습니다. 혼합 6은 선별에 사용되는 다중 스테인드 세포에 대한 네 개의 항체를 모두 포함합니다.
다음으로, 이러한 항체 믹스를 해당 번호가 매겨진 FACS 튜브로 이송한다. 이 솔루션을 섭씨 4도또는 어둠 속에서 얼음에 20분 동안 배양하십시오. 다음으로 각 튜브에 HBSS 2% FCS의 밀리리터 1밀리리터를 추가한 다음 원심분리기를 다시 추가합니다. 상체를 폐기한 다음 200 마이크로리터의 HBSS 2% FCS에서 펠릿을 다시 중단합니다. 마지막으로, 재중단된 펠릿을 새로운 레이블이 붙은 FACS 튜브로 옮기.
FACS를 수행하려면 먼저 선별기를 켭니다. 그런 다음 사이토미터 메뉴를 선택하고 유체 설정을 클릭합니다. 화면의 지침을 따르십시오.
스트림 탭에서 적십자를 클릭하여 스트림을 켜고 스트림이 안정화될 때까지 15분 간 기다립니다. 스트림 탭에 명확한 분리 된 드롭이 나타날 때까지 스트림의 진폭을 조정합니다. 그런 다음 달콤한 지점을 클릭하여 진폭 조정을 완료합니다. 레이저 앞에 중립 밀도 또는 ND를 삽입합니다.
화면 상단의 사이토미터 메뉴를 열고 사이토미터 설정 및 추적을 의미하는 CST를 선택합니다. 일일 품질 관리를 수행하기 위해 먼저 제조업체의 지침에 따라 FACS 튜브에 FACS 배지로 CST 구슬을 희석합니다. 그런 다음 튜브를 컴퓨터에 로드하고 CST 탭에서 실행을 클릭하여 CST 제어를 수행합니다.
CST 제어가 완료되면 ND 1.0 필터를 사이토미터의 ND 2.0 필터로 바꿉다. 다음으로 제조업체의 지시에 따라 FACS 매체의 낙하 지연 구슬을 희석한 다음 튜브를 FACS에 로드합니다. 적절한 정렬을 보장하려면 먼저 전압을 클릭한 다음 광학 필터를 클릭하여 드롭 지연을 수행합니다. 광학 필터의 오른쪽 사분면은 100%와 같아야 하며, 이는 낙하물의 100%가 기계에 의해 등록되었음을 나타냅니다. 필요한 경우, 오른쪽 사분면에서 100 %를 얻기 위해 사이토미터 왼쪽 또는 오른쪽에 빨간색 레이저 나사를 조정합니다. 스트림이 수집 튜브에 속하는지 확인하는 것이 중요합니다. 이렇게 하려면 폐기물 서랍을 클릭한 다음 정렬을 테스트하여 테스트 정렬을 수행합니다. 측면 스트림이 수집 튜브에 속하는지 확인합니다. 그렇지 않으면 정렬 탭 에서 전압을 조정할 때까지 조정합니다.
브라우저 탭을 선택하고 공유 보기를 클릭하여 실험 템플릿으로 이동합니다. 그런 다음 Accudrop_DROP DELAY 실험을 열고 정렬 레이아웃 단추를 클릭합니다. 이제 초당 3,000개의 이벤트에 도달할 때까지 유량을 조작하여 획득 대시보드의 임계값 속도를 변경합니다. 전압을 클릭한 다음 광학 필터를 클릭합니다. 왼쪽 사분면은 0과 같어야 하며 오른쪽 사분면은 100과 같아야 합니다.
마지막으로 정렬 레이아웃 창에서 정렬을 클릭한 다음 취소를 클릭합니다. 왼쪽 사분면은 100과 같어야 하며 오른쪽 사분면은 0과 같아야 합니다. 왼쪽 사분면이 95 미만이면 자동 지연을 클릭하여 소프트웨어에 전압을 자동으로 늘려 왼쪽 사분면의 100% 낙하를 얻도록 지시합니다.
흐름 세포 측정을 시작하려면 먼저 염색되지 않은 세포를 사용하여 세포 형태와 불소 크롬의 음수 피크를 정의할 것입니다. 이렇게 하려면 컴퓨터에 스테인드되지 않은 셀이 포함된 튜브 하나를 및 획득 대시보드 탭 클릭 로드 아래에 배치합니다. 사이토미터 탭에서 세포 집단을 화면에 점의 밀도 가중 농도로 볼 때까지 전방 및 측면 산란 전압을 조정합니다. 림프구는 작은 세포, 그래서 그들은 낮은 앞으로 분산 하 고 낮은 측면 산란을 해야합니다.
다음으로, 세포계 탭의 형광에 대한 전압을 조절하여 전 세계 워크시트 탭의 첫 10년 동안 세포 집단이 음수 수준일 때까지 배경 형광을 제거합니다. 사이토미터 메뉴에서 뷰 구성을 클릭하고 모든 불소 크롬이 있는지 확인합니다. 다음으로, 튜브를 사이토미터에 배치하고 부하를 클릭합니다. 음성 및 긍정 집단 중앙값이 전역 워크시트 탭에 정렬될 때까지 사이토미터 탭의 스펙트럼 중첩을 조정합니다. 획득 탭에서 이벤트를 설정하여 매개 변수를 10,000으로 기록하고 레코드를 클릭합니다. 튜브 3, 4, 5로 이 단계를 반복합니다.
다음으로, 다중 스테인드 셀을 포함하는 로드 튜브 6. B 림프구를 분리하려면 먼저 매개 변수를 설정하여 형태에 따라 세포를 정렬합니다. 첫 번째 창에서 x 축의 y축 및 SSC-A 측면 분산 영역에 FSC-A 전방 분산 영역을 플롯합니다. 분산 플롯에서 각 점은 셀을 나타냅니다. 전역 워크시트의 다각형 게이트를 클릭한 다음 앞으로 분산이 낮고 중간 면 분산이 있는 모집단을 선택합니다. 새 점 플롯 창에서 창을 마우스 오른쪽 단추로 클릭하고 메뉴에서 개체를 표시하고 P1을 클릭합니다.
그런 다음 새 창에서 x 축에서 y축 및 CD45에서 생존 가능성을 플로팅하여 실행 가능한 CD45 양수 셀을 게이트합니다. 다각형 게이트를 사용하여 생존 가능성이 낮고 CD45 신호가 높은 셀을 동그라미로 만들고 P2를 선택하여 선택한 셀을 새 창에 표시합니다. 다음 창에서 T 림프구를 제외한 CD45 양성 백혈구의 게이트. x축에 CD45와 y축의 CD3를 사용하면 높은 CD45 신호와 낮은 음수 CD3 신호로 인구를 동그라미로 동그라미를 치고 P3를 선택합니다. 마지막으로, B 림프구를 식별하는 CD19 양성 세포에 대한 게이트. x축의 y축 및 CD3에 CD19를 사용하면 높은 CD19 신호와 낮은 음수 CD3 신호로 인구를 동그라미로 동그라미를 치고 P4를 선택합니다.
이제 모든 정렬 매개 변수가 설정됩니다. 다음으로 정렬 레이아웃 창에서 게이트된 네 번째 인구인 관심-P4의 셀 모집단을 선택하고 기기에 B 림프구만 정렬하도록 지시합니다. 대상 이벤트를 10,000셀로 설정하고 정밀도를 순도로 설정합니다. 우리는 단지 하나의 인구를 분류하고 있습니다. 그러나 최대 4개의 다른 인구를 동시에 정렬할 수 있습니다. 준비가 되면 정렬 및 확인을 클릭합니다. 그런 다음 셀 정렬을 기다립니다.
세포 정렬이 완료되면 분류된 세포의 10마이크로리터를 HBSS 2% FCS의 90마이크로리터가 있는 새로운 FACS 튜브로 파이프하여 순도 제어를 수행합니다. 세포계에 튜브를 놓고 부하를 클릭한 다음 기록을 클릭하여 세포의 표현형을 분석하여 게이팅 전략이 의도한 대로 작동하는지 확인합니다.
이제 정렬된 세포를 분석하여 마우스 비장으로부터 분리된 백혈구 중 B 림프구의 백분율을 결정할 것입니다. 시작하려면 FlowJo 아이콘을 두 번 클릭하고 각 튜브의 파일을 모든 샘플 창으로 드래그합니다.
다각형을 클릭하고 이전 섹션에서 사용했던 게이팅 전략을 다시 만듭니다. 다음으로 레이아웃 편집기를 클릭하고 튜브 6에서 관심 있는 B 림프구 모집단과 순도 제어를 레이아웃 편집기 탭으로 드래그합니다. B 림프구를 나타내는 점 플롯이 나타납니다. 이 예에서, 오른쪽 상단의 플롯은 총 비장 세포 현탁액으로부터 정렬된 B 림프구를 나타내고 오른쪽 하단의 플롯은 순도 제어이다. 셀은 순도 제어에 관심있는 집단에만 나타나야 합니다.
정렬된 셀에서 B 림프구의 순도를 확인하려면 테이블 편집기를 클릭합니다. B 림프구 모집단을 튜브 6에서 드래그하고 테이블의 순도 제어를 끕다. 통계 메뉴에서 CD45 양성 세포의 주파수를 선택하여 이 세포 집단의 순도를 테스트합니다. 그런 다음 테이블 만들기를 클릭합니다. 매개 변수 값이 새 테이블에 나타납니다. 순도 제어 창에서, CD45 양성 세포 내의 B 림프구의 주파수를 확인, 이는 보다 높은해야 98%.
Subscription Required. Please recommend JoVE to your librarian.
Results
이 프로토콜에서, 우리는 FACS 기술을 사용하여 비장 B 림프구를 정제. 우리는 먼저 비장에서 백혈구를 분리하고 얼룩지게했습니다. B 셀 표면 마커의 조합을 사용하여 이를 정렬하는 게이팅 전략을 만들었습니다(그림 2, 상단 패널). 실험의 끝에서 우리는 수집 관내의 세포가 "순도 테스트"를 통해 B 세포인지 확인했습니다. 우리는 동일한 게이팅 전략을 유지하고 세포의 98 % 이상이 실제로 B 세포 (그림 2, 하단 패널)인 것을 관찰했습니다. 따라서, FACS는 순도의 높은 수준으로 면역 세포 인구를 격리하는 효과적인 프로토콜이다. 수집된 세포는 그 때 세포 배양, RT-qPCR 및 세포 독성 검사와 같은 다운스트림 실험에 사용될 수 있습니다.

그림 2: 게이팅 전략 및 테스트 포스트 정렬 순도. (A) 세포는 그들의 형태에 기초하여 먼저 게이트되었다 (왼쪽 : FSC-A, SSC-A), 다음 만 살아 (중간 왼쪽 : 생존력, CD45), CD45+ 셀 (CD45, CD3) CD19 및 CD3에 대해 플롯되었다. CD19+ 셀만 정렬되었습니다. (b) 세포 분류 후 얻은 세포의 분수의 순도 테스트 결과. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
유동 세포측정은 면역 세포 집단을 높은 순도로 특성화하고 분류하는 직접적인 기술입니다. 그것은 특정 세포 인구의 농축을 허용 하고 병원체에 면역 반응을 해독하는 것을 허용하기 때문에 연구 필드에 있는 원시 공구입니다. 사용 가능한 형광크롬 및 세포계의 수가 증가함에 따라 검출 가능한 매개 변수의 수가 크게 증가합니다. 그 결과, FACS 데이터의 생물학적 분석이 나타나기 시작했고 세포측정(3)을 흐르기 위한 새로운 지평을 열었습니다. 유동 세포측정은 진단 공구 개발에 사용되는 혈액학 및 종양학(4)에 있는 그밖 응용을 제공합니다.
Subscription Required. Please recommend JoVE to your librarian.
References
- Lanier, L. L. Just the FACS. The Journal of Immunology, 193 (5), 2043-2044 (2014).
- Walker, J. M. Epiblast Stem Cells IN Series Editor.
- Tung, J. W., Heydari, K., Tirouvanziam, R., Sahaf, B., Parks. D. R., Herzenberg, L. A., and Herzenberg. L. A. Modern Flow Cytometry: A Practical Approach. Clinics in Laboratory Medicine. 27 (3), 453-468 (2007).
- Walker, J. M. Tumor Angiogenesis Assays IN Series Editor.




