Overview
Quelle: Tilde Andersson1, Rolf Lood1
1 Institut für Klinische Wissenschaften Lund, Abteilung für Infektionsmedizin, Biomedical Center, Universität Lund, 221 00 Lund, Schweden
Die mikrobielle Biodiversität scheint unmöglich zu bestimmen, und die mikrobielle Artenvielfalt ist mit schätzungsweise einer Billion koexistierender Arten (1,2) wirklich erstaunlich. Obwohl besonders raue Klimazonen, wie die saure Umgebung des menschlichen Magens (3) oder die subglazialen Seen der Antarktis (4), von einer bestimmten Art dominiert werden können, sind Bakterien typischerweise in Mischkulturen zu finden. Da jede Sorte das Wachstum einer anderen (5) beeinflussen kann, ist die Fähigkeit, "reine" (nur aus einem Typ bestehende) Kolonien zu trennen und zu kultivieren, sowohl im klinischen als auch im akademischen Umfeld unerlässlich geworden. Reine Kulturen ermöglichen weitere genetische (6) und proteomische Untersuchungen (7), die Analyse der Probenreinheit und, vielleicht bemerkenswerter, die Identifizierung und Charakterisierung von Infektionserregern aus klinischen Proben.
Bakterien haben eine breite Palette von Wachstumsanforderungen und es gibt zahlreiche Arten von Nährstoffmedien, die entwickelt wurden, um sowohl die unanspruchsvollen als auch die anspruchsvollen Arten zu erhalten (8). Wachstumsmedien können entweder in flüssiger Form (als Brühe) oder in einer typisch engarbasierten (einem gelierenden Mittel aus Rotalgen) feste Form hergestellt werden. Während die direkte Impfung in die Brühe das Risiko birgt, eine genetisch vielfältige oder sogar gemischte Bakterienpopulation zu erzeugen, schafft die Beschichtung und Neuung eine reinere Kultur, in der jede Zelle ein sehr ähnliches genetisches Make-up hat. Die Streifenplattentechnik basiert auf der progressiven Verdünnung einer Probe (Abbildung 1), mit dem Ziel, einzelne Zellen voneinander zu trennen. Jede lebensfähige Zelle (im Folgenden als koloniebildende Einheit, KBE bezeichnet), die von den Medien und der bezeichneten Umgebung getragen wird, kann anschließend eine isolierte Kolonie von Tochterzellen durch binäre Spaltung finden. Trotz der schnellen Mutationsraten innerhalb bakterieller Gemeinschaften wird diese Zellgruppe allgemein als klonal betrachtet. Die Ernte und Erneute Verwesung dieser Population stellt somit sicher, dass die nachfolgende Arbeit nur einen einzigen bakteriellen Typ umfasst.
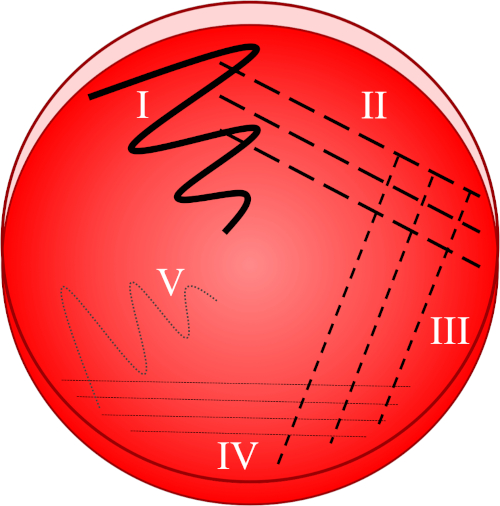
Abbildung 1: Eine Streifenplatte basiert auf der progressiven Verdünnung der Originalprobe. I) Das Inokulum wird zunächst mit einer Zick-Zack-Bewegung verteilt, wodurch ein Gebiet mit einer relativ dichten Bakterienpopulation entsteht. II-IV) Streifen werden aus dem vorhergehenden Bereich gezogen, wobei jedes Mal eine sterile Impfschleife verwendet wird, bis der vierte Quadrant erreicht ist. V) Eine letzte Zick-Zack-Bewegung, die auf die Mitte der Platte gerichtet ist, bildet einen Bereich, in dem das Inokulum deutlich verdünnt wurde, so dass Kolonien getrennt voneinander erscheinen können.
Die Streifenplattentechnik kann auch mit dem Einsatz selektiver und/oder differentialer Medien kombiniert werden. Ein selektives Medium hemmt das Wachstum bestimmter Organismen(z. B. durch Zugabe von Antibiotika), während ein Differenzmedium nur dazu beiträgt, sich voneinander zu unterscheiden(z. B. durch Hämolyse auf Blutagarplatten).
Allen Arbeiten in der Mikrobiologie liegt der Einsatz aseptischer (steriler) Techniken zugrunde. Jede Bakterienkultur sollte als potenziell pathogen betrachtet werden, da die Gefahr eines unbeabsichtigten Wachstums tückischer Stämme, Aerosolbildung und Kontamination von Geräten/Personal besteht. Um diese Risiken zu minimieren, werden alle Medien-, Kunststoff-, Metall- und Glaswaren in der Regel durch Autoklavieren vor und nach dem Gebrauch sterilisiert und mit hochdruckgesättigtem Dampf bei etwa 121°C belastet, der alle verweilenden Zellen effektiv auslöscht. Der Arbeitsbereich wird in der Regel mit Ethanol sowohl vor als auch nach der Verwendung desinfiziert. Labormantel und Handschuhe werden immer bei der Arbeit mit Infektionserregern getragen.
Procedure
1. Einrichten
- Alle Mikroben sollten so behandelt werden, als wären sie gefährlich. Tragen Sie immer einen Labormantel und Handschuhe, binden Sie lange Haare zurück und sorgen Sie dafür, dass alle Wunden besonders gut geschützt sind.
- Bereiten Sie den Arbeitsbereich bereit, indem Sie ihn mit 70% Ethanol sterilisieren.
- Stellen Sie sicher, dass Agarplatten, Probenlösung(en) und entweder eine Schachtel mit vorsterilisierten Kunststoff-Impfschlaufen oder eine Metallschlaufe plus eine Bunsenflamme in der Nähe sind. Einweg-Kunststoffschlaufen sind in der Regel vorsterilisiert. Metallschlaufen sollten in 70% Ethanol getaucht und dann in der Nähe des blauen Bereichs einer Bunsenflamme gehalten und erhitzt werden, bis es heiß ist. Lassen Sie den Draht abkühlen, indem Sie den Deckel der Platte anheben (nur leicht, um eine Kontamination zu verhindern) und ihn gegen das erstarrte Medium anzapfen.
- Beenden Sie jedes Verfahren mit einer wiederholten Sterilisation des Arbeitsbereichs und einer gründlichen Waschen/Sterilisation von Händen und Handgelenken.
2. Protokoll
- Vorbereitung von Medien
- Identifizieren und vorbereiten Sie ein festes Medium (in der Regel 1,5% (w/v) Agar), das die genutzte Bakterienart/-sorte aufrechterhält. Mischen Sie das Medium in einer Flasche in der Lage, das Doppelte der endgültigen Lautstärke zu halten, um Überlauf beim Autoklavieren zu vermeiden.
- Sterilisieren Sie die Medien, indem Sie die Flasche mit einer halbangezogenen Kappe in einem Autoklaven auf 121°C für 20 min setzen.
- Schließen Sie die Kappe richtig, sobald die Flasche aus dem Autoklaven entfernt wird. Wenn das Medium in Kürze verwendet werden soll, legen Sie die Flasche in ein Wasserbad, das auf 45°C eingestellt ist, um sie in einem flüssigen Zustand zu erhalten. Der Agar erstarrt sonst bei weniger als 32-40°C und kann später (typischerweise mit einer Mikrowelle) zu einem Schmelzpunkt bei 85°C wieder erhitzt werden.
- Zubereitung von Kulturplatten
- Markieren Sie die Basis steriler Petrischalen (in der Regel 100 x 15 mm) auf der Seite oder am Boden mit dem Namen des Experimentators, dem Datum und dem Medientyp.
- 20-25 ml 45°C Agarkulturmedium (zuvor zubereitet) in jede der beschrifteten Platten gießen. Sollte Schaum an den Rändern auftreten, sollte dieser mit einer normalen Pipette und einer sterilen Spitze schnell entfernt werden.
- Legen Sie sofort alle Deckel wieder auf das Geschirr, um eine Kontamination zu verhindern.
- Lassen Sie den Agar ca. 2 h bei Raumtemperatur oder über Nacht bei 4°C erstarren. Einmal gesetzt, sollten Bakterienkulturplatten anschließend kopfüber bei 4°C gelagert werden, um die Kondensation auf der mittleren Oberfläche zu minimieren.
- Streak-Beschichtung
- Eine sterile Schleife in das gewünschte Inokulum untertauchen und die gesammelte Probe sofort mit einer Zick-Zack-Bewegung auf den ersten Quadranten der Platte verteilen (Abbildung 1, I).
- Schließen Sie den Deckel und sterilisieren Sie die Impfschleife neu oder sammeln Sie eine neue sterile Einwegschleife.
- Machen Sie 3-4 Striche, die vom ersten Quadranten (der eine relativ dichte Bakterienpopulation enthält) in Richtung des zweiten Quadranten der Platte ausstrahlen(Abbildung 1, II).
- Schließen Sie den Deckel und sterilisieren Sie die Impfschleife neu oder entsorgen Sie die Einwegschleife und sammeln Sie eine neue sterile Schleife.
- Wiederholen Sie diese Streifzüge von 3-4 Schlägen vom zweiten in den dritten Quadranten und dann vom dritten zum vierten Quadranten, wobei sie jedes Mal eine sterile Schleife verwenden(Abbildung 1, III - IV).
- Mit einer sterilen Schleife, machen Sie einen letzten Schlag in einem Zick-Zack-Muster vom vierten Quadranten in Richtung der Mitte der Platte (Abbildung 1, V). Die bakterielle Prävalenz wird in diesem Bereich geringer sein, was idealerweise die Einrichtung einzelner Kolonien aus einer einzigen, lebensfähigen Mutterzelle ermöglicht.
- Schließen Sie den Deckel und (falls von der Bakterienart benötigt) Versiegelung mit Parafilm, um Luftstrom zu verhindern.
- Je nach Bakterienart/Stamm die Kulturplatte nach oben in eine geeignete Umgebung stellen und brüten, bis Bakterienkolonien sichtbar sind (getrennte Kolonien können in beiden Bereichen der Platte erscheinen, da die Anfangskonzentration variieren kann).
- Um eine klonale Bakterienpopulation zu erzeugen, streichen Sie eine weitere Platte aus und tauschen Sie das auf die ursprüngliche Platte plattierte Inokulum gegen Zellen aus einer einzigen Kolonie der ursprünglichen Platte.
Auf einer Petrischale, wenn ein einzelnes Bakterium mehrere Runden der asexuellen Fortpflanzung durchläuft, wird es zur Bildung einer Klonkolonie führen. Es kann jedoch schwierig sein, ein einzelnes Bakterium aus einer gemischten Probe, wie z. B. einer Bodensuspension, zu erhalten. Wenn man eine Schleife dieser heterogenen Kultur nimmt, kann sie bis zu einer Billion einzelne Bakterien enthalten. Um diese vielen Bakterien auf die Oberfläche einer Agarplatte zu verteilen und eine einzige Kolonie zu erhalten, selbst mit einem Zick-Zack-Muster, müsste die Schleife kontinuierlich über die Oberfläche von genügend Platten gezogen werden, die nebeneinander gesetzt werden, um die gesamte Liberty Island einzukreisen. Offensichtlich verwenden Wissenschaftler nicht wirklich so viele Platten. Stattdessen verwenden sie eine Technik namens Streak Plating.
Die Streifenplattentechnik basiert auf der progressiven Verdünnung einer bakteriellen Probe und wird über die Volumenmedienoberfläche einer einzelnen Petrischale durchgeführt. Zunächst wird die Medienoberfläche visuell in fünf Abschnitte unterteilt, indem vier Fragmente des Umfangs als die ersten vier Abschnitte und die Mitte der Platte als der fünfte zugewiesen werden. Dadurch werden effektiv fünf Medienplatten aus einer einzigen Petrischale erstellt. Als nächstes wird der erste Abschnitt mit einem Zick-Zack-Muster mit einer Schleife des gewünschten Inokulums gestreift. Dann wird entweder eine neue Einwegschleife verwendet, oder im Falle einer Drahtschlaufe wird sie mit einem Bunsenbrenner sterilisiert, der sie bis zu ihrer roten Hitze entlang der Länge des Drahtes flammt. Diese Verwendung einer neuen Schleife, oder Flammsterilisation Schleife, entfernt alle verbleibenden Bakterienzellen, hilft bei der Verdünnung der Bakterien. Die Hot Loop wird dann für einige Sekunden in der Luft gekühlt, bevor sie durch den ersten Abschnitt gezogen wird, um drei bis vier separate Linien zu erstellen, die jeweils nur einen Bruchteil der Bakterien in den zweiten Abschnitt tragen. Die übrigen Abschnitte werden auf die gleiche Weise gestreift, wobei jedes Mal eine sterile Schleife und ein einzelner Durchgang durch den vorherigen Streifen verwendet wird.
Mit diesem Zyklus des Streichens und Sterilisierens sollte die bakterienkonzentration in jedem nachfolgenden Abschnitt verdünnt werden, so dass der letzte Abschnitt nur wenige diskret lokalisierte Bakterien enthält. Bei der Inkubation vermehren sich diese diskreten Bakterien, um isolierte Klonkolonien von Tochterzellen zu produzieren, die als Koloniebildnereinheiten oder KBE bezeichnet werden. Diese können geerntet und neu gestreift werden, um sicherzustellen, dass die nachfolgende Arbeit nur einen einzigen Bakterientyp umfasst, der als reine Kultur bezeichnet wird. Neben der Isolierung einzelner Kolonien aus einer gemischt-bakteriellen Kultur wird die Streifenbeschichtungstechnik auch verwendet, um medienspezifische Stämme auszuwählen, die bakterielle Koloniemorphologie zu bestimmen oder verschiedene Bakterienarten zu identifizieren. In diesem Video zeigen wir, wie man einzelne bakterielle Kolonien von einer gemischt-bakteriellen Probensuspension mittels Streifenbeschichtungstechnik isoliert.
Zunächst einmal Laborhandschuhe und einen Labormantel anziehen. Als nächstes sterilisieren Sie den Arbeitsbereich mit 70% Ethanol. Als nächstes wählen Sie ein geeignetes Medium, das die genutzten Bakterienarten oder Stämme aufrechterhält, und beginnen Sie mit der Vorbereitung der Medien. Hier wird der gewöhnliche LB-Agar hergestellt, indem zehn Gramm vorformulierte, pulverisierte Medien und 7,5 Gramm Agar gewogen werden. Fügen Sie die gewogenen, getrockneten Komponenten in eine Glasflasche, die in der Lage ist, das Doppelte des endigen Volumens zu halten, um überlaufen zu vermeiden. Dann 500 Milliliter Wasser in die Flasche geben und halbfest verschließen. Sterilisieren Sie die Medien, indem Sie die Flasche in einem Autoklaven auf 121 Grad Celsius für zwanzig Minuten. Verwenden Sie nach Abschluss hitzebeständige Handschuhe oder ein Hotpad, um das Medium aus der Maschine zu entfernen, und drehen Sie dann sofort den Flaschenverschluss, um ihn fest zu schließen.
Lassen Sie die Medien für den gleichen Tag abkühlen, indem Sie die Flasche in ein auf ca. 45 Grad Celsius erhitztes Wasserbad legen, um die Medien in einem flüssigen Zustand zu erhalten. Alternativ können die Medien bei Raumtemperatur gelassen werden, um sie bei festem Zustand zu speichern. Bei Bedarf Mikrowelle die Flasche mit dem Deckel leicht geöffnet, um die Medien zu schmelzen, und lassen Sie die Medien mit einem 45 Grad Celsius Wasserbad abkühlen.
Als nächstes nehmen Sie eine Hülse mit sterilen Petri-Gerichten und mit einem permanenten Marker, kennzeichnen Sie sie mit dem Ermittler und Mediennamen sowie dem Datum. Übertragen Sie dann das benötigte Medienvolumen in ein steriles Gefäß und fügen Sie bei Bedarf Antibiotika oder andere empfindliche Komponenten hinzu. Hier werden 50 Milliliter Medien mit 100 Mikroliter Kanamycin für eine Endkonzentration von 25 Mikrogramm pro Milliliter gemischt. Wirbeln Sie das Rohr, um eine gleichmäßige Verteilung der hinzugefügten Komponenten über die Medien zu gewährleisten. Langsam, um Blasenbildung zu vermeiden, gießen Sie 20 bis 25 Milliliter von etwa 45 Grad Celsius Kulturmedium in jede der Platten. Wenn Blasen oder Schaum auftreten, schnell mit einer normalen Pipette und einer sterilen Spitze entfernen. Dann sofort alle Deckel austauschen, um eine Kontamination zu verhindern. Lassen Sie den Agar bei Raumtemperatur für mindestens zwei Stunden oder über Nacht erstarren. Nach der Erstarrung die Kulturplatten bei vier Grad Celsius auf den Kopf stellen, um die Kondensation auf der Oberfläche des Mediums zu minimieren.
Um die Kultur der Wahl zu streifen, nehmen Sie zuerst eine saubere Kulturplatte und entfernen Sie den Deckel. Schnell arbeiten, eine Einweg-, sterile Schleife in das gewünschte Inokulum tauchen und dann sofort die Schleife mit einer Zick-Zack-Bewegung über den ersten Quadranten der Platte wischen. Ersetzen Sie den Deckel der Schale, entsorgen Sie die verwendete Impfschleife, und wählen Sie dann eine neue sterile Schleife aus. Mit der neuen Schleife, machen drei bis vier Striche, die die ursprüngliche Tupferlinie aus dem ersten Quadranten, die eine relativ dichte Bakterienpopulation in den zweiten Quadranten enthalten sollte. Schließen Sie den Deckel noch einmal, und entsorgen Sie die Schleife. Mit einer neuen Schleife wiederholen Sie diese Aktion erneut, aber dieses Mal streifen von der zweiten in den dritten Quadranten. Dann, mit einer neuen Schleife wieder, machen sie einen weiteren Streifen vom dritten in den vierten Teil der Platte. Schließlich, mit einer frischen Schleife, machen Sie einen letzten Schlag in einem Zick-Zack-Muster vom vierten Quadranten in Richtung der Mitte der Platte. Die bakterielle Prävalenz wird in diesem Bereich geringer sein, idealerweise können einzelne Kolonien aus einer einzigen lebensfähigen Mutterzelle gebildet werden.
Ersetzen Sie den Plattendeckel, und, falls für die Bakterienarten geeignet, versiegeln Sie die Platte mit Parafolie, um Luftstrom zu verhindern. Drehen Sie die Kulturplatte auf den Kopf, um Kondensationstropfen zu verhindern, und platzieren Sie sie dann bei einer geeigneten Temperatur für das Wachstum. Hier wird ein Inkubator auf 37 Grad Celsius eingestellt. Lassen Sie die Platte brüten, bis Bakterienkolonien sichtbar sind. Um eine klonale Bakterienpopulation zu erzeugen, wählen Sie eine diskrete Kolonie aus dieser Platte aus. Berühren Sie nun mit der sterilen Schleife die Zielkolonie und machen Sie wie bisher einen Streifen im ersten Quadranten einer neuen Platte. Weiterhin die Schleife abwechselnd sterilisieren und die verbleibenden Quadranten der Platte, wie zuvor gezeigt, streifen, endend mit dem Zick-Zack zur Mitte. Schließen Sie die Platte, und legen Sie sie zu brüten, bis sich diskrete Kolonien bilden. Sobald diese Kolonien angebaut sind, stellen sie in der Regel reine klonale Stämme dar.
Die anfängliche Streifenplatte kann Kolonien enthalten, die aus Zellen verschiedener Bakterienarten oder Zellen mit unterschiedlicher genetischer Zusammensetzung stammen, abhängig von der Probenreinheit. Durch die nachfolgende Isolierung einer einzelnen Kolonie, bei der alle Einheiten aus einer gemeinsamen Mutterzelle abgeleitet sind, erzeugt das zweite Streifenverfahren eine relativ klonale Bakterienpopulation, die für eine weitere Charakterisierung oder Impfung in Brühe geeignet ist.
Subscription Required. Please recommend JoVE to your librarian.
Results
Die anfängliche Streifenplatte kann Kolonien enthalten, die aus Zellen mit unterschiedlicher genetischer Zusammensetzung oder (je nach Probenreinheit) von verschiedenen Bakterienarten stammen (Abbildung 2A).
Durch die nachfolgende Isolierung einer einzelnen Kolonie, bei der alle Einheiten aus einer gemeinsamen Mutterzelle abgeleitet sind, erzeugt das zweite Streifenverfahren eine relativ klonale Bakterienpopulation, die für eine weitere Charakterisierung oder Impfung in Brühe geeignet ist ( Abbildung 2B).

Abbildung 2: Eine reine Kultur kann aus einer gemischten Probe durch Isolierung einer einzelnen, abgeschiedenen Kolonie erzeugt werden. A) Das Wachstum einer einzelnen Bakterienzelle (KBE) erzeugte eine Klonkolonie, die von denen anderer Arten und Stämme getrennt war. Diese KBE wurde für das anschließende Streichen auf eine neue Platte B) Eine zweite Platte verwendet, bei der die Bakterienpopulation ausschließlich aus Zellen besteht, die aus der ursprünglichen CFU abgeleitet wurden.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
Die Fähigkeit, eine reine Bakterienkolonie zu erhalten und zu kultivieren, ist sowohl im klinischen als auch im akademischen Umfeld unerlässlich. Die Streak-Beschichtung ermöglicht die Isolierung einer relativ klonalen Zellpopulation, die aus einer gemeinsamen KBE stammt und während der Diagnose oder für eine zusätzliche Charakterisierung des Isolats von besonderem Interesse sein kann. Eine Probe wird auf ein geeignetes Nährmedium auf Agarbasis gestreift und inkubiert, bis Kolonien sichtbar werden. Eine isolierte Kolonie wird anschließend geerntet und auf eine zweite Platte zurückgestreift.
Subscription Required. Please recommend JoVE to your librarian.
References
- The Human Microbiome Project C. Structure, Function and Diversity of the Healthy Human Microbiome. Nature. 486:207-214. (2012)
- Locey KJ, Lennon JT. Scaling laws predict global microbial diversity. Proceedings of the National Academy of Sciences. 113 (21) 5970-5975 (2016)
- Skouloubris S, Thiberge JM, Labigne A, De Reuse H. The Helicobacter pylori UreI protein is not involved in urease activity but is essential for bacterial survival in vivo. Infection and Immunity. 66:4517-21. (1998)
- Mikucki JA, Auken E, Tulaczyk S, Virginia RA, Schamper C, Sørensen KI, Doran PT, Dugan H, Foley N. Deep groundwater and potential subsurface habitats beneath an Antarctic dry valley. Nature Communications. 6:6831. (2015)
- Mullineaux-Sanders C, Suez J, Elinav E, Frankel G. Sieving through gut models of colonization resistance. Nature Microbiology. 3:132-140. (2018)
- Fournier PE, Drancourt M, Raoult D. Bacterial genome sequencing and its use in infectious diseases. Lancet Infectious Diseases. 7:711-23 (2007)
- Yao Z, Li W, Lin Y, Wu Q, Yu F, Lin W, Lin X. Proteomic Analysis Reveals That Metabolic Flows Affect the Susceptibility of Aeromonas hydrophila to Antibiotics. Scientific Reports. 6:39413 (2016)
- Medina D, Walke JB, Gajewski Z, Becker MH, Swartwout MC, Belden LK. Culture Media and Individual Hosts Affect the Recovery of Culturable Bacterial Diversity from Amphibian Skin. Frontiers in Microbiology. 8:1574 (2017)




