9.4:
Energía de Enlace Nuclear
9.4:
Energía de Enlace Nuclear
La diferencia entre las masas calculadas y las medidas experimentalmente se conoce como el defecto de masa del átomo. En el caso del helio-4, el defecto de masa indica una “pérdida” en masa de 4,0331 uma – 4,0026 uma = 0,0305 uma. La pérdida de masa que acompaña a la formación de un átomo a partir de protones, neutrones y electrones se debe a la conversión de esa masa en energía que se produce a medida que se forma el átomo. La energía de enlace nuclear es la energía producida cuando los nucleones de los átomos están unidos; esta es también la energía necesaria para dividir un núcleo en sus protones y neutrones constituyentes. Los cambios energéticos asociados con las reacciones nucleares son mucho mayores que los de las reacciones químicas.
La conversión entre la masa y la energía se representa más identificablemente por la ecuación de equivalencia masa-energía, como lo indica Albert Einstein: E = mc2, donde E es energía, m es la masa de la materia que se está convirtiendo, y c es la velocidad de la luz en un vacío. Utilizando esta ecuación de equivalencia masa-energía, la energía de enlace nuclear de un determinado átomo puede calcularse a partir de su defecto de masa. Una variedad de unidades se utilizan comúnmente para las energías de enlace nuclear, incluyendo electronvoltios (eV), con 1 eV igual a la cantidad de energía necesaria para mover la carga de un electrón a través de una diferencia de potencial eléctrico de 1 voltio: 1,602 × 10−19 J.
Para calcular la energía de enlace a partir del defecto de masa, en primer lugar, exprese el defecto de masa en g/mol. Esto se hace fácilmente considerando la equivalencia numérica entre la masa atómica (uma) y la masa molar (g/mol) que resulta de las definiciones de las unidades de uma y mol. El defecto de masa para He-4 es, por lo tanto, de 0,0305 g/mol. Para acomodar las unidades de los otros términos en la ecuación masa-energía, la masa debe expresarse en kilogramos, ya que 1 J = 1 kg m2/s2. La conversión de gramos en kilogramos produce un defecto de masa de 3,05 × 10−5 kg/mol. Al sustituir esta cantidad en la ecuación de equivalencia masa-energía se obtiene:
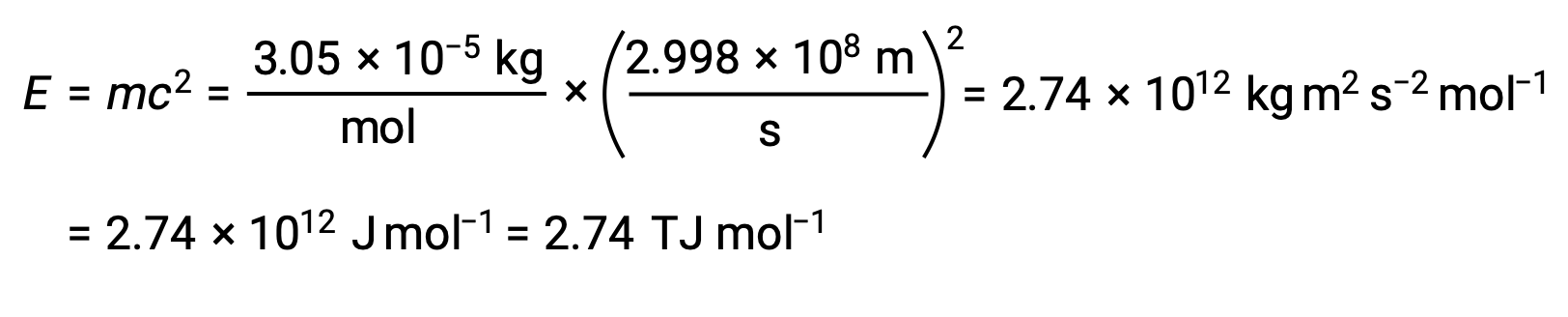
La energía de enlace para un solo núcleo se calcula a partir de la energía de enlace molar utilizando el número de Avogadro:
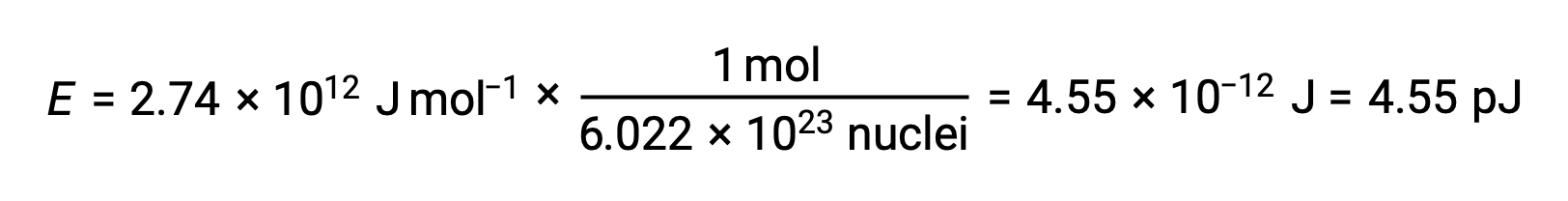
Recuerde que 1 eV = 1,602 × 10−19 J. utilizando la energía de enlace calculada:
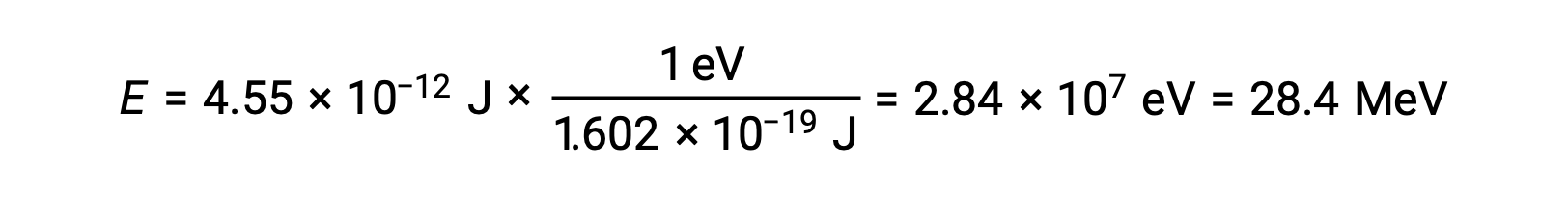
La estabilidad relativa de un núcleo está correlacionada con su energía de enlace por nucleón, la energía de enlace total del núcleo dividida por el número de nucleones presentes en ese núcleo. Por ejemplo, la energía de enlace para un núcleo de helio-4 es de 28,4 MeV. Por lo tanto, la energía de enlace por nucleón para un núcleo de helio-4 es:
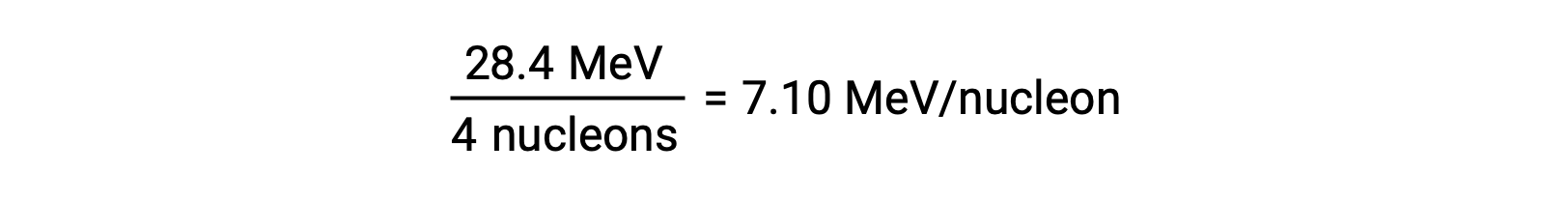
La energía de enlace por nucleón es mayor para los nucleidos con un número de masa de aproximadamente 56.
Este texto ha sido adaptado de Openstax, Química 2e, Sección 21.1: Estructura Nuclear y Estabilidad.
