19.4: طاقة الربط النووية
يُعرف الفرق بين الكتل المحسوبة والمقاسة تجريبياً باسم خلل الكتلة للذرة. في حالة الهيليوم-4، يشير الخلل الكتلي إلى “خسارة” في الكتلة تبلغ 4.0331 amu – 4.0026 amu = 0.0305 amu. يرجع فقدان الكتلة المصاحب لتكوين ذرة من البروتونات والنيوترونات والإلكترونات إلى تحويل تلك الكتلة إلى طاقة تتطور مع تشكل الذرة. تنتج الطاقة عندما ترتبط الذرات’ ببعضها البعض؛ هذه أيضًا هي الطاقة اللازمة لتكسير النواة إلى البروتونات والنيوترونات المكونة لها. تكون تغيرات الطاقة المرتبطة بالتفاعلات النووية أكبر بكثير من تلك الخاصة بالتفاعلات الكيميائية.
يمكن تحديد التحويل بين الكتلة والطاقة من خلال معادلة مكافئ الطاقة والكتلة– كما ذكر ألبرت أينشتاين: E = mc2، حيث أن E هي الطاقة، و m هي كتلة المادة التي يتم تحويلها، و c هي سرعة الضوء في الفراغ. باستخدام معادلة مكافئ الكتلة– الطاقة، يمكن حساب طاقة الارتباط النووية للنواة من خلل الكتلة. تُستخدم مجموعة متنوعة من الوحدات بشكل شائع لطاقات الربط النووي، بما في ذلك فولتات الإلكترون (eV) ، مع 1 eV يساوي كمية الطاقة اللازمة لتحريك شحنة الإلكترون عبر فرق الجهد الكهربائي 1 فولت: 1.602 × 10–19 J.
لحساب طاقة الارتباط من خلل الكتلة، عبر أولاً عن خلل الكتلة بوحدة جم/مول. يمكن القيام بذلك بسهولة مع الوضع في الاعتبار التكافؤ العددي للكتلة الذرية (amu) والكتلة المولية (غ/مول) الناتجة عن تعريف وحدات amu و مول. وبالتالي فإن خلل الكتلة لـ He-4 هو 0.0305 غ/مول. لاستيعاب وحدات المصطلحات الأخرى في معادلة الكتلة–؛ الطاقة، يجب التعبير عن الكتلة بالكيلوغرام، نظراً لأن 1 جول = 1 كغ m2/s2. ينتج عن تحويل الغرامات إلى كيلوغرامات خلل كتلة يبلغ 3.05 × 10–5 كغ/مول. ينتج عن استبدال هذه الكمية في معادلة مكافئ الطاقة–الكتلة:
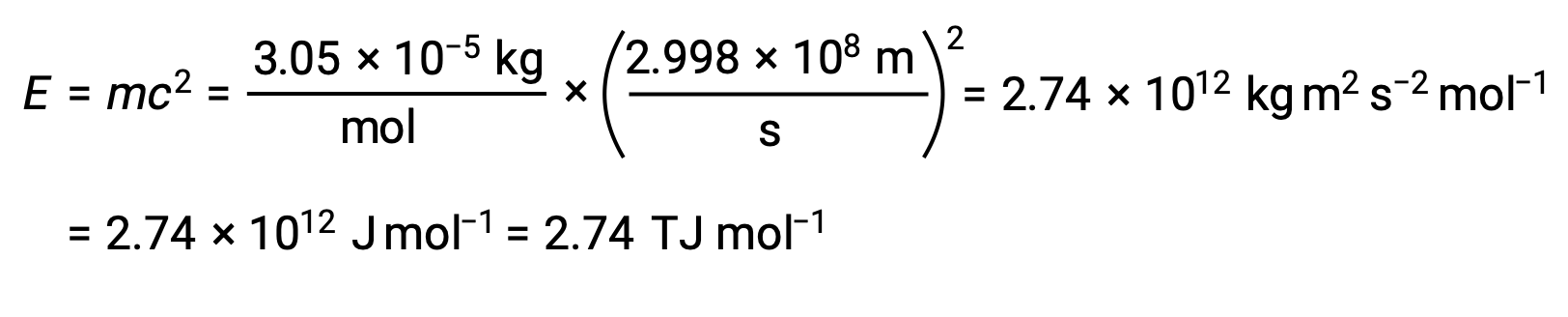
يتم حساب طاقة الربط لنواة واحدة من طاقة الربط المولية باستخدام رقم أفوجادرو’:
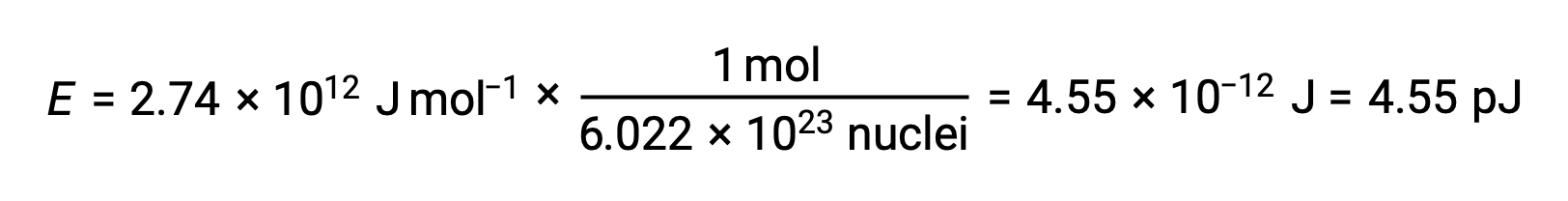
تذكر أن 1 eV = 1.602 × 10–19 جول. استخدام طاقة الربط المحسوبة:
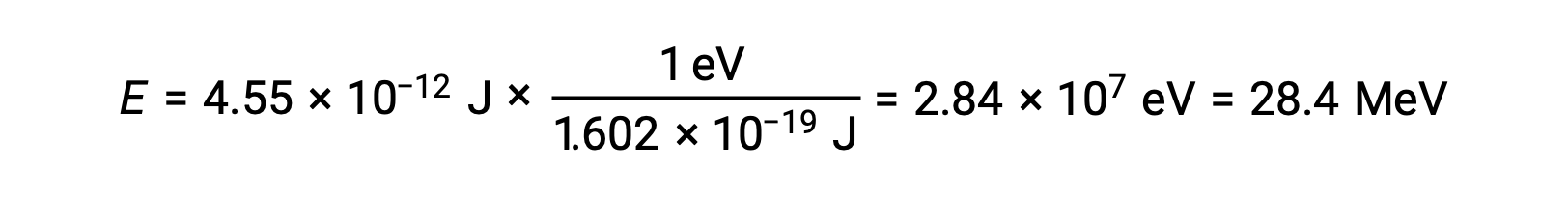
يرتبط الاستقرار النسبي للنواة بطاقتها الرابطة لكل نواة، وهي طاقة الربط الكلية للنواة مقسومة على عدد النوى في النواة. على سبيل المثال، طاقة الربط لنواة الهليوم-4 هي 28.4 ميغا إلكترون فولت. لذلك فإن طاقة الربط لكل نيوكليون لنواة الهليوم -4 هي:
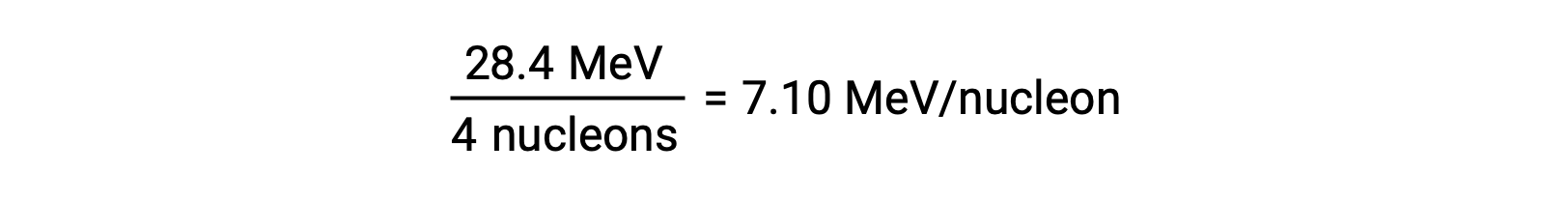
طاقة الربط لكل نيوكليون هي الأكبر بالنسبة للنوى التي يبلغ عدد كتلتها 56 تقريباً.
هذا النص مقتبس من Openstax, Chemistry 2e, Section 21.1: Nuclear Structure and Stability.


