Overview
מקור: המעבדה של ד"ר אנדריאס זוטל - מעבדות פדרליות שוויצריות למדע וטכנולוגיה של חומרים
חוק הגז האידיאלי מתאר את התנהגותם של רוב הגזים הנפוצים בתנאים כמעט סביבתיים ואת הנטייה של כל החומר הכימי במגבלת הדלילה. זהו קשר בסיסי בין שלושה משתני מערכת מקרוסקופיים מדידים (לחץ, טמפרטורה ונפח) לבין מספר מולקולות הגז במערכת, ולכן הוא קשר חיוני בין היקומים המיקרוסקופיים לבין היקומים המקרוסקופיים.
ההיסטוריה של חוק הגז האידיאלי מתוארכת לאמצע המאה ה-17 כאשר הקשר בין הלחץ לנפח האוויר נמצא פרופורציונלי הפוך, ביטוי שאושר על ידי רוברט בויל ואשר אנו מכנים כיום חוק בויל(משוואה 1).
P 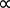 V-1 (משוואה 1)
V-1 (משוואה 1)
עבודות שלא פורסמו על ידי ז'אק צ'ארלס בשנות השמונים, שהורחבו לגזים ואדים רבים על ידי ג'וזף לואי גיי-לוסק ודווחו בשנת 1802, ביססו את הקשר היחסי הישיר בין הטמפרטורה המוחלטת לנפח הגז. מערכת יחסים זו נקראת חוק צ'ארלס(משוואה 2).
V 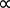 T (משוואה 2)
T (משוואה 2)
גיום אמונטון זוכה בדרך כלל לגלות לראשונה את הקשר בין הטמפרטורה והלחץ של האוויר בתוך נפח קבוע בתחילת המאה ה -18. חוק זה הורחב גם לגזים רבים אחרים על ידי ג'וזף לואי גיי-לוסק בתחילתהמאה ה -19 ולכן הוא מכונה גם חוק אמונטון או חוק הומו-Lussac, כאמור במשוואה 3.
P 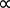 T (משוואה 3)
T (משוואה 3)
יחד, ניתן לשלב את שלושת קשרי הגומלין האלה כדי לתת את הקשר במשוואה 4.
V 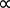 T (משוואה 4)
T (משוואה 4)
לבסוף, בשנת 1811, הוצע על ידי אמדאו אבוגאדרו כי כל שני גזים, המוחזקים באותו נפח ובאותה טמפרטורה ולחץ, מכילים את אותו מספר של מולקולות. זה הוביל למסקנה כי כל הגזים עשויים להיות מתוארים על ידי קבוע משותף, קבוע גז אידיאלי R, שאינו תלוי באופי הגז. זה ידוע בשם חוק הגז האידיאלי(משוואה 5). 1,2
PV 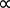 T (משוואה 5)
T (משוואה 5)
Principles
חוק הגז האידיאלי, ולכן R הקבוע האופייני לו, יכול גם להיות נגזר ברהיטות מתורת העקרונות הראשונים בדרכים רבות, שבהן ההנחות המפשטות החשובות הן שלמולקולות אין נפח אינהרנטי ואינן מתקשרות. הנחות אלה תקפות במגבלת החומר לדלל, כאשר נפח החלל הריק שנכבש על ידי כל מולקולה (למשל ~ 10-23 L בתנאי סביבה) גדול בהרבה מהמולקולה עצמה (~ 10-26 ליטר), והיכן אינטראקציות אינן סבירות. לכן ניתן להדגים אותו בקלות במספר דרכים באמצעות ציוד מעבדה משותף בטמפרטורת החדר, וניתן למדוד אותו במדויק באמצעות מגוון גזים בלחצים עד אפילו 10 בר(איור 1). עם זאת, חוק הגז האידיאלי אינו יכול להסביר במדויק את המאפיינים של גזים צפופים יותר בתנאים כמעט סביבתיים (למשל,פרופאן) או עבור עיבוי, תופעות המתעוררות כתוצאה מאינטראקציות בין-מולקולריות. מסיבה זו, משוואות מפורטות יותר של המדינה הצליחו את חוק הגז האידיאלי בשנים שחלפו מאז גילויו, ובדרך כלל הצטמצמו לחוק הגז האידיאלי במגבלת החומרים המדוללים. 1,2

איור 1. השוואה של צפיפות חוק הגז האידיאלית לגזים נפוצים שונים אחרים ב 25 °C (70 °F) ובין 0-100 בר.
במדריך זה, נמדוד בזהירות את הצפיפות של גז מימן בלחצים וטמפרטורות מוגברים בתוך נפח קבוע על ידי שקילה של מדגם מוצק מושעה של נפח ידוע: בלוק אלומיניום במכונה בדיוק. השינוי במשקל המדגם קשור ישירות לשינוי בצפיפות הנוזלים, שבו הוא צף, על ידי העיקרון של ארכימדס. אנו גם להדגים את החסרונות של שימוש בגז פחות אידיאלי (כגון פחמן דו חמצני) בלחצים גבוהים. לבסוף, אנו מדגימים חזותית ולאשר באופן איכותי את חוק הגז האידיאלי על ידי ביצוע ניסוי benchtop פשוט שבו השינוי בנפח של המערכת עקב שחרור מימן על ידי חומר אחסון מימן נמדד. באמצעות כל אחד מהניסויים הללו, אנו יכולים לקבוע את הקבוע האוניברסלי המתאר את הקשר בין לחץ, טמפרטורה ונפח עבור כמות נתונה של גז – קבוע הגז האידיאלי, R.
Subscription Required. Please recommend JoVE to your librarian.
Procedure
1. מדידת נפח המדגם
- נקו את הדגימה בקפידה וייבשו אותה.
- מלאו גליל מדורג ברזולוציה גבוהה עם מספיק מים מזוקקים כדי לכסות את הדגימה. שים לב לאמצעי האחסון ההתחלתי
- זרוק את הדגימה לתוך המים ושים לב לשינוי עוצמת הקול. זה הנפח של המדגם, וי.
- מוציאים את הדגימה ומייבשים אותה. הערה: לחלופין, מדד את אורך הצד של המדגם וחשב את עוצמת הקול שלה באמצעות גיאומטריה.
2. טען את המדגם באיזון
- לתלות את המדגם במאזן המתלים המגנטיים.
- התקן את תא הלחץ / הטמפרטורה סביב המדגם.
- לפנות את סביבת המדגם ולמלא בגז מימן, ל 1 בר.
- מדוד את משקל המדגם ב 1 בר וטמפרטורת החדר, w00.
3. מדוד משקל מדגם כפונקציה של לחץ בטמפרטורת החדר
- הגדל או הקטן את הלחץ בסביבת המדגם ל- Pi0.
- אפשר לסביבת המדגם להתפרק.
- למדוד את המשקל של המדגם, wi0.
- חזור על הפעולה 3.1-3.3 פעמים רבות.
4. למדוד משקל מדגם כפונקציה של לחץ בטמפרטורות שונות
- הגדר את הטמפרטורה ל- Tj ואפשר לה להתפרק.
- הגדר את הלחץ של גז מימן ל 1 בר.
- מדוד את משקל המדגם בבר אחד ו- Tj, w0j.
- להגביר או להקטין את הלחץ Pij ולאפשר לו שיווי משקל.
- למדוד את המשקל של המדגם, wij.
- חזור על הפעולה 4.4-4.5 פעמים רבות.
- חזור על 4.1-4.6 לפי הרצות.
5. חשב את קבוע הגז האידיאלי
- טאב את הערכים הנמדדים {Tj, Pij, ו-ij} שבו P0j הוא תמיד 1 בר ו- T0 הוא טמפרטורת החדר הנמדדת.
- חשב וכתוב טאבים את ההבדלים Δwij ו ΔPij בכל טמפרטורה Tj באמצעות משוואה 6 ומשוואה 7.
Δwij = wij - w0j (Equation 6)
Δwij = Pij - P0j = Pij - 1 bar (משוואה 7) - חשב Rij עבור כל מדידה, וממוצע על פני כל הערכים כדי לקבוע את קבוע הגז האידיאלי, R. לחלופין, להתוות את המוצר של ΔPij ו- V כפונקציה של המוצר של Δwij (מחולק על ידי המשקל המולקולרי, MW) ו- Tj, ולבצע ניתוח רגרסיה ליניארית כדי לקבוע את השיפוע, R. (משוואות 8 ו 9) עבור מימן, MW = 2.016 גרם/ מול.
ΔP V = Δn RT (משוואה 8) (משוואה 9)
(משוואה 9)
חוק הגז האידיאלי הוא מערכת יחסים בסיסית ושימושית במדע כפי שהוא מתאר את ההתנהגות של רוב הגזים הנפוצים בתנאים כמעט סביבתיים.
חוק הגז האידיאלי, PV =nRT, מגדיר את הקשר בין מספר מולקולות הגז במערכת סגורה לבין שלושה משתני מערכת מדידים: לחץ, טמפרטורה ונפח.
חוק הגז האידיאלי מסתמך על מספר הנחות. ראשית, שהנפח של מולקולות הגז קטן באופן זניח. שנית, שהמולקולות מתנהגות כספירות נוקשות המצייתות לחוקי התנועה של ניוטון. ולבסוף, כי אין כוחות אטרקטיביים בין מולקולות. הם מתקשרים אחד עם השני רק באמצעות התנגשויות אלסטיות, כך שאין אובדן נטו באנרגיה קינטית. גזים חורגים מהתנהגות אידיאלית זו בלחצים גבוהים, שבהם צפיפות הגז עולה, והנפח האמיתי של מולקולות הגז הופך להיות חשוב. באופן דומה, גזים לסטות בטמפרטורות נמוכות מאוד, שבו אינטראקציות בין מולקולרי אטרקטיבי להיות חשוב. גזים כבדים יותר עלולים לסטות אפילו בטמפרטורת הסביבה ובלחץ בשל הצפיפות הגבוהה יותר שלהם ואינטראקציות בין-מולקולריות חזקות יותר.
וידאו זה יאשר באופן ניסיוני את חוק הגז האידיאלי על ידי מדידת השינוי בצפיפות הגז כפונקציה של טמפרטורה ולחץ.
חוק הגז האידיאלי נגזר מארבע מערכות יחסים חשובות. ראשית, חוק בויל מתאר את היחסים היחסיים ההפוכים בין הלחץ והנפח של גז. לאחר מכן, החוק של גיי-לוסק קובע כי הטמפרטורה והלחץ הם פרופורציונליים. באופן דומה, חוק צ'ארלס הוא הצהרה על המידתיות בין טמפרטורה לנפח. שלוש מערכות יחסים אלה מהוות את חוק הגז המשולב, המאפשר השוואה של גז יחיד על פני תנאים רבים ושונים.
לבסוף, אבוגאדרו קבע כי כל שני גזים, המוחזקים באותו נפח, טמפרטורה ולחץ, מכילים את אותו מספר של מולקולות. מכיוון שגזים באותו מצב מתנהגים בדרך כלל באופן זהה, ניתן למצוא קבוע של מידתיות, הנקרא קבוע הגז האוניברסלי (R), המקשר בין פרמטרים אלה, ומאפשר השוואה של גזים שונים. ל-R יש יחידות אנרגיה לטמפרטורה למולקולה; לדוגמה, ג'אול לכל קלווין לכל חפרפרת.
חוק הגז האידיאלי הוא כלי רב ערך בהבנת יחסי המדינה במערכות גזיות. לדוגמה, במערכת של טמפרטורה ולחץ קבועים, תוספת של מולקולות גז נוספות גורמת לנפח מוגבר.
באופן דומה, בטמפרטורה קבועה במערכת סגורה, שבה לא מוסיפים או מפחיתים מולקולות, הלחץ של גז גדל כאשר הנפח יורד.
מאזן השעיה מגנטי יכול לשמש כדי לאשר את חוק הגז האידיאלי באופן ניסיוני על ידי מדידת התכונות הפיזיות של מערכת. המשקל של מדגם מוצק של מסה ונפח קבועים יכול לשמש בדיקה של המאפיינים של הגז סביבו.
ככל שהלחץ גובר במערכת, בנפח המערכת והטמפרטורה הקבועים, כמות מולקולות הגז במערכת עולה, ובכך מגדילה את צפיפות הגז. המדגם המוצק הנוקשה השקוע בגז זה נתון לציפה, ומשקלו לכאורה יורד למרות שמסתו אינה משתנה. את השינוי בצפיפות הגז ניתן לקבוע בשל עקרון ארכימדס, הקובע כי השינוי במשקל האובייקט שווה לשינוי במשקל הגז שנעקר.
ההתנהגויות המדויקות של צפיפות הגז בתנאי לחץ וטמפרטורה שונים יתאימו לחוק הגז האידיאלי אם הקירובים שתוארו בעבר נכונים, ויאפשרו חישוב פשוט של קבוע הגז האוניברסלי, R.
בסדרת הניסויים הבאה, מיקרו-איזון ישמש לאישור חוק הגז האידיאלי ולקביעת קבוע הגז האוניברסלי, R, על ידי מדידת צפיפות המימן כפונקציה של טמפרטורה ולחץ. ראשית, לנקות בזהירות את המדגם, במקרה זה בלוק אלומיניום במכונה דק, עם אצטון, ויבש. למדוד את נפח המדגם על ידי מילוי גליל מדורג עם מספיק מים מזוקקים כדי לכסות את המדגם. שים לב לאמצעי האחסון ההתחלתי. טבול את הדגימה במים ושים לב לשינוי עוצמת הקול.
מוציאים ומנקים ומייבשים בזהירות את הדגימה. לאחר מכן, לטעון אותו לתוך מאזן המתלים המגנטי, במקרה זה ממוקם בתוך תא כפפות. התקן את תא טמפרטורת הלחץ סביב המדגם. המדגם מושעה כעת באופן מגנטי במערכת סגורה, לא נוגע באף אחד מהקירות.
לפנות את סביבת המדגם ולמלא בגז מימן, ללחץ של 1 בר.
מודדים את משקל המדגם ומתייגים אותו כמשקל ההתחלתי בטמפרטורת החדר. לאחר מכן, להגביר את הלחץ בסביבת המדגם ל 2 בר, ולאפשר לו שיווי משקל. מדוד את המשקל בלחץ החדש. חזור על שלבים אלה מספר פעמים במספר לחצים, כדי לרכוש סדרה של משקולות מדגם בלחצים המתאימים, הכל בטמפרטורת החדר.
לאחר מכן, למדוד משקל כפונקציה של לחץ בטמפרטורה גבוהה יותר. ראשית לפנות את סביבת המדגם, ולאחר מכן להגדיל את הטמפרטורה ל 150 °C (50 °F) ולאפשר לו להתפרק. לאחר מכן, להגביר את הלחץ לבר אחד. מדוד את משקל המדגם, ולתייג אותו כמשקל הראשוני ב 150 °C (70 °F) ו 1 סרגל. להגביר את הלחץ, לאפשר לו להשתוות, ולמדוד את המשקל. חזור על שלבים אלה על מנת למדוד סדרה של משקולות מדגם בטווח של לחצים. כדי לקבל נתונים נוספים, חזור על סדרת מדידות המשקל בטמפרטורות ולחצים קבועים אחרים.
כדי לחשב את קבוע הגז האידיאלי, טבל את הערכים הנמדדים של משקל המדגם בכל טמפרטורה ולחץ.
לאחר מכן, לחשב את ההבדלים בין כל זוגות של משקולות מדגם בתוך סט טמפרטורה אחת כדי לקבל את כל השילובים האפשריים של השינוי במשקל כפונקציה של שינוי בלחץ, או Δw. שינוי זה שקול לשינוי במשקלו של גז המימן שנעקר על ידי המדגם.
באופן דומה, לחשב את כל ההבדלים המתאימים בלחץ כדי להשיג שינוי בלחץ, או ΔP. טבל את כל זוגות השינויים במשקל ובלחץ עבור כל טמפרטורה. להמיר את יחידות הטמפרטורה לקלווין ואת יחידות הלחץ לפסקלים.
מאז נפח וטמפרטורה להישאר קבוע עבור כל סדרה של מדידות, חוק הגז האידיאלי יכול להיות כתוב כמו ΔPV = ΔnRT. מאז Δn שווה Δw חלקי המשקל המולקולרי של מימן, לחשב כל ערך של Δn עבור כל ערך של Δw.
התווה את המוצר של שינוי לחץ ונפח מדגם, כפונקציה של המוצר של Δn וטמפרטורה. בצע ניתוח רגרסיה ליניארית כדי לקבוע את השיפוע, אשר יהיה שווה את קבוע הגז האוניברסלי אם נעשה כראוי.
משוואת הגז האידיאלית משמשת בתרחישים רבים בעולם האמיתי, בדרך כלל אלה המבוצעים עם גזים בטמפרטורת הסביבה ובלחץ. כל הגזים לסטות מהתנהגות אידיאלית בלחץ גבוה; עם זאת, חלק מהגזים, כגון פחמן דו חמצני, חורגים יותר מאחרים. בניסוי זה נמדדו סטיות מהתנהגות אידיאלית לגז דו תחמוצת הפחמן. ההליך היה זהה לניסוי הקודם שנערך עם מימן.
חלקה של לחץ כפול נפח לעומת מולים כפול הטמפרטורה הייתה שרטטה, וקבוע הגז האידיאלי מחושב מהמדרון של העלילה. פחמן דו חמצני סטה באופן משמעותי מהתנהגות אידיאלית, אפילו בתנאי סביבה. התנהגות זו נגרמה על ידי אינטראקציות בין-מולקולריות אטרקטיביות, אשר לא נצפתה עם מימן.
חוק הגז האידיאלי משמש לזיהוי וכימות של גזי נפץ בדגימות אוויר. תחום מחקר זה הוא בעל חשיבות רבה לצבא ולביטחון.
כאן, רכיבי נפץ של דגימת גז היו כימות באמצעות כרומטוגרפיה גז desorption טמפרטורה. הנתונים, כמו גם חוק הגז האידיאלי שימשו אז לכימות חומרים מסוכנים אלה.
הרגע צפית בהקדמה של ג'וב לחוק הגז האידיאלי. לאחר צפייה בסרטון זה, עליך להבין את מושג החוק, ומצבים שבהם המשוואה ישימה.
תודה שצפיתם!
Subscription Required. Please recommend JoVE to your librarian.
Results
חוק הגז האידיאלי הוא תיאור תקף של תכונות הגז בפועל של גזים נפוצים רבים בתנאים הקרובים להסביבה(איור 1 inset) ולכן הוא שימושי בהקשר של יישומים רבים. המגבלות של חוק הגז האידיאלי בתיאור מערכות בתנאים של לחצים גבוהים או טמפרטורות נמוכות יכולות להיות מוסברות על ידי החשיבות הגוברת של אינטראקציות מולקולריות ו / או הגודל הסופי של מולקולות הגז התורמות למאפייני המערכת. לכן, גזים עם אינטראקציות בין-מולקולריות חזקות ומושכות (הנובעות מאינטראקציות דיפול-דיפול, כולל מליטה מימן, אינטראקציות דיפוליון או אינטראקציות ואן דר ואלס) יציגו צפיפות גבוהה יותר מהגז האידיאלי. לכל הגזים יהיה גם מרכיב דוחה בצפיפות גבוהה בשל העובדה שיותר ממולקולה אחת אינה יכולה לתפוס את אותו מיקום, מה שמעניק ירידה בצפיפות על הגז האידיאלי. גזים כמו מימן והליום מראים תרומה משמעותית יותר מהכוח הדוחה בשל גודל מולקולרי סופי, ולכן יש להם דחיסויות מעט נמוכות יותר בלחצים גבוהים. מתאן ופחמן דו חמצני מראים תרומות משמעותיות הרבה יותר למאפיינים שלהם מאינטראקציות אטרקטיביות, ומעניקים להם צפיפות גבוהה יותר מהגז האידיאלי עד לחצים גבוהים מאוד, שם המונח הדוחה שולט (בהרבה יותר מ 100 בר ב 25 °C (25 °F).

איור 2. איזותרמיה ספיגת שיווי משקל של CO2 על שטח פנים גבוה, פחמן superactivated MSC-30, ב 25 °C (70 °F).
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
חוק הגז האידיאלי הוא משוואה כה בסיסית של מדעי הכימיה, שיש לה שפע של שימושים הן בפעילויות מעבדה יומיומיות והן בחישובים ובמודל של מערכות מורכבות אף יותר, לפחות להערכה ראשונה. תחולתו מוגבלת רק על ידי הקירובים הטמונים בחוק עצמו; בלחצים וטמפרטורות כמעט סביבתיים, שבהם חוק הגז האידיאלי תקף היטב עבור גזים נפוצים רבים, הוא נמצא בשימוש נרחב בפרשנות של מערכות ותהליכים מבוססי גז. שתי דוגמאות למכשירים הפועלים על בסיס עקרונות, אשר ניתן ליישב באמצעות שימוש בחוק הגז האידיאלי, הם מדחום הגז ומנוע סטירלינג.
יישום ספציפי אחד הוא במדידת כמות סופגת הגז (physisorption) על פני השטח של חומר מוצק. ספיחה היא התופעה הפיזית לפיה מולקולות גז עוזבות את שלב הגז ונכנסות לשלב מושפל ליד פני השטח של מוצק (או אולי נוזל) בשל אינטראקציות בין-מולקולריות אטרקטיביות (כוחות פיזור) בין המוצק לגז. התפקיד של ספיחה ניתן להזניח עבור חומרים רבים בתפזורת (כגון זכוכית ונירוסטה) פלדה בתנאי סביבה, אבל הופך להיות חשוב מאוד עבור חומרים נקבוביים עם שטח פנים נגיש גדול, במיוחד בטמפרטורות נמוכות. 3 השיטה של סיוורטס הנפחית והשיטה הכבידתית לכימות ספיח פיזי מסתמכות על הכרת משוואת מצב הגז במערכת. בלחצים נמוכים וטמפרטורת הסביבה, חוק הגז האידיאלי תקף לגזים רבים, וניתן להשתמש בו כדי לקבוע במדויק את כמות הגז הנסחפת באופן דומה כמתואר בפרוטוקול לקביעת R לעיל. לדוגמה, במדידות כבידתיות של הציפה של סורבט בשטח גבוה בתנאים שבהם חוק הגז האידיאלי תקף למעשה, ההבדל בין Δwבפועל נמדד לביןהאידיאל Δw מחושב באמצעות המשוואה האידיאלית של המדינה ניתן לייחס לשינוי במשקל של שלב ספיחה. (משוואה 10) איזותרמות של ספיחות גז שיווי משקל יכולות אפוא להימדד על ידי חישוב סטייה זו,מודעותΔw , כפונקציה של לחץ בטמפרטורה קבועה (ראה איור 2), הליך סטנדרטי באפיון של חומרים נקבוביים.
Δwads = Δwactual - Δwideal (Equation 10)
Subscription Required. Please recommend JoVE to your librarian.
References
- Zumdahl, S.S., Chemical Principles. Houghton Mifflin, New York, NY. (2002).
- Kotz, J., Treichel, P., Townsend, J. Chemistry and Chemical Reactivity. 8th ed. Brooks/Cole, Belmont, CA (2012).
- Rouquerol, F., Rouquerol, J., Sing, K.S.W., Llewellyn, P., Maurin, G. Adsorption by Powders and Porous Solids: Principles, Methodology and Applications.Academic Press, San Diego, CA. (2014).





 (משוואה 9)
(משוואה 9)