ERRATUM NOTICE
Important: There has been an erratum issued for this article. Read more …
Summary
Un metodo di basato su citometria di flusso per determinare quantitativamente l'attività citotossica delle cellule natural killer di umane è mostrato qui.
Abstract
All'interno del sistema immunitario innato, linfociti effettori conosciuti come cellule natural killer (NK) svolgono un ruolo essenziale nella difesa dell'ospite contro le cellule aberranti, in particolare eliminando tumorali e cellule infette viralmente. Circa 30 difetti noti monogenici, insieme a una serie di altre condizioni patologiche, causano la mancanza delle cellule NK sia funzionale o classica, che si manifesta ridotta o assente attività citotossica. Storicamente, la citotossicità è stata studiata con metodi radioattivi, che sono ingombranti, costosi e potenzialmente pericolose. Questo articolo viene descritto un metodo di base di cytometry di flusso aerodinamico, clinicamente applicabile per quantificare l'attività citotossica delle cellule NK. In questo saggio, cellule mononucleari del sangue periferico (PBMCs) o preparazioni purificate di cellule NK sono co-incubate a diversi rapporti con una linea cellulare di tumore destinazione conosciuta ad essere sensibili alla citotossicità cellulo-mediata NK (NKCC). Le cellule bersaglio sono pre-etichettate con un colorante fluorescente per permettere la loro distinzione dalle cellule effettrici (cellule NK). Dopo il periodo di incubazione, le cellule bersaglio uccisi sono identificate da una macchia di acido nucleico, che permea in modo specifico le cellule morte. Questo metodo è favorevole alla sia diagnostico e applicazioni di ricerca e, grazie alle funzionalità multi-parametro di citometria a flusso, presenta il vantaggio aggiunto di potenzialmente consentire un'analisi più approfondita del fenotipo delle cellule NK e funzione.
Introduction
Cellule natural killer (NK) sono un sottoinsieme sofisticato dei linfociti umani innati criticamente coinvolti nell'eliminazione delle cellule infettate viralmente, cellule trasformate e altri patogeni minacce 1,2. Granuli litici delle cellule di NK casa proteine citotossiche, come perforine e granzimi. Al momento dell'attivazione, le cellule NK formano una complessa interazione con i loro obiettivi conosciuto come sinapsi immunologica, per cui queste molecole citolitiche localmente vengono rilasciate, con conseguente lisi delle cellule bersaglio diretto e apoptosi, insieme al rilascio di citochine e chemochine e, infine, l'induzione di un infiammatorio stato 1,3,4.
Attivazione delle cellule NK coinvolge una stringa complessa di attivazione e inibitorie interazioni tra NK delle cellule recettori e ligandi espressi sulla superficie delle cellule bersaglio, formando un sistema strettamente regolato. Uno dei più studiati meccanismi di attivazione delle cellule NK è il "sé mancante". Infatti, mancanza di rilevazione di classe che maggiore istocompatibilità (MHC), o umano del leucocita (HLA) l'antigene molecole, il infetti o trasformato la citotossicità delle cellule NK di cellule trigger. Tumore e cellule infettate da virus generalmente downregulate questi antigeni di fuggire immunità comunicata per cellule di T, diventando così NK primario delle cellule target 1,3,4.
Valutazione della funzione delle cellule NK è principalmente suddivise in degranulazione o citotossicità saggi. Tuttavia, test di degranulazione, quali il rilevamento di cytometric di flusso del marcatore associato degranulazione CD107a, sono indicativi dell'attivazione delle cellule NK e non della loro funzione finale, l'uccisione diretta di destinazione celle 5,6,7,8. Quindi, questa limitazione ha attirato gli investigatori a saggi di citotossicità come un'alternativa più eloquente e più diretto.
Da sempre "gold standard" per la valutazione della attività citotossica cellulo-mediata delle cellule NK e T è il test di rilascio di cromo (CRA). CRA coinvolge radioattivo etichettatura delle cellule bersaglio con 51Cr e co-incubarle con cellule effettrici. Questo test è immersa nel principio che la lisi delle cellule provoca il rilascio di legato alle proteine 51Cr nel surnatante, che può essere misurato contando gamma. Questo test, mentre efficaci, è problematico per una serie di motivi: costi elevati di materiale, manipolazione e smaltimento di radioattivo 51Cr, rilascio spontaneo di 51Cr e difficile standardizzazione - rendendolo del tutto impraticabile 9,10.
Una serie di saggi non radioattivo, che coinvolgono etichettatura fluorescente, rilascio di enzimi e anche bioluminescenza, allora è stata sviluppata come alternative al CRA 11,12,13,14. Descriviamo qui un metodo di basato su citometria di flusso per la misura di attività delle cellule NK citotossica sulle cellule bersaglio K562 che è semplice, sensibile e riproducibile. Le cellule K562 sono una cellula umana eritroleucemiche linea con riduzione dell'espressione di molecole HLA di classe I ed espressione intensificata di ligandi per recettori NK attivatori, che li rende particolarmente suscettibili a NK Citotossicità cellulo-mediata 15. In questa analisi, le cellule K562 sono pre-etichettate con carboxyfluorescein diacetate succinimidyl ester (CFSE) e co-coltivate a vari rapporti con entrambi cellule mononucleari del sangue periferico (PBMCs) o purificata di cellule NK 1. CFSE è un colorante fluorescente stabile, legame che consente di discriminazione delle cellule bersaglio da effettore NK cellule 16,17. Dopo la co-incubazione, una macchia di acido nucleico, specificamente che permea la membrana di cellule morte, viene utilizzata per identificare le celle di destinazione ucciso (Vedi tabella dei materiali). I campioni vengono quindi acquisiti su un citometro a flusso per determinare la percentuale di morti (cioè, macchia +) CFSE + cellule bersaglio.
Questa analisi può essere usata come uno screening diagnostico per malattie monogenici difetti che interessano il compartimento cellulare NK, di cui ci sono circa 30 difetti noti causando carenza di cellule NK o funzionale o classica, e per il lymphohistiocytosis hemophagocytic primario o secondario. È anche utile indagare l'attività delle cellule NK in pazienti con infezioni virali da herpes ricorrente, grave, di valutare la ricostituzione immunitaria dopo trapianto di cellule ematopoietiche o post immunomodulatori terapia 18,19,20e per una miriade di applicazioni di ricerca di base.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
Prima di impostare il dosaggio, si consiglia vivamente che contenuto delle cellule NK essere valutata nella popolazione dell'effettore di scelta. La figura 1 Mostra una tipica colorazione CD56 prima (luce blu) e dopo arricchimento di cellule NK (rosso). Le cellule NK comprendono fino a 15% di PBMCs e devono essere almeno 80% puro dopo arricchimento.
Analisi cytometric di flusso in questo test comporta la rilevazione di due parametri: CFSE, rilevabile nella stessa canalina di FITC; e una macchia di cellula morta, rilevabile nel canale stesso come APC (Figura 2AB). Dopo l'acquisizione di dati, la strategia di gating nella Figura 2 viene utilizzata per analizzare i dati. Le cellule K562 destinazione morti (cioè, cellule morte macchia +) sono gated fuori CFSE + popolazione, fornendo la % di cellule uccise all'interno della popolazione bersaglio.
Condizioni di controllo sono fondamentali nel garantire l'efficacia del test stesso e dei suoi componenti separati. In ordine per il dosaggio può essere considerata valida, il seguente dovrebbe essere previsto in condizioni di controllo (6-8): cellule solo (condizione 6) dovrebbe provocare la morte delle cellule bersaglio < 15% (Figura 3A). Dovrebbe essere rilevato alcun segnale CFSE per cellule effettrici solo (condizione 7), e la morte delle cellule dovrebbe essere < 5% (Figura 3B). Per interpolazione l'uccisione delle cellule bersaglio (condizione 8), dovrebbe essere la morte delle cellule > 85% (Figura 3).
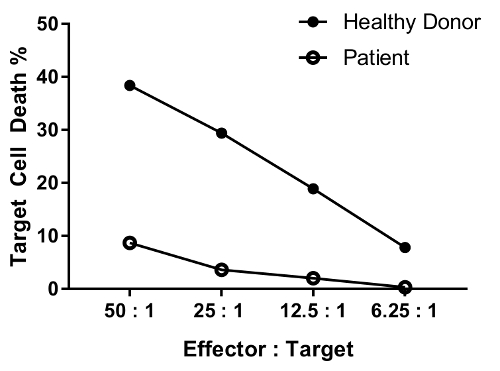
Un paziente con difetto nella funzione delle cellule NK è previsto di aver ridotto al massimo attività uccisione o tutti i rapporti testato rispetto ad un individuo sano. Il parallelo di donatore sano e paziente cellule nella Figura 4 viene illustrato il differenziale, significativa riduzione nella morte delle cellule bersaglio con la diminuzione del rapporto delle cellule effettrici-destinazione.

Figura 1: valutazione del contenuto delle cellule NK all'interno della popolazione di effector. Rappresentanza istogramma dopo colorazione totale PBMCs (blu chiaro) o purificato le cellule NK (rosse) per CD56. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 2: strategia per la rilevazione delle cellule bersaglio di Gating. A) il cancello iniziale è impostato in una trama di FITC-A/SSC-A. Le cellule K562 sono gated come CFSE + eventi. B) cellule K562 morto (cioè, macchia positiva per cellule morte) sono gestita la trama di APC-A/SSC-A successive all'interno della popolazione di cellule bersaglio CFSE +. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 3: dati rappresentativi per controllare le condizioni. A) percentuale di cellule morte macchia + K562 cellule all'interno di CFSE + cancello (gating strategia come in Figura 2) nella condizione 6 (solo cellule bersaglio) - controllo negativo per la morte di cellule K562. B) macchia di CFSE e cellula morta rilevamento in condizione 7 (effettrici cellule solo - PBMCs totale). C) percentuale di cellule morte macchia + K562 cellule all'interno del cancello CFSE + (gating strategia come in Figura 2) in condizione 8 (cellule bersaglio + Tween) - controllo positivo per la morte di cellule K562. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 4: dati rappresentativi per l'effetto di diluizione di rapporto delle cellule dell'effettore-obiettivo di vari. I rapporti di cellule effettrici: destinazione testati sono come segue: 50: 1, 25: 1; 12.5: 1; 6.25:1. dati sono sfondo (condizione #6)-rimosso. Clicca qui per visualizzare una versione più grande di questa figura.
| Campione | Condizione | Effettrici (E): Target (T) |
| PBMC | 1 - controllo positivo per citotossicità delle cellule NK | 50:1 + IL-2 |
| 2 | 50: 1 | |
| 3 | 25: 1 | |
| 4 | 12.5: 1 | |
| 5 | 6.25: 1 | |
| 6 | Solo T | |
| 7 - controllo negativo per la morte di K562 | E solo | |
| 8 - controllo positivo per la morte di K562 | T + Tween | |
| Cellule NK (purificate) | 1 - controllo positivo per citotossicità delle cellule NK | 5:1 + IL-2 |
| 2 | 5: 1 | |
| 3 | 2.5: 1 | |
| 4 | 1.25: 1 | |
| 5 | 0.625: 1 | |
| 6 | Solo T | |
| 7 - controllo negativo per la morte di K562 | E solo | |
| 8 - controllo positivo per la morte di K562 | T + Tween |
Tabella 1
Subscription Required. Please recommend JoVE to your librarian.
Discussion
Il metodo qui descritto fornisce un'alternativa semplice e conveniente per il test di rilascio di Cr tradizionale 51per valutare l'attività citotossica delle cellule NK. Questo metodo è sensibile, riproducibile e richiede meno tempo rispetto ai metodi standard precedenti, come CRA e può essere usato per entrambi clinici e applicazioni di ricerca.
Mentre il dosaggio funziona sia con totale PBMCs e arricchito le cellule NK, l'opzione per utilizzare PBMCs senza la necessità di purificare le popolazioni delle cellule è un grande vantaggio quando si tratta di piccoli volumi di sangue prelevato o celle di pochi o di scarsa qualità da campioni dei pazienti. Questo test utilizza solo CFSE e cellula morta esclusione attuabilità macchia. Guardando questi due parametri da solo fornisce informazioni succinte e sufficiente per scopi diagnostici, con l'ulteriore vantaggio di non richiedere un'ulteriore compensazione in analisi cytometric di flusso.
Questo metodo può essere utilizzato anche per studiare la biologia delle cellule NK e testare nuove terapie di targeting delle cellule NK. A questo proposito, le capacità di espansione di citometri a flusso introducono un elemento prezioso della versatilità di questo test, consentendo analisi multiparametrica delle cellule NK e la loro attività non possibile in precedenza con dosaggi come CRA. Alternativa cellulare tracciamento e coloranti di vitalità, che reagiscono in altri canali, sono disponibili per soddisfare le esigenze degli investigatori.
Questo protocollo è ottimizzato per l'utilizzo con l'obiettivo di cellule NK prototipo linea cellulare K562. Tuttavia, può essere adattato alle linee di cellule bersaglio alternativo sospensione con vari gradi di sensibilità alla citotossicità delle cellule NK, come HL-60, DiPietro, U937 e Ruffo. A questo proposito, è importante notare che la concentrazione di colorante fluorescente e di siero utilizzato durante destinazione cella etichettatura potrebbe dover essere ottimizzata per ogni linea cellulare di destinazione, come diverse linee cellulari potrebbero prendere l'etichetta fluorescente in modo diverso e per ogni citometro a flusso. Mentre in genere si raccomanda di evitare l'uso del siero durante etichettatura, abbiamo optato per tempra leggera con 0,5% di FBS per due motivi. In primo luogo, aiuta a ridurre lo stress di cella di destinazione e quindi sfondo macchia; in secondo luogo, essa porta segnale CFSE entro l'intervallo appropriato di rilevazione del nostro citometro a flusso senza richiedere regolazioni impostazioni quotidiana, aiutando così la riproducibilità del dosaggio. Variazioni del protocollo aggiuntivo potrebbero includere il test E:T diversi rapporti e tempi di incubazione per adattare il dosaggio alle condizioni di attivazione differente. La durata della co-cultura di cellule effettrici e destinazione per testare la citotossicità NK ha storicamente variava da 4-16 h, anche se periodi più lunghi tendono a provocare il rilascio spontaneo aumentato 9,16. Nel nostro metodo, incubazione più lungo potrebbe anche comportare perdita di fluorescente etichettatura da parte delle cellule bersaglio a causa di uccisione o proliferazione, come questi coloranti fluorescenti sono diluiti al momento della divisione cellulare. Così, le incubazioni nella parte bassa della finestra temporale sono generalmente preferite e non devono superare una notte incubazione 6,16,22.
È importante prendere nota di quali variabili potenzialmente possono influenzare l'esito di questo test. Nella nostra esperienza, le cellule bersaglio K562 sono particolarmente sensibili alle variazioni di temperatura. Pertanto, le cellule K562 dovrebbero non essere refrigerate ma piuttosto conservate a temperatura ambiente o messo in un incubatore CO2 , a 37 ° C prima del loro utilizzo. Per lo stesso motivo, tutti i reagenti devono essere portati a temperature appropriate come indicato nel protocollo. Un altro parametro che colpisce queste cellule è la velocità di centrifugazione, che dovrebbe essere ridotto al minimo stress cellulare. Inoltre, limitando il tempo di ritardo tra preparazione dell'effettore/obiettivo e l'inizio co-dell'incubazione a meno di 30 min è essenziale per garantire attività massima uccisione e la riproducibilità del test. Allo stesso modo, come segnale CFSE è generalmente robusto, pipettaggio accurata, corretta miscelazione delle cellule e incubazione preciso tempo quando etichettatura e tempra sono cruciali per garantire la coerenza nella macchiatura. Infine, capacità citotossica delle cellule NK è molto variabile anche in individui in buona salute ed è influenzato da una serie di fattori, tra cui Stadio di sviluppo, sesso, età e peso 23,24,25. Inoltre, fino al 30% dei controlli sani display una riduzione significativa o perdita completa della capacità citotossica se testato più di 24 ore dopo il prelievo del sangue. Pertanto, si consiglia di PBMCs uso appena purificato o NK cellule quando possibile.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Gli autori non dichiarano conflitti di interesse finanziario.
Acknowledgments
Vorremmo ringraziare Jill Narciso, UCLA Immunogenetics Center, per la sua assistenza con la preparazione del manoscritto.
Materials
| Name | Company | Catalog Number | Comments |
| Phosphate-buffered Saline (1x, w/o Ca2+ and Mg2+) | Corning (Cellgro) | 21-040-CM | |
| Ficoll-Paque PLUS | GE Healthcare | 17-1440-02 | |
| Tween-20 | Sigma | BP337-100 | |
| RPMI 1640 Media | Corning (Cellgro) | 10-040-CV | |
| Heat-inactivated Fetal Bovine Serum | Omega Scientific | FB-02 | |
| Penicillin Streptomycin | Life Technologies | 15140-163 | Stock solution at 10,000 U/mL |
| IL-2 | R&D Systems | 202-IL-050 | Lyophilized from a 0.2 μm filtered solution in Acetonitrile and TFA with BSA as a carrier protein. Reconstitute with 500 ul at 100 μg/mL in sterile 100 mM Acetic Acid containing at least 0.1% bovine serum albumin (2.1x10E6 IU/ml) |
| K562 Cells | ATCC | CCL-243 | Cancer cell line |
| T-75 cell culture flasks | Corning | 431464 | |
| CFSE cell proliferation kit | Life Technologies (CellTrace) | C34554 | Reconstitute I vial with 18 ul DMSO to prepare a 5mM stock solution. Do not freeze/thaw. |
| Sytox Red | Life Technologies | S34859 | Stock solution is provided at 5 μM in 1 mL DMSO. The DMSO solution may be subjected to multiple freeze-thaw cycles without reagent degradation. |
| Sodium/lithium heparin blood collection tubes | BD | 02-687-95 | |
| U-bottom 96-well plate | Corning | CLS3897 | |
| Serological pipettes | BD Falcon | ||
| Polystyrene round-bottom tubes (5mL) | BD Falcon | 14959-5 | |
| 50 mL polypropylene conical tube | BD Falcon | 352070 | |
| 15 mL polypropylene conical tube | BD Falcon | 352097 | |
| Reagent reservoir | USA Scientific | 2321-2230 | |
| Human NK cell enrichment cocktail | StemCell Technologies (RosetteSep) | 15065 |
References
- Iannello, A., Debbeche, O., Samarani, S., Ahmad, A. Antiviral NK cell responses in HIV infection: I. NK cell receptor genes as determinants of HIV resistance and progression to AIDS. J Leukoc Biol. 84 (1), 1-26 (2008).
- Caligiuri, M. A. Human natural killer cells. Blood. 112 (3), 461-469 (2008).
- Topham, N. J., Hewitt, E. W. Natural killer cell cytotoxicity: how do they pull the trigger? Immunology. 128 (1), 7-15 (2009).
- Warren, H. S., Smyth, M. J. NK cells and apoptosis. Immunol Cell Biol. 77 (1), 64-75 (1999).
- Tognarelli, S., Jacobs, B., Staiger, N., Ullrich, E. Flow Cytometry-based Assay for the Monitoring of NK Cell Functions. J Vis Exp. (116), (2016).
- Somanchi, S. S., McCulley, K. J., Somanchi, A., Chan, L. L., Lee, D. A. A Novel Method for Assessment of Natural Killer Cell Cytotoxicity Using Image Cytometry. PLoS One. 10 (10), e0141074 (2015).
- Alter, G., Malenfant, J. M., Altfeld, M. CD107a as a functional marker for the identification of natural killer cell activity. J Immunol Methods. 294 (1-2), 15-22 (2004).
- Atkinson, E. A., Gerrard, J. M., Hildes, G. E., Greenberg, A. H. Studies of the mechanism of natural killer (NK) degranulation and cytotoxicity. J Leukoc Biol. 47 (1), 39-48 (1990).
- Kim, G. G., Donnenberg, V. S., Donnenberg, A. D., Gooding, W., Whiteside, T. L. A novel multiparametric flow cytometry-based cytotoxicity assay simultaneously immunophenotypes effector cells: comparisons to a 4 h 51Cr-release assay. J Immunol Methods. 325 (1-2), 51-66 (2007).
- Kane, K. L., Ashton, F. A., Schmitz, J. L., Folds, J. D. Determination of natural killer cell function by flow cytometry. Clin Diagn Lab Immunol. 3 (3), 295-300 (1996).
- Jang, Y. Y., et al. An improved flow cytometry-based natural killer cytotoxicity assay involving calcein AM staining of effector cells. Ann Clin Lab Sci. 42 (1), 42-49 (2012).
- Korzeniewski, C., Callewaert, D. M. An enzyme-release assay for natural cytotoxicity. J Immunol Methods. 64 (3), 313-320 (1983).
- Karimi, M. A., et al. Measuring cytotoxicity by bioluminescence imaging outperforms the standard chromium-51 release assay. PLoS One. 9 (2), e89357 (2014).
- Oppenheim, D. E., et al. Glyco-engineered anti-EGFR mAb elicits ADCC by NK cells from colorectal cancer patients irrespective of chemotherapy. Br J Cancer. 110 (5), 1221-1227 (2014).
- West, W. H., Cannon, G. B., Kay, H. D., Bonnard, G. D., Herberman, R. B. Natural cytotoxic reactivity of human lymphocytes against a myeloid cell line: characterization of effector cells. J Immunol. 118 (1), 355-361 (1977).
- Jedema, I., van der Werff, N. M., Barge, R. M., Willemze, R., Falkenburg, J. H. New CFSE-based assay to determine susceptibility to lysis by cytotoxic T cells of leukemic precursor cells within a heterogeneous target cell population. Blood. 103 (7), 2677-2682 (2004).
- Lecoeur, H., Fevrier, M., Garcia, S., Riviere, Y., Gougeon, M. L. A novel flow cytometric assay for quantitation and multiparametric characterization of cell-mediated cytotoxicity. J Immunol Methods. 253 (1-2), 177-187 (2001).
- Carotta, S. Targeting NK Cells for Anticancer Immunotherapy: Clinical and Preclinical Approaches. Front Immunol. 7, 152 (2016).
- Mandal, A., Viswanathan, C. Natural killer cells: In health and disease. Hematol Oncol Stem Cell Ther. 8 (2), 47-55 (2015).
- Rezvani, K., Rouce, R. H. The Application of Natural Killer Cell Immunotherapy for the Treatment of Cancer. Front Immunol. 6, 578 (2015).
- Angelo, L. S., et al. Practical NK cell phenotyping and variability in healthy adults. Immunol Res. 62 (3), 341-356 (2015).
- Zons, P., et al. Comparison of europium and chromium release assays: cytotoxicity in healthy individuals and patients with cervical carcinoma. Clin Diagn Lab Immunol. 4 (2), 202-207 (1997).
- Yovel, G., Shakhar, K., Ben-Eliyahu, S. The effects of sex, menstrual cycle, and oral contraceptives on the number and activity of natural killer cells. Gynecol Oncol. 81 (2), 254-262 (2001).
- Laue, T., et al. Altered NK cell function in obese healthy humans. BMC Obes. 2, 1 (2015).
- Hazeldine, J., Lord, J. M. The impact of ageing on natural killer cell function and potential consequences for health in older adults. Ageing Res Rev. 12 (4), 1069-1078 (2013).
Tags
Immunologia problema 126 natural killer cellule NK citotossicità lisi cellulare uccisione K562 citometria a flusso rilascio di cromo la citotossicità delle cellule NK CFSE delle celluleErratum
Formal Correction: Erratum: A Flow Cytometry-Based Cytotoxicity Assay for the Assessment of Human NK Cell Activity
Posted by JoVE Editors on 09/10/2017.
Citeable Link.
An erratum was issued for: A Flow Cytometry-Based Cytotoxicity Assay for the Assessment of Human NK Cell Activity. Figure 4 has been corrected to show background-corrected data.
Figure 4 was corrected from:
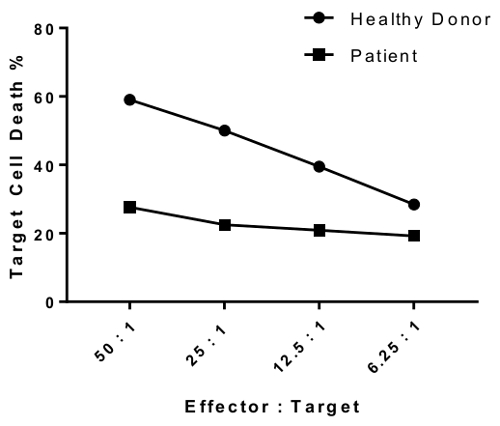
to: