Beredning av Neuronal Co-kulturer med Single Cell Precision
Summary
Protokoll för enda neuron mikroflödes ordnande och vatten maskering för in-chip plasma mönstring av biomaterial beläggningar beskrivs. Tätt sammanlänkad samkulturer kan framställas med användning av minimala cellingångar.
Abstract
Mikroflödes utföranden av Campenot kammare har rönt stort intresse från neurovetenskap samhället. Dessa sammankopplade co-kultur-plattformar kan användas för att undersöka en rad olika frågor, som spänner över utvecklings och funktionell neurobiology till infektion och sjukdomsutbredning. Men konventionella system kräver betydande cellulära ingångar (många tusen per fack), otillräcklig för att studera låga överflöd celler, såsom primär dopaminerga substantia nigra, spiral ganglier, och Drosophilia melanogaster nervceller, och opraktiskt för hög genomströmning experiment. De täta kulturer är också starkt lokalt intrasslade med få utväxter (<10%) som sammanbinder de två kulturerna. I detta papper okomplicerade microfluidic och mönstring protokoll beskrivs som itu med dessa utmaningar: (i) en mikroflödes enda neuron grupperande metod, och (ii) ett vattenmaskningsmetod för plasma mönstring biomaterial beläggningar till REGIster nervceller och främja utväxt mellan fack. Minimalistic neuronala samkulturer bereddes med hög nivå (> 85%) intercompartment anslutning och kan användas vid hög genomströmning neurobiology experiment med enstaka cell precision.
Introduction
Neuronal vävnad är mycket komplexa; en heterogen cellblandning som rumsligt beställs inom definierade lager och fack och med plast anslutning via cellkontakter och speciellt via axon och dendrit utväxter. Nya tekniker behövs för att ge ökad experimentell frihet att få djupare insikter och avslöja mekanismer centrala för sjukdomen, utveckling, och friska funktion. Den Campenot kammare 1,2 och mer nyligen mikrofabricerade utföringsformema 3,4 kan användas för ex vivo-framställning av nätverks neuronala samkulturer med förmågan att selektivt störa de olika somatiska populationer och även deras neurite utväxter. Dessa mikroflödessystem enheter har till exempel använts för att studera axon degeneration och regeneration följande kemiska 5,6 eller laser axotomy 6-8, tauopathy 9, viral spridning 10,11, och mRNA-lokalisering i axoner 4.
ent ">För att utöka räckvidden för de neurobiologists, är den tekniska utvecklingen som krävs för att förbereda minimalistiska neuronala co-kulturer. Detta möjliggör lösgörande av det neuronala nätverket för undersökning av det system med enskild cell och sub-cellulära precision. Kravet på minsta cell nummer öppnar möjligheten att analysera sällsynta celltyper, inklusive dopaminerga substantia nigra celler relevanta för Parkinsons sjukdom, spiral ganglier från örat, perifera nervceller, och stamceller. Utöver detta, är cellulära ekonomi relevans för 3R-initiativet. Med hjälp av dessa mikroflödes plattformar, toxicitet skärmar storskaliga eller annan hög genomströmning kan data rika försöksserier som kräver djur nervceller nu beaktas.
I detta papper protokoll för tillverkning och användning av en mikrofluidanordning beskrivs. Microfluidic ordnande i kombination med en in situ biomaterial mönstring metod kan användas för registrering av starkt sammankopplade neuronala co-kulturer som använder minimal cell nummer. Microfluidic grupperings är baserad på en differentialflödes metod 12-15, varvid mikrostrukturerade fällor är placerade inom en fluidkrets (illustrerad tillsammans med SEM-bilderna i fig 1). Vägen 0 → 1 har den nedre fluidic motståndet (R2> R1) för transport av nervceller till en linjär grupp av mikrostrukturerade öppningar – inloppen till de neuritutväxt kanalerna. Inflyttning i fällan av en enda cell lokalt hindrar flödet för att avleda de effektiviserar för att fånga efterföljande celler i grann fällor. Komplett beläggning av fällorna i arrayen växlar fluidic förhållandet (R1> R2) för att avleda de strömlinjerna i den slingrande väg (0 → 2) för att producera en bypass driftsform för att avlägsna överskott av nervceller.
<p class = "jove_content" fo: keep-together.within-page = "alltid">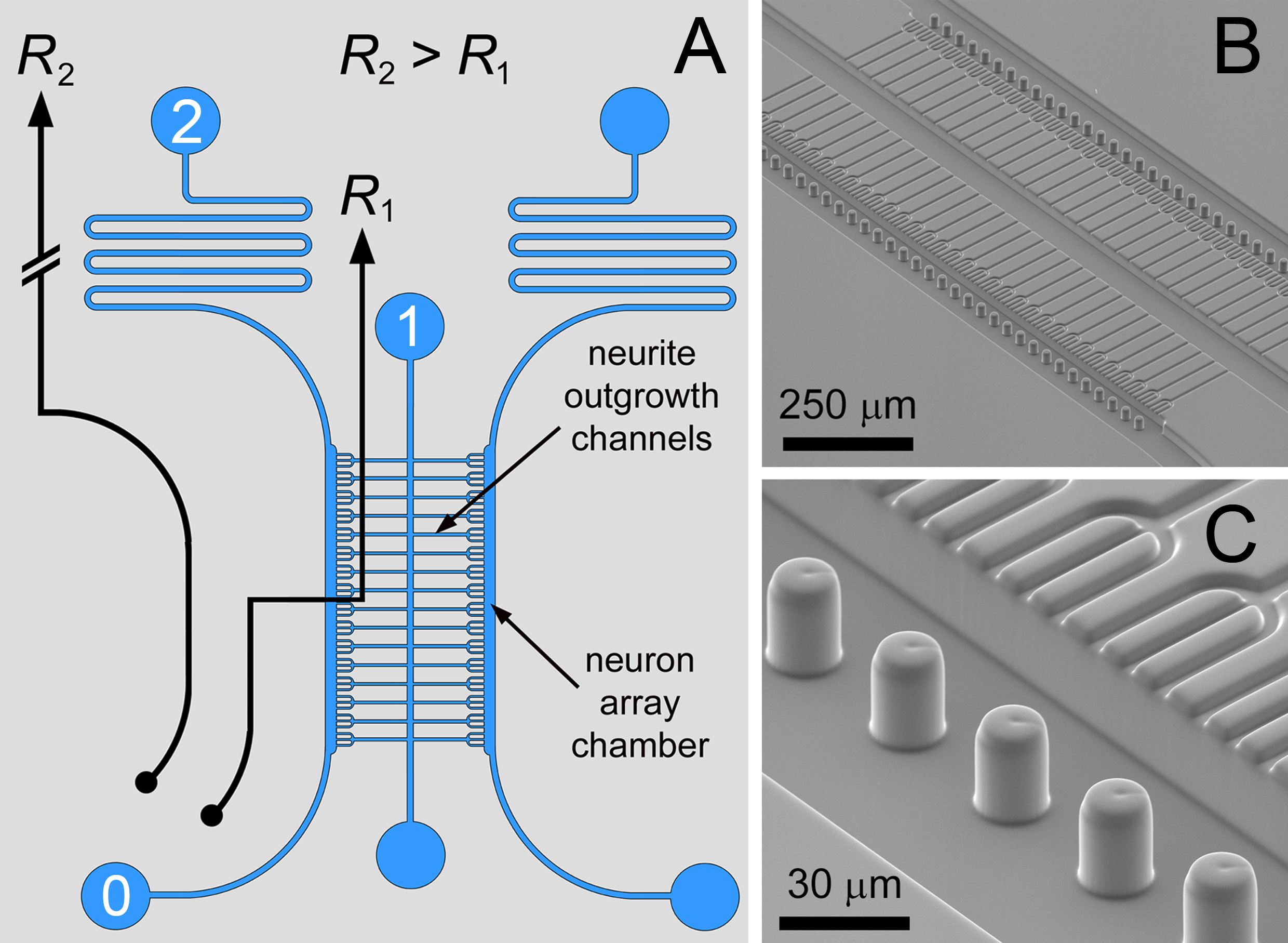
Figur 1. Microfluidic Circuit. A) Den differentiella motstånd fluidkrets för enda neuron grupperings, med flankerande odlingskamrarna är sammankopplade av neuritutväxt kanaler. B, C) SEM-bilder av dubbelskiktet compartmentalized neuron samodling array med menisk pinning micropillars. Med denna konstruktion var treudd formade neuron fångst strukturer användas för att främja fascikulering av neurite utväxter. Bild och legend återges med tillstånd av Royal Society of Chemistry (RSC) 12. Klicka här för att visa en större bild.
Beredningen av micropatterned neuronala nätverk på plana underlag kan lätt uppnås (för exampl es från vår grupp, se Frimat et al. 16 och Heike et al. 17). Men kapsla in bioaktiva materialmönster inom PDMS-enheter och med kravet på mikrometerskala anpassning av dessa till mikroflödessystem kanaler innebär en stor teknisk utmaning. I avsnitt 3.1 ett protokoll för i-chip, eller in situ, beredning av biomaterial mönster presenteras. Dessa mönster aktivera neuron registrering under långa kulturtidsramar och främja utväxter mellan fack. Menisk-pinning mikrostrukturerna används för att rikta in ett så kallat vatten mask med neuronen grupperande platser och neuritutväxt kanaler. Vattnet mask skyddar adhesionsmolekyl beläggningar under plasmabehandling, medan exponerade ytor sönderdelas för att definiera biomaterial mönstret. Dessutom är protokoll tillhandahålls för cellodling och för fluidic isolering är nödvändig för selektiv behandling av de olika sam-odlings fack.
ve_content "> är De protokoll som syftar till att utnyttja de användarvänliga principer för mjuk litografi för replikering av poly (dimetylsiloxan) (PDMS) mikrofluidikanordningar 18. På samma sätt, in situ biomaterial mönstring är okomplicerad, utnyttja avdunstning och ytspänning fenomen, och endast kräver en billig handhållen plasmakälla. Den mikroflödeskretsen effektivt program cell lastning och fack specifika behandlingar gör dessa operationer bara om att fördela material i rätt nedre porten och aspire ovanifrån. På detta sätt den är avsedd att ge neurobiologists friheten att förbereda och använda mikroflödessystem enheter i sina egna laboratorier.Protocol
Representative Results
Discussion
Den mikroflödesgrupperings teknik är den första i sitt slag som gör det möjligt för upprättande av minimalistiska kulturer precision enda neuron hantering. Tillsammans med in situ biomaterialmönstringsmetod, en kraftfull metod för att justera cellmönster med mikroflödesstrukturer, dessa minimalistiska kulturer har höga intercompartment anslutningsnivåer med minskad lokal sammanflätning. Dessa funktioner kan användas för effektiv undersökning av mellanutrymmet transmission, och med enkla konstru…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Författarna är tacksamma för Ulrich Marggraf (ISA) för SU-8 tillverkning och Maria Becker (ISA) för SEM avbildning. Forskningen har genomförts med finansiellt stöd från Deutsche Forschungsgemeinschaft (DFG WE3737/3-1), en Bundesministerium für Bildung und Forschung bidrag (BMBF 0101-31P6541) och av Ministerium für Innovation, Wissenschaft und Forschung des Landes Nordrhein-Westfalen. Heike Hardelauf tackar Internationella Leibniz forskarskolan "Systembiologi Lab-on-a-chip" för ekonomiskt stöd.
Materials
| PDMS Sylgard 184 | Dow Corning | ||
| PDMS Elastosil RT 601 | Wacker | ||
| Coverslips | VWR | 630-1590 | 130-160 mm thick |
| 3 mm Biopsy Punches | Kai Medical | Handle with care – extremely sharp | |
| Tygon Tubing | Fisher Scientific | S-50-HL | 1.65 mm ID; 3.35 mm OD |
| 1 mL Syringe (Inkjekt and Omnifix) | Braun | 6064204 | |
| 4-Way Tubing Connector | VWR or Fisher Scientific | ||
| Flow Regulator | Harvard Apparatus | 722645 | |
| 0.5 mm Pins | Dressmaking Departments | ||
| PLL-g-PEG | SuSoS | PLL(20)-g[3.5]-PEG(5) | Stability in storage can be an issue |
| poly-D-lysine | Sigma-Aldrich | P6407 | |
| poly-lysine-FITC | Sigma-Aldrich | P3069 | |
| poly-ornithine | Sigma-Aldrich | P4957 | |
| fibronectin | Sigma-Aldrich | F2006 | |
| laminin | Sigma-Aldrich | L2020 | |
| PBS | Sigma-Aldrich | P4417 | |
| Inverted Fluorescent Microscope | |||
| Example Aspiration Pump | KNF Neuberger, Laboport | N811KVP | |
| Hand Held Corona Discharge Device | Leybold-Heraeus, USA | VP23 | May not comply with your country's safety standards |
| Femto Plasma Oven | Diener Electronic | ||
| Vacuum Dessicator or Centrifuge |
References
- Campenot, R. B. Local control of neurite development by nerve growth factor. Proc Natl Acad Sci USA. 74 (10), 4516-4519 (1997).
- Campenot, R. B. Development of sympathetic neurons in compartmentalized cultures. I. Local control of neurite growth by nerve growth factor. Dev Biol. 93 (1), 1-12 (1982).
- Taylor, A. M., et al. Microfluidic multicompartment device for neuroscience research. Langmuir. 19, 1551-1556 (2003).
- Taylor, A. M., et al. A microfluidic culture platform for CNS axonal injury, regeneration and transport. Nat Methods. 2 (8), 559-565 (2005).
- Kilinc, D., et al. Wallerian-like degeneration of central neurons after synchronized and geometrically registered mass axotomy in a three-compartmental microfluidic chip. Neurotox. Res. 19, 149-161 (2011).
- Li, L., et al. Spatiotemporally controlled and multifactor involved assay of neuronal regeneration after chemical injury in an integrated microfluidics. Anal. Chem. 84 (15), 6444-6453 (2012).
- Kim, Y. T., Karthikeyan, K., Chirvi, S., Dave, D. P. Neuro-optical microfluidic platform to study injury and regeneration of single axons. Lab Chip. 9, 2576-2581 (2009).
- Hellman, A. N., et al. Examination of axonal injury and regeneration in micropatterned neuronal culture using pulsed laser microbeam dissection. Lab Chip. 10 (16), 2083-2092 (2010).
- Kunze, A., et al. Co-pathological connected primary neurons in a microfluidic device for Alzheimer studies. Biotechnol. Bioeng. 108 (9), 2241-2245 (2011).
- Liu, W. W., Goodhouse, J., Jeon, N. L., Enquist, L. W. A microfluidic chamber for analysis of neuron-to-cell spread and axonal transport of an alpha-herpesvirus. PLoS One. 3 (6), (2008).
- Markus, A., et al. Varicella-Zoster virus (VZV) infection of neurons derived from human embryonic stem cells: Direct demonstration of axonal infection, transport of VZV, and productive neuronal infection. J. Virol. 85 (13), 6220-6233 (2011).
- Dinh, N. D., et al. Microfluidic construction of minimalistic neuronal co-cultures. Lab Chip. 13 (7), 1402-1412 (2013).
- Tan, W. H., Takeuchi, S. A trap-and-release integrated microfluidic system for dynamic microarray applications. Proc. Natl. Acad. Sci. USA. 104 (4), 1146-1151 (2007).
- Frimat, J. -. P., et al. A microfluidic array with cellular valving for single cell co-culture. Lab Chip. 11 (2), 231-237 (2011).
- Di Carlo, D., Aghdam, N., Lee, L. P. Single-cell enzyme concentrations, kinetics, and inhibition analysis using high-density hydrodynamic cell isolation arrays. Anal. Chem. 78 (14), 4925-4930 (2006).
- Frimat, J. P., et al. The network formation assay: A spatially standardized neurite outgrowth analytical display for neurotoxicity screening. Lab Chip. 10, 701-709 (2010).
- Hardelauf, H., et al. High fidelity neuronal networks formed by plasma masking with a bilayer membrane: analysis of neurodegenerative and neuroprotective processes. Lab Chip. 11 (16), 2763-2771 (2011).
- Whitesides, G. M., et al. Soft lithography in biology and biochemistry. Annu. Rev. Biomed. Eng. 3, 335-373 (2001).
- Haubert, K., Drier, T., Beebe, D. PDMS bonding by means of a portable, low-cost corona system. Lab Chip. 6, 1548-1549 (2006).
- Frimat, J. P., et al. Plasma stencilling methods for cell patterning. Anal. Bioanal. Chem. 395 (3), 601-609 (2009).
- Huang, N. P., et al. Poly(L-lysine)-g-poly(ethylene glycol) layers on metal oxide surfaces: surface-analytical characterization and resistance to serum and fibrinogen adsorption. Langmuir. 17, 489-498 (2001).
- Li, N., Folch, A. Integration of topographical and biochemical cues by axons during growth on microfabricated 3-D substrates. Exp. Cell Res. 311 (2), 307-316 (2005).
- Huang, L. R., Cox, E. C., Austin, R. H., Sturm, J. C. Continuous particle separation through deterministic lateral displacement. Science. 304 (5673), 987-990 (2004).
- Yang, Z., et al. A review of nanoparticle functionality and toxicity on the central nervous system. J. R. Soc. Interface. 7, (2010).
- Brenneman, K. A., et al. Direct olfactory transport of inhaled manganese ((MnCl2)-Mn-54) to the rat brain: Toxicokinetic investigations in a unilateral nasal occlusion model. Toxicol. Appl. Pharm. 169 (3), 238-248 (2000).
- Magalães, A. C., et al. Uptake and neuritic transport of scrapie prion protein coincident with infection of neuronal cells. J. Neurosci. 25 (21), 5207-5216 (2005).
- Diogenes, M. J., et al. Extracellular alpha-synuclein oligomers modulate synaptic transmission and impair LTP via NMDA-receptor activation. J Neurosci. 32 (34), 11750-11762 (2012).
- Egger, B., et al. In vitro imaging of primary neural cell culture from Drosophila. Nat. Protoc. 8 (5), 958-965 (2013).

