Preparazione della neuronali Co-culture con precisione singola cella
Summary
Sono descritti protocolli per singolo neurone microfluidica arraying e mascheramento acqua per il patterning plasma in-chip di rivestimenti biomateriale. Co-colture altamente interconnessi possono essere preparati utilizzando gli ingressi di cellule minimali.
Abstract
Realizzazioni microfluidica della camera Campenot hanno suscitato un grande interesse da parte della comunità neuroscienze. Queste piattaforme di co-coltura interconnessi possono essere utilizzati per indagare su una serie di domande, che coprono neurobiologia dello sviluppo e funzionale alle infezioni e la propagazione della malattia. Tuttavia, i sistemi tradizionali richiedono input significativi cellulari (molte migliaia per compartimento), inadeguati per lo studio delle cellule poco abbondanti, come primaria nigra dopaminergici della substantia, gangli spirale, e Drosophilia neuroni melanogaster, e poco pratico per un throughput elevato sperimentazione. Le colture dense sono impigliati molto localmente, con poche escrescenze (<10%) che interconnettono i due culture. In questo documento sono descritti semplici protocolli di microfluidica e patterning che affrontare tali sfide: (i) una microfluidica singolo neurone metodo arraying, e (ii) un metodo di mascheramento acqua per rivestimenti biomateriale patterning plasma Register neuroni e promuovere conseguenza tra i compartimenti. Neuronali co-colture minimalista sono stati preparati con alto livello (> 85%), la connettività intercompartment e possono essere utilizzati per esperimenti di neurobiologia ad alto rendimento con precisione singola cellula.
Introduction
Tessuto neuronale è molto complesso; una miscela cellulare eterogenea che è spazialmente ordinato entro livelli e comparti definiti e con connettività di plastica tramite contatti cellulari e soprattutto tramite assoni e dendriti escrescenze. Nuove tecniche sono tenuti a conferire una maggiore libertà di sperimentazione per acquisire conoscenze più profonde e meccanismi a svelare centrali per malattia, lo sviluppo e la funzione sana. La camera Campenot 1,2 e più recentemente microfabricated realizzazioni 3,4 possono essere utilizzati per la preparazione di ex vivo neuronali co-colture in rete con la capacità di perturbare selettivamente le diverse popolazioni somatiche e anche loro escrescenze neuriti. Questi dispositivi microfluidici sono per esempio stati utilizzati per studiare assonale degenerazione e rigenerazione seguenti sostanze chimiche 5,6 o laser assotomia 6-8, tauopathy 9, la diffusione virale 10,11, e mRNA localizzazione in assoni 4.
ent ">Per estendere la portata dei neurobiologi, gli sviluppi tecnologici sono tenute a redigere neuronali co-culture minimalista. Ciò consente disentanglement della rete neuronale per la ricerca del sistema con singola cella e precisione sub-cellulare. Il requisito per il numero di cellule minime apre la possibilità di analizzare tipi di cellule rare, comprese dopaminergici della substantia nigra cellule pertinenti alla malattia di Parkinson, gangli spirale dall'orecchio, neuroni periferici, e cellule staminali. Al di là di questo, economia cellulare è rilevante per l'iniziativa 3R. Utilizzando queste piattaforme microfluidica, schermi di tossicità su larga scala o altro throughput elevato, i dati ricca serie sperimentali che richiedono neuroni di animali può essere considerato.
In questo documento sono descritti protocolli per la fabbricazione e l'uso di un dispositivo microfluidica. Arraying microfluidica in combinazione con un in situ biomateripatterning al metodo può essere utilizzato per la registrazione di co-colture neuronali altamente interconnesse utilizzando il numero di cellule minime. Arraying microfluidica è basato su un approccio differenziale di flusso 12-15, in cui trappole microstrutturata sono posizionati all'interno di un circuito fluidico (illustrato con immagini SEM di Figura 1). Il percorso 0 → 1 ha la resistenza fluida inferiore (R 2> R 1) per il trasporto di neuroni di una schiera lineare di aperture microstrutturati – le insenature ai canali crescita dei neuriti. Occupazione della trappola da una singola cellula impedisce localmente il flusso per deviare le linee di corrente per la cattura di celle successive in trappole vicini. Occupazione completa delle trappole nella matrice commuta il rapporto fluidico (R 1> R 2) per deviare le linee di flusso nel percorso a serpentina (0 → 2) per produrre un bypass di operazione per la rimozione dei neuroni in eccesso.
<p class = "jove_content" fo: keep-together.within-page = "always">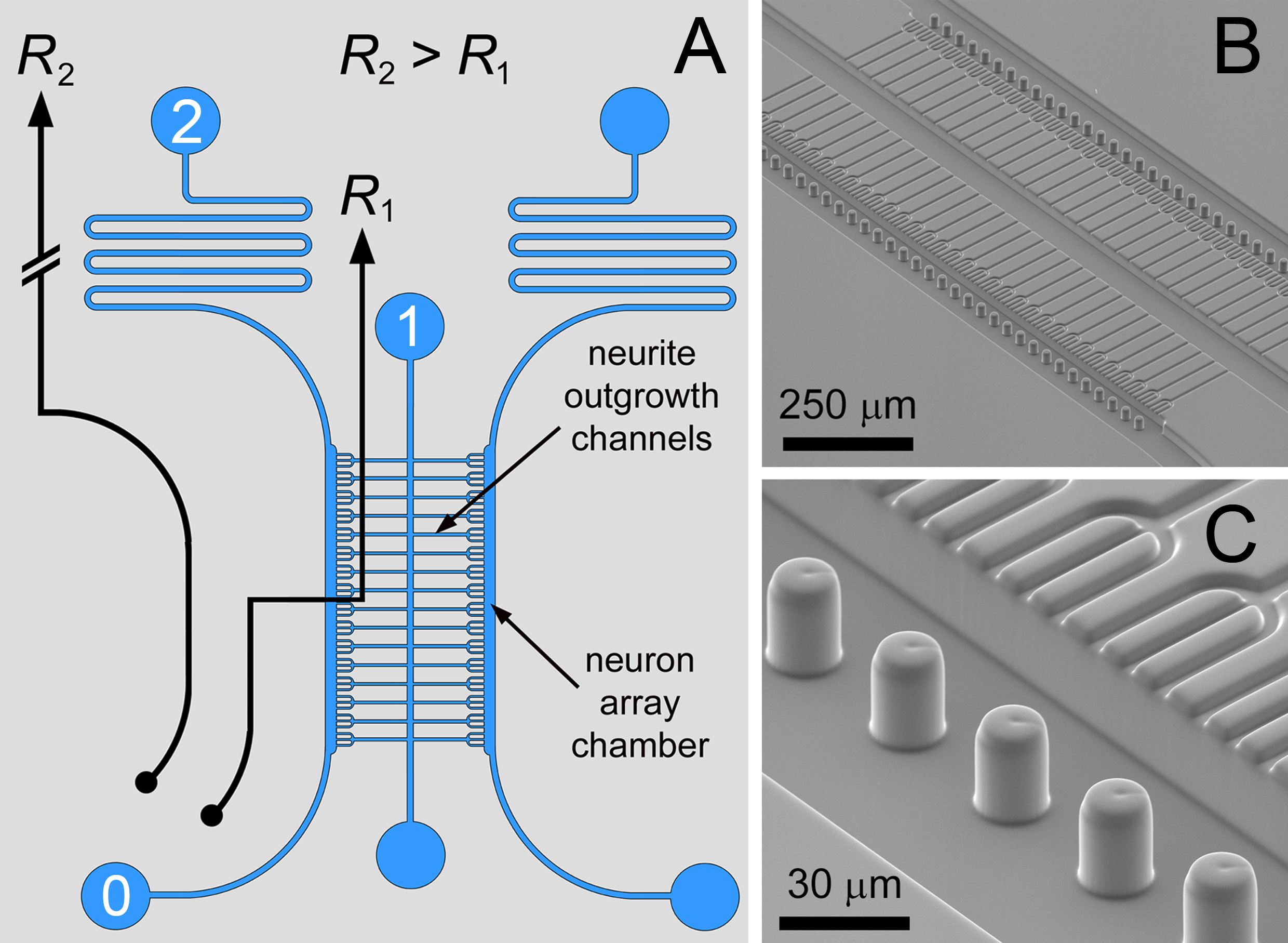
Figura 1. Microfluidic Circuit. A) Il circuito di resistenza differenziale di fluido per formare gli array singolo neurone, con accompagnamento camere di coltura collegati tra loro da canali crescita dei neuriti. B, immagini C) SEM del doppio strato neurone compartimenti matrice co-coltura con menisco pinning micropillars. Con questo progetto, le strutture neurone di cattura a forma di tridente sono stati utilizzati per promuovere la fascicolazione delle escrescenze neuriti. Figure e leggenda riprodotta con il permesso della Royal Society of Chemistry (RSC) 12. Clicca qui per vedere l'immagine ingrandita.
La preparazione delle reti neuronali micropatterned su substrati planari può facilmente essere ottenuto (per exampl es dal nostro gruppo, vedere Frimat et al. 16 e Heike et al. 17). Tuttavia, incapsulando materiale modelli bioattive all'interno dei dispositivi PDMS e con l'esigenza di allineamento micrometro scala di questi per i canali microfluidica rappresenta una grande sfida tecnica. Nella sezione 3.1 un protocollo per la a-chip, o in situ, preparazione di modelli biomateriale è presentato. Questi modelli consentono la registrazione dei neuroni durante tempi lunghi della cultura e promuovere escrescenze tra i compartimenti. Microstrutture menisco-pinning sono usati per allineare una cosiddetta maschera acqua con il neurone arraying siti e canali crescita dei neuriti. La maschera d'acqua protegge i rivestimenti molecole di adesione durante il trattamento al plasma, mentre le superfici esposte sono disintegrati per definire il modello di biomateriale. Inoltre, sono disponibili protocolli per colture cellulari e per l'isolamento fluidico necessaria per il trattamento selettivo dei vari comparti co-coltura.
ve_content "> I protocolli sono progettati per sfruttare i principi user-friendly di litografia soft per la replica di poli (dimetilsilossano) (PDMS) dispositivi microfluidici 18. Allo stesso modo, in situ biomateriale patterning è semplice, sfruttando evaporazione e superficiali fenomeni di tensione, e solo richiede una sorgente di plasma portatile poco costoso. Il circuito microfluidica efficace i programmi di carico e vano cella trattamenti specifici che queste operazioni semplicemente di erogazione di materiali nella porta inferiore corretta ed aspirando dall'alto. In questo modo, si intende dare le neurobiologists la libertà di preparare e utilizzare i dispositivi microfluidici nei propri laboratori.Protocol
Representative Results
Discussion
La tecnica per formare gli array microfluidica è il primo del suo genere che permette precisione un'unica movimentazione neurone per stabilire le culture minimalista. Accoppiato con il metodo in situ patterning biomateriale, un approccio efficace per allineare i modelli di cellulari con le strutture microfluidica, queste culture minimalista hanno livelli di connettività ad alta intercompartment con ridotta entanglement locale. Queste funzioni possono essere utilizzate per lo studio efficace di trasmission…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Gli autori sono grati a Ulrich Marggraf (SISSA) di SU-8 fabbricazione e Maria Becker (SISSA) per l'imaging SEM. La ricerca è stata sostenuta finanziariamente dalla Deutsche Forschungsgemeinschaft (DFG WE3737/3-1), un Bundesministerium für Bildung und Forschung concessione (BMBF 0101-31P6541) e dalla Ministerium für Innovation, Wissenschaft und Forschung des Landes Nordrhein-Westfalen. Heike Hardelauf grazie Leibniz Scuola di Dottorato Internazionale "Systems Biology Lab-on-a-Chip" per il sostegno finanziario.
Materials
| PDMS Sylgard 184 | Dow Corning | ||
| PDMS Elastosil RT 601 | Wacker | ||
| Coverslips | VWR | 630-1590 | 130-160 mm thick |
| 3 mm Biopsy Punches | Kai Medical | Handle with care – extremely sharp | |
| Tygon Tubing | Fisher Scientific | S-50-HL | 1.65 mm ID; 3.35 mm OD |
| 1 mL Syringe (Inkjekt and Omnifix) | Braun | 6064204 | |
| 4-Way Tubing Connector | VWR or Fisher Scientific | ||
| Flow Regulator | Harvard Apparatus | 722645 | |
| 0.5 mm Pins | Dressmaking Departments | ||
| PLL-g-PEG | SuSoS | PLL(20)-g[3.5]-PEG(5) | Stability in storage can be an issue |
| poly-D-lysine | Sigma-Aldrich | P6407 | |
| poly-lysine-FITC | Sigma-Aldrich | P3069 | |
| poly-ornithine | Sigma-Aldrich | P4957 | |
| fibronectin | Sigma-Aldrich | F2006 | |
| laminin | Sigma-Aldrich | L2020 | |
| PBS | Sigma-Aldrich | P4417 | |
| Inverted Fluorescent Microscope | |||
| Example Aspiration Pump | KNF Neuberger, Laboport | N811KVP | |
| Hand Held Corona Discharge Device | Leybold-Heraeus, USA | VP23 | May not comply with your country's safety standards |
| Femto Plasma Oven | Diener Electronic | ||
| Vacuum Dessicator or Centrifuge |
References
- Campenot, R. B. Local control of neurite development by nerve growth factor. Proc Natl Acad Sci USA. 74 (10), 4516-4519 (1997).
- Campenot, R. B. Development of sympathetic neurons in compartmentalized cultures. I. Local control of neurite growth by nerve growth factor. Dev Biol. 93 (1), 1-12 (1982).
- Taylor, A. M., et al. Microfluidic multicompartment device for neuroscience research. Langmuir. 19, 1551-1556 (2003).
- Taylor, A. M., et al. A microfluidic culture platform for CNS axonal injury, regeneration and transport. Nat Methods. 2 (8), 559-565 (2005).
- Kilinc, D., et al. Wallerian-like degeneration of central neurons after synchronized and geometrically registered mass axotomy in a three-compartmental microfluidic chip. Neurotox. Res. 19, 149-161 (2011).
- Li, L., et al. Spatiotemporally controlled and multifactor involved assay of neuronal regeneration after chemical injury in an integrated microfluidics. Anal. Chem. 84 (15), 6444-6453 (2012).
- Kim, Y. T., Karthikeyan, K., Chirvi, S., Dave, D. P. Neuro-optical microfluidic platform to study injury and regeneration of single axons. Lab Chip. 9, 2576-2581 (2009).
- Hellman, A. N., et al. Examination of axonal injury and regeneration in micropatterned neuronal culture using pulsed laser microbeam dissection. Lab Chip. 10 (16), 2083-2092 (2010).
- Kunze, A., et al. Co-pathological connected primary neurons in a microfluidic device for Alzheimer studies. Biotechnol. Bioeng. 108 (9), 2241-2245 (2011).
- Liu, W. W., Goodhouse, J., Jeon, N. L., Enquist, L. W. A microfluidic chamber for analysis of neuron-to-cell spread and axonal transport of an alpha-herpesvirus. PLoS One. 3 (6), (2008).
- Markus, A., et al. Varicella-Zoster virus (VZV) infection of neurons derived from human embryonic stem cells: Direct demonstration of axonal infection, transport of VZV, and productive neuronal infection. J. Virol. 85 (13), 6220-6233 (2011).
- Dinh, N. D., et al. Microfluidic construction of minimalistic neuronal co-cultures. Lab Chip. 13 (7), 1402-1412 (2013).
- Tan, W. H., Takeuchi, S. A trap-and-release integrated microfluidic system for dynamic microarray applications. Proc. Natl. Acad. Sci. USA. 104 (4), 1146-1151 (2007).
- Frimat, J. -. P., et al. A microfluidic array with cellular valving for single cell co-culture. Lab Chip. 11 (2), 231-237 (2011).
- Di Carlo, D., Aghdam, N., Lee, L. P. Single-cell enzyme concentrations, kinetics, and inhibition analysis using high-density hydrodynamic cell isolation arrays. Anal. Chem. 78 (14), 4925-4930 (2006).
- Frimat, J. P., et al. The network formation assay: A spatially standardized neurite outgrowth analytical display for neurotoxicity screening. Lab Chip. 10, 701-709 (2010).
- Hardelauf, H., et al. High fidelity neuronal networks formed by plasma masking with a bilayer membrane: analysis of neurodegenerative and neuroprotective processes. Lab Chip. 11 (16), 2763-2771 (2011).
- Whitesides, G. M., et al. Soft lithography in biology and biochemistry. Annu. Rev. Biomed. Eng. 3, 335-373 (2001).
- Haubert, K., Drier, T., Beebe, D. PDMS bonding by means of a portable, low-cost corona system. Lab Chip. 6, 1548-1549 (2006).
- Frimat, J. P., et al. Plasma stencilling methods for cell patterning. Anal. Bioanal. Chem. 395 (3), 601-609 (2009).
- Huang, N. P., et al. Poly(L-lysine)-g-poly(ethylene glycol) layers on metal oxide surfaces: surface-analytical characterization and resistance to serum and fibrinogen adsorption. Langmuir. 17, 489-498 (2001).
- Li, N., Folch, A. Integration of topographical and biochemical cues by axons during growth on microfabricated 3-D substrates. Exp. Cell Res. 311 (2), 307-316 (2005).
- Huang, L. R., Cox, E. C., Austin, R. H., Sturm, J. C. Continuous particle separation through deterministic lateral displacement. Science. 304 (5673), 987-990 (2004).
- Yang, Z., et al. A review of nanoparticle functionality and toxicity on the central nervous system. J. R. Soc. Interface. 7, (2010).
- Brenneman, K. A., et al. Direct olfactory transport of inhaled manganese ((MnCl2)-Mn-54) to the rat brain: Toxicokinetic investigations in a unilateral nasal occlusion model. Toxicol. Appl. Pharm. 169 (3), 238-248 (2000).
- Magalães, A. C., et al. Uptake and neuritic transport of scrapie prion protein coincident with infection of neuronal cells. J. Neurosci. 25 (21), 5207-5216 (2005).
- Diogenes, M. J., et al. Extracellular alpha-synuclein oligomers modulate synaptic transmission and impair LTP via NMDA-receptor activation. J Neurosci. 32 (34), 11750-11762 (2012).
- Egger, B., et al. In vitro imaging of primary neural cell culture from Drosophila. Nat. Protoc. 8 (5), 958-965 (2013).

