Utarbeidelse av Neuronal Co-kulturer med Single Cell Precision
Summary
Protokoller for enkelt nevron microfluidic Oppstillings og vann maskering for i-chip plasma fordelingen av biomateriale belegg er beskrevet. Meget sammenhengende co-kulturer kan være forberedt på å bruke minimalt med celle innganger.
Abstract
Microfluidic utførelser av Campenot kammeret har tiltrukket seg stor interesse fra nevrovitenskap samfunnet. Disse sammenhengende co-kultur plattformer kan brukes til å undersøke en rekke spørsmål, som strekker seg over utviklingsmessige og funksjonelle nevrobiologi for smitte og sykdom forplantning. Men konvensjonelle systemer krever betydelige cellulære innganger (mange tusen per rom), utilstrekkelig for å studere lav overflod celler, slik som primær dopaminerge substantia nigra, spiral ganglier, og Drosophilia melanogaster nevroner, og upraktisk for høy gjennomstrømming eksperimentering. Den tette kulturer er også svært lokalt viklet, med noen utvekster (<10%) sammenhengende de to kulturene. I dette papiret enkle microfluidic og mønster protokoller er beskrevet som løse disse utfordringene: (i) en microfluidic enkelt nevron arraying metode, og (ii) en vann maskering metode for plasma mønster biomateriale belegg for å RegiSter nevroner og fremme utvekst mellom avdelinger. Minimalistic neuronale ko-kulturer ble fremstilt med høyt nivå (> 85%) intercompartment tilkobling og kan anvendes for høy gjennomstrømning neurobiology forsøk med enkeltcelle presisjon.
Introduction
Nevronale vev er svært sammensatt; en heterogen celle blanding som er romlig organisert innenfor definerte lag og avdelinger, og med plast tilkobling via celle kontakter og spesielt via axon og dendrite utvekster. Nye teknikker er nødvendig for å gi større eksperimentell frihet til å få dypere innsikt og avdekke mekanismene er sentrale for sykdom, utvikling og sunn funksjon. Den Campenot kammeret 1,2 og mer nylig microfabricated utførelses 3,4 kan anvendes for ex vivo fremstilling av nettverks neuronale ko-kulturer med evne til selektivt å forstyrre de forskjellige somatiske populasjoner og også deres neurite utvekster. Disse microfluidic enheter har for eksempel blitt brukt til å studere axon degenerasjon og regenerasjon følgende kjemiske 5,6 eller laser axotomy 6-8, tauopathy 9, viral spredning 10,11, og mRNA lokalisering i axons fire.
ent ">For å utvide rekkevidden av nevrobiologer, er den teknologiske utviklingen som kreves for å forberede minimalis nevrale co-kulturer. Dette gjør det mulig floke av nevronale nettverk for etterforskningen av systemet med én celle og sub-cellulære presisjon. Kravet til minimale celletall åpner muligheten for å analysere sjeldne celletyper, inkludert substantia nigra dopaminerge celler som er relevante for Parkinsons sykdom, spiral ganglia fra øret, perifere nerveceller, og stamceller. Utover dette, er mobilnettet økonomi relevant for 3Rs initiativet. Ved hjelp av disse microfluidic plattformer, storskala toksisitets skjermer eller annen høy gjennomstrømning, kan data rik eksperimentelle serien krever dyre nevroner nå vurderes.
I dette papir protokoller for fremstilling og bruk av en mikrofluidenhet er beskrevet. Microfluidic Oppstillings i kombinasjon med en in situ biomaterial mønster metoden kan brukes for registrering av sterkt sammenhengende neuronale ko-kulturer ved bruk av minimale antall celler. Microfluidic oppstillings er basert på en differensialstrømnings tilnærming 12-15, idet mikrostrukturerte feller er plassert innenfor et fluidic krets (illustrert sammen med SEM-bilder i figur 1). Banen 0 → 1 har det nedre fluidic motstand (R 2> R 1) for transport av neuroner på en lineær oppstilling av mikrostrukturerte åpninger – inntakene til de neurite utvekst kanaler. Occupancy av fellen av en enkelt celle lokalt hindrer flyten å avlede strømlinjene for fangst påfølgende celler i nabo feller. Fullstendig belegg av fellene i matrisen kopler fluidic forholdet (R1> R 2) for å avlede strømlinjene i det serpentinbane (0 → 2) for å frembringe en bypass-modus for operasjonen for fjerning av overskytende neuroner.
<p class = "jove_content" fo: keep-together.within-page = "always">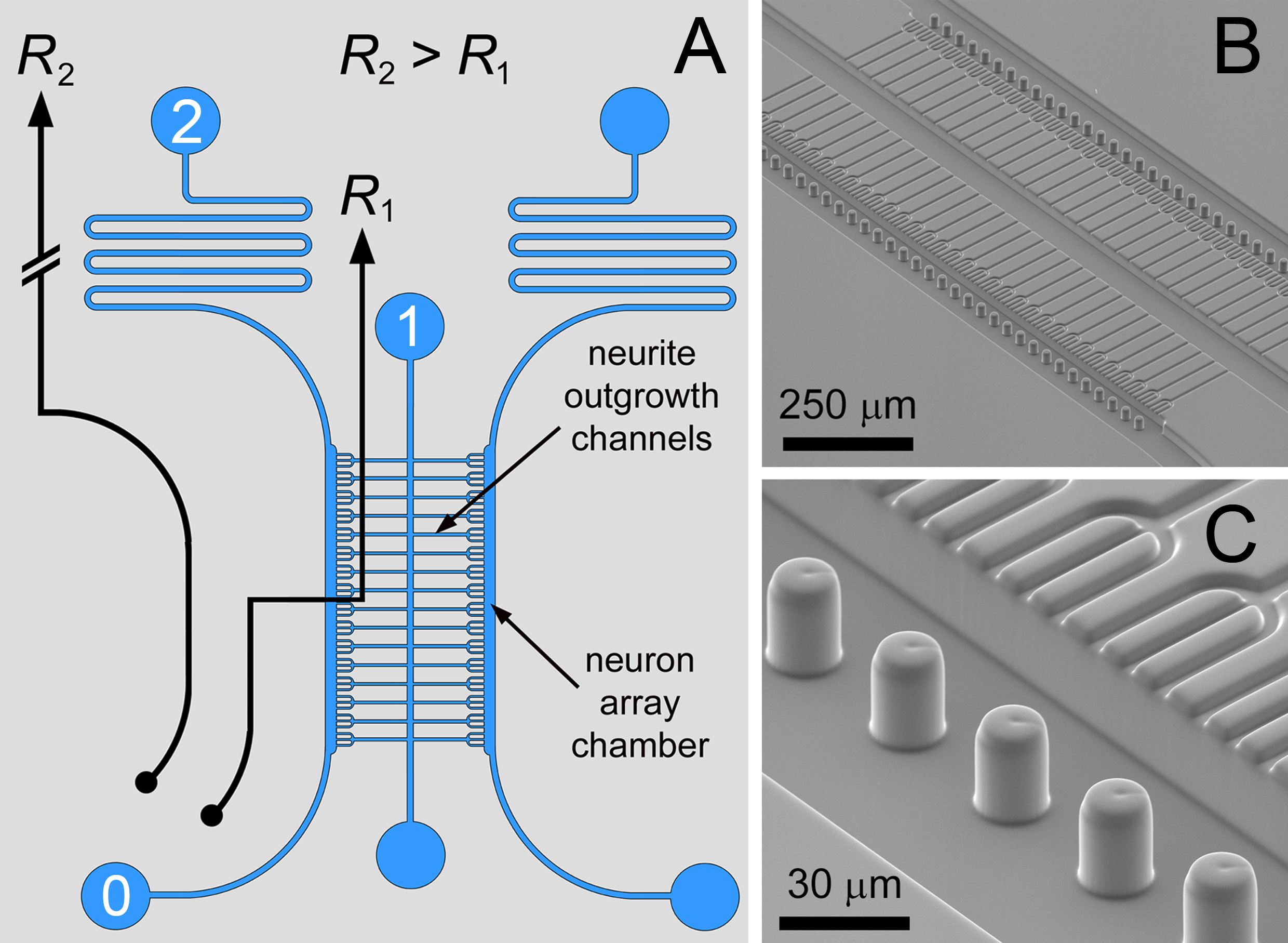
Figur 1 Microfluidic Circuit.. A) Den differensielle motstand fluidic krets for enkelt neuron oppstillings, med flankekulturkamre sammen av neurite utvekst kanaler. B, C) SEM bilder av bilayer compartmentalized neuron ko-kultur matrise med menisk låsing micropillars. Med denne designen, ble Trident-formet nevron fangst strukturer brukes til å fremme Fascikulasjoner av neurite utvekster. Figur og legende gjengitt med tillatelse fra Royal Society of Chemistry (RSC) 12. Klikk her for å se større bilde.
Fremstillingen av micropatterned nevrale nettverk på plane underlag kan lett oppnås (for exampl es fra vår gruppe, se Frimat et al. 16 og Heike et al. 17). Men innkapsle bioaktive materielle mønstre innen PDMS-enheter og med kravet om mikrometer-skala justering av disse til microfluidic kanalene utgjør en stor teknisk utfordring. I avsnitt 3.1 en protokoll for i-chip, eller in situ, utarbeidelse av biomateriale mønstre presenteres. Disse mønstrene gjør at nervecellen registrering under langvarige kultur tidsrammer og fremme utvekster mellom avdelinger. Menisk-låsing mikrostrukturer brukes til å justere en såkalt vann maske med nervecellen arraying nettsteder og neurite utvekst kanaler. Vannet masken beskytter adhesjonsmolekyl belegg under plasmabehandling, mens det eksponerte overflater er oppløst for å definere biomateriale mønster. I tillegg er protokoller levert for cellekultur, og for fluidic isolasjon som er nødvendig for selektiv behandling av de forskjellige ko-kultur seksjonene.
ve_content "> er Protokollene utviklet for å utnytte brukervennlige prinsipper for myk litografi for replikering av poly (dimethylsiloxane) (PDMS) microfluidic enheter 18. Tilsvarende, i situ biomateriale mønster er grei, utnytte fordampning og overflatespenning fenomener, og bare krever en billig håndplasmakilde. microfluidic kretsen effektivt programmer celle lasting og kupé spesifikke behandlinger gjør disse operasjonene bare et spørsmål om dispensermaterialer inn i riktig bunn port og aspirere ovenfra. På denne måte er det til hensikt å gi neurobiologists frihet til å forberede og bruke microfluidic enheter i egne laboratorier.Protocol
Representative Results
Discussion
Microfluidic formerings teknikken er den første av sitt slag som gjør presisjon enkelt nevron håndtering for å etablere minimalistiske kulturer. Sammen med in situ biomateriale mønster metode, en kraftig tilnærming for å justere celle mønstre med microfluidic strukturer, disse minimalistiske kulturer har høy intercompartment tilkoblings nivåer med redusert lokal forviklinger. Disse funksjonene kan benyttes for effektiv undersøkelse av inter-transmisjonsseksjonen, og med enkle design modifikasjoner ha…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne er takknemlige for Ulrich Marggraf (ISAS) for SU-8 fabrikasjon og Maria Becker (ISAS) for SEM bildebehandling. Forskningen ble støttet av Deutsche Forschungsgemeinschaft (DFG WE3737/3-1), en Bundesministerium für Bildung und Forschung stipend (BMBF 0101-31P6541) og ved Ministerium für Innovation, Wissenschaft und Forschung des Landes Nordrhein-Westfalen. Heike Hardelauf takker International Leibniz Graduate School "Systems Biology Lab-on-a-Chip" for økonomisk støtte.
Materials
| PDMS Sylgard 184 | Dow Corning | ||
| PDMS Elastosil RT 601 | Wacker | ||
| Coverslips | VWR | 630-1590 | 130-160 mm thick |
| 3 mm Biopsy Punches | Kai Medical | Handle with care – extremely sharp | |
| Tygon Tubing | Fisher Scientific | S-50-HL | 1.65 mm ID; 3.35 mm OD |
| 1 mL Syringe (Inkjekt and Omnifix) | Braun | 6064204 | |
| 4-Way Tubing Connector | VWR or Fisher Scientific | ||
| Flow Regulator | Harvard Apparatus | 722645 | |
| 0.5 mm Pins | Dressmaking Departments | ||
| PLL-g-PEG | SuSoS | PLL(20)-g[3.5]-PEG(5) | Stability in storage can be an issue |
| poly-D-lysine | Sigma-Aldrich | P6407 | |
| poly-lysine-FITC | Sigma-Aldrich | P3069 | |
| poly-ornithine | Sigma-Aldrich | P4957 | |
| fibronectin | Sigma-Aldrich | F2006 | |
| laminin | Sigma-Aldrich | L2020 | |
| PBS | Sigma-Aldrich | P4417 | |
| Inverted Fluorescent Microscope | |||
| Example Aspiration Pump | KNF Neuberger, Laboport | N811KVP | |
| Hand Held Corona Discharge Device | Leybold-Heraeus, USA | VP23 | May not comply with your country's safety standards |
| Femto Plasma Oven | Diener Electronic | ||
| Vacuum Dessicator or Centrifuge |
References
- Campenot, R. B. Local control of neurite development by nerve growth factor. Proc Natl Acad Sci USA. 74 (10), 4516-4519 (1997).
- Campenot, R. B. Development of sympathetic neurons in compartmentalized cultures. I. Local control of neurite growth by nerve growth factor. Dev Biol. 93 (1), 1-12 (1982).
- Taylor, A. M., et al. Microfluidic multicompartment device for neuroscience research. Langmuir. 19, 1551-1556 (2003).
- Taylor, A. M., et al. A microfluidic culture platform for CNS axonal injury, regeneration and transport. Nat Methods. 2 (8), 559-565 (2005).
- Kilinc, D., et al. Wallerian-like degeneration of central neurons after synchronized and geometrically registered mass axotomy in a three-compartmental microfluidic chip. Neurotox. Res. 19, 149-161 (2011).
- Li, L., et al. Spatiotemporally controlled and multifactor involved assay of neuronal regeneration after chemical injury in an integrated microfluidics. Anal. Chem. 84 (15), 6444-6453 (2012).
- Kim, Y. T., Karthikeyan, K., Chirvi, S., Dave, D. P. Neuro-optical microfluidic platform to study injury and regeneration of single axons. Lab Chip. 9, 2576-2581 (2009).
- Hellman, A. N., et al. Examination of axonal injury and regeneration in micropatterned neuronal culture using pulsed laser microbeam dissection. Lab Chip. 10 (16), 2083-2092 (2010).
- Kunze, A., et al. Co-pathological connected primary neurons in a microfluidic device for Alzheimer studies. Biotechnol. Bioeng. 108 (9), 2241-2245 (2011).
- Liu, W. W., Goodhouse, J., Jeon, N. L., Enquist, L. W. A microfluidic chamber for analysis of neuron-to-cell spread and axonal transport of an alpha-herpesvirus. PLoS One. 3 (6), (2008).
- Markus, A., et al. Varicella-Zoster virus (VZV) infection of neurons derived from human embryonic stem cells: Direct demonstration of axonal infection, transport of VZV, and productive neuronal infection. J. Virol. 85 (13), 6220-6233 (2011).
- Dinh, N. D., et al. Microfluidic construction of minimalistic neuronal co-cultures. Lab Chip. 13 (7), 1402-1412 (2013).
- Tan, W. H., Takeuchi, S. A trap-and-release integrated microfluidic system for dynamic microarray applications. Proc. Natl. Acad. Sci. USA. 104 (4), 1146-1151 (2007).
- Frimat, J. -. P., et al. A microfluidic array with cellular valving for single cell co-culture. Lab Chip. 11 (2), 231-237 (2011).
- Di Carlo, D., Aghdam, N., Lee, L. P. Single-cell enzyme concentrations, kinetics, and inhibition analysis using high-density hydrodynamic cell isolation arrays. Anal. Chem. 78 (14), 4925-4930 (2006).
- Frimat, J. P., et al. The network formation assay: A spatially standardized neurite outgrowth analytical display for neurotoxicity screening. Lab Chip. 10, 701-709 (2010).
- Hardelauf, H., et al. High fidelity neuronal networks formed by plasma masking with a bilayer membrane: analysis of neurodegenerative and neuroprotective processes. Lab Chip. 11 (16), 2763-2771 (2011).
- Whitesides, G. M., et al. Soft lithography in biology and biochemistry. Annu. Rev. Biomed. Eng. 3, 335-373 (2001).
- Haubert, K., Drier, T., Beebe, D. PDMS bonding by means of a portable, low-cost corona system. Lab Chip. 6, 1548-1549 (2006).
- Frimat, J. P., et al. Plasma stencilling methods for cell patterning. Anal. Bioanal. Chem. 395 (3), 601-609 (2009).
- Huang, N. P., et al. Poly(L-lysine)-g-poly(ethylene glycol) layers on metal oxide surfaces: surface-analytical characterization and resistance to serum and fibrinogen adsorption. Langmuir. 17, 489-498 (2001).
- Li, N., Folch, A. Integration of topographical and biochemical cues by axons during growth on microfabricated 3-D substrates. Exp. Cell Res. 311 (2), 307-316 (2005).
- Huang, L. R., Cox, E. C., Austin, R. H., Sturm, J. C. Continuous particle separation through deterministic lateral displacement. Science. 304 (5673), 987-990 (2004).
- Yang, Z., et al. A review of nanoparticle functionality and toxicity on the central nervous system. J. R. Soc. Interface. 7, (2010).
- Brenneman, K. A., et al. Direct olfactory transport of inhaled manganese ((MnCl2)-Mn-54) to the rat brain: Toxicokinetic investigations in a unilateral nasal occlusion model. Toxicol. Appl. Pharm. 169 (3), 238-248 (2000).
- Magalães, A. C., et al. Uptake and neuritic transport of scrapie prion protein coincident with infection of neuronal cells. J. Neurosci. 25 (21), 5207-5216 (2005).
- Diogenes, M. J., et al. Extracellular alpha-synuclein oligomers modulate synaptic transmission and impair LTP via NMDA-receptor activation. J Neurosci. 32 (34), 11750-11762 (2012).
- Egger, B., et al. In vitro imaging of primary neural cell culture from Drosophila. Nat. Protoc. 8 (5), 958-965 (2013).

