Подготовка нейронных сопредседателей культур с одной клетки Precision
Summary
Протоколы для одного нейрона микрофлюидных выстроив и воды маскировки для в-чипе плазмы паттерна биоматериала покрытий описаны. Тесно взаимосвязаны со-культуры могут быть получены с использованием входов минимальные клеток.
Abstract
Микрофлюидных варианты камеры Campenot привлекли большой интерес от нейронауки сообщества. Эти взаимосвязанные платформы со-культура может быть использован для исследования разнообразных вопросов, охватывающих с развитием и функциональный нейробиологии к инфекции и распространения заболеваний. Тем не менее, традиционные системы требуют значительных сотовой входы (многие тысячи в отсеке), неадекватные для изучения низкие клетки изобилии, такие как первичной дофаминергической черной субстанции, винтовая ганглиев и Drosophilia MELANOGASTER нейронов и непрактично для высокой пропускной экспериментов. Плотные культуры также весьма локально запутанными, с несколько выростов (<10%), соединяющих две культуры. В этой статье прямые микрофлюидных и паттерна протоколы описаны которые решения этих проблем: (я) микрофлюидных один нейрон метод выстроив, и (II) методом вода маскировка для плазмы паттерна биоматериала покрытия для Regiстер нейроны и способствовать вырост между отсеками. Минималистичные нейронов со-культуры были приготовлены с высокого уровня (> 85%) соединения intercompartment и может быть использован для высокой пропускной нейробиологии экспериментов с точностью одной ячейки.
Introduction
Нервной ткани является весьма сложным; гетерогенная сотовой смесь, которая пространственно приказал в определенных слоев и отсеков и с пластиковой подключения через сотовые контактов и особенно через аксонов и дендритов выростов. Новые методы, необходимые для придания большей экспериментальной свободу, чтобы получить более глубокое понимание и разгадать механизмы центральные к болезни, развития и нормального функционирования. Campenot камера 1,2, а в последнее микроизготовленном варианты 3,4 могут быть использованы для экс виво подготовки сетевых нейронов совместных культурах с возможностью избирательно возмущают различные соматические популяции, а также их нейритов наростов. Эти микрофлюидных устройства например был использован для изучения аксонов дегенерации и регенерации следующие химической 5,6 или лазерного аксотомии 6-8 tauopathy 9, вирусного распространения 10,11 и мРНК локализации в аксонов 4.
ЛОР ">Чтобы расширить сферу из нейробиологов, технологические разработки должны подготовить минималистичные нейронные совместно культур. Это позволяет распутывание нейронной сети для исследования системы с одной клетки и субклеточном точностью. Требование минимального количества клеток открывает возможность для анализа редких типов клеток, в том числе дофаминергических черной субстанции клеток, имеющих отношение к болезни Паркинсона, винтовая ганглиев от уха, периферических нейронах, и стволовые клетки. Помимо этого, сотовые экономика имеет отношение к инициативе 3Rs. Используя эти микрофлюидных платформы, крупномасштабные экраны токсичности или других высокую пропускную способность, данные богатых серии экспериментов, требующих нейроны животных теперь можно считать.
В данной работе протоколы для изготовления и использования микрожидкостных устройств описаны. Микрофлюидных выстроив в сочетании с в месте biomateriСпособ рисунка др. могут быть использованы для регистрации сильно взаимосвязанных нейронных совместных культурах с использованием минимального количества клеток. Микрофлюидных упорядоченный массив основан на подходе дифференциального потока 12-15, в результате чего микроструктурированных ловушки расположены внутри контура текучей (на примере вместе с изображениями SEM на фиг.1). Путь 0 → 1 имеет более низкую жидкостный сопротивление (R 2> R 1) для транспортировки нейронов к линейному массиву микроструктурированном отверстий – впускных отверстий на рост аксонов каналов. Заполняемость в ловушку одной клетки локально препятствует потоку, чтобы отвлечь линии тока для улавливания последующие клетки в соседних ловушек. Полное размещение ловушек в массиве переключает жидкостный коэффициент (R 1> R 2), чтобы отвлечь линии тока в волнообразной траектории (0 → 2) для получения обходного режима работы для удаления избыточных нейронов.
<p claсс = "jove_content" FO: держать-together.within-страницу = "всегда">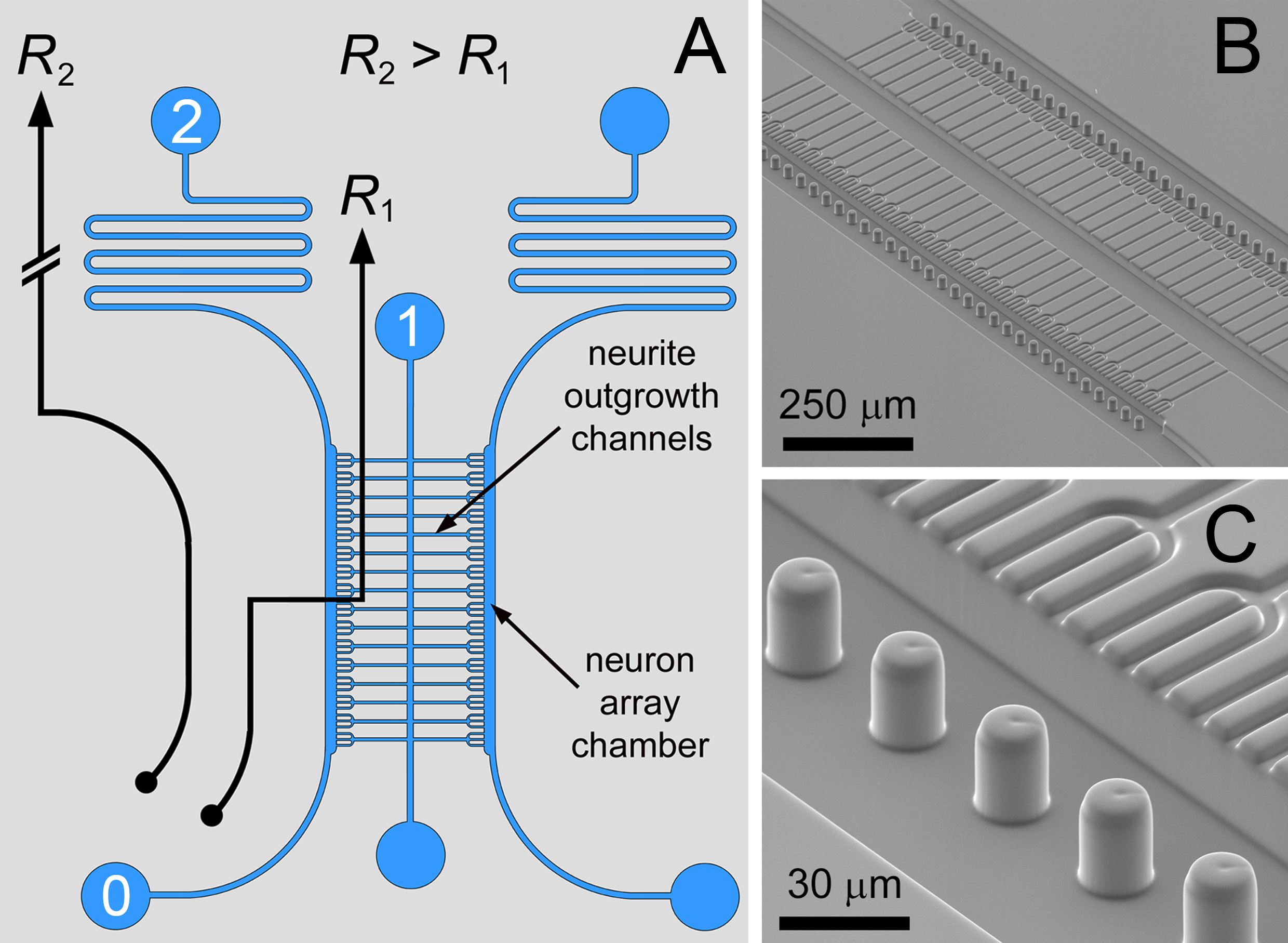
Рисунок 1. Микрофлюидных цепи. А) жидкостный контур дифференциальное сопротивление для одного нейрона выстроив, с фланговые культуры камер, соединенных между собой рост аксонов каналов. B, C) СЭМ изображения двухслойной разобщенным нейрона массива сокультуры с мениска закрепления микростолбиков. При такой конструкции, Trident-образный нейрон захвата структуры были использованы для содействия пучками из нейритов наростов. Рисунок и легенда воспроизведена с разрешения Королевского химического общества (RSC) 12. Кликните здесь, чтобы посмотреть увеличенное изображение.
Подготовка micropatterned нейронных сетей на плоских подложек может быть легко достигнуто (для exampl эс из нашей группы, см. Frimat др.. 16 и Хайке и др.. 17). Тем не менее, инкапсуляции биоактивных материалов паттерны в устройствах PDMS и с требованием микронных выравнивания их с микроканалов создает серьезную техническую проблему. В разделе 3.1 протокол для в-чипе, или в месте, подготовка биоматериала моделей представлена. Эти модели можно было регистрировать нейронов во время длительных сроков культуры и продвижения выросты между отсеками. Мениска-пиннинга микроструктуры используют для выравнивания так называемую маску воды с нейрон упорядоченный массив сайты и нейритов каналов. Маска вода защищает молекул адгезии покрытий во плазменной обработки, в то время как открытые поверхности распадаются определить биоматериала шаблон. Кроме того, протоколы предназначены для культуры клеток и для текучей изоляции, необходимой для селективного лечения различных отсеках со-культуры.
ve_content "> Протоколы предназначены для привлечения в удобных принципов мягкой литографии для репликации поли (диметилсилоксанового) (PDMS) микрожидкостных устройств 18. Кроме того, в Ситу биоматериала паттерна проста, эксплуатируя испарения и поверхностные явления напряженности, и только требуя недорогой переносной источник плазмы. Микрожидкостных схема эффективно программы загрузки клеток и отсек конкретные процедуры делает эти операции просто вопрос выдачи материалов в правильное нижнему порту и аспирационных сверху. Таким образом, он предназначен, чтобы дать нейробиологов свобода получать и использовать микрожидкостных устройств в своих собственных лабораториях.Protocol
Representative Results
Discussion
Микрожидкостных техника выстроив является первым в своем роде, который позволяет точности одного обращения нейронов для установления минималистичные культур. В сочетании с месте биоматериала методом структуризации в, мощный подход к выравнивания моделей сотовых с микрофл?…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Авторы благодарны Ульрих Маргграф (МСА) для СУ-8 изготовление и Мария Беккер (МСА) для работы с изображениями SEM. Исследование было при финансовой поддержке Deutsche Forschungsgemeinschaft (DFG WE3737/3-1), в Bundesministerium für Bildung унд Forschung гранта (BMBF 0101-31P6541) и по Ministerium für Innovation, Wissenschaft унд Forschung де Ланды Северный Рейн-Вестфалия. Хайке Hardelauf благодарит Международный Лейбниц Высшая школа "Системная биология Лаборатории-на-чипе" за финансовую поддержку.
Materials
| PDMS Sylgard 184 | Dow Corning | ||
| PDMS Elastosil RT 601 | Wacker | ||
| Coverslips | VWR | 630-1590 | 130-160 mm thick |
| 3 mm Biopsy Punches | Kai Medical | Handle with care – extremely sharp | |
| Tygon Tubing | Fisher Scientific | S-50-HL | 1.65 mm ID; 3.35 mm OD |
| 1 mL Syringe (Inkjekt and Omnifix) | Braun | 6064204 | |
| 4-Way Tubing Connector | VWR or Fisher Scientific | ||
| Flow Regulator | Harvard Apparatus | 722645 | |
| 0.5 mm Pins | Dressmaking Departments | ||
| PLL-g-PEG | SuSoS | PLL(20)-g[3.5]-PEG(5) | Stability in storage can be an issue |
| poly-D-lysine | Sigma-Aldrich | P6407 | |
| poly-lysine-FITC | Sigma-Aldrich | P3069 | |
| poly-ornithine | Sigma-Aldrich | P4957 | |
| fibronectin | Sigma-Aldrich | F2006 | |
| laminin | Sigma-Aldrich | L2020 | |
| PBS | Sigma-Aldrich | P4417 | |
| Inverted Fluorescent Microscope | |||
| Example Aspiration Pump | KNF Neuberger, Laboport | N811KVP | |
| Hand Held Corona Discharge Device | Leybold-Heraeus, USA | VP23 | May not comply with your country's safety standards |
| Femto Plasma Oven | Diener Electronic | ||
| Vacuum Dessicator or Centrifuge |
References
- Campenot, R. B. Local control of neurite development by nerve growth factor. Proc Natl Acad Sci USA. 74 (10), 4516-4519 (1997).
- Campenot, R. B. Development of sympathetic neurons in compartmentalized cultures. I. Local control of neurite growth by nerve growth factor. Dev Biol. 93 (1), 1-12 (1982).
- Taylor, A. M., et al. Microfluidic multicompartment device for neuroscience research. Langmuir. 19, 1551-1556 (2003).
- Taylor, A. M., et al. A microfluidic culture platform for CNS axonal injury, regeneration and transport. Nat Methods. 2 (8), 559-565 (2005).
- Kilinc, D., et al. Wallerian-like degeneration of central neurons after synchronized and geometrically registered mass axotomy in a three-compartmental microfluidic chip. Neurotox. Res. 19, 149-161 (2011).
- Li, L., et al. Spatiotemporally controlled and multifactor involved assay of neuronal regeneration after chemical injury in an integrated microfluidics. Anal. Chem. 84 (15), 6444-6453 (2012).
- Kim, Y. T., Karthikeyan, K., Chirvi, S., Dave, D. P. Neuro-optical microfluidic platform to study injury and regeneration of single axons. Lab Chip. 9, 2576-2581 (2009).
- Hellman, A. N., et al. Examination of axonal injury and regeneration in micropatterned neuronal culture using pulsed laser microbeam dissection. Lab Chip. 10 (16), 2083-2092 (2010).
- Kunze, A., et al. Co-pathological connected primary neurons in a microfluidic device for Alzheimer studies. Biotechnol. Bioeng. 108 (9), 2241-2245 (2011).
- Liu, W. W., Goodhouse, J., Jeon, N. L., Enquist, L. W. A microfluidic chamber for analysis of neuron-to-cell spread and axonal transport of an alpha-herpesvirus. PLoS One. 3 (6), (2008).
- Markus, A., et al. Varicella-Zoster virus (VZV) infection of neurons derived from human embryonic stem cells: Direct demonstration of axonal infection, transport of VZV, and productive neuronal infection. J. Virol. 85 (13), 6220-6233 (2011).
- Dinh, N. D., et al. Microfluidic construction of minimalistic neuronal co-cultures. Lab Chip. 13 (7), 1402-1412 (2013).
- Tan, W. H., Takeuchi, S. A trap-and-release integrated microfluidic system for dynamic microarray applications. Proc. Natl. Acad. Sci. USA. 104 (4), 1146-1151 (2007).
- Frimat, J. -. P., et al. A microfluidic array with cellular valving for single cell co-culture. Lab Chip. 11 (2), 231-237 (2011).
- Di Carlo, D., Aghdam, N., Lee, L. P. Single-cell enzyme concentrations, kinetics, and inhibition analysis using high-density hydrodynamic cell isolation arrays. Anal. Chem. 78 (14), 4925-4930 (2006).
- Frimat, J. P., et al. The network formation assay: A spatially standardized neurite outgrowth analytical display for neurotoxicity screening. Lab Chip. 10, 701-709 (2010).
- Hardelauf, H., et al. High fidelity neuronal networks formed by plasma masking with a bilayer membrane: analysis of neurodegenerative and neuroprotective processes. Lab Chip. 11 (16), 2763-2771 (2011).
- Whitesides, G. M., et al. Soft lithography in biology and biochemistry. Annu. Rev. Biomed. Eng. 3, 335-373 (2001).
- Haubert, K., Drier, T., Beebe, D. PDMS bonding by means of a portable, low-cost corona system. Lab Chip. 6, 1548-1549 (2006).
- Frimat, J. P., et al. Plasma stencilling methods for cell patterning. Anal. Bioanal. Chem. 395 (3), 601-609 (2009).
- Huang, N. P., et al. Poly(L-lysine)-g-poly(ethylene glycol) layers on metal oxide surfaces: surface-analytical characterization and resistance to serum and fibrinogen adsorption. Langmuir. 17, 489-498 (2001).
- Li, N., Folch, A. Integration of topographical and biochemical cues by axons during growth on microfabricated 3-D substrates. Exp. Cell Res. 311 (2), 307-316 (2005).
- Huang, L. R., Cox, E. C., Austin, R. H., Sturm, J. C. Continuous particle separation through deterministic lateral displacement. Science. 304 (5673), 987-990 (2004).
- Yang, Z., et al. A review of nanoparticle functionality and toxicity on the central nervous system. J. R. Soc. Interface. 7, (2010).
- Brenneman, K. A., et al. Direct olfactory transport of inhaled manganese ((MnCl2)-Mn-54) to the rat brain: Toxicokinetic investigations in a unilateral nasal occlusion model. Toxicol. Appl. Pharm. 169 (3), 238-248 (2000).
- Magalães, A. C., et al. Uptake and neuritic transport of scrapie prion protein coincident with infection of neuronal cells. J. Neurosci. 25 (21), 5207-5216 (2005).
- Diogenes, M. J., et al. Extracellular alpha-synuclein oligomers modulate synaptic transmission and impair LTP via NMDA-receptor activation. J Neurosci. 32 (34), 11750-11762 (2012).
- Egger, B., et al. In vitro imaging of primary neural cell culture from Drosophila. Nat. Protoc. 8 (5), 958-965 (2013).

