핵 자기 공명 (NMR) 분광기
English
Share
Overview
출처: 헨릭 순데른 박사연구소 – 찰머스 공과대학
핵 자기 공명 (NMR) 분광기는 유기 화학자에게 중요한 분석 기술입니다. NMR의 도움으로 유기농 실험실의 작업이 대단히 촉진되었습니다. 분자의 구조에 대한 정보를 제공할 뿐만 아니라 시료의 내용과 순도를 결정할 수 있습니다. 열 분석 및 질량 분석(MS)과 같은 유기 화학자에게 일반적으로 발생하는 다른 기술과 비교하여 NMR은 시료의 회수가 중요할 때 가치가 있는 비파괴적 방법입니다.
유기 화학자에게 가장 자주 사용되는 NMR 기술중 하나는 양성자(1H) NMR입니다. 분자에 존재하는 양성자는 주변 화학 환경에 따라 다르게 작동하여 구조를 해명 할 수 있습니다. 더욱이, 시작 물질의 NMR 스펙트럼을 최종 제품의 것과 비교하여 반응의 완성을 모니터링할 수 있다.
이 비디오는 NMR 분광법을 유기 화학자의 일상 업무에서 어떻게 사용할 수 있는지 를 보여줍니다. 다음은 다음과 같습니다: i) NMR 샘플의 준비. ii) 반응을모니터링하기 위해 1 H NMR을 사용합니다. iii) 1H NMR의 반응으로부터 얻은 제품을 식별합니다. 도시될 반응은 알데히드(1)와케톤(2)(계획1)로부터E-샬콘(3)의 합성이다. 1
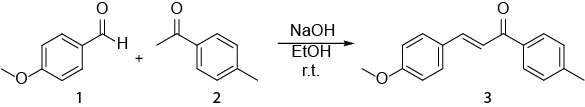
계획 1. 합성 (2E)-3-(4-메톡시페닐)-1-(4-메틸페닐)-2-propen-1-1.
Principles
Procedure
Results
By comparing the spectra of the starting materials (Figures 1 and 2) to that of the final product (Figure 5) a clear difference between the spectra can be observed, indicating formation of the chalcone. The endpoint of the reaction can be determines by taking NMR samples at different time-intervals; for example, the aldehyde proton peak (C(=O)H) (1) can be seen in Figure 3 but not in Figure 4, signifying completion of the reaction after 3 h. By looking at the integrals, splitting patterns, and J-couplings of the peaks, it is possible to validate the structure of the chalcone. The integrals of the peaks (numbers under the peak, Figure 5) show the relative amount of hydrogens present which should correlate to the amount of hydrogens found in the product. Furthermore, the splitting pattern gives an indication of the number of neighbors; for example, peak (5) and (1) — both singlets — indicate no neighbors nearby with integrals of 3 correlates with the MeO- and the Me-group respectively. By comparing the chemical shifts in the spectra with Table 1 it is possible to elucidate that the MeO-group corresponds to the singlet at 3.80 ppm and the Me-group to 2.45 ppm. Moreover, formation of the double bond can be seen as two doublets (Figure 5), 7.80 and 7.44 ppm. Looking at the J-coupling of 16 Hz indicates formation of an E-alkene; the Z-alkene typically has a smaller value of 10–12 Hz.3 Assigning the aromatic peaks verifies the structure (Figure 5).4

Figure 1. Assigned 1H NMR spectra of 4-methylacetophenone Please click here to view a larger version of this figure.

Figure 2. Assigned 1H NMR spectra of 4-methoxybenzaldehyde. Please click here to view a larger version of this figure.

Figure 3. Crude 1H NMR spectra after 30 min showing the residual aldehyde peak. Please click here to view a larger version of this figure.

Figure 4. Crude 1H NMR spectra after 3 h showing no aldehyde residual peak. Please click here to view a larger version of this figure.

Figure 5. 1H NMR spectra of the obtained product after work-up. The inserted picture shows the J-couplings of the alkene. Please click here to view a larger version of this figure.
Applications and Summary
NMR can, for example, be used to detect reaction intermediates, facilitating the work in elucidation of a reaction mechanism. With the help of NMR it is also possible to observe molecular motions and interactions important for drug development. Furthermore, NMR can give structural information about solid materials; for instance to provide a rationale for observed material properties. Other applications of NMR can be found in the field of medicine, where magnetic resonance imaging (MRI) is frequently used for medical diagnosis. NMR has also been used in metabolomics to detect different metabolites excreted by an organism thus providing a metabolic fingerprint. The uses of NMR are wide; from determining the structure of a single molecule to imaging of the human brain.
References
- Ta, L., Axelsson, A., Bijl, J., Haukka, M., Sundén, H., Ionic Liquids as Precatalysts in the Highly Stereoselective Conjugate Addition of α,β-Unsaturated Aldehydes to Chalcones. Chem. Eur. J. 20 (43), 13889-13893 (2014).
- Table adapted from Graham Solomons, T. W. Fryhle, C. B., Organic Chemistry, 10th edition, Wiley, p. 387, 418 (2011).
- Clayden, J., Greeves, N., Warren, S., Wothers, P. Proton nuclear magnetic resonance. Organic Chemistry, Chapter 11, Oxford University Press, 269 (2001).
- Wu, X.-F., Neumann, H., Spannenberg, A., Schulz, T., Jiao, H., Beller, M.,Development of a General Palladium-Catalyzed Carbonylative Heck Reaction of Aryl Halides. J. Am. Chem. Soc. 132 (41), 14596-14602 (2010).
Transcript
Nuclear magnetic resonance, or NMR, spectroscopy is an important method for determining the molecular structure and purity of samples in organic chemistry.
In NMR spectroscopy samples are exposed to a strong magnetic field. Upon exposure certain nuclei transition, or resonate, between discreet energy levels. The energy gap between these levels can be measured and visualized as spectra. This data can be used to elucidate the chemical structure of the sample.
Not all nuclei have the required properties to be NMR-active. Common isotopes studied are 1H, 2H, 13C, 19F, and 31P.
This video will introduce the principles behind NMR, step through example preparations of NMR samples from different stages of a chemical reaction, and discuss several applications.
In the NMR instrument, liquid nitrogen and helium are used to cool a super-conducting magnet. The magnet applies a constant magnetic field to a sample. Within the sample, atomic nuclei with an odd number of protons and/or neutrons will align either with the field, adopting a low-energy state, or against it, adopting a high-energy state.
The energy difference between the two levels is the resonant frequency, which depends on the strength of the applied field and the type of nucleus. For the magnets used in NMR, the value is in the radio frequency, or RF, range.
An RF coil excites the sample with a radio frequency pulse, moving the low energy nuclei to the higher state, before reverting back. The coil detects these changes in magnetization, which are displayed as peaks.
The strength of NMR lies in its ability to distinguish nuclei, in this case hydrogen, by their chemical environment. Electrons on neighboring atoms will block, or “shield”, the nuclei from some of the magnetic field. This effective field changes the resonant frequency for the particular nuclei, called a chemical shift. In ethanol the methylene, hydroxyl, and methyl protons all have unique resonance frequencies. Determining the area under each peak elucidates the number of each type of proton.
Since instruments with different magnetic strengths will shift the resonant frequencies, they are referenced to a standard molecule added to the sample, often tetramethylsilane, or TMS. The chemical shift of the frequencies is very small, often reported in parts per million, or ppm.
When using a strong magnet with high resolution, peaks will sometimes split into subpeaks. This is caused by the neighboring nuclei, some of which are aligned with the magnetic field, some against; further changing the effective field applied to the nuclei. In ethanol, the 2 methylene protons split the methyl peak twice into a triplet, and the 3 methyl protons split the methylene peak thrice into a quartet. The distance of the splitting, or J-coupling, is related to the distance of the nuclei, aiding in qualitative discovery.
Now that you understand the basic principles behind NMR, let’s review an example procedure that uses proton NMR to monitor the synthesis of chalcone from an aldehyde and ketone.
Begin by using a Pasteur pipette to add a tiny amount of the starting material to a beaker. Move into the fume hood, and dilute the starting material with 0.7 mL of deuterated solvent. Deuterated solvents are used, as deuterium’s resonant frequency is outside the range for protons.
Use a Pasteur pipette to add 0.7 mL of the diluted starting material into a clean 5 mm NMR tube, filling the bottom 4.5–5 cm. Cap the NMR tube and label it. Gently shake the tube, taking care to avoid contact between the sample and the cap. Then, insert the tube into the spinner.
Clean the outside of tube and spinner using 2-propanol and lab tissues. Then place the sample assembly into the depth gauge and calibrate the insertion depth.
After calibration, load the sample assembly into the NMR spectrometer either manually or using an auto-sampler. Finally, use a computer workstation to acquire the NMR spectrum.
Generate NMR spectra using this procedure for each of the reaction’s starting materials. For the synthesis of chalcone, spectra should be generated for both methoxybenzaldehyde and methylacetophenone.
Next, perform the sample synthesis by combining the starting materials and reagents in a flask to begin the reaction.
At 30 min intervals, remove a small aliquot of the reaction mixture using a Pasteur pipette and add 3 drops to a clean NMR tube.
Dilute this crude reaction product with deuterated solvent, and prepare for NMR using the previously described procedure.
As the reaction progresses, a yellow precipitate will form. When the reaction is complete, wash and filter the precipitate and generate NMR spectra for the purified reaction product.
Now that we’ve generated NMR spectra at each stage of the chemical reaction, let’s analyze them.
The peaks of the NMR spectra for each of the starting materials are assigned to different proton groups within the molecule according to their chemical shifts and the number of protons contributing to each peak. Here, we assign the 4 major proton groups for methylacetophenone and methoxybenzaldehyde, noting the aldehyde peak between 9.5 and 10.5 ppm. By comparing the NMR spectra of the crude reaction products at different time-points, the evolution of the chemical reaction that synthesizes chalcone is elucidated. For example, the aldehyde peak from the starting material methoxybenzaldehyde is still present after 30 min of reaction, but is completely gone after 3 h, signifying the completion of the reaction.
By examining the spectrum of the purified product we can assign each peak to a proton group in chalcone’s structure. For example, examining peaks 3 and 4 we see their integrals are both one, corresponding to groups containing just one proton.
Peaks 3 and 4 are so called doublets indicating one neighboring proton. Both have J-coupling constants of 16 Hz, suggesting that the protons are situated across an E-double bond. By assigning all of the NMR peaks of the purified reaction product, we confirm the synthesis of a pure chalcone.
NMR spectroscopy has a wide range of applications and is used in many scientific and medical fields.
In this application, proton NMR is used to verify the synthesis and structure of both diamidocarbene and mononoamidocarbine, whose NMR spectra have different peak-splitting patterns. These carbenes also generated seemingly different reaction products when combined with white phosphorus; DAC1 generated a bright red reaction product, whereas MAAC2 produced a bright orange product. These differences in reaction products were confirmed using a second application of NMR, 31P NMR, which generates spectra based on differences in the resonant frequency of phosphorus nuclei.
Here, nuclear magnetic resonance imaging, or MRI, was used to generate an anatomical map of the brain and to select the brain regions of interest. Then NMR spectroscopy was used to generate spectra of key metabolites. Finally, using MRI changes in brain metabolism in different experimental conditions were evaluated.
In this application, NMR was used to analyze the binding properties and propose a 3D structure of a copper-binding peptide. First, NMR spectra were compared for the peptide’s unbound and copper-bound states. Then, using more advanced 2-dimensional NMR techniques, different potential conformations of the peptide’s structure were evaluated. Finally, these NMR-derived structural constraints were used to develop a proposed 3-Dimensional structure for the unbound peptide.
You’ve just watched JoVE’s introduction to NMR Analysis. You should now understand the underlying principles behind NMR spectra generation and analysis, as well as a procedure for NMR sample preparation.
Thanks for watching!
