A subscription to JoVE is required to view this content. Sign in or start your free trial.
JoVE Journal
Medicine
Orthotopic Rat Kidney Transplantation: A Novel and Simplified Surgical Approach
Chapters
- 00:04Title
- 00:53Donor Procedure
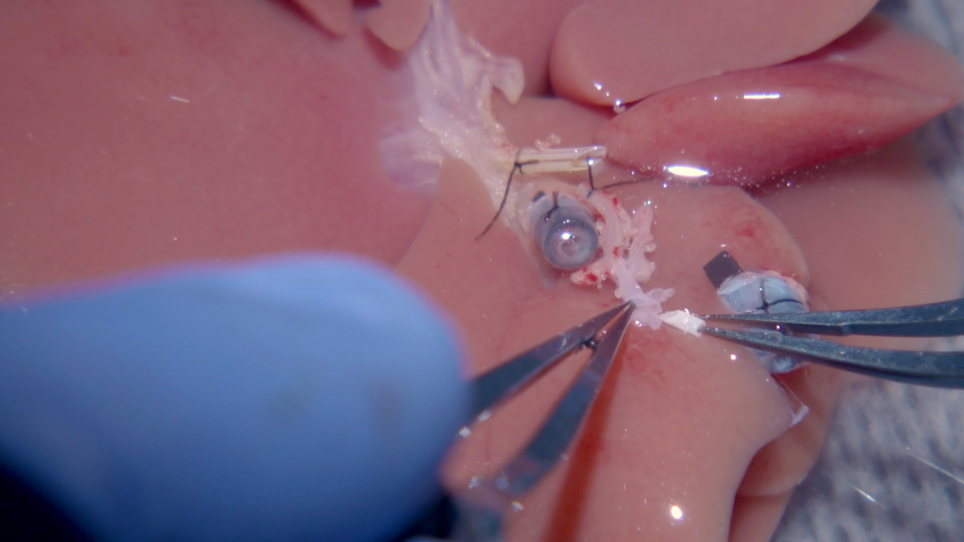
- 04:25Recipient Procedure
- 07:23Results: Kidney Transplant Survival
- 08:51Conclusion
The purpose of this manuscript and protocol is to explain and demonstrate in detail the surgical procedure of orthotopic kidney transplantation in rats. This method is simplified to achieve the correct perfusion of the donor kidney and shorten the reperfusion time by using the venous and ureteral cuff anastomosis technique.