Diluciones en serie y enchapado: enumeración microbiana
English
Share
Overview
Fuente: Jonathan F. Blaize1, Elizabeth Suter1y Christopher P. Corbo1
1 Departamento de Ciencias Biológicas, Wagner College, 1 Campus Road, Staten Island NY, 10301
La evaluación cuantitativa de los prokaryotes puede ser onerosa dada su abundancia, propensión a la proliferación exponencial, diversidad de especies dentro de una población y necesidades fisiológicas específicas. Acomenda este desafío, está la naturaleza de cuatro fases en la que las bacterias se replican (retraso, registro, estacionario y muerte). La capacidad de estimar con precisión la concentración de microorganismos es necesaria para una identificación, aislamiento, cultivo y caracterización exitosas (6). Como tal, los microbiólogos han empleado la dilución en serie y diversas técnicas de chapado durante más de un siglo para cuantificar de forma fiable la carga bacteriana y viral en entornos clínicos, industriales, farmacéuticos y académicos de laboratorio (2,4,6). Las descripciones de esta metodología aparecieron por primera vez en 1883 cuando el científico y médico alemán Robert Koch publicó su trabajo sobre agentes causantes de enfermedades infecciosas (2). A menudo conocido como el padre de la bacteriología moderna, las técnicas de Koch se han convertido en el estándar de oro para la enumeración de microorganismos, cultivables o de otro tipo, en todo el mundo.
La dilución en serie es una reducción sistemática de una entidad conocida o desconocida (un soluto, organismo, etc.) mediante la resuspensión sucesiva de una solución inicial (solución0)en volúmenes fijos de un diluyente líquido (en blanco). Estos espacios en blanco suelen consistir en 0,45% de salina, aunque la composición puede ser variada (7). Mientras que un experimentador puede elegir cualquier volumen para cada diluyente, más a menudo es un múltiplo de 10, facilitando la reducción logarítmica de la muestra. Por ejemplo, la solución0 contiene un total de 100 células de E. coli suspendidas en 10 ml de caldo nutritivo. Si se retira 1 ml de la solución0 y se añade a 9 ml de solución salina (diluyente1), la nueva solución (solución1) contendría 1/10de la concentración inicial de E. coli. En este ejemplo, la nueva solución (solución1) contendría 10 células de E. coli. Repetir este proceso eliminando 1 ml de la solución1 y añadiéndola a otros 9 ml de solución salina (diluyente2)produciría la solución2,que contiene sólo una sola célula de E. coli. Dado que cada nueva solución (9 ml de diluyente + 1 ml de solución) contiene un total de 10 ml, podemos concluir que el factor de dilución para esta reducción es de 10 o que se trataba de una dilución serial de 10 veces(Figura 1). Puesto que sólo comenzamos con 100 células en este ejemplo y nos estamos diluyendo por un factor de 10, sólo se requieren dos pasos para alcanzar la concentración mínima absoluta de 1 célula.
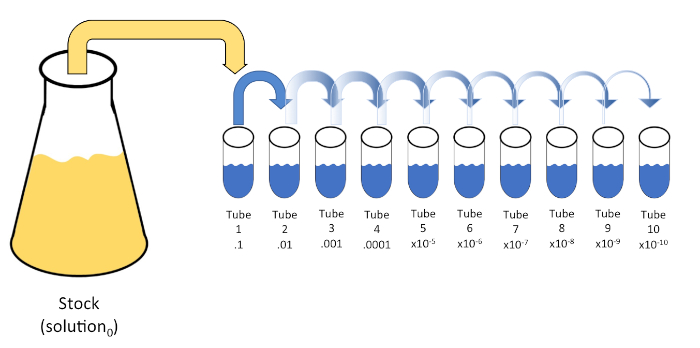
Figura 1: Dilución en serie de una solución de stock. Se añade una alícuota de 1 ml de la solución en stock (solución0) al tubo 1 que contiene 9 ml de solución salina al 0,45% (dilent1); el producto de esta mezcla es la solución1. Repita alístique1 ml de la solución recién creada1 y agregándola al tubo 2. La alícuota y la resuspensión continúan de esta manera hasta que se alcanza el tubo final, diluyendo la concentración de stock por un factor de 10 cada uno con cada paso. Haga clic aquí para ver una versión más grande de esta figura.
La dilución en serie es la técnica más sencilla para obtener concentraciones manejables de un organismo deseado y se complementa con el rayado y la propagación de la placa de petri, sólo dos de las muchas técnicas de chapado utilizadas por los microbiólogos. Este beneficio de este enfoque es que el experimentador puede cosechar cepas puras de una sola especie o cepas separadas de una población mixta (7). El rayado se logra introduciendo un organismo en un medio sólido (generalmente consistente en agarosa) sobre el que crecerá si se dispone de los nutrientes adecuados. Barrer suavemente un bucle inoculante estéril a través del medio (de modo que quede una racha sutil) en un patrón sinusoidal rígido distribuirá el organismo proporcionalmente a la frecuencia de la forma de onda del experimentador. Dividir la placa Petri en tercios o cuartos (racha de cuadrante) y disminuir la frecuencia de cada racha a medida que se introduce una nueva región del plato reducirá gradualmente el número de microorganismos que pueden ocupar esa región, produciendo colonias únicas en lugar de una césped bacteriano incuantificable. El revestimiento extendido no diluye además las muestras; un esparcidor de vidrio estéril se utiliza para distribuir una alícuota de medios de suspensión a través de un plato de petri completo(Figura 2). Las colonias que crecen en la placa de propagación surgen de una sola célula y cada colonia en el plato se puede contar para estimar el número de unidades formadoras de colonias por mililitro (CFU) en una suspensión dada, representada como CFU/mL (6)(Figura 3) Agar suave y réplica El revestimiento son variaciones de las técnicas antes mencionadas y permiten el aislamiento de bacteriófagos y cribado mutante, respectivamente (1,7).
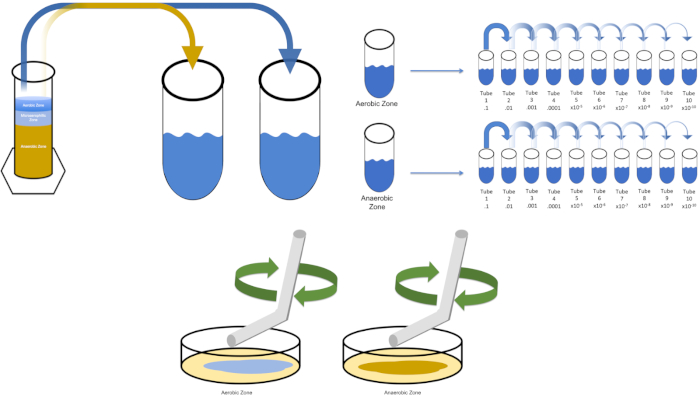
Figura 2: Rayado de placas para la enumeración bacteriana y aislamiento de deformación unitaria. Etiquete la parte inferior de una placa de petri con información de identificación (nombre de bacteria, fecha, medios) y divídala en tercios. Después de seleccionar una dilución adecuada de la muestra de stock, tome un bucle de inoculado estéril (desechable o flameado) y sumerja el tubo de ensayo (aquí, T3). Levante ligeramente la cubierta de la placa de petri en un lado para que sólo el bucle inoculado pueda acceder al agar. Deslice el bucle inoculante a través de la parte superior de los medios de comunicación de una manera en zig-zag teniendo cuidado de no comprometer el agar. Gire la placa aproximadamente 1/3rd (118o) y reduzca la frecuencia del movimiento en zig-zag. Gire una última vez y reduzca la frecuencia en zig-zag una vez más. Haga clic aquí para ver una versión más grande de esta figura.
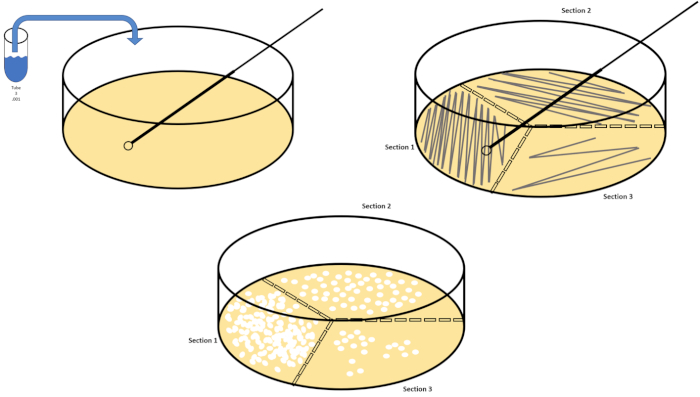
Figura 3: Extender el revestimiento. 1 g de la zona aeróbica se resuspendió en T1 y luego se diluyó en serie. Para distribuir el inóculo por cada plato se utiliza una varilla de esparcimiento desechable de vidrio estéril o plástico para distribuir el inóculo. Esto se repitió con 1 g de la zona anaeróbica. Haga clic aquí para ver una versión más grande de esta figura.
Al igual que con las diluciones en serie, se emplea una escala logarítmica para expresar la concentración del organismo. El número de colonias cultivadas en platos de petri estándar de 100 mm x 15 mm se puede enumerar manualmente (o automatizar con la ayuda del procesamiento computacional) mediante la identificación de racimos aislados de crecimiento. Cuenta que el total de menos de 30 o más de 300 debe definirse como demasiado pocos para contar (TFTC) o demasiado numerosos para contar (TNTC), respectivamente. En el caso de este último, se debe realizar una dilución en serie para reducir la concentración antes de volver a rayar una nueva placa de petri. Promediar el número de colonias autónomas identificadas a partir de tres platos de petri separados y multiplicar la media por el factor de dilución producirá CFU/ml; trazando el registro10 de CFU/ml contra el tiempo revelará el tiempo medio de generación del organismo (7).
Procedure
Applications and Summary
Bacterial enumeration and strain isolation by plating requires manageable concentrations of target organisms. Successful plating is therefore contingent upon serial dilution. As such, the aforementioned techniques remain the cornerstone of microbiological examination and experimentation. Though simple by design, dilution factors and plating technique can be modified to by the experimenter to bolster outcomes without compromising the integrity of each method. Plotting the four phases of bacterial growth can be helpful when characterizing desired microbes. These phases, lag, log, stationary, and death, are marked by changes in bacterial replication. The lag phase features slow growth due to physiological adaptation, the log phase is the period of maximum proliferation featuring an exponential rise in viable cells, stationary phase is then reached due to environmental limitations and accumulations of toxins, before the death phase where cell counts begin to fall. This can be accomplished by serially diluting (or 1-step diluting to avoid confusion) Solution0 every hour for a total of 8 hours, beginning at Time0 (Solution0 should be returned to a shaking incubator after each dilution). Calculate the log10 of CFU/ml for a single diluent of Time0 and plot on the Y-axis. Repeat this calculation for the sample Time1 (make sure calculate CFU/mL using the same dilution factor as Time0). Repeat until each time (Time1-Time8) are plotted on the X-axis.
References
- Allen, M.E., Gyure, R.A. (2013) An Undergraduate Laboratory Activity Demonstrating Bacteriophage Specificity. Journal of Microbial Biological Education 14: 84-92.
- Ben-David, A., Davidson, C.E. (2014) Estimation Method for Serial Dilution Experiments. Journal of Microbiological Methods 107:214-221.
- Goldman, E., Green, L.H. (2008) Practical Handbook of Microbiology.
- Koch, R. (1883) New Research Methods for Detection of Microcosms in Soil, Air and Water.
- Lederberg, J., Lederberg, E.M. (1952) Replica Plating and Indirect Selection of Bacterial Mutants. Journal of Bacteriology 63:399-406
- Pepper, I., Gerba, C., Ikner, L. (2019) Bacterial Growth Curve Analysis and its Environmental Changes. JoVE Science Education Database. Environmental Microbiology.
- Sanders., E.R. (2012) Aseptic Laboratory Technique: Plating Methods. JoVE 63:e3063.
Transcript
Sometimes, in order to identify and study bacteria we first need to isolate and enrich them from a sample. For example, samples obtained from a Winogradsky Column are mixed, meaning they contain multiple species or strains of bacteria, so studying an individual bacterium or enumerating the different kinds present can be challenging. To this end, serial dilution and plating techniques are typically employed to reliably quantify bacterial load and isolate individual colonies.
Serial dilution is a process through which the concentration of an organism, bacteria in this example, is systematically reduced through successive resuspension in fixed volumes of liquid diluent. Usually the volume of the diluent is a multiple of 10 to facilitate logarithmic reduction of the sample organism. For example, one gram of sediment is first removed from the Winogradsky zone of interest and added to 10 milliliters of an appropriate liquid medium. Then, one milliliter of this first dilution is added to another tube containing nine milliliters of medium. The process can be repeated until several different concentrations of bacteria have been prepared. Serial dilution is the key to enumeration of bacteria in this example, since mixed samples from a Winogradsky Column contain an unknown, often large, number of bacteria.
Next, streak plating and spread plating enable the isolation and enumeration of bacteria within a sample, respectively. Streaking is accomplished by introducing a diluted sample to one section of the solid medium supplemented with nutrient, which is divided into thirds. This inoculum is then spread over each third of the plate in a zig-zag pattern. As different sections of the plate are streaked, crossing from the previous sample only once, the sample is spread more thinly. This means that you may only need to streak from one dilution to achieve individual colonies in the later sections. After incubation, the streaked plates allow for observations of colony morphology, information that can help differentiate between different bacterial species.
Alternatively, if the main goal is the enumeration of the bacteria in the sample spread plating may be used. In spread plating, an aliquot of a single sample is spread evenly over the entire surface of solid medium. Typically, because we don’t know the bacterial numbers in the mixed sample, a spread plate is made for each of the dilutions or a representative sample of them. After incubation, enumeration can be performed using these spread plates. Any plates with colony counts fewer than 30 should be discarded, since small counts are subject to greater error. Similarly, any counts over 300 should be discarded because colony crowding and overlapping can lead to underestimation of colony count. If the colony counts of each of these remaining dishes is recorded and multiplied by the dilution factor, and then divided by the volume plated, this yields the colony forming units, or CFUs, per milliliter of suspension. In this video, you will learn how to qualitatively and quantitatively evaluate a sample containing a known bacterium, and the microbial communities contained in various regions of a Winogradsky Column via serial dilution, spread plating, and streak plating.
First, put on any appropriate personal protective equipment including a lab coat, gloves, and goggles. Next, sterilize the workspace with 70% ethanol and wipe down the surface. Next, gather two 500 milliliter Erlenmeyer flasks and label one broth and the other agar. To prepare LB agar solution, mix approximately 6.25 grams of LB agar, three grams of technical agar, and 250 milliliters of distilled water in the flask labeled agar.
Then, prepare LB broth by combining 2. 5 grams of LB media and 100 milliliters of distilled water in the flask labeled broth. After autoclaving the flasks, use a heat resistant glove to remove the flasks from the autoclave and place them in a 40 to 50 degree Celsius water bath. Once the flasks are 50 degrees Celsius, carefully prepare three 100 milliliter aliquots of the broth solution and label each aliquot solution zero. Next, gather 10 sterile petri dishes and label them with the date, name, type of media used, and the Winogradsky Column zone that the organisms will be harvested from. Pipette 15 milliliters of agar from the agar flask into each petri dish. Then, use the pipette tip to remove any bubbles, replace the plate lids, and allow them to solidify on the bench top overnight.
The next day, wipe down the bench top with 70% ethanol. Next, label 10 20 milliliter test tubes T1 through T10 and place them in a rack. Pipette nine milliliters of .45% saline into each tube. Now, cover each of the 10 test tubes loosely with their caps and transfer them to an autoclave-compatible test tube rack. After the cycle is complete, remove the saline blanks using heat resistant gloves and allow them to cool. Store the tubes at room temperature until they have reached approximately 22 degrees Celsius.
To cultivate a known target organism, E. coli in this example, inoculate 100 milliliters of solution zero with a single colony from a previously streaked plate. Then, cover the tube and incubate it over night at 37 degrees Celsius. To evaluate the regions of a Winogradsky Column, add approximately one gram of material from the aerobic zone to T1 and resuspend by vortexing. Then, repeat this process with one gram of material from the anaerobic zone.
Remove the tube containing solution zero inoculated with E. coli from the incubator and shake it. Then, pipette one milliliter of the solution into a T1 test tube and vortex to mix. Remove one milliliter of solution from T1 and transfer it to T2, vortexing to mix. Repeat this process through tube T10. To evaluate the aerobic and anaerobic zones of the Winogradsky Column, remove one milliliter of solution from each of the previously prepared T1 tubes and transfer it to the appropriate T2 tubes. Then, continue the serial dilutions through the T10 tubes as previously demonstrated.
To spread plate, pipette 100 microliters of the diluted sample from each T3 tube on to the corresponding petri dish. Then, use a sterile spreading rod to gently distribute the sample on to the petri dish and replace the plate lid. Repeat this process for the T6 and T9 dilutions, as previously demonstrated. Incubate the plates containing aerobic organisms in a 37 degree Celsius incubator for 24 hours. Incubate the plates containing anaerobic organisms in an anaerobic chamber set to 37 degrees Celsius for 24 hours. The next day remove the T3, T6, and T9 dilution plates from the incubator and the anaerobic chamber and transfer them to the bench top. Working with one plate at a time, glide a sterile inoculating loop across the top of the media in a zig-zag pattern. Then, replace the petri dish lid. Next, rotate the plate by 1/3 and sterilize the loop to reduce the frequency of the previously made zig-zag pattern. Again, after sterilizing the loop, rotate the plate by 1/3, reduce the frequency of the zig-zag pattern one last time, and replace the lid. Repeat this streaking method for the remaining plates, as previously shown. Then, place the streaked plates containing aerobic organisms in a 37 degree Celsius incubator overnight and the streaked plates containing anaerobic organisms in an anaerobic chamber set to 37 degrees Celsius overnight.
Cultures were harvested from the aerobic and anaerobic zones of a seven day Winogradsky Column. Then, the cultures were serially diluted prior to streaking and spreading on LB agar plates. Streaking revealed a mixed population from each of the evaluated Winogradsky zones, and the spread plates produced similar results. A plate streaked from a mixed population will result in bacterial colonies of different shapes, sizes, textures, and colors. In contrast, the streaked and spread plates containing the known organism, E. coli, demonstrated a homologous population. Generally, it is best to calculate CFUs per milliliter using the average colony count of three plates spread with the same sample and dilution factor. Multiply the average number of colonies by the dilution factor and divide by the amount aliquoted. Finally, isolated colonies chosen from each plate can be used in further enrichment assays to determine species identity.
