Summary
تعديل بروتوكول لتوليف 1، 2-ديثيولاني الببتيد، ووصف بنيات سوبراموليكولار الناتجة عن الببتيد التجميع الذاتي.
Abstract
الذاتي تجميع هذا التقرير يركز على توليف 1 و 2-ديثيولاني ن-تيرمينوس تعديل الببتيد تجميع ذاتي والتوصيف لما يترتب على ذلك هياكل سوبراموليكولار. الطريق الاصطناعية يستفيد من الببتيد الصلبة-مرحلة التوليف مع اقتران على راتنج جزيء السلائف ديثيولاني، (أسيتيلثيو)-2-3-حمض بروبانويك (أسيتيلثيوميثيل)، وثيواسيتاتي مساعدة الموجات ديبروتيكشن من الببتيد تعديل تيرمينوس ن قبل الانقسام النهائي من الراتنج تسفر عن 1، 2-ديثيولاني الببتيد. بعد تنقية كروماتوغرافيا سائلة عالية الأداء ([هبلك]) الببتيد ديثيولاني 1 و 2، المستمدة من صميم نوكلياتينج الببتيد Aβ المرتبطة بمرض الزهايمر، ويرد الببتيد لتجميع ذاتي إلى ألياف اميلويد بيتا الصليب. يتم عرض البروتوكولات لتوصيف الألياف اميلويد بتحويل فورييه مطيافية الأشعة تحت الحمراء (الأشعة تحت الحمراء مترا) والتحليل الطيفي تلوانيه دائرية (CD) ومجهر إلكتروني (TEM). يمكن الآن استكشاف أساليب تعديل الطرفي ن مع مجموعة ديثيولاني 1 و 2 الببتيدات تجميع ذاتي تتسم جيدا كنظم نموذجية لوضع استراتيجيات الجمعية بعد التعديل واستكشاف الكيمياء الحيوية التساهمية في الببتيد سوبراموليكولار نانوفيبير الأسطح.
Introduction
السندات ببتيد قوية تشكل الكيمياء تشارك في توليف الببتيد المرحلة الصلبة والقدرة على التحكم في طول التسلسل وتشكيل الببتيدات التي ذاتية التجمع في هياكل supramolecular حقل بحث بشكل كبير. العوامل التي تتحكم في واستقرار هياكل الببتيد تجميعها ذاتيا، بما في ذلك سلسلة جانبية الفراغية والتفاعلات الالكتروستاتيكي، وارتباط الهيدروجين والآثار مسعور1، تكون بمثابة مجموعة من قواعد التصميم. كما تواصل البحث في هذه القواعد الأساسية تصميم إحراز تقدم، الخطوة المنطقية التالية في الببتيد التجميع الذاتي ينطوي على توسيع نطاق تنوع الهياكل القائمة على الببتيد والوظائف. أثناء تجميع ذاتي الببتيدات يتم مادة بيولوجية متعددة الاستخدامات التي تم استخدامها للعديد من التطبيقات الطبية الحيوية بضبط الببتيد تسلسل أو الجمعية الشروط2،3،4، وضع استراتيجيات وتظل الجمعية بعد إدخال تعديلات على الببتيد النانو5،،من67،،من89 منطقة غير مستكشفة نسبيا.
ثنائي كبريتيد دينامية التبادل وثيول الكيمياء على سطح هياكل سوبراموليكولار هو أحد المجالات التي يمكن أن تسفر عن الحيوية الجديدة والوظيفية. إدراج 1، 2-ديثيولاني مويتيس (عادة مشتق من حمض ليبويك (la) أو حمض أسباراجوسيك (أإ)) أبلغ في الحويصلية نظم10،11، كتلة البوليمرات الإسهامية12،13، وكما تنظيم المراسي في الأسطح14،15. هنا، نحن التقرير التوليفي وتوصيف الببتيد تجميع ذاتي المستمدة من جوهر الببتيد Aβ المرتبطة بمرض الزهايمر التي تم تعديلها في المحطة-ن مع 1، 2--ديثيولاني مجموعة الوظيفية16، نوكلياتينج 17. ألياف سوبراموليكولار الناجمة عن ذلك الآن بمثابة منصة تجريبية لدراسة مفاعليه تبادل ثنائي كبريتيد وثيول على سطح سوبراموليكولار من ألياف اميلويد18.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1-تجميع وتنقية من 1، 2-ديثيولاني تعديل الببتيد
- توليف للسلائف ديثيولاني، (أسيتيلثيو)-2-3-حمض بروبانويك (أسيتيلثيوميثيل)19.
- أضف 1 ز 3-برومو-2-(بروموميثيل) حمض البروبيونيك (1 equiv.) حلت في الحد الأدنى من 1 M هيدروكسيد الصوديوم (حوالي 4 مل) إلى قاع جولة 25 مل رد فعل قارورة مع التحريك في 55 درجة مئوية. ختم قارورة رد فعل مع سيتا وإخضاع النيتروجين الغلاف الجوي.
- تحضير محلول يحتوي على 1.49 g ثيواسيتاتي البوتاسيوم (3.2 equiv.) في 4 مل من المياه و 3 مل من حامض الكبريتيك 2 متر (ح2هكذا4) لإنشاء ثيواسيتيك الحمضية في الموقع.
- سحب الحل حمض ثيواسيتيك في محقن بلاستيك المتاح 10 مل ووضع إبرة في المحاقن. إضافة الخليط dropwise إلى قارورة رد فعل بثقب من خلال سيتا مع الإبرة. مواصلة التفاعل بين عشية وضحاها في 55 درجة مئوية.
- مراقبة رد فعل بطبقة رقيقة اللوني (TLC) على ألواح254 هلام السليكا و 60 باستخدام خليط من الميثانول والميثان (1:9). تصور رد فعل التقدم بوصمة عار بروموكريسول الخضراء. المنتج قد Rf = 0.57.
- بعد أن رد الفعل كاملة والمبردة على درجة حرارة الغرفة، أسيديفي الخليط على درجة الحموضة 1 مع 2 م ح2حتى4. يفصل زيت أصفر من الحل.
- استخراج المنتج مع كلوروفورم الباردة (40 مل × 3). الجمع بين الطبقات العضوية وجاف على سلفات المغنيزيوم. إزالة كلوروفورم تحت ضغط انخفاض.
- تأكيد هوية المنتج معزولة، 1، بواسطة مطيافية الرنين المغناطيسي النووي (الرنين المغناطيسي النووي) كما هو موضح في الأرقام 1 باء و جيم. توقع النتائج التالية: 1"ح الرنين المغناطيسي"، كدكل3، 300 ميغاهرتز: د = 10.1 (ب، ح 1)، 3.2 (م، ح 4)، 2.9 (م، ح 1)، 2.4 (ق، ح 6)؛ 13 الرنين المغناطيسي النووي ج، كدكل3، 75 ميغاهرتز: د = 195.1 (CH3جOS-)، 177.6 (-أوهج)، 45.1 (-جح2S-)، 30.5 (جح)، 29.2 (-منظمة شانغهاي للتعاون حج3).
ملاحظة: المنتج هو زيت أصفر وعائد الإجمالي 83 في المائة. استخدام المنتج دون مزيد من التنقية.
- الكائنة واقتران على راتنج من السلائف ديثيولاني
ملاحظة: قد أجرى توليف المرحلة الصلبة الببتيد المبينة أدناه المزج الآلي ببتيد، عقب البروتوكولات الموصى بها الشركة المصنعة. قد تكون إعدادات والكواشف تكييف الصكوك التجارية الأخرى أو عند استخدام الأحماض الأمينية المتخصصة.- تزن بها ز 0.156 حلبة أميد 4-ميثيلبينزيدريلاميني (مبها) راتنج (0.1 ميللي مول) ووضع في وعاء تفاعل. تضخم الراتنج في dimethylformamide (DMF) لمدة 15 دقيقة على الأقل قبل بدء التوليف.
- تزن من 4 معادلات لكل فلورينيلميثيلوكسيكاربونيل (معتدلاً) محمية من الأحماض الأمينية (0.4 ملمول) في تسلسل و 0.152 ز من ن، ن، ن '، ن'-ميثيل-س-(1ح-بينوتريازول-1-يل) اليورانيوم سداسي فلوروفوسفات (0.4 ملمول، هبتو) عن كل الأحماض الأمينية في التسلسل. كل خرطوشة تحتوي على كلا من الأحماض الأمينية المحمية معتدلاً وهبتو.
- بعد تشغيل توليف قبل جميع الشيكات على المزج (الملء الكواشف، مسح خطوط الكاشف والضغط كل كاشف زجاجات)، ضع الخراطيش من الأحماض الأمينية إلى دائري في C 'إلى N' اتجاه المحطة. ضع خرطوشة فارغة بعد الموقف النهائي من الأحماض الأمينية للخطوة النهائية deprotection معتدلاً الطرفي ن.
- توليف الببتيد باستخدام الإعدادات القياسية الموصى بها.
- ديبروتيكت المجموعة معتدلاً من الراتنج مع 5 مل من بيبيريديني 20% في DMF (5 دقيقة × 2).
- أغسل الراتنج مع DMF (6 × 5 مل) قبل الخطوة اقتران.
- لخطوة اقتران واحد، إضافة 4 مل من 0.4 م ن-ميثيلمورفوليني في DMF إلى محمية معتدلاً من الأحماض الأمينية وهبتو. تنشيط الحل المحمية معتدلاً من الأحماض الأمينية لمدة 30 ثانية قبل نقل الحل إلى وعاء التفاعل.
ملاحظة: المزج الآلي الببتيد يمزج الراتنج والحل بالغاز2 ن محتدما كل 30 ثانية لمدة 20 دقيقة بينما رد فعل اقتران يأخذ أماكن. لتوليف الببتيد اليدوي، مكان السفينة رد فعل على شاكر مداري سرعة منخفضة لمدة الخطوة اقتران. - واستنزاف الحل أغسل الراتنج مع DMF (3 x 5 مل).
- كرر الخطوات 1.2.4.1 عن طريق 1.2.4.4 لكل من الأحماض الأمينية المحمية معتدلاً في سي 'إلى N'-الاتجاه تيرمينوس توليف الببتيد للفائدة.
- بعد الخطوة الأخيرة deprotection الطرفي ن، نقل الراتنج في محقن فريتيد المتاح. أغسل الراتنج مع DMF (3 x 5 مل)، والميثان (DCM، مل 3 × 5).
ملاحظة: يمكن تخزين الراتنج بعد DCM غسالة بمجفف فراغ. إذا تم تخزين الراتنج السابقة إلى اقتران، ضمان لتضخم الراتنج في DMF قبل رد فعل اقتران. - زوجان السلائف ديثيولاني (1) إلى N-محطة الببتيد على راتنج بإضافة مكافئات 4 1، 5 مل DMF، مكافئات 4 من هبتو ومكافئات 10 ن، ن-دييسوبروبيليثيلاميني (ديبا). قبل تنشيط اقتران الخليط لمدة 10 دقائق قبل إضافة إلى الراتنج الذي يحتوي على حقنه فريتيد.
- اهتز رد فعل اقتران ح 2. بعد ح 2، يغسل الراتنج مع DMF (3 x 5 مل) وكرر رد فعل اقتران مع المصافحة بين عشية وضحاها.
- بعد اقتران الثانية، يغسل الراتنج مع DMF (3 x 5 مل) و DCM (3 x 5 مل).
ملاحظة: يمكن تخزين الراتنج عند هذه النقطة تحت الفراغ حتى الانقسام.
- Deprotection ثيواسيتاتي والانقسام الببتيد من الراتنج
- ديبروتيكت مجموعة ثيواسيتاتي من السلائف ديثيولاني ن تيرمينوس، نقل راتنج المجففة إلى أنبوب رد فعل الموجات الدقيقة 10 مل وإضافة 2 مل DMF. تسمح الراتنج تضخم، وإضافة شريط إثارة مغناطيسية صغيرة للسفينة، وإعادة تعليق مع انخفاض سرعة إثارة المغناطيسية لمدة 15 دقيقة.
- إضافة 2 مل هيدروكسيد الأمونيوم مركزة وكاب وعاء التفاعل مع سيتا السيليكون ووضع وعاء التفاعل في مفاعل يعمل بالموجات الدقيقة باستخدام إعدادات الموجات الدقيقة 75 درجة مئوية لمدة 45 دقيقة مع التحريك.
- بعد الانتهاء من رد فعل الموجات الدقيقة، نقل الراتنج في محقن فريتيد نظيفة يمكن التخلص منها. يغسل مع DMF (2 × 5 مل) والميثانول (ميوه، مل 2 × 5).
- إضافة حل لتركيز هيدروكسيد الأمونيوم في الميثانول (1:4)، لإجمالي حجم 5 مل. اترك لهزة بين عشية وضحاها زيادة أكسدة ثنائي كبريتيد السندات في خاتم ديثيولاني إينتراموليكولار.
- أغسل الراتنج مع ميوه (2 × 5 مل) و DCM (3 x 5 مل).
ملاحظة: راتنج المجففة قد تكون مخزنة في مجفف فراغ في هذه المرحلة. - إضافة كوكتيل الانقسام إلى الراتنج تحتوي على المحاقن مع تهتز برفق ح 1.5. انشقاق الكوكتيل المستخدمة هي 95% حامض trifluoroacetic (تفا)، ترييسوبروبيلسيلاني 2.5% (نصائح)، والماء 2.5 في المائة في إجمالي حجم 5 مل.
تنبيه: العمل تحت غطاء الأبخرة الكيميائية فقط. تفا متقلبة والتآكل.
ملاحظة: لأغلبية الببتيد تسلسل والأحماض الأمينية sidechain حماية الفئات، أعلاه الانقسام كوكتيل الحل كافية؛ ومع ذلك، الكوكتيل الانقسام البديلة قد يلزم لسلسلة الجانب من الأحماض الأمينية معينة حماية المجموعات (بخاصة الببتيدات المحتوية على Cys Met والراديكالي والأرجنتين) أو غيرها الراتنج كيمياء20. - يعجل الببتيد الخام إلى 25 مل أثير ثنائي إثيل الباردة في أنبوب مخروطي 50 مل بالإضافة دروبويسي من حقنه فريتيد. الببتيد رواسب صلبة بيضاء. بيليه بالطرد المركزي في 1300 غ س للحد الأدنى 10 الببتيد بعناية صب الاثير ثنائي إثيل في حاوية منفصلة لجمع النفايات.
- إضافة آخر 25 مل من الاثير ثنائي إثيل للأنبوبة المخروطية وإعادة تعليق متسرعا واسطة فورتيكسينج. تكرار استخدام الطرد المركزي في 1300 س ز لمدة 10 دقائق، وصب الاثير ثنائي إثيل مرة أخرى. جاف بيليه تحت الفراغ.
- تعديل تنقية من 1، 2-ديثيولاني الببتيد
ملاحظة: تنقية الببتيد الخام بعكس المرحلة-[هبلك]. جمع، والجمع بين قمم الببتيد وتأكيد الكتلة باستخدام TOF الكتلي.- حل بيليه الببتيد الخام في الحد الأدنى من الاسيتو الانيتريل مع 0.1% تفا. نتيجة hydrophobicity الببتيد ونزوع التجميع، بلطف حرارة العينة عند 40 درجة مئوية المعونة في الذوبان.
ملاحظة: تجنب ارتفاع درجات الحرارة وسونيكيشن من الببتيد بغية منع المحتملة ثنائي كبريتيد تبادل ردود الفعل21،،من2223. - لتحضير 1 مل ببتيد الخام لتنقية [هبلك]، إضافة 400 ميكروليتر من مخزون الببتيد تتركز في الاسيتو الانيتريل إلى ميكروليتر 600 من ح2س مع 0.1% تفا وتصفية من خلال عامل تصفية حقنه ميكرومترات 22 في قنينة [هبلك]. يمكن إضافة الايزوبروبانول 5% إضافية لمنع تراكم الببتيد وهطول الأمطار.
- تنقية الببتيد استخدام عمود C-18 شبه محضرة بمعدل تدفق 3 مل/دقيقة عبر تدرج خطي من الاسيتو الانيتريل 15-55% في 20 دقيقة مجموعة كاشفات الأشعة فوق البنفسجية إلى 222 نيوتن متر (أميد العمود الفقري) و 330 نانومتر (ثنائي كبريتيد بوند). جمع، والجمع بين قمم الفائدة (الشكل 2A).
- وتؤكد الكتلة الببتيد المنتج باستخدام TOF مطياف الشامل في وضع ريفليكترون (الشكل 2). لتحليل، مزيج ميكروليتر 0.5 من الذروة التي تم جمعها استخدام لوحة مع ميكروليتر 0.5 2.5-ديهيدروكسيبينزويك حامض (المجالس الصحية المحلية) مصفوفة (10 ملغ/مل المجالس الصحية المحلية في الاسيتو الانيتريل 50%، 0.1% تفا).
ملاحظة: أدوكتس المشتركة في استخدام TOF الكتلي تشمل الصوديوم وملح البوتاسيوم أدوكت ([م + غ]+ و [M + K]+) قمم. ينصح الملحي العينة قبل التحليل إذا قمع قمم adduct الملح إشارة الذروة [M + H]+ الرئيسي. بالإضافة إلى ذلك، ذروة المؤكسدة من [م + س]+ أيضا الكشف عن في الببتيد 1 و 2-ديثيولاني تعديل. تقرير عن الأكسدة الليزر التي يسببها من التأين استخدام استخدام مصفوفة المجالس الصحية المحلية تشير إلى أنه يمكن تعديل عوامل بما في ذلك تركيز العينة، والمذيبات، وكثافة الليزر للحد من القطع الأثرية الأكسدة الناجمة عن استخدام24. - بعد تأكيد استخدام TOF الشامل الصحيح، ليوفيليزي الببتيد بعد تجميد فلاش. الحفاظ على المسحوق الببتيد المجففة بالتبريد تحت الفراغ حتى الجمعية.
- حل بيليه الببتيد الخام في الحد الأدنى من الاسيتو الانيتريل مع 0.1% تفا. نتيجة hydrophobicity الببتيد ونزوع التجميع، بلطف حرارة العينة عند 40 درجة مئوية المعونة في الذوبان.
2-توصيف Supramolecular هياكل التجميع الذاتي
-
تشكيل ألياف اميلويد
- إعداد التجميع الذاتي الحل، تزن من 1 ملغ مسحوق الببتيد استخدام رصيد التحليلي. يذوب في خليط (درجة الحموضة 7.5) من 20% الاسيتو الانيتريل و 10 ملم (4-(2-hydroxyethyl)-1-بيبيرازينيثانيسولفونيك حامض (حبيس) في أنبوب ميكروسينتريفوجي 1.5 مل، بتركيز 1 ملغ/مل الببتيد الجمعية الخليط نهائي. دوامة حل الجمعية وإجازة التجمع عند درجة حرارة الغرفة.
-
توصيف الطيفية لألياف اميلويد
- متابعة عملية الجمعية الببتيد عن طريق تحويل فورييه الأشعة تحت الحمراء (FTIR) التحليل الطيفي كل بضعة أيام. هو ذروة واسعة تتمحور حول 1670 سم-1 توقيع الأشعة تحت الحمراء الناجمة عن الببتيدات مفككة في عينة17. عادة ما تأخذ عينات الجمعية الببتيد مدة أسبوع أو أسبوعين لذروة مفككة واسعة لتختفي والوصول إلى النضج.
- الجاف قاسمة من 8-10 ميكروليتر من حل الجمعية كطبقة رقيقة على الكريستال الماس ATR. رصد اختفاء ذروة المياه كبيرة وواسعة من 1640 إلى 1630 سم-1 كأشكال الفيلم الجافة.
- اكتساب أطياف الأشعة تحت الحمراء من 1500-1800 سم-1 في المتوسط 50 بمسح بدقة-1 سم 2. اكتساب وطرح بمسح الخلفية قبل كل عملية مسح العينة. توقيع الأشعة تحت الحمراء للجمعية ورقة بيتا ذروة حادة بين 1625 و 1635 سم-1 (الشكل 3A)25،26.
- تميز الجمعية الببتيد في الهياكل سوبراموليكولار الغنية β-ورقة بالتعميم تلوانيه (CD). تسجيل الأطياف استخدام سبيكتروبولاريميتير مؤتمر نزع السلاح مع نظام مراقبة درجة حرارة الصفيحة.
- "الماصة؛" ميكروليتر 30 من حل الجمعية في ميكروكوفيتي طول مسار 0.1 مم.
ملاحظة: يلزم حامل خلية المشبك وموضع الخلية طول مسار قصير في الصك. - لكل طائفة، تعيين هذا الصك مؤتمر نزع السلاح إلى المعلمات التالية: مسح الأطوال موجية 300 نانومتر إلى 180 نانومتر، ومعدل المسح من 100/دقيقة، عرض النطاق الترددي 1 نانومتر، 25 درجة مئوية، ومتوسط بفحص ثلاثة.
- جمع طائفة من المخزن المؤقت (20% الاسيتو الانيتريل/10 مم حبيس، درجة الحموضة 7.5) وطرح من كل عملية مسح عينة كعنصر تحكم. توقيع القرص المضغوط لبيتا-أوراق تركزت اليبتيسيتي الحد أدنى حوالي 220 نانومتر (الشكل 3B)27.
- "الماصة؛" ميكروليتر 30 من حل الجمعية في ميكروكوفيتي طول مسار 0.1 مم.
- متابعة عملية الجمعية الببتيد عن طريق تحويل فورييه الأشعة تحت الحمراء (FTIR) التحليل الطيفي كل بضعة أيام. هو ذروة واسعة تتمحور حول 1670 سم-1 توقيع الأشعة تحت الحمراء الناجمة عن الببتيدات مفككة في عينة17. عادة ما تأخذ عينات الجمعية الببتيد مدة أسبوع أو أسبوعين لذروة مفككة واسعة لتختفي والوصول إلى النضج.
-
الفحص المجهري للألياف اميلويد
- السماح لأسبوعين أو ثلاثة أسابيع للعينات الببتيد لتنضج في هياكل supramolecular الغنية β-ورقة.
ملاحظة: يمكن تصويرها التجميعات باستخدام مجهر إلكتروني (TEM) في المراحل المبكرة من عملية الجمعية العامة كذلك.- "الماصة؛" 10 ميكروليتر من حل الجمعية الببتيد إلى سطح الشبكة الكربون TEM.
ملاحظة: الحرص على عدم لمس طرف الماصة على سطح الشبكة. دقة عالية، وذاتية الإغلاق وتستخدم الملقط عقد الشبكة تيم أثناء إعداد. - الانتظار 1-2 دقيقة للسماح للجمعيات الجسميات على سطح الشبكة. إزالة عينة الزائدة بلمس أوراق الترشيح إلى حافة الشبكة.
- تعد وصمة عار خلات اليورانيل 2% بإضافة 100 ميكروليتر من المياه المتاحة تجارياً خلات اليورانيل 4%. "الماصة؛" 10 ميكروليتر من وصمة خلات اليورانيل 2% على سطح الشبكة واحتضان لمدة 2-3 دقائق. بعد الاحتضان، إزالة وصمة عار الزائدة بلمس أوراق الترشيح إلى حافة الشبكة.
- وضع شبكات تيم في مجفف فراغ بين عشية وضحاها. تخزين تحت الفراغ حتى التصوير.
- الصور عينات المعدة مع تيم (الشكل 3). معايير نموذجية للفحص المجهري، على النحو التالي: الصور في تكبير تتراوح بين 9,300 X 23، 000 X، خيوط التنغستن مع جهد متسارع من 120 كيلوفولت.
ملاحظة: يمكن استخدام إيماجيج لقياس عرض متوسط الألياف من هياكل سوبراموليكولار المكتسبة من الصور ال28.
تنبيه: يرجى استشارة جميع صحائف بيانات السلامة ذات الصلة (SDS) قبل الاستخدام. العديد من المواد الكيميائية المستخدمة في التوليف، تنقية، ووصف الببتيدات ذاتية تجميع وصف 1، 2-ديثيولاني تعديل التآكل أو سامة ويجب أن تستخدم إلا تحت غطاء الأبخرة كيميائية. دائماً استخدام معدات الوقاية الشخصية المناسبة (بما في ذلك سلامة النظارات، ومعطف مختبر، كامل طول السراويل، أحذية أغلقت تو) عند العمل في المختبر.
- "الماصة؛" 10 ميكروليتر من حل الجمعية الببتيد إلى سطح الشبكة الكربون TEM.
- السماح لأسبوعين أو ثلاثة أسابيع للعينات الببتيد لتنضج في هياكل supramolecular الغنية β-ورقة.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
وبصرف النظر عن التوليف الأولى خطوة واحدة للجزيء السلائف ديثيولاني، تحدث بقية التوليف الببتيد 1 و 2-ديثيولاني تعديل على دعم قوي (الشكل 1A). تحويل 3-برومو-2-(بروموميثيل) حمض البروبيونيك (أسيتيلثيو)-2-3-حمض بروبانويك (أسيتيلثيوميثيل)، والسلائف ديثيولاني، ما يؤكده 1ح و 13"ج الرنين المغناطيسي النووي" (الشكل 1 باء و جيم) قبل أن يقترن بالحر ن-تيرمينوس أمين من الببتيد لا تزال على راتنج. Deprotection ثيواسيتاتي إلى ثيولس مع هيدروكسيد الأمونيوم تتم باستخدام مفاعل يعمل بالموجات الدقيقة وهو تتأكسد 1، 2-ديثيولاني بين عشية وضحاها في الميثانول قبل هو المشقوق الببتيد 1 و 2-ديثيولاني تعديل من الراتنج. الببتيد الخام يتم تنقيتها بعكس المرحلة [هبلك] (الشكل 2A) وكتلة المنتج هو ما يؤكده TOF استخدام الطيف الكتلي (الشكل 2).
الببتيد ديثيولاني 1 و 2 المنقي تجميع ذاتي إلى ألياف اميلويد ناضجة على مدى فترة 2-3 أسابيع. قدم الأشعة تحت الحمراء (الشكل 3A) والتحليل الطيفي CD (الشكل 3B) تستخدم لمتابعة عملية الجمعية وتميز تكيف β-الورقة الموسعة. يتم تصويرها الألياف بال (الشكل 3).
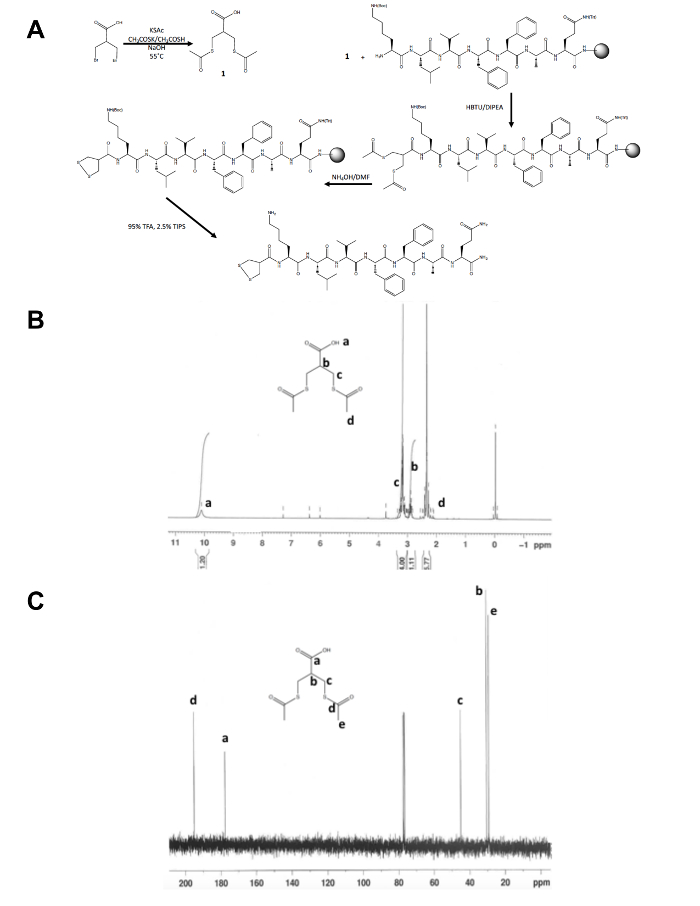
رقم 1. مخطط الاصطناعية لوصف جزيء السلائف 1، 2--ديثيولاني- (أ) مخطط الاصطناعية من الببتيد 1 و 2-ديثيولاني النهائية المعدلة، 1، 2--ديثيولاني--كلففاق--NH2. (ب) 1ح-الرنين المغناطيسي النووي (أسيتيلثيو)-2-3-حمض بروبانويك (أسيتيلثيوميثيل) في كدكل3 في 300 ميغاهرتز. (ج)13ج-الرنين المغناطيسي النووي (أسيتيلثيو)-2-3-حمض بروبانويك (أسيتيلثيوميثيل) في كدكل3 في 75 ميغاهيرتز. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم-

رقم 2. تعديل توليف 1، 2-ديثيولاني الببتيد. تشروماتوجرام (A) [هبلك] من تنقية 1، 2--ديثيولاني--كلففاق--NH2. (ب) يؤكد TOF استخدام الطيف الشامل الذروة الرئيسية من تنقية [هبلك] (الاحتفاظ بزمن ~17.5 دقيقة) في وضع ريفليكترون باستخدام مصفوفة المجالس الصحية المحلية المحسوبة كتلة 1، 2--ديثيولاني--كلففاق--NH2. أدوكتس المشتركة وحددت أيضا. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-

الشكل 3. تعديل وصف 1، 2--ديثيولاني سوبراموليكولار الببتيد. (أ) متر، الأشعة تحت الحمراء ألياف 1، 2--ديثيولاني--كلففاق--NH2 1 ملغ/مل تجميعها في 10 ملم حبيس، درجة الحموضة 7.5 في 20% CH3CN. الذروة في سم 1627-1 يتسق مع الببتيدات تجميعها في تكيف β-ورقة. (ب) مؤتمر نزع السلاح من ألياف 1، 2--ديثيولاني--كلففاق--NH2 1 ملغ/مل تجميعها في 10 ملم حبيس، درجة الحموضة 7.5 في 20% CH3CN. اليبتيسيتي الدنيا في 218 نانومتر ويتسق مع الببتيدات تجميعها في تكيف β-ورقة. (ج) صورة الألياف اميلويد 1، 2--ديثيولاني--كلففاق--NH2 (وصمة سلبية من خلات اليورانيل 2%) بال. شريط الحجم هو 100 نانومتر. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
Subscription Required. Please recommend JoVE to your librarian.
Discussion
تتناول هذه المقالة تفاصيل التقرير التوليفي على حد سواء وتنقية الطرفي ن 1 و 2-ديثيولاني تعديل الببتيد تجميع ذاتي ووصف بنيات سوبراموليكولار الناجمة عن ذلك. تركيب الببتيد ديثيولاني 1 و 2 وذكرت هنا بالمزايا، بما في ذلك تجميع خطوة واحدة لإنتاج السلائف ديثيولاني، (أسيتيلثيو)-2-3-حمض بروبانويك (أسيتيلثيوميثيل)، وعلى الراتنج الميكروويف deprotection رد فعل السلائف ثيواسيتاتي حماية المجموعة الاستسلام moiety المؤكسد 1، 2-ديثيولاني استخدام هيدروكسيد الأمونيوم كما سبق بديلاً أكثر أماناً ل deprotection الهيدرازين السامة29. يمكن تعديل تركيب الببتيد المرحلة الصلبة عموما الببتيد 1، 2-ديثيولاني (الشكل 1A) بسهولة عن طريق تغيير طول التسلسل وتكوينها، بما في ذلك استخدام الأحماض الأمينية غير طبيعية محمية معتدلاً، والكيمياء راتنج ج--المحطة الطرفية لتناسب العديد من التطبيقات البحثية المختلفة.
من أجل منع المنتجات الببتيد غير المرغوب فيها عندما تكون الأحماض الأمينية مع سلاسل تفاعلات جانبية أو الأحماض الأمينية مع حماية مجموعات المنتجات الانقسام القائم على رد الفعل، تضاف الزبالين إضافية إلى الانقسام وكوكتيل20. قد يتم تنفيذ انقسام واختبار نسبة صغيرة (أقل من 10% من مجموع الراتنج) قبل الخطوة deprotection على راتنج الموجات الدقيقة لضمان ارتفاع عائد من اقتران رد فعل. استخدام عمود و [هبلك] الشروط الموصوفة في التقرير، التيس ذروة الببتيد السلائف المحمية 1، 2--ديثيولاني ثيواسيتاتي 5 دقائق بعد الببتيد أونكوبليد أمين مجاناً. إذا تبقى قدرا كبيرا من الببتيد أمين مجاناً، خطوة أخرى اقتران مع (أسيتيلثيو)-2-3-ويوصي بحمض بروبانويك (أسيتيلثيوميثيل). الكشف عن السندات ثنائي كبريتيد إينتراموليكولار 1 و 2-ديثيولاني على [هبلك] برصد امتصاص السندات ثنائي كبريتيد ضعيفة في 330 نانومتر. ويؤكد الذروة [هبلك] الموافق 1 و 2-ديثيولاني المؤكسد إضافة 100 لتر tris(2-carboxyethyl)phosphine(TCEP) 100 مم إلى عينة ببتيد في [هبلك] منفصلة تشغيل. وسيكون ثيول تسيب خفضت المحتوية على الببتيد فترة استبقاء مختلفة من الببتيد ثنائي كبريتيد المؤكسد. ثيول المحتوية على الببتيد التيس حوالي 1 دقيقة يتجاوز الببتيد ثنائي كبريتيد باستخدام العمود والشروط الموضحة في التقرير. مصفوفة استخدام بديل مناسب الببتيدات هو حمض α-سينو-4-هيدروكسيسيناميك (شكا) وهي مستعدة بإضافة 1 مل من الاسيتو الانيتريل 50% مع 0.1% تفا 5 ملغ من شكا. يمكن أن يكون ديسالتيد العينات باستخدام C18 الرمز بريدي نصيحة قبل استخدام TOF التحليل الشامل إذا قمع قمم adduct الملح (Na+ وك+) إلى حد كبير في الذروة [M + H]+ .
التسلسل الببتيد الذي اختير لهذه الدراسات مشتق من المسخ الهولندية من Aβ-الببتيد المرتبطة بمرض الزهايمر30، وقد تبين سابقا لتجميع ذاتي إلى ألياف اميلويد موازية β-أوراق16،17 . كما هو موضح في نتائج تمثيلية، الشكل 3 ألف-جيم، تجميع الببتيد 1، 2--ديثيولاني--كلففاق--NH2 أيضا إلى ألياف اميلويد. أميد فتير أنا تمتد تركزت في سم 1627-1 ومؤتمر نزع السلاح اليبتيسيتي الدنيا في 218 نانومتر هي التوقيعات الطيفية التجميعات β-ورقة25،،من2627، وتمتد الكربونيل CO في 1676 سم-1 المقابلة لأمر الجلوتامين الجانب سلسلة تفاعلات تشير إلى أن يتم تنظيم الببتيدات في β-مسارات متوازية16،،من3132.
صور المجهر الإلكتروني انتقال، استخدام 2% خلات اليورانيل وصمة سلبية، تظهر ألياف سوبراموليكولار الموسعة والتواء هي حوالي 10 نانومتر في العرض. الألياف الببتيد ن--المحطة الطرفية أسيتيلاتيد، ميلان-كلففاق-NH2، على نحو سلس ومستقيم، مع عرض أكبر قليلاً من شمال البحر الأبيض المتوسط ما يقرب من 1216. منذ إعداد الشبكات تيم وحيازة الصور عملية مكثفة وقت، فمن الأفضل لإعداد شبكات تيم العديد من نفس العينة الجمعية مرة واحدة لاختلاف تركيزات الببتيد. إعداد عينة مخفف لل (01:50 أو 1: 100) جنبا إلى جنب مع العينة حل الجمعية الأصلية. ألياف اميلويد في تركيزات عالية قد تنضم إلى الشبكة في كتل أو بقع وحيازة صور للألياف الفردية قد يكون صعباً. من المهم أن نرى حواف الألياف الفردية لقياسات العرض والتصور من الألياف الظاهرة غالباً ما تحجب عينات مكتظة.
كما يجري استكشاف المزيد من التطبيقات باستخدام سوبراموليكولار الحيوية، هناك حاجة إلى دمج رد الفعل المحتمل من المجموعات الوظيفية التي متعامد على عملية التجميع الذاتي في مونومرات تجميع ذاتي. الأساليب المذكورة في هذا التقرير تسليط الضوء على نهج على راتنج لتوليف الببتيد 1 و 2-ديثيولاني تعديل تجميع ذاتي وتوصيف الطيفية للهياكل سوبراموليكولار.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
الكتاب ليس لها علاقة بالكشف عن.
Acknowledgments
يود المؤلفون أن أشكر الدكتور باء الين سكانليي لها التدريب التقني والمساعدة في استخدام ال في ولاية كونيتيكت الدولة الكليات والجامعات (كسكو) مركز لتكنولوجيا النانو، والدكتور إيشيتا مكرجي في جامعة ويسليان للوصول إلى القرص المضغوط لها جهاز المطياف الضوئي. كان دعم عمل ذكرت في جزء من معهد العلوم في جامعة فيرفيلد، "الكونسورتيوم منحة مساحة كونيتيكت ناسا"، والمؤسسة الوطنية للعلوم تحت عدد المنح تشي-1624774.
Materials
| Name | Company | Catalog Number | Comments |
| Rink amide MBHA resin, high load | Gyros Protein Technologies | RAM-5-HL | Avoid contact with skin and eyes; do not inhale |
| N,N-Dimethylformamide | Fisher Scientific | D119-4 | Flammable liquid and vapor; irritating to eyes and skin; Use personal protective equipment; keep away from open flame |
| Fmoc-L-Val-OH | Gyros Protein Technologies | FLA-25-V | Wear personal protective equipment; do not inhale |
| Fmoc-L-Leu-OH | Gyros Protein Technologies | FLA-25-L | Wear personal protective equipment; do not inhale |
| Fmoc-L-Lys(Boc)-OH | Gyros Protein Technologies | FLA-25-KBC | Wear personal protective equipment; do not inhale |
| Fmoc-L-Phe-OH | Gyros Protein Technologies | FLA-25-F | Wear personal protective equipment; do not inhale |
| Fmoc-L-Ala-OH | Gyros Protein Technologies | FLA-25-A | Wear personal protective equipment; do not inhale |
| Fmoc-L-Gln(Trt)-OH | Gyros Protein Technologies | FLA-25-QT | Wear personal protective equipment; do not inhale |
| N,N,N′,N′-Tetramethyl-O-(1H-benzotriazol-1-yl)uronium hexafluorophosphate | Gyros Protein Technologies | 26432 | Causes skin, eye and respiratory irritation; do not inhale; use under hood or in well ventilated area |
| 0.4 M N-methylmorpholine in DMF | Gyros Protein Technologies | PS3-MM-L | highly flammable; wear personal protective equipment; keep away from heat and keep container tightly closed; do not inhale or swallow; wash skin thoroughly after handling |
| 20% piperidine in DMF | Gyros Protein Technologies | PS3-PPR-L | Causes severe eye and skin burns; Flammable Liquid and vapor; Do not inhale |
| dichloromethane | Fisher Scientific | D37-4 | May cause cancer; Do not inhale; Wear personal protective equipment; use under hood only; if contacted rise with water for at least 15 minutes and obtain medical attention |
| acetonitrile | Fisher Scientific | A998-4 | Flammable; irritating to eyes; Use personal protective equipment; Use only under a fume hood; keep away from open flame or hot surface; if contacted rinse wiith water for at least 15 minutes and obtain medical attention |
| trifluoroacetic acid | Fisher Scientific | A116-50 | Causes severe burns; do not inhale; harmful to aquatic life; use personal protective equipment; use only under fume hood; if contacted rinse with water for at least 15 minutes and obain immediate medical attention |
| 4% uranyl acetate | Electron Microscopy Sciences | 22400-4 | Do not inhale; harmful to aquatic life |
| 4-(2-Hydroxyethyl)piperazine-1-ethanesulfonic acid | Acros Organics | AC172571000 | Do not inhale; use outdoors or in well-ventilated area |
| nitrogen Gas | TechAir | Contents under pressure, may explode if heated | |
| 3-bromo-2-(bromomethyl)propionic acid | Alfa Aesar | AAA1963014 | Do not inhale; causes irritation to skin and eyes; corrosive |
| sodium hydroxide | Fisher Scientific | S318-100 | Use personal protective equipment; use only under fume hood; if contact rinse area for at least 15 minutes and obtain medical attention |
| potassium thioacetate | Acros Organics | AC221300250 | Causes skin and eye irritation; do not inhale; use personal protective equipment |
| sulfuric acid | Fisher Scientific | SA213 | Causes burns; keep away from water; keep away from combustible material; do not inhale; use personal protective equipment; if contact rinse area for at least 15 minutes and obtain medical attention |
| chloroform-d | Acros Organics | AC320690075 | Possible cancer hazard; irritating to skin and eyes; do not inhale; Use personal protective equipment; use only under fume hood; If contact rinse area for at least 15 minutes and obtain medical attention |
| chloroform | Fisher Scientific | C298-4 | Possible cancer hazard; irritating to skin and eyes; do not inhale; Use personal protective equipment; use only under fume hood; If contact rinse area for at least 15 minutes and obtain medical attention |
| N,N-diisopropylethylamine | Acros Organics | AC367841000 | Highly flammable; harmful to aquatic life; wear personal protective equipment; do not swallow |
| ammonium hydroxide | Fisher Scientific | A669S-500 | Corrosive; do not inhale |
| methanol | Fisher Scientific | A452-4 | Flammable liquid and vapor; use personal protective equipment; do not inhale; If contact rinse area for at least 15 minutes and obtain medical attention |
| triisopropylsilane | Sigma Aldrich | 233781 | Flammable; use personal proctective safety equipment; keep container tightly closed |
| diethyl ether | Fisher Scientific | E138-1 | Extremely flammable; Irritating to skin and eyes; Use personal protective equipment |
| 2,5-dihydroxybenzoic acid | Sigma Aldrich | 39319-10x10MG-F | do not inhale; irritating to skin and eyes |
| alpha-cyano-4-hydroxycinnamic acid | Alfa Aesar | AAJ67635EXK | |
| c18 zip-tip | Millipore | ZTC18S096 | |
| tris(2-carboxyethyl) phospine hydrochloride | Thermo Scientific | PI20490 | |
| silica gel 60 F254 coated aluminum-backed TLC sheets | EMD Millipore | 1.05549.0001 | |
| Thin walled Precision NMR tubes | Bel-Art | 663000585 | 5mm O.D. |
| All-plastic Norm-Ject syringes | Air Tite | AL10 | |
| single-use needle | BD PrecisionGlide | BD 305185 | used needles get disposed on in sharps waste container |
| disposable fritted syringe | Torviq | SF1000LL | 10mL fritted syringes were used in the report, but larger syringes are avaibale if needed for larger scale synthesis. |
| carbon grid | Ted Pella, Inc. | CF200-CU | Make sure to prepare samples and staining on the carbon grid side, not the shiny copper side of grid |
| self-closing tweezers | Electron Microscopy Sciences | 78318-3X | very sharp tips, length: 120 mm |
| 0.1 mm short path length cell | Starna Cells, Inc. | 20/C-Q-0.1 | Fragile |
| 10mL Vessel Caps | CEM | 909210 | |
| 10mL Pressure Vessels | CEM | 908035 | |
| Aeris Semi-Prep HPLC column | Phenomenex | 00F-4632-N0 | 150 x 10mm |
| cell holder | Starna Cells, Inc. | CH-2049 | Needed when using short pathlength cells |
| PS3 peptide synthesizer | Gyros Protein Technologies | ||
| DiscoverSP Microwave Reactor | CEM | ||
| centrifuge | HERMLE | Z 206 A | used a fixed 6x50 mL rotor |
| HPLC | Shimadzu | UV Detector | |
| nuclear magnetic resonance spectrometer | Avance, Bruker | 300 MHz | |
| MALDI-TOF mass spectrometer | Axima Confidence, Shimadzu | ||
| lyophilizer | Millrock Technology | BT85A | |
| Fourier-Transform Infrared Spectrometer | Alpha Tensor, Bruker | ||
| Transmission Electron Microscope | Tecnai Spirit, FEI | Used with Gatan Orius Fiberoptic CCD digital camera. Accessed at CSCU Center for Nanotechnology | |
| Circular Dichroism Spectropolarimeter | J-810, JASCO | Used with a six-cell Peltier temperature controller. Accessed at Wesleyan University. |
References
- Wang, J., Liu, K., Xing, R., Yan, X. Peptide self-assembly: Thermodynamics and kinetics. Chemical Society Reviews. 45, 5589-5604 (2016).
- Dong, R., et al. Functional supramolecular polymers for biomedical applications. Advanced Materials. 27, 498-526 (2015).
- Edwards-Gayle, C. J. C., Hamley, I. W. Self-assembly of bioactive peptides, peptide conjugates, and peptide mimetic materials. Organic and Biomolecular Chemistry. 15, 5867-5876 (2017).
- Goor, O. J. G. M., Hendrikse, S. I. S., Dankers, P. Y. W., Meijer, E. W. From supramolecular polymers to multi-component biomaterials. Chemical Society Reviews. 46, 6621-6637 (2017).
- DiMaio, J. T. M., Doran, T. M., Ryan, D. M., Raymond, D. M., Nilsson, B. L. Modulating supramolecular peptide hydrogel viscoelasticity using biomolecular recognition. Biomacromolecules. 18, 3591-3599 (2017).
- DiMaio, J. T. M., Raymond, D. M., Nilsson, B. L. Display of functional proteins on supramolecular peptide nanofibrils using a split-protein strategy. Organic and Biomolecular Chemistry. 15, 5279-5283 (2017).
- Mahmoud, Z. N., Gunnoo, S. B., Thomson, A. R., Fletcher, J. M., Woolfson, D. N. Bioorthogonal dual functionalization of self-assembling peptide fibers. Biomaterials. 32, 3712-3720 (2011).
- Petkau-Milroy, K., Uhlenheuer, D. A., Spiering, A. J. H., Vekemans, J. A. J. M., Brunsveld, L. Dynamic and bio-orthogonal protein assembly along a supramolecular polymer. Chemical Science. 4, 2886-2891 (2013).
- Li, A., et al. Neurofibrillar tangle surrogates: Histone H1 binding to patterned phosphotyrosine peptide nanotubes. Biochemistry. 53, 4225-4227 (2014).
- Sadownik, A., Stefely, J., Regen, S. L. Polymerized liposomes formed under extremely mild conditions. Journal of the American Chemical Society. 108, 7789-7791 (1986).
- Zhang, N., et al. ATN-161 Peptide functionalized reversibly cross-linked polymersomes mediate targeted doxorubicin delivery into melanoma-bearing C57BL/6 mice. Molecular Pharmaceutics. 14, 2538-2547 (2017).
- Margulis, K., et al. Formation of polymeric nanocubes by self-assembly and crystallization of dithiolane-containing triblock copolymers. Angewandte Chemie International Edition. 56, 16357-16362 (2017).
- Zhang, X., Waymouth, R. 1,2-Dithiolane-Derived Dynamic, Covalent Materials: Cooperative Self-Assembly and Reversible Cross-Linking. Journal of the American Chemical Society. 139, 3822-3833 (2017).
- Sakia, N., Matile, S. Stack exchange strategies for the synthesis of covalent double-channel photosystems by self-organizing surface-initiated polymerization. Journal of the American Chemical Society. 133, 18542-18545 (2011).
- Uji, H., Morita, T., Kimura, S. Molecular direction dependence of single-molecule conductance of a helical peptide in molecular junction. Physical Chemistry Chemical Physics. 15, 757-760 (2013).
- Liang, C., Ni, R., Smith, J. E., Childers, W. S., Mehta, A. K., Lynn, D. G. Kinetic intermediates in amyloid assembly. Journal of the American Chemical Society. 136, 15116-15149 (2014).
- Smith, J. E., et al. Defining the dynamic conformational network of cross-β peptide assembly. Israel Journal of Chemistry. 55, 763-769 (2015).
- Black, S. P., Sanders, J. K. M., Stefankiewicz, A. R. Disulfide exchange: Exposing supramolecular reactivity through dynamic covalent chemistry. Chemical Society Reviews. 43, 1861-1872 (2014).
- Vendetti, A., et al. Dihydroasparagusic acid: Antioxidant and tyrosinase inhibitory activities and improved synthesis. Journal of Agricultural and Food Chemistry. 61, 6848-6855 (2013).
- Stawikowski, M., Fields, G. B. Introduction to peptide synthesis. Current Protocols in Protein Science. 26, (2002).
- Canadell, J., Goossens, H., Klumperman, B. Self-healing materials based on disulfide links. Macromolecules. 44, 2536-2541 (2011).
- Lafont, U., van Zeijl, H., van der Zwaag, S. Influence of cross-linkers on the cohesive and adhesive self-healing ability of polydisulfide-based thermosets. ACS Applied Materials and Interfaces. 4, 6280-6288 (2012).
- Komaromy, D., Stuart, M. C. A., Santiago, G. M., Tezcan, M., Krasnikov, V. V., Otto, S. Self-assembly can direct dynamic covalent bond formation toward diversity or specificity. Journal of the American Chemical Society. 139, 6234-6241 (2017).
- McAvery, K. M., Guan, B., Fortier, C. A., Tarr, M. A., Cole, R. B. Laser-induced oxidation of cholesterol observed during MALDI-TOF mass spectrometry. Journal of the American Society for Mass Spectrometry. 22, 659-669 (2011).
- Krimm, S., Bandekar, J. Vibrational spectroscopy and conformation of peptides, polypeptides, and proteins. Advances in Protein Chemistry. 38, 181-364 (1986).
- Halverson, K. J., Sucholeiki, I., Ashburn, T. T., Lansbury, P. T. Location of β-sheet-forming sequences in amyloid proteins by FTIR. Journal of the American Chemical Society. 113, 6701-6703 (1991).
- Greenfield, N., Fasman, G. D. Computed circular dichroism spectra for the evaluation of protein confirmation. Biochemistry. 8, 4108-4116 (1969).
- Rasband, W. S. ImageJ. , National Institutes of Health. Bethesda, Maryland, USA. Available from: https://imagej.nih.gov/ij (2016).
- Roy, S., Shinde, S., Hamilton, G. A., Hartnett, H. E., Jones, A. K. Artificial [FeFe]-hydrogenase: On resin modification of an amino acid to anchor a hexacarbonyldiiron cluster in a peptide framework. European Journal of Inorganic Chemistry. 2011, 1050-1055 (2011).
- Van Duinen, S. G., Castano, E. M., Prelli, F., Bots, G. T. A. B., Luyendijk, W., Frangione, B. Hereditary cerebral hemorrhage with amyloidosis in patients of Dutch origin is related to Alzheimer disease. Proceedings of the National Academy of Sciences of the United States of America. 84, 5991-5994 (1987).
- Barth, A. The infrared absorption of amino acid sidechains. Progress in Biophysics and Molecular Biology. 74, 141-173 (2000).
- Jayaraman, M., et al. Slow amyloid nucleation via α-helix-rich oligomeric intermediates in short polyglutamine-containing Huntingtin fragments. Journal of Molecular Biology. 415, 881-899 (2012).



