Universal och effektivt elektroporationprotokoll för genteknik av gastrointestinala organoider
Summary
Detta protokoll beskriver en effektiv elektroporationmetod för transfection av fyra olika gastrointestinala organoidenheter med större plasmider (i den grad av 10 kB). Det kan utföras inom en dag och behöver inte omfattande förberedelse eller speciella, kostnadsintensiva elektroporation buffertar.
Abstract
Elektroporation är en vanlig metod för transfection med olika typer av molekyler genom elektrisk permeabilisering av plasmamembranet. Med den ökande användningen av organoider som en odlingsmetod för primärt patientmaterial under de senaste åren, effektiva överföringsmetoder av komponenter för genteknik i detta 3D-kultursystem är i behov. Speciellt för organoider beror effektiviteten av genetiska manipulationer på en framgångsrik transfection. Således utvecklades detta protokoll för att underlätta elektroporation av organoider och att bevisa sin universella funktionalitet i olika enheter. Human kolorektal, pankreas, lever och magcancer organoider var framgångsrikt elektroporated med små och stora plasmider i jämförelse. Baserat på GFP-kodningsvektorer bestämdes transfectioneffektiviteten av FACS. Ingen omfattande beredning av cellerna eller speciella, kostnadsintensiva elektroporationbuffertar är nödvändiga, och protokollet kan utföras inom en dag.
Introduction
Under de senaste åren har ett nytt 3D-cellskultursystem, kallat organoider, utvecklats för olika normala och cancerogena vävnader. Organoider är funktionellt och morfologiskt mycket nära sin vävnad av ursprung. De kan genereras från olika arter, är lätt utbyggbara, genomiskt stabila och genetiskt modifierbara, vilket gör dem till ett idealiskt modellsystem för genetiska undersökningar1,2,3. Genteknik tekniker som CRISPR (Clustered Regelbundet Interspaced Short Palindromic Upprepar)/Cas9-systemet möjliggör olika manipulationer. Valet av kloner kan realiseras genom definierade medievillkor, till exempel av WNT ligand tillbakadragande för APC (Adenomatosis Polyposis Coli) knockout kloner4,5. Alternativt måste urvalsmarkörer införas genom homologriktad reparation av en inriktningsvektor6,7. På grund av det faktum att ofta mer än en plasmid måste införas, blir en effektiv transfection en avgörande parameter. Dessutom, för att minska ospecifika off-target effekter, ett övergående uttryck för Cas9 endonuclease är önskvärt8.
Elektroporation är en jämförelsevis enkel metod för transfect celler med DNA, RNA, proteiner eller andra makromolekyler. Med hjälp av elektriska pulser blir cellmembranet mer genomsläppligt och orsakar ett ökat upptag9. I ett tidigare publicerat elektroporationsprotokoll av kolonorganoider nåddes en 30% effektivitet med en piggy-bac GFP (grönt fluorescerande protein) som uttrycker vektor (7,4 kB) i ett fyra dagar förfarande10. Följande protokoll utvecklades för att underlätta en effektiv transfection av cancerogena eller friska organoider med stora plasmider kodning för enda guide RNA (sgRNA) och Cas9 endonuclease sekvens (t.ex. px458 som vektor med 9,3 kb). Hela elektroporationsprocessen kan utföras inom en dag, utan speciella elektroporationsbuffertar, och med åtminstone jämförbara effektivitetsvinster mellan olika gastrointestinala organoider, nämligen bukspottskörteln duktal adenocarcinom (PDAC), kolorektal cancer (CRC), cholangiocarcinoma (CCC) och magcancer (GC) organoider.
Protocol
Representative Results
Discussion
Detta protokoll ger detaljerade instruktioner för en effektiv, snabb och lätt att utföra elektroporation av olika organoidenheter. Utöver den presenterade tumör organoider från PDAC, CRC, CCC och GC, det fungerar framgångsrikt för organoider som härrör från frisk vävnad också. Protokollet kan utföras inom en dag. I publicerade organoid transfection protokoll hela förfarandet varade fyra dagar inklusive två dagar av preparat med olika typer av odlingsmedier10,21. I vårt protokoll krävs ingen särskild förbehandling. Genom att tvätta med elektroporation buffert innan elektroporation de antibiotiska komponenterna i media spolades ut och en justering av mättnadkoncentrationer för optimala impedansvärden uppnåddes. Vissa kritiska aspekter bör dock övervägas för en framgångsrik elektroporation:
Celler
I elektroporationprotokollet av Fujii et al.10 rekommenderas att ta isär organoider till enstaka celler och filtrera dem genom en 20 μm cellsil. I våra händer matsmältningen till enstaka celler minskar starkt överlevnadsförmågan hos celler. Som föreslås i Merenda et al.21,vi också separerat organoider till kluster av 10-15 celler och kunde inte bestämma en minskad effektivitet jämfört med enstaka celldissociation. Efter elektroporation är det ett mycket viktigt steg för att separera det vita skummet, så att inga bifogade celler går vilse.
För 2D cellkultur har det visat sig att en regenereringstid efter elektroporation på mer än 10 min upp till 40 min ökar överlevnadsförmågan och transfection effektivitet särskilt av stora plasmider22. I testexperiment kan detsamma dokumenteras för organoider, vilket leder till ett inkubationssteg på 40 min efter elektroporation i detta protokoll. För att öka återhämtningen från elektroporationen odlade vi dem med Rho-associerade proteinkinas (ROCK) hämmare Y-27632 i fem till sju dagar23. På samma sätt är ytterligare tillskott av glykogen syntas kinas 3 (GSK3) hämmare CHIR99021 tänkt att hjälpa enstaka celler att återhämta sig10.
Inställningar
En av fördelarna med den använda elektroporatorären är att impedansen kan mätas före elektroporation för optimala förhållanden. Enligt tillverkaren ska impedansvärdena vara 30-55 Ω. I våra händer har impedansvärden på 30-40 Ω visat optimal effektivitet. I ett preliminärt experiment varierades olika spänningar och pulslängdsvärden i poringpulsen för att hitta den optimala andelen effektivitet till överlevnadsförmåga. Sammanfattningsvis kan vi bekräfta de beskrivna värdena för Fujii et al.10 i de olika enheter som beskrivs här.
Dna
Effekten av olika DNA-mängder testades i preliminära experiment upp till 45 μg DNA per prov. Inga cytotoxiska effekter kunde upptäckas. Transfection effektiviteten ökade på ett dosberoende sätt med mättnad > 30 μg. Så använde vi 30 μg per prov i slutprotokollet, men naturligtvis kan det ökas (t.ex. för elektroporation av fler plasmider parallellt). Dessutom verkar renhet och koncentration av DNA vara mycket viktigt. En koncentration som överstiger 5 μg/μL har visat optimal transfection effektivitet.
Som väntat kan 9,3 kB plasmid transfected med en lägre effektivitet än den mindre 4,2 kB plasmid (se figur 4). Användningen av ännu större plasmider än 10 kB förväntas ytterligare minska effektiviteten. För framtida tillämpningar kan det vara intressant att testa minicircle DNA som vektor, eftersom dessa genbärare saknar bakterieryggraden i en plasmid som gör dem mindre24. Detta bör leda till en förbättrad transfection effektivitet. Dessutom, för CRISPR-baserade manipulationer av organoider en direkt elektroporation av sgRNAs bunden till Cas9 som en ribonucleoprotein (RNP) komplex kan vara ett alternativ eller tillägg25.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi tackar Juliane Fohgrub, Ann-Christin Meinecke och Max Heiduk för utmärkt teknisk hjälp. Finansiering tillhandahölls av Deutsche Krebshilfe (nr 111350 och 70112925), Sander Stiftung (nr 2014.104.1), Hector Stiftung (nr M65.2) och Europeiska unionen (ERC nr 639050).
Materials
| For establishment and culture medium | |||
| [Leu15] Gastrin | Sigma-Aldrich | G9145 | |
| A83-01 | Tocris Bioscience | 2939 | |
| Advanced DMEM/F-12 | Invitrogen | 12634010 | |
| B27 | Invitrogen | 17504044 | |
| B27 Supplement, minus vitamin A | Thermo Fisher Scientific | 12587010 | |
| CHIR99021 | Stemgent | 04-0004 | |
| Collagenase II | Life Technologies | 17101-015 | |
| Collagenase XI | Sigma-Aldrich | C9407-100MG | |
| Collagenase D | Roche | 11088866001 | |
| Dispase II | Roche | 4942078001 | |
| Dnase I | Sigma-Aldrich | D5319 | |
| D-sorbitol | Roth | 6213.1 | |
| Dithiothreitol | Thermo Scientific | 1859330 | |
| EDTA | Roth | 8040 | |
| Forskolin | Tocris Bioscience | 1099 | |
| Glutamax | Life Technologies | 35050061 | |
| Hepes | Thermo Fisher Scientific | 15630106 | |
| hFGF-10 | Preprotech | 100-26 | |
| KCl | Sigma-Aldrich | P9541 | |
| KH2PO4 | Roth | 3904.2 | |
| Matrigel | Corning | 356231 | basement matrix |
| mEGF | Invitrogen | PMG8043 | |
| N2 | Invitrogen | 17502048 | |
| NaCl | Roth | 3957.1 | |
| Na2HPO4 | Roth | K300.2 | |
| N-Acetyl-L-Cystein | Sigma-Aldrich | A9165 | |
| Nicotinamid | Sigma-Aldrich | N0636 | |
| Noggin | n.a. | n.a. | Conditioned medium produced from HEK293 cells (Hek293-mNoggin-Fc) |
| PBS | Gibco | 14190169 | |
| Penicillin Streptomycin | Life Technologies | 15140122 | |
| Primocin | InvivoGen | ant-pm-1 | |
| Prostaglandin E2 | Tocris Bioscience | 2296 | |
| Recombinant Human HGF | Preprotech | 100-39H | |
| Rspondin | n.a. | n.a. | Conditioned medium produced from HEK293 cells (HA-Rspo1-Fc-293T) |
| SB202190 | Sigma-Aldrich | S7067 | |
| Sucrose | VWR | 27,480,294 | |
| TrypLE Express | Gibco | 12604021 | Dissociation reagent |
| Wnt3A | n.a. | n.a. | Conditioned medium produced from L-Wnt3a cells (from Sylvia Boj) |
| Y-27632 | Sigma-Aldrich | Y0503 | |
| Consumables | |||
| Cell Strainer 100 µm | Falcon | 352360 | |
| 48-well plate | Corning | 3548 | |
| Nepa Electroporation Cuvettes 2mm gap w/pipettes | Nepa Gene Co., Ltd. | EC-002S | |
| Tubes 15 ml | Greiner | 188271 | |
| Tubes 15 ml low binding | Eppendorf | 30122208 | Tubes for FACS preparing |
| Equipment | |||
| Electroporator Nepa21 | Nepa Gene Co., Ltd. | n.a. | |
| EVOS FL Auto | Invitrogen | AMAFD1000 | Fluorescence microscope |
| LSRFortessa | BD Bioscience | 647800E6 | FACS |
| Reagents and plasmids | |||
| Live/dead fixable blue dead cell stain kit | Invitrogen | L34962 | Includes antibody for live/dead staining for FACS analysis |
| EndoFree Plasmid Maxi Kit | Qiagen | 12362 | |
| Nutlin-3 | Selleckchem | S1061/07 | |
| Opti-MEM | Gibco | 31985047 | Electroporation buffer |
| 2 gRNA concatemer vector | AddGene | 84879 | |
| pCMV-EGFP | Nepa Gene Co., Ltd. | n.a. | |
| px458 plasmid | AddGene | 48138 | coding for sgRNA and Cas9 |
| px458_Conc2 plasmid | AddGene | 134449 | px458 plasmid containing 2x U6 promotors for two different sgRNAs |
| sgRNA_hTP53_1a | Eurofins Genomics | n.a. | 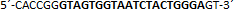 |
| sgRNA_hTP53_1b | Eurofins Genomics | n.a. | 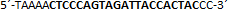 |
| sgRNA_hTP53_2a | Eurofins Genomics | n.a. | 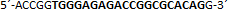 |
| sgRNA_hTP53_2b | Eurofins Genomics | n.a. | 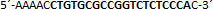 |
References
- Huch, M., et al. Long-term culture of genome-stable bipotent stem cells from adult human liver. Cell. 160 (1-2), 299-312 (2015).
- Werner, K., Weitz, J., Stange, D. E. Organoids as Model Systems for Gastrointestinal Diseases: Tissue Engineering Meets Genetic Engineering. Current Pathobiology Reports. 4 (1), 1-9 (2016).
- Olayanju, A., Jones, L., Greco, K., Goldring, C. E., Ansari, T. Application of porcine gastrointestinal organoid units as a potential in vitro tool for drug discovery and development. Journal of applied toxicology. 39 (1), 4-15 (2019).
- Drost, J., et al. Sequential cancer mutations in cultured human intestinal stem cells. Nature. 521 (7550), 43-47 (2015).
- Matano, M., et al. Modeling colorectal cancer using CRISPR-Cas9-mediated engineering of human intestinal organoids. Nature Medicine. 21 (3), 256-262 (2015).
- Schwank, G., et al. Functional repair of CFTR by CRISPR/Cas9 in intestinal stem cell organoids of cystic fibrosis patients. Cell Stem Cell. 13 (6), 653-658 (2013).
- Drost, J., et al. Use of CRISPR-modified human stem cell organoids to study the origin of mutational signatures in cancer. Science. 358 (6360), 234-238 (2017).
- Zhang, X. H., Tee, L. Y., Wang, X. G., Huang, Q. S., Yang, S. H. Off-target Effects in CRISPR/Cas9-mediated Genome Engineering. Molecular Therapy Nucleic Acids. 4, e264 (2015).
- Tsong, T. Y. Electroporation of cell membranes. Biophysical journal. 60 (2), 297-306 (1991).
- Fujii, M., Matano, M., Nanki, K., Sato, T. Efficient genetic engineering of human intestinal organoids using electroporation. Nature Protocols. 10 (10), 1474-1485 (2015).
- Sato, T., et al. Long-term expansion of epithelial organoids from human colon, adenoma, adenocarcinoma, and Barrett’s epithelium. Gastroenterology. 141 (5), 1762-1772 (2011).
- Bartfeld, S., et al. In vitro expansion of human gastric epithelial stem cells and their responses to bacterial infection. Gastroenterology. 148 (1), 126-136 (2015).
- Boj, S. F., et al. Organoid models of human and mouse ductal pancreatic cancer. Cell. 160 (1-2), 324-338 (2015).
- Broutier, L., et al. Culture and establishment of self-renewing human and mouse adult liver and pancreas 3D organoids and their genetic manipulation. Nature Protocols. 11 (9), 1724-1743 (2016).
- Broutier, L., et al. Human primary liver cancer-derived organoid cultures for disease modeling and drug screening. Nature Medicine. 23 (12), 1424-1435 (2017).
- Hennig, A., et al. CFTR Expression Analysis for Subtyping of Human Pancreatic Cancer Organoids. Stem Cells Int. 2019, 1024614 (2019).
- Seidlitz, T., et al. Human gastric cancer modelling using organoids. Gut. 68 (2), 207-217 (2019).
- Stepanenko, O. V., Verkhusha, V. V., Kuznetsova, I. M., Uversky, V. N., Turoverov, K. K. Fluorescent proteins as biomarkers and biosensors: throwing color lights on molecular and cellular processes. Current protein & peptide science. 9 (4), 338-369 (2008).
- Andersson-Rolf, A., et al. Simultaneous paralogue knockout using a CRISPR-concatemer in mouse small intestinal organoids. Dev Biol. 420 (2), 271-277 (2016).
- Ran, F. A., et al. Genome engineering using the CRISPR-Cas9 system. Nature Protocols. 8, 2281 (2013).
- Merenda, A., et al. A Protocol for Multiple Gene Knockout in Mouse Small Intestinal Organoids Using a CRISPR-concatemer. Journal of Visualized Experiments. (125), (2017).
- Lesueur, L. L., Mir, L. M., Andre, F. M. Overcoming the Specific Toxicity of Large Plasmids Electrotransfer in Primary Cells In Vitro. Molecular Therapy Nucleic Acids. 5, e291 (2016).
- Watanabe, K., et al. A ROCK inhibitor permits survival of dissociated human embryonic stem cells. Nature Biotechnology. 25 (6), 681-686 (2007).
- Darquet, A. M., Cameron, B., Wils, P., Scherman, D., Crouzet, J. A new DNA vehicle for nonviral gene delivery: supercoiled minicircle. Gene Therapy. 4 (12), 1341-1349 (1997).
- Jacobi, A. M., et al. Simplified CRISPR tools for efficient genome editing and streamlined protocols for their delivery into mammalian cells and mouse zygotes. Methods. 121-122, 16-28 (2017).

