Summary
Denne protokol er dedikeret til microtubule plus-end visualisering af EB3 protein transfection at studere deres dynamiske egenskaber i primær cellekultur. Protokollen blev implementeret på humane primære hudfibroblaster fra patienter med Huntingtons Sygdom.
Abstract
Transfection med et fluorescerende mærket markørprotein af interesse i kombination med time-lapse videomikroskopi er en klassisk metode til at studere cytoskeletons dynamiske egenskaber. Denne protokol tilbyder en teknik til human primær fibroblast transfection, som kan være vanskeligt på grund af detaljerne i primære celle dyrkning betingelser. Derudover kræver cytoskeleton dynamisk ejendomsvedligeholdelse et lavt niveau af transfection for at opnå et godt signal-til-støj-forhold uden at forårsage mikrotubulestabilisering. Det er vigtigt at træffe foranstaltninger til at beskytte cellerne mod lys-induceret stress og fluorescerende farvestof fading. I løbet af vores arbejde testede vi forskellige transfection metoder og protokoller samt forskellige vektorer for at vælge den bedste kombination af betingelser egnet til humane primære fibroblast undersøgelser. Vi analyserede de resulterende time-lapse videoer og beregnet microtubule dynamik ved hjælp af ImageJ. Dynamikken i mikrotubules plus-enderne i de forskellige celledele er ikke ens, så vi opdelte analysen i undergrupper - centrosome-regionen, lamellaen og halen af fibroblaster. Især kan denne protokol bruges til in vitro-analyse af cytoskeleton dynamik i patientprøver, hvilket gør det muligt for det næste skridt i retning af at forstå dynamikken i de forskellige sygdomsudvikling.
Introduction
Huntingtons Sygdom (HS) er en uhelbredelig neurodegenerativ patologi forårsaget af et mutationsgenkodningsjægerprotein (HTT). HTT er primært forbundet med vesikler og mikrotubuler og er sandsynligvis involveret i mikrotubuleafhængige transportprocesser1,2. For at studere indflydelsen af mutant HTT på mikrotubuledynamikken brugte vi in vitro-visualiseringen af EB3-proteinet, der regulerer mikrotubulernes dynamiske egenskaber ved at binde og stabilisere de voksende plus-ends. For at indlæse fluorescerende mærket EB3 i human hud fibroblaster, plasmid transfection blev anvendt. Vi brugte den primære fibroblastkultur, der blev opnået fra HS-patienternes hudbiopsi, til denne undersøgelse.
Mutationen i HTT-proteingenet fører til forlængelse af polyglutaminkanalen3. HTT har en rolle i sådanne cellulære processer som endokytose4, celletransport1,2, proteinforringelse5osv. Væsentlig del af disse processer involverer forskellige elementer i cellen cytoskeleton, herunder mikrotubuler.
Menneskelige primære celler er den bedste model til at reproducere hændelser, der forekommer i patientceller så tæt som muligt. For at skabe sådanne modeller skal man isolere celler fra humant biopsimateriale (f.eks. fra kirurgiske prøver). Den resulterende primære cellelinje er egnet til at studere patogenese ved hjælp af forskellige genetiske, biokemiske, molekylære og cellebiologiske metoder. Også menneskelige primære cellekulturer tjener som en forløber for at skabe forskellige transdifferentierede og transgene kulturer6.
Men i modsætning til udødeliggjorte cellekulturer er den betydelige ulempe ved primære celler deres begrænsede passagekapacitet. Derfor anbefaler vi at bruge celler i de tidlige passager fase (op til 15). Ældre kulturer degenererer meget hurtigt og mister deres unikke egenskaber. Således bør de nyerhvervede primære celler holdes frosne til langtidsopbevaring.
Primære cellekulturer er modtagelige for dyrkningsforhold. Derfor kræver de ofte unikke tilgange og optimering af vækstbetingelser. Især er den menneskelige hud primære fibroblaster, der anvendes i vores eksperimenter krævende på substratet. Derfor brugte vi forskellige ekstra belægninger (f.eks. gelatine eller fibronectin) afhængigt af eksperimenttypen.
Cellen cytoskeleton bestemmer celleform, mobilitet og bevægelse. Dynamikken i cytoskeleton er afgørende for mange intracellulære processer både i interfase og mitose. Især cytoskeleton polymeriseret fra tubulin, er meget dynamiske og polære strukturer, der muliggør motor protein-medieret rettet intracellulær transport. Mikrotubulernes ender er i konstant omlejring, deres samlingsfaser veksler med demonteringsfaserne, og denne funktionsmåde kaldes "dynamisk ustabilitet"7,8,9. Forskellige tilknyttede proteiner flytter ligevægten i polymeriseringsreaktionen, hvilket fører enten til polymerdannelsen eller proteinmonomerdannelsen. Tilsætning af tubulinunderenheder forekommer hovedsageligt i plus-enden af mikrotubuler10. Den endelige-bindende (EB) proteiner familie består af tre medlemmer: EB1, EB2, og EB3. De tjener som plus-end-tracking proteiner (+TIPs) og regulerer mikrotubulernes dynamiske egenskaber ved at binde og stabilisere deres voksende plus-ends11.
Mange undersøgelser bruger fluorescerende molekyle-mærket tubulin mikroinjection eller transfection med time-lapse imaging og video analyse til at visualisere mikrotubules in vitro. Disse metoder kan være invasive og skadelige for celler, især primære menneskelige celler. Det mest udfordrende skridt er at finde betingelser for celletransfekt. Vi forsøgte at nå det højest mulige niveau af transfection uden at påvirke levedygtigheden og native cellemorfologi. Denne undersøgelse anvender den klassiske metode til at studere forskellene i mikrotubuledynamikken i hudfibroblaster hos raske donorer og patienter med Huntingtons Sygdom.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
Denne protokol følger retningslinjerne fra Federal Research and Clinical Center of Physical-Chemical Medicine of Federal Medical Biological Agency dateret september 08, 2015.
BEMÆRK: Figur 1 giver et overblik over protokollen.
1. Opnåelse af en primær kultur af human hud fibroblaster (Figur 2)
- Levere biopsien til et laboratorium inden for få timer i Dulbecco's Modified Eagle Media (DMEM) medium suppleret med 50 μg/mL penicillin og 50 U/mL streptomycin.
BEMÆRK: En hudbiopsi skal udføres under sterile tilstande af en læge, efter at en patient har givet et informeret samtykke. - Placer biopsivævet i en 6 cm petriskål sammen med en lille mængde af mediet.
- Ved hjælp af en steril skalpel skæres biopsiprøven i stykker på ca. 0,5-1 mm i størrelse. Placer 1-2 opnåede fragmenter i en 3,5 cm Petriskål og læg et sterilt coverlip over biopsistykkerne. Tilsæt langsomt 1,5 mL af et vækstmedium til følgende sammensætning: DMEM, 50 U/mL penicillin-streptomycin og 10% fosterkvægsserum (FBS).
- Kulturfibrøster i vækstmediet inde i en CO 2-inkubator, der holdes ved 5 % CO2, 37 °C, 80 % fugtighed.
BEMÆRK: Efter 4-7 dage begynder først keratinocytter, derefter fibroblaster, at migrere fra vævet til bunden af skålen.
2. Opbevaring, frysning og frigørelse af primærkulturen
- Fjern celler fra kulturskålen (se punkt 3.2-3.4).
- Celleaffjedringen overføres til et 15 mL konisk rør og centrifuge i 5 min ved 200 x g. Kassér derefter supernatanten og genbrug cellepillen i 900 μL af afkølet FBS.
- Overfør til et kryopræserveringsrør dråbe for dråbe og tilsæt 100 μL dimethylsulfoxid (DMSO).
- Placer kryoproberen i en fryser ved -80 °C. 24 timer senere overføres kryovialten til flydende nitrogen (−196 °C) til langtidsopbevaring.
- Hvis du vil optø de kryopreserverede celler, fjernes kryovialen fra kvælstofopbevaring og inden for 1 min. overføres 1 minut af indholdet til et 15 mL konisk rør, der indeholder 9 mL af transportmediet, der er forvarmet til 37 °C.
- Forsigtigt resuspend og derefter centrifugere røret i 5 min ved 200 x g. Kassér supernatanten, genbrug cellepillen i vækstmediets krævede volumen og læg dem på en petriskål med den krævede diameter.
3. Celledyrkning
- Dæk fadbunden med autoklavet 0,1% gelatineopløsning tilberedt i destilleret vand. Inkuber i 15 min.
BEMÆRK: Ved transfektionsvisualisering bør glasbundspladeretter (konfokale retter med glastykkelse 170 μm) anvendes. - Forbered et kulturmedium med følgende sammensætning: DMEM suppleret med 10% FBS, 2 mM L-alanyl-L-glutamin, 50 U/mL penicillin-streptomycin. Bland grundigt og opbevares ved 4 °C. Varm mediet til 37 °C, før der tilsættes til cellerne.
- Vurder kulturen under mikroskopet. Fjern mediet og vask fibroblaster med Dulbeccos fosfatsaltopløsning (DPBS).
- Der tilsættes 1 mL forvarmet 0,25% trypsinopløsning til cellerne. Kontroller cellerne under mikroskopet, hvis de løsner sig helt fra substratet. Deaktiver trypsin med 1 mL af kulturmediet.
- Overfør celleaffjedringen til et 15 mL konisk rør. Centrifugere røret ved 200 x g i 5 min, fjerne supernatant, og genbruge cellepillen i 1 mL af kulturmediet.
- Tæl antallet af celler. Beregn det nødvendige antal celler til at så dem med en massefylde på 8-15 x 103/cm2 og genanvendes i 2 mL af kulturmediet.
- Fjern gelatineopløsningen fra kulturskålen, og tilsæt straks 2 ml af celleaffjedringen. Dyrke fibroblaster ved 37 °C i en CO 2-inkubator.
- Opdater mediet hver 2-4. dag.
BEMÆRK: Til eksperimenter skal du bruge cellerne i 4-11 passager.
4. Transfection
- Udskift kulturmediet med et frisk kulturmedium 24 timer før transfektion.
BEMÆRK: Cellekonfluensen skal være 70-80%. - Forbered et DNA-lipid kompleks baseret på området og tætheden af celle såning. Brug fedtsugningsbaseret transfektmiddel.
BEMÆRK: Brug cellesåningstætheden som 1 x 104 celler/cm2. - Der tilsættes 3 μL kommercielt transfektionsreagens til 125 μL optimalt minimalt essentielt medium (Opti-MEM), der ikke indeholder antibiotika, uden at røre rørets vægge. Forsigtigt genbruges.
- Fortynd plasmid-DNA (GFP-EB3) ved at tilsætte 1 μg af plasmid-DNA'et til 125 μL opti-MEM. Forsigtigt genbruges.
BEMÆRK: Ekspresvektorkodning GFP-EB311 blev modtaget som en venlig gave fra Dr. I. Kaverina (Vanderbilt University, Nashville) med tilladelse fra Dr. A. Akhmanova (Erasmus University, Rotterdam)11. - Tilsæt fortyndet plasmid-DNA til hvert rør af fortyndet transfektionsreagens (1:1). Inkuber i 30 min.
- Tilsæt DNA-lipid komplekset til 6 cm Petriskål indeholdende celler og bland med en cruciform swing for 30 s. Inkuber celler med et transfektionsmiddel i 24 timer og skift derefter til frisk medium. Analyser effektiviteten af transfection efter 24 timer og 48 timer.
BEMÆRK: 24 timer efter transfektion var effektiviteten 10-15%, og efter 48 timer op til 40%.
5. Forberedelse til billeddannelse
- Før levende billeddannelse af celler skal du ændre kulturmediet til et medium uden pH-indikatorfarve for at reducere autofluorescence.
- Påfør forsigtigt mineralsk olie på den mellemstore overflade for helt at dække mediet og isolere det fra det ydre miljø for at reducere O 2-indtrængningen og medium fordampning.
- Brug en kviksølv lampe og olie nedsænkning 60x eller 100x objektiv linse med en høj tal blænde til at tage billederne.
BEMÆRK: Ved in vivoobservationer skal mikroskopet være udstyret med en inkubator for at opretholde de nødvendige betingelser for cellerne, herunder opvarmning af objekttabellen og objektivet til +37 °C, et lukket kammer med CO2-forsyning og fugtighedsniveaustøtte. Brug dobbelt destilleret vand til at skabe fugtighed. Kontroller niveauet af dobbelt destilleret vand før optagelserne. - Anbring den konfokale skål med cellerne i mikroskopholderen før billeddannelse. Sørg for, at fadet og kameraet er forsvarligt fastgjort til holderen for at undgå at drive, mens du tager billeder.
6. Indstilling af billedparametre
- Vælg de lave eksponeringsværdier, da lys fremkalder celleskadende reaktive iltarter (ROS).
BEMÆRK: For at studere dynamikken i mikrotubuler i human hud fibroblaster, en 300 ms eksponering blev valgt. - Fokuser på genstanden for interesse.
BEMÆRK: Ved langvarig tidsforskydning skal du bruge det automatiske fokusstabiliseringssystem til at kompensere for et muligt skift langs z-aksen. - Vælg de optimale billeddannelsesforhold afhængigt af cellernes lysfølsomhed og fluorokromningens hastighed.
BEMÆRK: Da mikrotubuler er meget dynamiske strukturer, kan der vælges et rimeligt kort tidsinterval, og billedhastigheden skal være tilstrækkelig høj. For at undersøge mikrotubule dynamikken i huden fibroblaster, vi brugte med en frekvens på 1 ramme / s i 3-5 min. - Når du markerer det næste objekt for at hente billedet, skal du flytte væk fra det allerede afbildede område. Da dette område var under påvirkning af lys, vil der være mærkbar foto-blegning.
BEMÆRK: Da der blev brugt en relativt høj billedfrekvens, lukkede lukker lukkeren ikke mellem billeder, og lampen blev tændt i hele billeddannelsesperioden, hvorfor fading steg. - Vælg den optimale video til at studere mikrotubulernes dynamik visuelt under hensyntagen til transfectionens kvalitet, kvaliteten af mikrotubulernes billeder (optimalt signal-til-støj-forhold) og fraværet af drift i tilfælde af den analyserede celle (Figur 3).
- Brug de valgte videoer til at studere mikrotubulernes plus-ends dynamik ved at spore dem i ImageJ- eller Fiji-programmet (Figur 4).
BEMÆRK: For kvantitative analyseinstruktioner henvises til supplerende figur 2 og supplerende fil 1.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
De resulterende GFP-EB3-film, der er produceret ved hjælp af protokollen (Figur 1), illustrerer mikrotubulernes dynamiske egenskaber. Mikrotubuler er involveret i forskellige celleprocesser, og deres dynamiske egenskaber påvirker forskellige livskarakteristika i den primære menneskelige cellekultur fra patienternes biopsimateriale (Figur 2).
Følgende parametre bestemmer mikrotubulernes dynamiske ustabilitet: vækstraterne (polymerisering) og faldende (depolymerisering); hyppigheden af katastrofer (overgang fra polymerisering til depolymerisering); hyppigheden af redninger (overgang fra depolymerisering til polymerisering) samt pauser - stater, når microtubule ikke polymerisere og ikke depolymerize 12. Alle parametre er stramt reguleret, og satserne for polymerisering og depolymerisering af individuelle mikrotubuler kan variere betydeligt både i samme og forskellige celletyper13,14,15,16,17.
Det er nødvendigt at overveje for analysen, at mikrotubuler kan have forskellige dynamikker afhængigt af deres position i cellen. Mikrotubuler placeret i regionen af kernen og centrosome opfører sig anderledes i forhold til dem på cellenperiferien 19. For at opnå et pålideligt resultat lavede vi derfor mikrotubulernes dynamiske målinger i tre separate områder af cellen: den centrale del, forkanten og haledelen (Figur 3). For at kontrollere den korrekte fordeling af GFP-EB3-mærket i forskellige celledele brugte vi humanpulmonalpulsåre endotelceller (HPAEC) (se supplerende figur 1).
Specialiserede programmer, såsom ImageJ eller Fiji (ImageJ 2 v1. 53i), gør det muligt at analysere videoerne med følgende parametre: (1) hastigheden af mikrotubulernes vækst; 2) hyppigheden af katastrofer 3) hyppigheden af redningsaktioner 4) hyppigheden af pauser og (5) varigheden af pauser. Derudover tillader unikke programindstillinger og plugins automatisk sporing18 eller manuelt19 (Figur 4). Den manuelle sporingsmetode fungerede bedre i vores eksperimenter, da automatiske målinger er tilbøjelige til større fejl og kræver flere gentagelser for et mere præcist resultat. Detaljerede instruktioner om analyse af mikrotubuler dynamics data findes i supplerende figur 2 og supplerende fil 1.
Billedparametrene kan kræve justeringer under billeddannelsesprocessen. Varigheden af en cellebilleddannelse og eksponeringsværdierne kan f.eks. Sådanne indstillinger er nyttige, hvis der er en hurtig signaludbrændthed, eller cellen krymper (Figur 5).

Figur 1: Den generelle ordning for GFP-EB3 transfection protokol for human hud primære fibroblaster kultur. Protokollen indeholder følgende trin: prøveløsningen af celler, der skal frigøre celler. trypsin inaktivering af medium tilføjelse; centrifugering af den resulterende forbindelse; beregning af cellekoncentration cellesåning til glasbunden (konfokalt fad) belagt med gelatine; cellekulturtransfektion ved plasmid-DNA (med GFP-EB3) med fedtomaltransfection reagens; inkubation 24-48 h; og analyse under et mikroskop. Klik her for at se en større version af dette tal.

Figur 2: Human hud fibroblaster primære kultur forberedelse ordning. En hudbiopsi skal udføres under sterile tilstande af en læge, efter at en patient har givet et informeret samtykke. Derefter transporteres et stykke væv i en lille mængde af mediet uden FBS til laboratoriet i en petriskål. Et stort vævsfragment skæres i stykker på 0,5-1 mm i størrelse, og de er dækket af et dækglas med tilsætning af mediet med FBS. Derefter placeres petriskålen i en CO 2-inkubator, hvor fibroblaster efter 4-7 dage migrerer fra vævsfragmentet til glasbunden. Klik her for at se en større version af dette tal.

Figur 3: GFP-EB3-markør (grøn) i forskellige områder af transfected human fibroblaster, fremstillet af HS-patienters hudbiopsi: forkant (toppanel); hale (midterste panel); central del af fibroblast (zone omkring centrosomet) (bundpanel). Skalalinje = 10 μm. Billedfrekvensen er 1 ramme/s. Lysstofrørskopi i bred felt. Klik her for at se en større version af dette tal.

Figur 4: GFP-EB3 manuel sporing af ImageJ plugin MTrackJ. Spor, der afspejler væksten af mikrotubuler, blev opnået som følge af manuel mærkning af GFP-EB3-etiketterne i plus-enderne i løbet af 20 s billeddannelse. Transfected kultiverede fibroblaster, fremstillet af HS-patienters hudbiopsi. Billedfrekvensen er 1 ramme/s. Lysstofrørskopi i bred felt. Skalalinje = 10 μm. Klik her for at se en større version af dette tal.

Figur 5: Fejlfinding under billeddannelse af GFP-EB3-mærkede mikrotubulers plus-ends. (A) Fluorescerende mikrotubuler er ude af fokus på grund af fraværet af et fokussystem. (B) Mikrotubuler stabiliseres og mister deres dynamiske egenskaber på grund af overekspression af GFP-EB3 i cellen på grund af lang inkubation med transfectingblandingen. (C) Indskrænkning af cellelameller som følge af fototoksicitet som følge af frigivelsen af ROS. (D) Signalintensiteten falder under billeddannelse - hurtig fotobleaching. Transfected kultiverede fibroblaster, fremstillet af HS-patienters hudbiopsi. Billedfrekvensen er 1 ramme i sekundet. Lysstofrørskopi i bred felt. Skalalinjer = 10 μm. Klik her for at se en større version af dette tal.
Supplerende figur 1: Selektiv visualisering af voksende microtubule plus-ends. GFP-EB3 markør (grøn) i forskellige områder af transfected menneskelige endotelcelle (kultur af HPAEC: Human Pulmonal Artery Endotel Cells) i forkant, hale og centrale område (zone omkring centrosomet). Skalastænger 10 μm. Billedfrekvensen er 1 ramme/s fluorescerende mikroskopi i bred felt. Klik her for at downloade denne fil.
Supplerende figur 2: Microtubule dynamics analysis af GFP-EB3-etiket efter manuel sporing ved hjælp af ImageJ plugin MTrackJ. (A,B) EB3-spor opnået ved EB3-GFP-patches forskydning på time-lapse serie af transfected kulsyrer, fremstillet af HS-patienters hudbiopsi (er farvet individuelt). (A) EB3 spor (lilla, No46) opnået ved EB3-GFP patches forskydning i løbet af 18 sekunder. (B) EB3-spor (rød, nr. 37) opnået ved EB3-GFP-patches forskydning i løbet af 9 sekunder. (C) Kvantificering af plus-endere forskydning af mikrotubuler af humane HS-patienters hudfibrobrøst vist i (A). (D) Kvantificering af plus-endere forskydning af mikrotubuler vist i litraB). Grafen viser, at mellem 6-8 sekunder er der en pause i væksten af microtubule (der er ingen bevægelse af plus-end). Klik her for at downloade denne fil.
Supplerende fil 1: Kvantitativ analyse af dynamikken i EB3-GFP mærket mikrotubuler plus-ends. Klik her for at downloade denne fil.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
Bedre kvalitetsresultater til mikrotubules dynamikanalyse kan fås fra mikroskopiske billeder af høj kvalitet. Det er vigtigt at overholde alle de nødvendige betingelser for time-lapse imaging af levende celler og at justere billeddannelsesparametrene korrekt. Brug af specielle cellekulturretter med en glasbund (konfokale retter) er vigtigt, da glas har et andet brydningsindeks for lys end plast. Tykkelsen af glasset og dets ensartethed over hele dets område er også ekstremt vigtigt, da disse parametre er afgørende for normal prøvefokusering. Overtrædelse af disse parametre fører uundgåeligt til en fejl i det perfekte fokussystem, hvilket resulterer i dårlig fokusering, hvilket gør det umuligt at bruge en sådan video uden for fokus til analyse (Figur 5A). En anden vigtig betingelse for live-celle billeddannelse er deres beskyttelse mod ROS. Forskellige reagenser kan anvendes til sådanne formål20. I vores arbejde bruger vi mineralsk olie, som fuldstændig isolerer kulturmediet fra atmosfæren og forhindrer gasudveksling. På samme måde kan det ROS-reducerende oxyrase bruges, men dette enzym er ikke egnet til alle celletyper og er oftere anvendeligt til billeddannelse med øget tid.
Når du vælger den optimale inkubationstid for celler efter transfektion (24 eller 48 timer), skal der lægges vægt på antallet af transfected celler. Et tal, der er mindre end det maksimale antal celler, der udtrykker det mærkede protein, er allerede tilstrækkeligt til analysen. Overekspression bør ikke tillades, fordi mikrotubuler i sådanne tilfælde stabiliseres, og deres dynamiske egenskaber ikke kan analyseres (Figur 5B).
I nogle tilfælde kan det være nødvendigt at justere billeddiagnostiske parametre i overensstemmelse med cellernes reaktion efter starten af videooptagelsen. For eksempel er det muligt at observere cellelameller krympe på grund af høj følsomhed over for lys (fototoksicitet) (Figur 5C). Når ophidset, de fluorescerende molekyler typisk reagerer med molekylær ilt til at danne frie radikaler, der kan skade cellekomponenter21. Ved udformningen af forsøg bør fluorophorer med størst mulig excitationsbølgelængde vælges for at minimere celleskader under kortbølgebelysning. Derudover er der rapporter om, at visse komponenter i standardkulturmedier, herunder riboflavin-vitaminet og tryptofan aminosyren, også kan bidrage til de negative virkninger af lys på dyrkede celler22. Det kan blandt andet skyldes en for stor mængde fluorescerende etiketter i én celle. I disse tilfælde bliver det nødvendigt at reducere optagelsens varighed og intensiteten af belysningen. Et andet muligt problem kan også være hurtig fotografering - reduktion af signalintensiteten under optagelsen (Figur 5D). Denne effekt skal tages i betragtning, når du vælger det næste objekt på den samme eksperimentelle skål, da de nærliggende celler omkring det afbildede område også er udbrændte.
Det skal nævnes, at der er andre metoder til mikrotubule visualisering i levende celler som mikroinjektion af fluorescerende-mærket tubulin i cellen eller celle transduktion ved hjælp af vira. Som med enhver anden metode er der fordele og ulemper ved transfektionsmetoden. Men fra vores synspunkt er transfektion i sammenligning med injektionsmetoden mere effektiv og gør det muligt at opnå masseindtagelse af udtryksvektorer i cellerne, hvilket resulterer i et stort antal fluorescerende celler til analyse. Transfektionsmetoden kræver heller ikke særligt udstyr og færdigheder fra forskeren. Metoden til viral transduktion viser gode resultater og kan anvendes. Alligevel er det ikke egnet til alle cellekulturer (især er det mindre egnet til humane fibroblaster, fremstillet af HS-patienters hudbiopsi).
Det mest kritiske skridt i denne protokol er den transinfektion, der udføres for at sikre tilstrækkeligt proteinudtryk. Et godt signal-til-støj-forhold, ingen fotobleaching af mikrotubuler og fraværet af celledrift under time-lapse videooptagelse er helt afgørende for effektiv mikrotubules billeddannelse. I vores eksperimentgiver visualisering af mikrotubuler og den dynamiske analyse vigtige oplysninger om mikrotubuleegenskaber og adfærd i cellerne med mutant HTT. Vores protokol gælder for undersøgelser af andre sygdomme, for hvilke patologi implicerer dynamiske egenskaber af mikrotubuler.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Forfatterne har intet at afsløre.
Acknowledgments
Denne forskning blev finansieret af Ministeriet for Videnskab og Videregående Uddannelse i Den Russiske Føderation, tilskud nr. 075-15-2019-1669 (transfection af fibroblaster), af Den Russiske Videnskabsfond, tilskud nr. 19-15-00425 (alle andre værker om dyrkning af fibroblaster in vitro). Det blev delvist støttet af Lomonosov Moskva State University Development program PNR5.13 (billedbehandling og analyse). Forfatterne anerkender støtte fra Nikon Center of Excellence på A. N. Belozersky Institute of Physico-Chemical Biology. Vi ønsker at tilbyde vores særlige tak til Ekaterina Taran for hendes hjælp med stemmeskuespil. Forfatterne takker også Pavel Belikov for hans hjælp med videoredigeringen. Figurer i manuskriptet blev skabt med BioRender.com.
Materials
| Name | Company | Catalog Number | Comments |
| Instrumentation | |||
| Camera iXon DU897 EMCCD | Andor Technology | ||
| Eppendorf Centrifuge 5804 R | Eppendorf Corporate | ||
| Fluorescence filter set HYQ FITC | Nikon | Alternative: Leica, Olympus, Zeiss | |
| LUNA-II Automated Cell Counte | Logos Biosystems | L40002 | |
| Microscope incubator for lifetime filming | Okolab | Temperature controller H301-T-UNIT-BL-PLUS | |
| Gas controller CO2-O2-UNIT-BL | |||
| Objective lens CFI Plan Apo Lambda 60x Oil 1.4 (WD 0.13) | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Widefield fluorescence light microscope Eclipse Ti-E | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Software | |||
| Fiji (Image J version 2.1.0/1.53c) | Open source image processing software | ||
| NIS Elements | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Additional reagents | |||
| Mineral oil (Light white oil) | MP | 151694 | |
| Cell culture dish | |||
| Cell Culture Dish | SPL Lifesciences | 20035 | |
| Confocal Dish (glass thickness 170 µm) | SPL Lifesciences | 211350 | Alternative: MatTek |
| Conical Centrifuge tube | SPL Lifesciences | 50015 | |
| Cryogenic Vials | Corning-Costar | 430659 | |
| Microcentrifuge Tube | Nest | 615001 | |
| Cultivation | |||
| Lipofectamine 3000 Transfection Reagent | Thermo Fisher Scientific | L3000001 | |
| Dimethyl sulfoxide | PanEko | 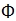 135 135 |
|
| DMEM (Dulbecco's Modified Eagle Media) | PanEko | C420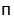 |
|
| DPBS (Dulbecco's phosphate-salt solution) | PanEko | P060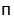 |
|
| Fetal bovine serum (FBS) | Hyclone | K053/SH30071.03 | |
| Gelatin (bovine skin) | PanEko | 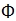 070 070 |
|
| GlutaMAX | Thermo Fisher Scientific | 35050038 | |
| Opti-MEM (1x) + Glutamax | Gibco | 519850026 | |
| Penicillin-streptomycin | PanEko | A063 |
|
| Trypsin-EDTA (0.25%) | Thermo Fisher Scientific | 25200072 | |
| Transfection | |||
| Plasmid DNA with EB3-GFP | Kind gift of Dr. I. Kaverina [Vanderbilt University, Nashville] with permission from Dr. A. Akhmanova [Erasmus University, Rotterdam] |
Stepanova et al., 2003 DOI: 10.1523/JNEUROSCI.23-07-02655.2003 |
References
- Engelender, S., et al. Huntingtin-associated Protein 1 (HAP1) Interacts with the p150 Glued Bubunit of Dynactin. Human Molecular Genetics. 6 (13), 2205-2212 (1997).
- Caviston, J. P., Ross, J. L., Antony, S. M., Tokito, M., Holzbaur, E. L. Huntingtin facilitates dynein/dynactin-mediated vesicle transport. Proceedings of the National Academy of Sciences. 104 (24), 10045-10050 (2007).
- MacMillan, J. C., et al. Molecular analysis and clinical correlations of the Huntington's disease mutation. The Lancet. 342 (8877), 954-958 (1993).
- Proskura, A. L., Vechkapova, S. O., Zapara, T. A., Ratushniak, A. S. Protein-protein interactions of huntingtin in the hippocampus. Molecular Biology. 51 (4), 647-653 (2017).
- Steffan, J. S., et al. The Huntington's disease protein interacts with p53 and CREB-binding protein and represses transcription. Proceedings of the National Academy of Sciences. 97 (12), 6763-6768 (2000).
- Nekrasov, E. D., et al. Manifestation of Huntington's disease pathology in human induced pluripotent stem cell-derived neurons. Molecular Neurodegeneration. 11 (1), 1-15 (2016).
- Mitchison, T., Kirschner, M. Dynamic instability of microtubule growth. Nature. 312 (5991), 237-242 (1984).
- Walker, R. A., et al. Dynamic instability of individual microtubules analyzed by video light microscopy: rate constants and transition frequencies. The Journal of Cell Biology. 107 (4), 1437-1448 (1988).
- Desai, A., Mitchison, T. J. Microtubule polymerization dynamics. Annual Review of Cell and Developmental Biology. 13 (1), 83-117 (1997).
- Allen, C., Borisy, G. G. Structural polarity and directional growth of microtubules of Chlamydomonas flagella. Journal of Molecular Biology. 90 (2), 381-402 (1974).
- Stepanova, T., et al. Visualization of microtubule growth in cultured neurons via the use of EB3-GFP (end-binding protein 3-green fluorescent protein). Journal of Neuroscience. 23 (7), 2655-2664 (2003).
- Shelden, E., Wadsworth, P. Observation and quantification of individual microtubule behavior in vivo: microtubule dynamics are cell-type specific. Journal of Cell Biology. 120 (4), 935-945 (1993).
- O'Brien, E. T., Salmon, E. D., Walker, R. A., Erickson, H. P. Effects of magnesium on the dynamic instability of individual microtubules. Biochemistry. 29 (28), 6648-6656 (1990).
- Drechsel, D. N., Hyman, A. A., Cobb, M. H., Kirschner, M. W. Modulation of the dynamic instability of tubulin assembly by the microtubule-associated protein tau. Molecular Biology of the Cell. 3 (10), 1141-1154 (1992).
- Gildersleeve, R. F., Cross, A. R., Cullen, K. E., Fagen, A. P., Williams, R. C. Microtubules grow and shorten at intrinsically variable rates. Journal of Biological Chemistry. 267 (12), 7995-8006 (1992).
- Penazzi, L., Bakota, L., Brandt, R. Microtubule dynamics in neuronal development, plasticity, and neurodegeneration. International Review of Cell and Molecular Biology. 321, 89-169 (2016).
- van de Willige, D., Hoogenraad, C. C., Akhmanova, A. Microtubule plus-end tracking proteins in neuronal development. Cellular and Molecular Life Sciences. 73 (10), 2053-2077 (2016).
- Applegate, K. T., et al. plusTipTracker: Quantitative image analysis software for the measurement of microtubule dynamics. Journal of Structural Biology. 176 (2), 168-184 (2011).
- Komarova, Y. A., Vorobjev, I. A., Borisy, G. G. Life cycle of MTs: persistent growth in the cell interior, asymmetric transition frequencies and effects of the cell boundary. Journal of Cell Science. 115 (17), 3527-3539 (2002).
- Nahidiazar, L., Agronskaia, A. V., Broertjes, J., vanden Broek, B., Jalink, K. Optimizing imaging conditions for demanding multi-color super resolution localization microscopy. PLoS One. 11 (7), 0158884 (2016).
- Dixit, R., Cyr, R. Cell damage and reactive oxygen species production induced by fluorescence microscopy: effect on mitosis and guidelines for non-invasive fluorescence microscopy. The Plant Journal. 36 (2), 280-290 (2003).
- Grzelak, A., Rychlik, B., Bartosz, G. Light-dependent generation of reactive oxygen species in cell culture media. Free Radical Biology and Medicine. 30 (12), 1418-1425 (2001).



