A subscription to JoVE is required to view this content. Sign in or start your free trial.
JoVE Journal
Medicine
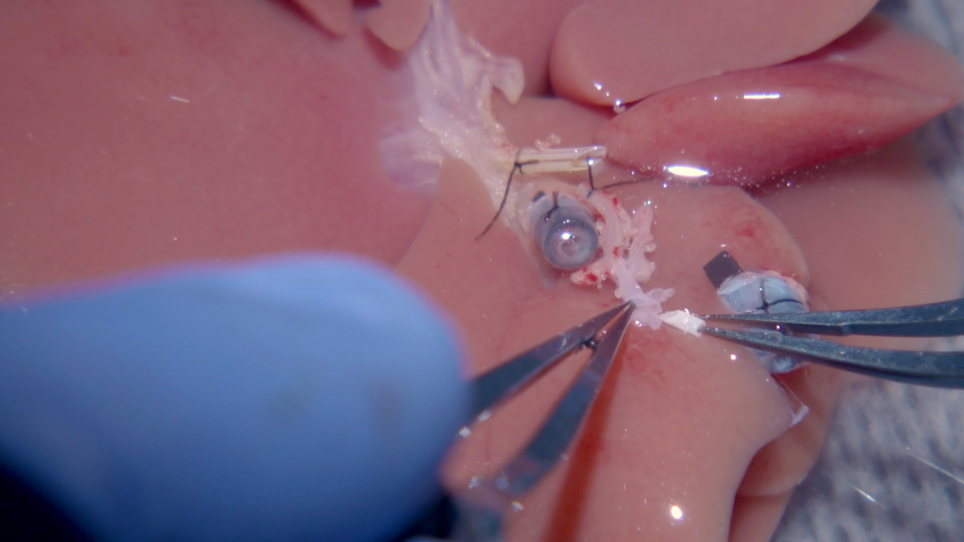
Heterotopic Auxiliary Rat Liver Transplantation With Flow-regulated Portal Vein Arterialization in Acute Hepatic Failure
Chapters
- 00:00Title
- 01:30Procedure
- 03:09Surgical Procedures
- 03:11Donor Operation
- 07:16Recipient Operation
- 11:28Results
- 13:20Discussion
Auxiliary liver transplantation provides a temporary support in acute hepatic failure, until regeneration of the failing liver. The heterotopic auxiliary liver transplantation (HALT) with portal vein arterialization (PVA) renders sufficient liver function. We developed an analogous technique in the rat, to examine the influence of the portal vein arterialization on the morphology and function of the graft.