Phagen-Transduktion: Eine Methode zur Übertragung der Ampicillinresistenz von einem Spender auf den Empfänger E. coli
English
Share
Overview
Quelle: Alexander S. Gold1, Tonya M. Colpitts1
1 Department of Microbiology, Boston University School of Medicine, National Emerging Infections Diseases Laboratories, Boston, MA
Transduktion ist eine Form des genetischen Austauschs zwischen Bakterien, die Bakteriophagen oder Phagen verwenden, eine Klasse von Viren, die ausschließlich prokaryotische Organismen infiziert. Diese Form der DNA-Übertragung, von einem Bakterium zum anderen durch einen Phagen, wurde 1951 von Norton Zinder und Joshua Ledererg entdeckt, die den Prozess als “Transduktion” bezeichneten (1). Bakteriophagen wurden erstmals 1915 vom britischen Bakteriologen Frederick Twort entdeckt, 1917 vom französisch-kanadischen Mikrobiologen Felix d’Herelle (2) selbstständig wieder entdeckt. Seitdem sind die Struktur und Funktion dieser Phagen weithin charakterisiert (3), wodurch diese Phagen in zwei Klassen unterteilt wurden. Die erste dieser Klassen sind die lytischen Phagen, die sich bei einer Infektion innerhalb des Wirtsbakteriums vermehren, den bakteriellen Stoffwechsel stören, die Zelle lysieren und Nachkommenphagen freisetzen (4). Als Ergebnis dieser antibakteriellen Aktivität und der zunehmenden Prävalenz antibiotikaresistenter Bakterien haben sich diese lytischen Phagen in letzter Zeit als Ersatzbehandlung für Antibiotika erwiesen. Die zweite dieser Klassen sind die lysogene Phagen, die sich entweder innerhalb des Wirts über den lytischen Zyklus vermehren können oder in einen ruhestillenden Zustand eintreten, in dem ihr Genom in das des Wirts integriert ist (Abbildung 1), ein Prozess, der als Lysogenie bekannt ist, mit der Fähigkeit für Phagen Produktion in mehreren späteren Generationen induziert werden (4).
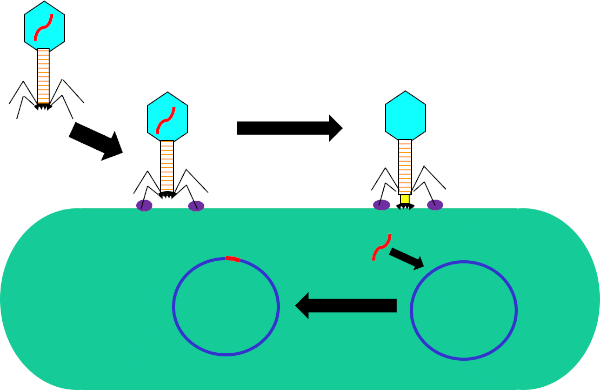
Abbildung 1: Infektion der Wirtszelle durch Bakteriophagen. Adsorption durch den Phagen an die bakterielle Zellwand über Wechselwirkungen zwischen den Schwanzfasern und dem Rezeptor (lila). Einmal auf der Zelloberfläche angekommen, wird der Phagen irreversibel mit der Grundplatte (schwarz) an der Bakterienzelle befestigt, die durch den kontraktilen Mantel (gelb) zur Zellwand bewegt wird. Das Phage-Genom (rot) gelangt dann in die Zelle und integriert sich in das Genom der Wirtszelle.
Während bakterielle Transduktion ein natürlich vorkommender Prozess ist, wurde sie mit moderner Technologie für den Transfer von Genen in Bakterien im Labor verfahren. Durch das Einfügen von Genen von Interesse in das Genom eines lysogenen Phagens, wie Phagen, ist man in der Lage, diese Gene in die Genome von Bakterien zu übertragen und folglich innerhalb dieser Zellen auszudrücken. Während andere Methoden des Gentransfers, wie die Transformation, ein Plasmid für Gentransfer und Expression verwenden, hat die Einfügung des Phagengenoms in das des Empfängerbakteriums nicht nur das Potenzial, diesem Bakterium neue Merkmale zu verleihen, sondern ermöglicht auch natürlich vorkommende Mutationen und andere Faktoren der zellulären Umgebung, um die Funktion des übertragenen Gens zu verändern.
Im Vergleich zu anderen Methoden des horizontalen Gentransfers, wie z. B. Konjugation, ist die Transduktion in den Kriterien, die für Spender- und Empfängerzellen erforderlich sind, ziemlich flexibel. Jedes genetische Element, das in das Genom des verwendeten Phagens passen kann, kann von jedem Stamm von Spenderbakterien auf jeden Stamm von Empfängerbakterien übertragen werden, solange beide für den Phagen freisind, was die Expression der notwendigen Phagenrezeptoren auf der Zelloberflächen. Sobald dieses Gen aus dem Spendergenom herausgebracht und in den Phagen verpackt ist, kann es an den Empfänger übertragen werden. Nach der Transduktion ist es notwendig, für EmpfängerBakterien auszuwählen, die das Gen von Interesse enthalten, für die ausgewählt werden muss. Dies könnte durch die Verwendung eines genetischen Markers, wie z. B. eines FLAG-Tags oder Polyhistidin-Tags, erfolgen, um das Gen von Interesse oder die intrinsische Funktion des Gens im Falle von Genen zu kennzeichnen, die für Antibiotikaresistenzen kodieren. Darüber hinaus könnte PCR verwendet werden, um eine erfolgreiche Transduktion weiter zu bestätigen. Durch die Verwendung von Primern für eine Region innerhalb des Gens von Interesse und den Vergleich von Signal enden mit einer positiven Kontrolle, Bakterien, die das Gen von Interesse haben, und einer negativen Kontrolle, Bakterien, die die gleichen Schritte wie die Transduktionsreaktion ohne Phagen durchliefen. Während die bakterielle Transduktion ein nützliches Werkzeug in der Molekularbiologie ist, spielt sie eine wichtige Rolle bei der Evolution von Bakterien, insbesondere im Hinblick auf den jüngsten Anstieg der Antibiotikaresistenz.
In diesem Experiment wurde die bakterielle Transduktion verwendet, um die Genkodierung für die Resistenz gegen das Antibiotikum Ampicillin vom W3110-Stamm von E.coli auf den J53-Stamm über das P1-Bakteriophagen (5) zu übertragen. Dieses Experiment bestand aus zwei Hauptschritten. Erstens die Herstellung von P1-Phagen, das das Ampicillin-Resistenzgen aus dem Spenderstamm enthält. Zweitens die Übertragung dieses Gens auf den Empfängerstamm durch Transduktion mit dem P1-Phagen (Abbildung 1). Nach der Durchführung konnte die erfolgreiche Übertragung des Ampicillinresistenzgens durch qPCR bestimmt werden (Abbildung 2). Wenn die Transduktion erfolgreich wäre, wäre der J53-Stamm von E. coli resistent gegen Ampicillin und das Gen, das diese Resistenz durch qPCR nachweisbar macht. Bei einem Erfolglosen würde es keinen Nachweis des Ampicillinresistenzgens geben und Ampicillin würde immer noch als wirksames Antibiotikum gegen den J53-Stamm wirken.
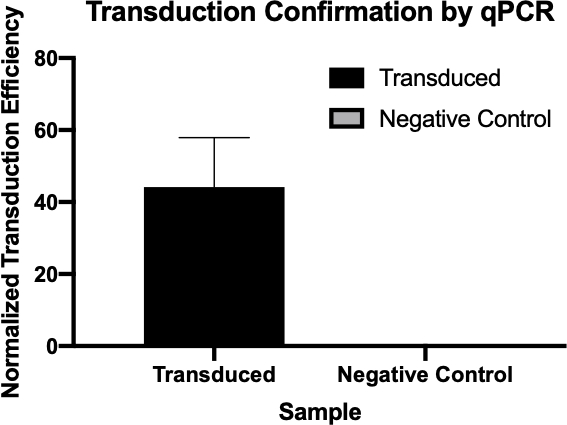
Abbildung 2: Bestätigung einer erfolgreichen Transduktion durch qPCR. Durch den Vergleich der C q-Werte, die für das Gen von Interesse aus der Transduktionsreaktion und der Negativkontrollreaktion nachgewiesen wurden, und die Normalisierung dieser Werte mit einem Housekeeping-Gen konnte man bestätigen, dass die bakterielle Transduktion erfolgreich war.
Procedure
Applications and Summary
The transfer of genes to and from bacteria by bacteriophage, while a natural process, has proved extremely useful for a multitude of research purposes. While other methods of gene transfer such as transformation and conjugation are possible, transduction uniquely uses bacteriophages; not only allowing for gene integration into the host genome, but also for gene delivery to multiple bacteria that are not susceptible to other methods. This process, while especially useful in the laboratory, has also been used in the recently emerging field of gene therapy, more specifically in alternative gene therapy, a therapeutic strategy that utilizes bacteria to deliver therapeutics to target tissues, many of which are not susceptible to other delivery methods and have much clinical relevance (8,9).
References
- Lederberg J, Lederberg E.M., Zinder, N.D., et al. Recombination analysis of bacterial heredity. Cold Spring Harbor symposia Quantitative Biol. 1951;16:413-43.
- Duckworth DH. "Who Discovered Bacteriophage?". Bacteriology Reviews. 1976;40:793-802.
- Yap ML, Rossman, M.G. Structure and Function of Bacteriophage T4. Future Microbiol. 2014;9:1319-27.
- Sulakvelidze A, Alavidze, Z., Morris, J. G. Bacteriophage Therapy Antimicrobial Agents and Chemotherapy 2001;45(3):649-59.
- Moore S. Sauer:P1vir phage transduction 2010 [Available from: https://openwetware.org/wiki/Sauer:P1vir_phage_transduction].
- Kobayashi A, et al. Growth Phase-Dependent Expression of Drug Exporters in
- Escherichia coli and Its Contribution to Drug Tolerance. Journal of Bacteriology. 2006;188(16):5693-703.
- Rocha D, Santos, CS, Pacheco LG. Bacterial reference genes for gene expression studies by RT-qPCR: survey and analysis. Antonie Van Leeuwenhoek. 2015;108:685-93.
- Pálffy R. et al. Bacteria in gene therapy: bactofection versus alternative gene therapy. Gene Ther. 2006 13:101-5.
- O'Neill JM, et al. Intestinal delivery of non-viral gene therapeutics: physiological barriers and preclinical models. Drug Discovery Today. 2011;16:203-2018.
Transcript
Bacteria can adapt quickly to a fast-changing environment by exchanging genetic material and one way they can do this is via transduction, the exchange of genetic material mediated by bacterial viruses. A bacteriophage, often abbreviated to phage, is a type of virus that infects bacteria by first attaching to the surface of the host and then injecting its DNA into the bacterial cell. It then degrades the host cell’s own DNA and replicates its viral genome, whilst hijacking the cell’s machinery to synthesize many copies of its proteins. These phage proteins then self-assemble and package the phage genomes to form multiple progeny. However, due to the low fidelity of the DNA packaging mechanism, occasionally, the phage packages fragments of bacterial DNA into the phage capsid. After inducing the lysis of the host, the phage progeny are released and, once such a phage infects another host cell, it transfers the DNA fragment of its previous host. This can then recombine and become permanently incorporated into the new host’s chromosome, thereby mediating gene transfer between the two bacteria.
To carry out phage transduction in the laboratory requires a donor strain that contains a gene of interest, a recipient strain that lacks it, a phage that can infect both the strains, and a method to select the transduced bacteria. In most cases, this will be a selective solid growth media that supports the growth of transduced bacteria but inhibits the growth of non-transduced ones. To begin, the donor strain that contains the gene of interest is cultured in a liquid growth medium. When all the bacteria are actively dividing in the log phase of their growth, the culture is inoculated with the target phage. After three to four hours of incubation, when nearly all the bacteria have lysed and released the phage particles, the donor phage lysate is inoculated into a freshly grown culture of the recipient bacterial strain. After a brief incubation of one hour, the culture should now contain a mixture of transduced and non-transduced bacterial cells and this is screened for the transduced cells by spreading a fraction of the suspension onto an appropriate selective solid growth media. Upon further incubation, the transduced cells should grow and multiply to yield visible colonies. These colonies can then be selected for further analysis using a variety of methods to further confirm successful transduction, such as colony PCR, DNA sequencing, or quantitative PCR.
Before starting the procedure, put on any appropriate personal protective equipment, including a lab coat and gloves. Next, sterilize the workspace with 70% ethanol and wipe down the surface.
After this, prepare three one-milliliter aliquots of LB salt solution. Now, prepare a donor strain culture by adding 100 microliters of E. coli to a 15 milliliter conical vial containing five milliliters of LB growth medium with 500 micrograms of ampicillin. Then, grow the culture overnight at 37 degrees Celsius with aeration and shaking at 220 rpm. The next day, wipe down the bench top with 70% ethanol before removing the culture from the shaking incubator. Next, dilute the overnight culture one to 100 by adding 10 microliters of donor strain to 990 microliters of fresh LB supplemented with salt solution.
Allow the bacterial dilution to grow at 37 degrees Celsius for two hours with aeration and shaking at 220 rpm. Once the cells have reached early log phase, remove the culture from the incubator, add 40 microliters of P1 phage to the culture and incubate again. Continue to monitor the cells for one to three hours until the culture has lysed. Next, add 50 to 100 microliters of chloroform to the lysate and mix by vortexing. Then, centrifuge the lysate to remove debris and transfer the supernatant to a fresh tube. Add a few drops of chloroform to the supernatant and store it at four degrees Celsius for no more than one day.
To begin the transduction procedure, obtain a one milliliter culture of recipient strain. Next, transfer 100 microliters of donor phage lysate into a 1.5 milliliter microcentrifuge tube and incubate it at 37 degrees Celsius with the cap open for 30 minutes to allow any remaining chloroform to evaporate. While the donor phage lysate incubates, pellet the recipient strain cells via gentle centrifugation. Discard the supernatant and resuspend the cell pellet in 300 microliters of fresh LB containing 100 millimolar magnesium sulfate and five millimolar calcium chloride.
Next, set up the transduction reaction by combining 100 microliters of the recipient strain and 100 microliters of the donor phage lysate in a microcentrifuge tube. Then, set up the negative control by combining 100 microliters of the recipient strain and 100 microliters of the LB with magnesium sulfate and calcium chloride. After incubation, add 200 microliters of one molar sodium citrate and one milliliter of LB to both tubes, and mix by gently pipetting up and down. Then, after the tubes have been incubated for an hour, gently pellet the cells via centrifugation.
After centrifuging, discard the supernatant and resuspend the pelleted cells in 100 microliters of LB with 100 millimolar sodium citrate. Vortex the solutions and pipette the entire transduced sample onto an LB agar plate with 1X ampicillin. Finally, pipette the entire volume of the negative control cell mixture onto an LB agar plate without ampicillin. After incubating the plates overnight at 37 degrees Celsius, use a sterile pipette tip to pick three to four colonies from the transduction plate and streak them onto a new LB agar plate containing 1X ampicillin and 100 microliters of one molar sodium citrate. Repeat this plating method for the negative control on another LB agar plate containing only 100 microliters of one molar sodium citrate. Then, incubate the plates at 37 degrees Celsius overnight to allow colonies free of phage to grow.
The next day, wipe down the bench top with 70% ethanol before removing your plates from the incubator. Using a sterile pipette tip, pick three colonies from the transduction plate and add them each to a separate tube containing five milliliters of LB media. Then, select three colonies from the negative control plate and add them to another tube containing five milliliters of LB media. Grow the cultures overnight at 37 degrees Celsius with aeration and shaking at 220 rpm. After sterilizing the bench top as previously demonstrated, use a DNA miniprep kit to isolate DNA from 4.5 milliliters of each culture according to the manufacturer’s instructions. Then, elute the DNA with 35 microliters of nuclease-free water and measure the resulting concentration by lab spectrophotometer. Finally, prepare glycerol stocks by adding the remaining 0.5 milliliters of both bacterial solutions to 0.5 milliliters of 100% glycerol.
To confirm transduction, first prepare two qPCR master mixes for 24 qPCR reactions. For the first master mix, add 150 microliters of qPCR buffer mix to a microcentrifuge tube and 12 microliters each of a forward and reverse primer designed to amplify the ampicillin resistance gene. Next, prepare a second qPCR master mix by adding 150 microliters of qPCR master mix to a microcentrifuge tube and then adding 12 microliters each of a forward primer and reverse primer designed to amplify a housekeeping gene.
For each qPCR reaction, combine 100 micrograms of experimental DNA from each reaction with 14.5 microliters of qPCR master mix. Now, prepare the remaining reactions as previously demonstrated. Transfer the reactions to a thermocycler preheated to 94 degrees Celsius and then initiate the program. Finally, use the cycle quantification, or Cq, values generated by qPCR to calculate the normalized transduction efficiency of the ampicillin resistance gene.
The cycle quantitation, or Cq, values for the genes of interest were tabulated for each of the negative controls and transduced samples. Low Cq values, typically below 29 cycles, like the transduced samples in this example indicate high amounts of the target sequence.
A housekeeping gene, also tabulated here, is used as a loading control to normalize the amount of DNA in each reaction and as a positive control to ensure the qPCR is working. Provided the same amounts of the housekeeping gene are loaded, it is found at relatively the same rate in each sample.
Next, to calculate the delta Cq value for each sample, subtract the Cq value of the housekeeping gene for each sample from the Cq value of its corresponding target gene. For example, the delta Cq of the first negative control is 13.54. Then, use this value to calculate the normalized transduction efficiency of each sample using the formula shown here. Finally, the average normalized transduction efficiency for each sample group can be calculated.
