Flödescytometri protokoll för Surface och intracellulära Antigen Analyser av neurala celltyper
Summary
We provide a detailed description of a protocol for flow cytometric analysis of surface antigens and/or intracellular antigens in neural cell types. Critical aspects of experimental planning, step-by-step methodological procedures, and fundamental principles of flow cytometry are explained in order to enable neurobiologists to exploit this powerful technology.
Abstract
Flow cytometry has been extensively used to define cell populations in immunology, hematology and oncology. Here, we provide a detailed description of protocols for flow cytometric analysis of the cluster of differentiation (CD) surface antigens and intracellular antigens in neural cell types. Our step-by-step description of the methodological procedures include: the harvesting of neural in vitro cultures, an optional carboxyfluorescein succinimidyl ester (CFSE)-labeling step, followed by surface antigen staining with conjugated CD antibodies (e.g., CD24, CD54), and subsequent intracellar antigen detection via primary/secondary antibodies or fluorescently labeled Fab fragments (Zenon labeling). The video demonstrates the most critical steps. Moreover, principles of experimental planning, the inclusion of critical controls, and fundamentals of flow cytometric analysis (identification of target population and exclusion of debris; gating strategy; compensation for spectral overlap) are briefly explained in order to enable neurobiologists with limited prior knowledge or specific training in flow cytometry to assess its utility and to better exploit this powerful methodology.
Introduction
Flödescytometri har i stor utsträckning utnyttjats i immunologi, hematologi och onkologi att definiera cellpopulationer via inneboende spridningsegenskaper, cellytantigen uttryck och andra fluorescensparametrar 1-3. Våra insikter blodslinje utveckling och sjukdom är ett resultat av en betydande grad av kontinuerlig förfining av denna metod efter dess genomförande 4,5. Ökad medvetenhet om den kvantitativa och övergripande analytisk potential flödescytometri har nyligen uppmuntrat dess mer utbredd användning inom stamcellsforskning och kan möjliggöra på liknande djupgående framsteg på kortare tidsram 6. Däremot har tillämpningen av flödescytometri att specifikt analysera och isolera neurala populationer länge uppfattats som en utmaning. I motsats till hematopoetiska celler som naturligt finns i suspension, är neurala celltyper vanligen skördas från alltför komplicerade källor som kan innehålla glia och olika other omgivande celler såväl som ett intrikat nätverk av processbärande neuroner. Följaktligen måste neurobiologi ännu inte genomfört mångsidighet flödescytometri till dess fullständiga potential i dagliga forskningsrutiner. Men så länge som kan alstras en livskraftig enkelcellsuspension (och protokoll har utarbetats och optimerats för detta ändamål 7), flödescytometri och fluorescensaktiverad cellsortering (FACS) kan anses vara en värdefull del av den analytiska repertoar i neurobiologi 8-11.
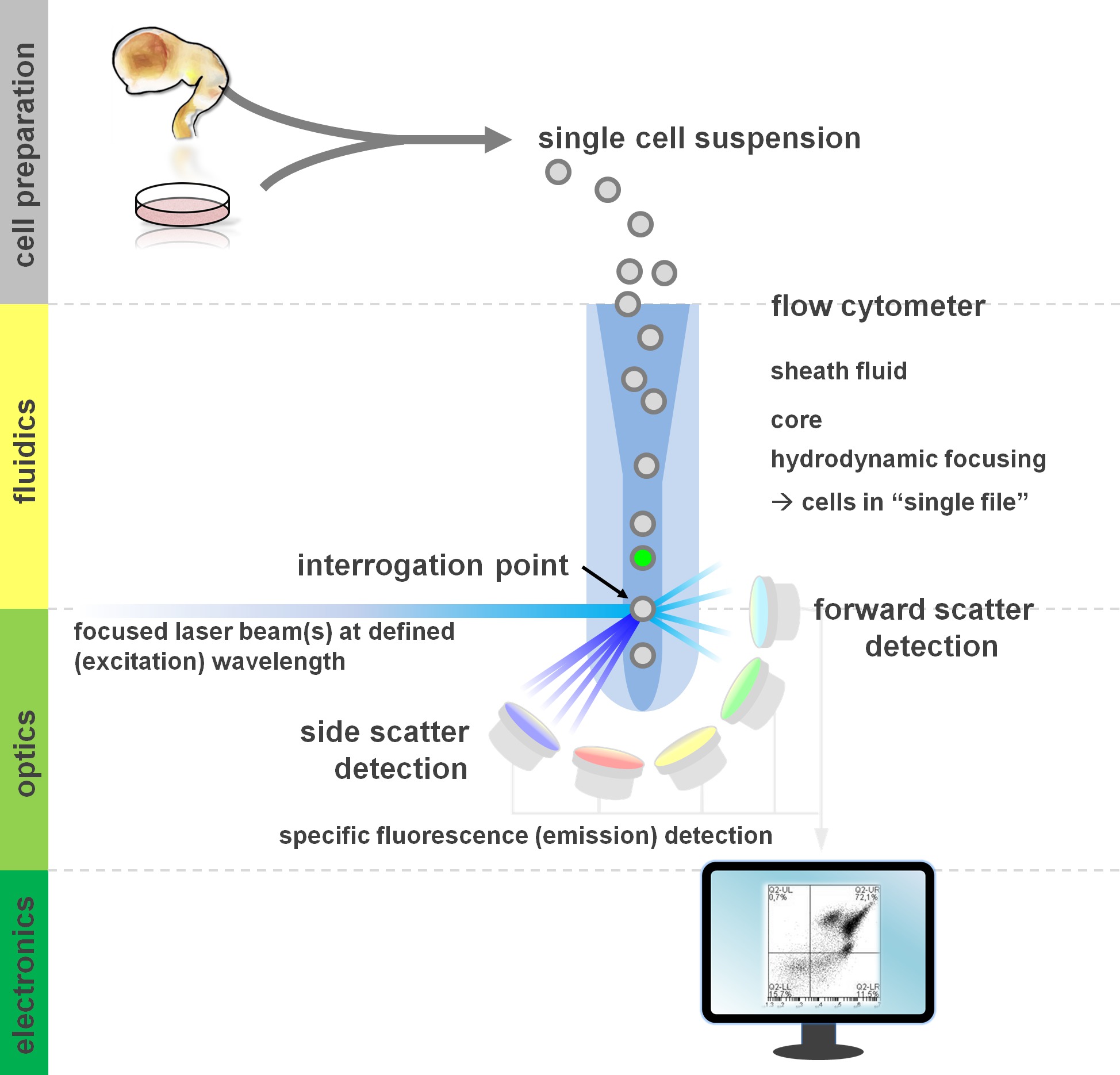
. Figur 1. Principen om flödescytometrianalyser och komponenter i en flödescytometer flödescytometrar omfattar tre huvudsystem: flödeskunskap, optik och elektronik. En strömlinjeformat flöde av celler i suspension (framställd från primär vävnad eller odling in vitro) åstadkommes genom manteln fluid via hydrodynamisk fokusering, begränsa urvalet till dess centrum kärna. De optiska delarna är sammansatta av lasrar som belyser flödet av celler och optiska filter som dirigerar signalen till lämpliga detektorer. Ljussignalerna detekterade omvandlas till elektroniska signaler, därefter behandlas av en dator och visualiseras på en bildskärm för dataanalys och gating. Klicka här för att se en större version av denna siffra.
Användare av flödescytometriska metoder vinst från åtminstone en grundläggande förståelse för de underliggande fundamenta, inklusive en cytometer byggstenar (för översikt se 12,13; se även figur 1). En laserstråle skär med en hydrodynamiskt fokuserad fluidic ström som innehåller celler i suspension, vilket i sin tur passerar genom laserstrålen i "enstaka fil" en efter en. Den interceptipå av en cell (eller någon annan partikel, för den delen) med laserresulterar i spridning av ljus från denna identifieringspunkt. Spritt ljus kan detekteras i fortsättning av laserriktningen (framåtspridning, associerad med storleken av partikeln), såväl som vinkelrätt mot dess riktning (sidospridning, vilket återspeglar granulosity av partikeln / cell). Dessa ovannämnda spridningsegenskaper inte kräver särskild märkning, vilket är anledningen till att en omärkt prov (eller också cellrester, luftbubblor, etc.) kommer att generera en signal (event) på bivariata framåtspridning mot sidopunktdiagram som vanligen används för inledande gating. Genom att använda lämpliga lasrar och filter specifika för motsvarande excitations- och emissionsspektra, kan en cell analyseras för dess positivitet, grad av styrka, eller frånvaro av fluorescerande markörer. Majoriteten av flödesapplikationer cytometrisk har fokuserat på karakterisering via cellytantigener. Till skillnad från det hematopoietiska lineage, har det neurala härstamning förblivit mindre utsträckning definieras enligt ytan epitop uttrycksmönster 5. En fördel med att utnyttja ytantigener är att levande celler kan utsättas för cellsortering paradigm såsom FACS. Däremot kräver intracellulär antigen färgning fixering och permeabilisering steg för att medla epitop-antikroppsinteraktion, utgör hinder tillämpningar efter som kräver levande celler. Notera sådana metoder kan fortfarande för många kvantitativa analyser 14 samt analyser nedströms för RNA och proteinuttryck 15. Hematologi, immunologi och onkologi har ofta använt mer än ett dussin markörer tillsammans för att definiera särskilda subpopulationer 16. Dessutom kan mass cytometri eller CyTOF nu användas för att analysera upp till 30 parametrar samtidigt 17,18.
För neurala stamceller samt primära kulturer 14,19,20 heterogeniteten av celler ivitro är ett vanligt fenomen 21-23. Cellerna inte representerar målgruppen intressanta förkroppsligar ett potentiellt confounding faktor för experimentell avläsning 24,25. Bekvämt, de olika cellulära delmängder som finns inom en heterogen cellsuspension bära distinkta (kända eller ännu Att att dechiffreras) antigen uttryck profiler, som kan användas för att definiera dessa olika populationer. Flödescytometri kan därmed spela en avgörande roll för att lösa cellulär heterogenitet och därigenom underlätta biomedicinska tillämpningar (in vitro-analyser, cellterapi) och optimera kvantitativa avläsning genom att fokusera på de mest relevanta delmängd 24,26. Olika ytantigen kombinationer har identifierats under de senaste åren för att göra det möjligt för kvantifiering och isolering av specifika neurala celltyper. Detta inkluderar CD133 för anrikning av neurala stamceller 27, en kombination av CD15 / CD24 / CD29 ytantigener för isolering av NSC, differentieringted neuron och neurallist celler 28 eller CD15 / CD24 / CD44 / CD184 / CD271 att isolera neurala och gliaceller delmängder 25, bland annat signaturer 29,30. Bortom neuroner, gliaceller markörer inkluderar A2B5 31, CD44 25, NG2 32 och GLAST 33. En färsk publikation har utnyttjat mitthjärnan floorplate gångaren markör CORIN 34,35 att anrika dopaminerga prekursorer vid Parkinsons celltransplantation paradigm 36. CD-molekyler är inte bara markörer, men funktionellt relevanta förmedlare av cell-cell interaktioner och i en cell förmåga att reagera på signaler från extracellulära matrixmolekyler och tillväxtfaktorer 37. En strategi för att ytterligare förbättra den arsenal av kombinatoriska CD antigener att karakterisera neurala härstamning utveckling är att använda kända intracellulära markörer för att screena för och definiera CD antigenkombinationer för en viss celltyp av intresse. Vi har nyligen utnyttjat ett sådant tillvägagångssätt och identifierade CD49f – / CD200 höga kombiuttrycksmönster som en ny metod för att berika neuronala delmängder från neuralt differentierade inducerad pluripotenta stamceller kultursystem 38. Här inkluderar vi och diskuterar det senare protokollet (och valfria variationer därav) där färgning yta och intracellulär färgning kan användas samtidigt för att definiera neurala cellsubpopulationer med flödescytometri.

Figur 2. Flödesdiagram av experimentella protokollalternativ. Figuren visar en schematisk representation av de viktigaste stegen i protokollet. Valfria steg (CFSE dye eller intracellulär antigen märkning) anges med ljusgrå lådor. Efter skörden, är det viktigt att bedöma lönsamheten och cell antal neurala cellsuspensioner före cellytan färgning. Positivt somsåväl som negativa kontroller måste ingå förutom de prover av intresse. Prover kan analyseras genom flödescytometrisk analys och / eller används i cellsortering paradigm. Klicka här för att se en större version av denna siffra.
Medan vi tidigare har använt primära antikroppen i kombination med sekundär antikropp för intracellulär färgning 38, introducerar vi nu icke kovalent märkning av den primära antikroppen via fluorescerande Fab-fragment (Zenon märkning) som en liten variation, vilket minskar stegen cellmanipulation 39. Dessutom som ytterligare ett exempel på protokollet mångsidighet, anställer vi en valfri märkning av en experimentell delmängd av karboxifluorescein succinimidylester (CFSE) före ytan antigen färgning. Sådana CFSE pre-märkning möjliggör omedelbara direkt jämförelse av två cellinjer eller experimentella förhållanden (CFSE-märkta vs. omärkt) inom en enda provrör, minska variansen eller subtila skillnader i inkubationstid och spara antikropp. CFSE är en etablerad fluorescerande färgämne som ofta används för att spåra cell 40, i spridnings 41,42 och streckkoder experiment 43,44. Slutligen medan faktiska sorteringssteg (FACS, immunomagnetisk cellseparations eller immunopanning) är inte en del av detta protokoll, i princip, avverknings- och märkningsförfaranden som beskrivs här gör avkastnings prover som kan utsättas för ytan antigen- eller intracellulära märkning baserade sorterings applikationer 15 25,28.
Med denna artikel vill vi: sammanfatta en livskraftig ytantigen färgningsprotokollet 25,28, sammanfatta ett protokoll för detektion av intracellulära mål samt kombinerad yta och intracellulär antigenanalys 38, presentera en intracellulär CFSE färgämne märkning steg 41,45 som en experimentell alternativ för comjämförande analyser av neurala cellpopulationer, och sammanfatta metoder för att flödescytometrianalyser (lämpliga kontroller 13,46, grind strategi och presentation av data 47).
Protocol
Representative Results
Discussion
Protokollet presenteras här är väl etablerad för neurala cellkulturer härledda från humana stamceller, men kan också tillämpas på andra neurala cellkällor inklusive primär vävnad eller neurala cellinjer. Förutom embryonala källor kan neurala stamceller eller progenitorceller extraheras från de neurogena regionerna av vuxna hjärnan 27. Dessutom flödescytometri och FACS kan utnyttjas för att kvantifiera, analysera och isolera olika cellpopulationer inklusive mogna nervceller 54, ast…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Our research program is funded through the Emmy Noether-Program of the German Research Foundation (DFG), grant PR1132/3-1. Further support by the Müller-Fahnenberg Foundation of the University of Freiburg is gratefully acknowledged. This study was supported in part by the Excellence Initiative of the German Research Foundation (GSC-4, Spemann Graduate School).
Materials
| DMEM/F12 (1:1) (Dulbecco's Modified Eagle Medium/Nutrient Mixture F-12) | Life Technologies | 11330057 | www.lifetechnologies.com | |
| DPBS without Ca2+ Mg2+ | Life Technologies | 14190169 | www.lifetechnologies.com | |
| Fetal bovine serum, qualified, E.U.-approved, South America origin (FBS) | Life Technologies | 10270-106 | www.lifetechnologies.com | |
| MEM Non-essential amino acids (100 x) | Life Technologies | 11140035 | www.lifetechnologies.com | |
| TrypLE Express | Life Technologies | 12604013 | www.lifetechnologies.com | |
| Trypan blue solution, 0.4% | Life Technologies | 15250061 | www.lifetechnologies.com | |
| Paraformaldehyde | Carl Roth | 335.3 | www.carlroth.com | |
| Bovine serum albumin (BSA) Fraction V | PAA Laboratories, Coelbe | K41-001 | www.gelifesciences.com | |
| Tween-20 Detergent | Calbiochem | 655205 | www.merckmillipore.de | |
| Carboxyfluorescein succinimidyl ester (CFSE) | eBioscience | 65-0850-84 | www.ebioscience.com | |
| DMSO | AppliChem | A1584 | www.applichem.com | |
| Bottle top filters express plus 0.22 µm, 250 ml | Millipore | SCGPU02RE | www.millipore.com | |
| Cell culture treated flasks (T 25) | NUNC | 156367 | www.thermoscientific.com | |
| Cell culture treated flasks (T 75) | NUNC | 156499 | www.thermoscientific.com | |
| Conical tubes (15 ml) | Greiner Bio-One | 188271 | www.greinerbioone.com | |
| Conical tubes (50 ml) | Greiner Bio-One | 227261 | www.greinerbioone.com | |
| Pasteur pipet, glass (150 mm) | STEIN Labortechnik, Remchingen | S03710150 | www.stein-labortechnik.de | |
| Pipet tips (0.1-10 µl) | Corning | 4125 | www.corning.com | |
| Pipet tips (1-200 µl) | Corning | 4126 | www.corning.com | |
| Pipet tips (100-1000 µl) | Corning | 4129 | www.corning.com | |
| Serological pipets, 5 ml | Corning | 4051 | www.corning.com | |
| Serological pipets, 10 ml | Corning | 4101 | www.corning.com | |
| Serological pipets, 25 ml | Corning | 4251 | www.corning.com | |
| Microcentrifuge tubes (0.5 ml) | Sarstedt | 72,699 | www.sarstedt.com | |
| Microcentrifuge tubes (1.5 ml) | Greiner Bio-One | 616201 | www.greinerbioone.com | |
| Microcentrifuge tubes (2.0 ml) | Sarstedt | 72,695,500 | www.sarstedt.com | |
| Anti-Human CD24 APC monoclonal antibody | eBioscience | 17-0247-42 | www.ebioscience.com Working dilution 1:50 |
|
| Anti-Human CD54 PE monoclonal antibody | eBioscience | 12-0549-42 | www.ebioscience.com Working dilution 1:50 |
|
| Neuronal Class III β-Tubulin (Tuj1) polyclonal antibody | Covance | PRB-435P | www.covance.com Working dilution 1:2000 |
|
| Alexa Fluor 488 Donkey anti Rabbit | Life Technologies | A21206 | www.lifetechnologies.com Working dilution 1:2000 |
|
| Zenon® Fluorescein Rabbit IgG Labeling Kit | Life Technologies | Z-25342 | www.lifetechnologies.com | |
| Neubauer-Improved counting chamber | Marienfeld | 0640010 | www.marienfeld-superior.com | |
| Vortex | Scientific Industries | G560E | www.scientificindustries.com | |
| Thermomixer comfort | Eppendorf | 5355 000.001 | www.eppendorf.com | |
| Accuri C6 flow cytometer | Becton Dickinson (BD) | 653118 | www.bdbiosciences.com/instruments/accuri | |
| Microcentrifuge refrigerated, PerfectSpin 24 R | Peqlab | 91-PSPIN-24R | www.peqlab.de | |
| Orbital shaker, Unimax 1010 | Heidolph | 543-12310-00 | www.heidolph-instruments.de | |
| Centrifuge refrigerated, Rotanta 96 RC | Hettich | 4480-50 | www.hettichlab.com | |
| Class II Biological safety cabinet Safe 2020 | Thermo Scientific | 51026640 | www.thermoscientific.com | |
| CO2 Incubator, Heracell 240i | Thermo Scientific | 51026331 | www.thermoscientific.com | |
| Vacuum system, Vacusafe comfort | Integra Biosciences | 158320 | www.integra-biosciences.de | |
| Microscope, Axiovert 40 CFL | Zeiss | 451212 | www.zeiss.de | |
| Pipet controller, accu-jet pro | Brand | 26303 | www.brand.de | |
| Micropipet, Pipetman neo P20N (2-20 µl) | Gilson | F144563 | www.gilson.com | |
| Micropipet, Pipetman neo P200N (20-200 µl) | Gilson | F144565 | www.gilson.com | |
| Micropipet, Pipetman neo P1000N (100-1000 µl) | Gilson | F144566 | www.gilson.com |
References
- Herzenberg, L. A., et al. The History and Future of the Fluorescence Activated Cell Sorter and Flow Cytometry: A View from. 48 (10), 1819-1827 (2002).
- Chattopadhyay, P. K., Roederer, M. Cytometry: today’s technology and tomorrow’s horizons. Methods (San Diego, Calif). 57 (3), 251-258 (2012).
- Jaye, D. L., Bray, R. A., Gebel, H. M., Harris, W. A. C., Waller, E. K. Translational applications of flow cytometry in clinical practice). J. Immunol. 188 (10), 4715-4719 (2012).
- Henel, G., Schmitz, J. Basic Theory and Clinical Applications of Flow Cytometry. Lab Med. 38 (7), 428-436 (2007).
- Seita, J., Weissman, I. L. Hematopoietic stem cell: self-renewal versus differentiation. Wiley Interdiscip. Rev. Syst. Biol. Med. 2 (6), 640-653 (2010).
- Ulrich, H., Bocsi, J. Phenotypes of stem cells from diverse origin. Cytometry. A. 77 (1), 6-10 (2010).
- Panchision, D. M., et al. Optimized flow cytometric analysis of central nervous system tissue reveals novel functional relationships among cells expressing CD133, CD15, and CD24. Stem cells. 25 (6), 1560-1570 (2007).
- Meyer, R. A., Zaruba, M. E., McKhann, G. M. Flow cytometry of isolated cells from the brain. Anal. Quant. Cytol. 2 (1), 66-74 (1980).
- Junger, H., Junger, W. G. CNTF and GDNF, but not NT-4, support corticospinal motor neuron growth via direct mechanisms. Neuroreport. 9 (16), 3749-3754 (1998).
- McLaren, F. H., Svendsen, C. N., Vander Meide, P., Joly, E. Analysis of neural stem cells by flow cytometry: cellular differentiation modifies patterns of MHC expression. J. Neuroimmunol. 112 (1-2), 35-46 (2001).
- Wang, S., Roy, N. S., Benraiss, A., Goldman, S. A. Promoter-based isolation and fluorescence-activated sorting of mitotic neuronal progenitor cells from the adult mammalian ependymal/subependymal. 22 (1-2), 167-176 (2000).
- Tanke, H. J., vander Keur, M. Selection of defined cell types by flow-cytometric cell sorting. Trends Biotechnol. 11 (2), 55-62 (1993).
- Baumgarth, N., Roederer, M. A practical approach to multicolor flow cytometry for immunophenotyping. J. Immunol. Methods. 243 (1-2), 77-97 (2000).
- Sergent-Tanguy, S., Chagneau, C., Neveu, I., Naveilhan, P. Fluorescent activated cell sorting (FACS): a rapid and reliable method to estimate the number of neurons in a mixed population. J. Neurosci. Methods. 129 (1), 73-79 (2003).
- Ernst, A., et al. Neurogenesis in the striatum of the adult human brain. Cell. 156 (5), 1072-1083 (2014).
- Perfetto, S. P., Chattopadhyay, P. K., Roederer, M. Seventeen-colour flow cytometry: unravelling the immune system. Nat. Rev. Immunol. 4 (8), 648-655 (2004).
- Bandura, D. R., et al. Mass cytometry: technique for real time single cell multitarget immunoassay based on inductively coupled plasma time-of-flight mass spectrometry. Anal. Chem. 81 (16), 6813-6822 (2009).
- Bendall, S. C., et al. Single-cell mass cytometry of differential immune and drug responses across a human hematopoietic continuum. Science. 332 (6030), 687-696 (2011).
- Neveu, I., Rémy, S., Naveilhan, P. The neuropeptide Y receptors, Y1 and Y2, are transiently and differentially expressed in the developing cerebellum. Neuroscience. 113 (4), 767-777 (2002).
- Pruszak, J., Just, L., Isacson, O., Nikkhah, G. Isolation and culture of ventral mesencephalic precursor cells and dopaminergic neurons from rodent brains. Curr. Protoc. Stem Cell Biol. 2 (Unit 2D.5), (2009).
- Suslov, O. N., Kukekov, V. G., Ignatova, T. N., Steindler, D. A. Neural stem cell heterogeneity demonstrated by molecular phenotyping of clonal neurospheres. Proc. Natl. Acad. Sci. U.S.A. 99 (22), 14506-14511 (2002).
- Bez, A., et al. Neurosphere and neurosphere-forming cells: morphological and ultrastructural characterization. Brain Res. 993 (1-2), 18-29 (2003).
- Pruszak, J., Isacson, O. Molecular and cellular determinants for generating ES-cell derived dopamine neurons for cell therapy. Adv. Exp. Med. Biol. 651, 112-123 (2009).
- Carson, C. T., Aigner, S., Gage, F. H. Stem cells: the good, bad and barely in control. Nat. Med. 12 (11), 1237-1238 (2006).
- Yuan, S. H., et al. Cell-surface marker signatures for the isolation of neural stem cells, glia and neurons derived from human pluripotent stem cells. PloS One. 6 (3), e17540 (2011).
- Roy, N. S., Cleren, C., Singh, S. K., Yang, L., Beal, M. F., Goldman, S. Functional engraftment of human ES cell-derived dopaminergic neurons enriched by coculture with telomerase-immortalized midbrain astrocytes. Nat. Med. 12 (11), 1259-1268 (2006).
- Uchida, N., et al. Direct isolation of human central nervous system stem cells. Proc. Natl. Acad. Sci. U. S. A. 97 (26), 14720-14725 (2000).
- Pruszak, J., Ludwig, W., Blak, A., Alavian, K., Isacson, O. CD15, CD24, and CD29 define a surface biomarker code for neural lineage differentiation of stem cells. Stem Cells. 27 (12), 2928-2940 (2009).
- Peh, G. S. -. L., Lang, R. J., Pera, M. F., Hawes, S. M. CD133 expression by neural progenitors derived from human embryonic stem cells and its use for their prospective isolation. Stem Cells Dev. 18 (2), 269-282 (2009).
- Golebiewska, A., Atkinson, S. P., Lako, M., Armstrong, L. Epigenetic landscaping during hESC differentiation to neural cells. Stem Cells. 27 (6), 1298-1308 (2009).
- Dietrich, J., Noble, M., Mayer-Proschel, M. Characterization of A2B5+ glial precursor cells from cryopreserved human fetal brain progenitor cells. Glia. 40 (1), 65-77 (2002).
- Nishiyama, A. NG2 cells in the brain: a novel glial cell population. Hum. Cell. 14 (1), 77-82 (2001).
- Jungblut, M., et al. Isolation and characterization of living primary astroglial cells using the new GLAST-specific monoclonal antibody ACSA-1. Glia. 60 (6), 894-907 (2012).
- Ono, Y., et al. Differences in neurogenic potential in floor plate cells along an anteroposterior location: midbrain dopaminergic neurons originate from mesencephalic floor plate cells. Development. 134 (17), 3213-3225 (2007).
- Chung, S., et al. ES cell-derived renewable and functional midbrain dopaminergic progenitors. Proc. Natl. Acad. Sci. U.S.A. 108 (23), 9703-9708 (2011).
- Doi, D., et al. Isolation of Human Induced Pluripotent Stem Cell-Derived Dopaminergic Progenitors by Cell Sorting for Successful Transplantation. Stem Cell Reports. 2 (3), 337-350 (2014).
- Solozobova, V., Wyvekens, N., Pruszak, J. Lessons from the embryonic neural stem cell niche for neural lineage differentiation of pluripotent stem cells. Stem Cell Rev. 8 (3), (2012).
- Turaç, G., et al. Combined flow cytometric analysis of surface and intracellular antigens reveals surface molecule markers of human neuropoiesis. PloS One. 8 (6), e68519 (2013).
- Buchwalow, I. B., Böcker, W. Chapter 2. Immunohistochemistry: Basics and Methods. , 9-17 (2010).
- Tario, J. D., et al. Optimized staining and proliferation modeling methods for cell division monitoring using cell tracking dyes. J. Vis. Exp. (70), e4287 (2012).
- Lyons, A. B., Parish, C. R. Determination of lymphocyte division by flow cytometry. J. Immunol. Methods. 171 (1), 131-137 (1994).
- Hawkins, E. D., et al. Measuring lymphocyte proliferation, survival and differentiation using CFSE time-series data. Nat. Protoc. 2 (9), 2057-2067 (2007).
- Quah, B. J. C., Parish, C. R. The use of carboxyfluorescein diacetate succinimidyl ester (CFSE) to monitor lymphocyte proliferation. J. Vis. Exp. 44, (2010).
- Sukhdeo, K., et al. Multiplex flow cytometry barcoding and antibody arrays identify surface antigen profiles of primary and metastatic colon cancer cell lines. PloS One. 8 (1), e53015 (2013).
- Jiang, L., et al. Daucosterol promotes the proliferation of neural stem cells. The J. Steroid Biochem. Mol. Biol. 140, 90-99 (2014).
- Hulspas, R., et al. Considerations for the control of background fluorescence in clinical flow cytometry. Cytometry. B. 76 (6), 355-364 (2009).
- Moloney, M., Shreffler, W. G. Basic science for the practicing physician: flow cytometry and cell sorting. Annals of Allergy, Asthm., & Immunology: Official Publication of the American College of Allergy, Asthma., & Immunology. 101 (5), 544-549 (2008).
- Siebzehnrubl, F. A., et al. Isolation and characterization of adult neural stem cells. Methods Mol. Biol. 750, 61-77 (2011).
- Guez-Barber, D., et al. FACS purification of immunolabeled cell types from adult rat brain). J. Neurosci. Methods. 203 (1), 10-18 (2012).
- Tham, C. -. S., Lin, F. -. F., Rao, T. S., Yu, N., Webb, M. Microglial activation state and lysophospholipid acid receptor expression. Int. J. Dev. Neurosci. 21 (8), 431-443 (2003).
- Nguyen, H. X., Beck, K. D., Anderson, A. J. Quantitative assessment of immune cells in the injured spinal cord tissue by flow cytometry: a novel use for a cell purification method. J. Vis. Exp. (50), e2698 (2011).
- Marchenko, S., Flanagan, L. Counting human neural stem cells. J. Vis. Exp. (7), 262 (2007).
- Brunlid, G., Pruszak, J., Holmes, B., Isacson, O., Sonntag, K. C. Immature and neurally differentiated mouse embryonic stem cells do not express a functional Fas/Fas ligand system. Stem Cells. 25 (10), 2551-2558 (2007).
- Brewer, G. J. Isolation and culture of adult rat hippocampal neurons. J. Neurosci. Methods. 71 (2), 143-155 (1997).
- Cardona, A. E., Huang, D., Sasse, M. E., Ransohoff, R. M. Isolation of murine microglial cells for RNA analysis or flow cytometry. Nat. Protoc. 1 (4), 1947-1951 (2006).
- Nielsen, J. A., Maric, D., Lau, P., Barker, J. L., Hudson, L. D. Identification of a novel oligodendrocyte cell adhesion protein using gene expression profiling. J. Neurosci. 26 (39), 9881-9891 (2006).
- Daneman, R., et al. The mouse blood-brain barrier transcriptome: a new resource for understanding the development and function of brain endothelial cells. PloS One. 5 (10), e13741 (2010).
- Gräbner, R., Till, U., Heller, R. Flow cytometric determination of E-selectin, vascular cell adhesion molecule-1, and intercellular cell adhesion molecule-1 in formaldehyde-fixed endothelial cell monolayers. Cytometry. 40 (3), 238-244 (2000).
- Quah, B. J. C., Parish, C. R. New and improved methods for measuring lymphocyte proliferation in vitro and in vivo using CFSE-like fluorescent dyes. J. Immunol. Methods. 379 (1-2), 1-14 (2012).
- Lathia, J. D., et al. High-throughput flow cytometry screening reveals a role for junctional adhesion molecule a as a cancer stem cell maintenance factor. Cell Rep. 6 (1), 117-129 (2014).
- Ganat, Y. M., et al. Identification of embryonic stem cell-derived midbrain dopaminergic neurons for engraftment. J. Clin. Invest. 122 (8), 2928-2939 (2012).
- Hedlund, E., et al. Embryonic stem cell-derived Pitx3-enhanced green fluorescent protein midbrain dopamine neurons survive enrichment by fluorescence-activated cell sorting and function in an animal model of Parkinson’s disease. Stem Cells. 26 (6), 1526-1536 (2008).
- Maroof, A. M., et al. Directed differentiation and functional maturation of cortical interneurons from human embryonic stem cells. Cell Stem Cell. 12 (5), 559-572 (2013).
- Chivet, M., Hemming, F., Pernet-Gallay, K., Fraboulet, S., Sadoul, R. Emerging role of neuronal exosomes in the central nervous system. Front. Physiol. 3, 145 (2012).
- Graner, M. W., et al. Proteomic and immunologic analyses of brain tumor exosomes. FASEB J. 23 (5), 1541-1557 (2009).
- Eldh, M., Lötvall, J. Isolation and characterization of RNA-containing exosomes. J. Vis. Exp. (59), e3037 (2012).
- Capela, A., Temple, S. LeX is expressed by principle progenitor cells in the embryonic nervous system, is secreted into their environment and binds Wnt-1. Dev. Biol. 291 (2), 300-313 (2006).
- Nieoullon, V., Belvindrah, R., Rougon, G., Chazal, G. mCD24 regulates proliferation of neuronal committed precursors in the subventricular zone. Mol. Cell. Neurosci. 28 (3), 462-474 (2005).
- Nagato, M., et al. Prospective characterization of neural stem cells by flow cytometry analysis using a combination of surface markers. J. Neurosci. Res. 80 (4), 456-466 (2005).
- Hall, P. E., Lathia, J. D., Miller, N. G. A., Caldwell, M. A., French-Constant, C. Integrins are markers of human neural stem cells. Stem Cells. 24 (9), 2078-2084 (2006).
- Hargus, G., et al. Differentiated Parkinson patient-derived induced pluripotent stem cells grow in the adult rodent brain and reduce motor asymmetry in Parkinsonian rats. Proc. Natl. Acad. Sci. U.S.A. 107 (36), 15921-15926 (2010).
- Elkabetz, Y., et al. Human ES cell-derived neural rosettes reveal a functionally distinct early neural stem cell stage. Genes Dev. 22 (2), 152-165 (2008).

