Flowcytometrisystemer protokoller for Surface og Intracellulær Antigen Analyser av Neural celletyper
Summary
We provide a detailed description of a protocol for flow cytometric analysis of surface antigens and/or intracellular antigens in neural cell types. Critical aspects of experimental planning, step-by-step methodological procedures, and fundamental principles of flow cytometry are explained in order to enable neurobiologists to exploit this powerful technology.
Abstract
Flow cytometry has been extensively used to define cell populations in immunology, hematology and oncology. Here, we provide a detailed description of protocols for flow cytometric analysis of the cluster of differentiation (CD) surface antigens and intracellular antigens in neural cell types. Our step-by-step description of the methodological procedures include: the harvesting of neural in vitro cultures, an optional carboxyfluorescein succinimidyl ester (CFSE)-labeling step, followed by surface antigen staining with conjugated CD antibodies (e.g., CD24, CD54), and subsequent intracellar antigen detection via primary/secondary antibodies or fluorescently labeled Fab fragments (Zenon labeling). The video demonstrates the most critical steps. Moreover, principles of experimental planning, the inclusion of critical controls, and fundamentals of flow cytometric analysis (identification of target population and exclusion of debris; gating strategy; compensation for spectral overlap) are briefly explained in order to enable neurobiologists with limited prior knowledge or specific training in flow cytometry to assess its utility and to better exploit this powerful methodology.
Introduction
Flowcytometri har blitt grundig utnyttet i immunologi, hematologi og onkologi å definere celle populasjoner via iboende scatter egenskaper, celleoverflateantigen uttrykk og andre fluorescens parametre 1-3. Våre innsikt i blod avstamning utvikling og sykdom er et resultat av en betydelig grad av den kontinuerlige forbedringer av denne metoden etter dens første 4,5 gjennomføringen. Økt bevissthet om kvantitative og generell analytisk potensial flowcytometri har nylig oppfordret sine mer utbredt bruk i stamcelleforskning, og kan gjøre det mulig tilsvar dyp fremgang i en kortere tidsramme 6. Imidlertid har anvendelsen av flowcytometri for spesifikt å analysere og isolere nervepopulasjoner lenge vært oppfattet som utfordrende. I motsetning til hematopoetiske celler som naturlig finnes i suspensjonen, er neurale celletyper vanligvis høstet fra overdrevent komplekse kilder som kan innbefatte gliaceller og diverse other omliggende celler samt et intrikat nettverk av prosessbærende nevroner. Derfor har nevrobiologi ennå å implementere allsidigheten flowcytometri til sin fullstendige potensialet i daglige forsknings rutiner. Imidlertid, så lenge som en levedyktig, enkel cellesuspensjon kan genereres (og protokoller er utviklet og optimalisert for det formålet 7), flowcytometri og fluorescens-aktivert cellesortering (FACS) kan betraktes som en verdifull del av analyse repertoar i neurobiology 8-11.
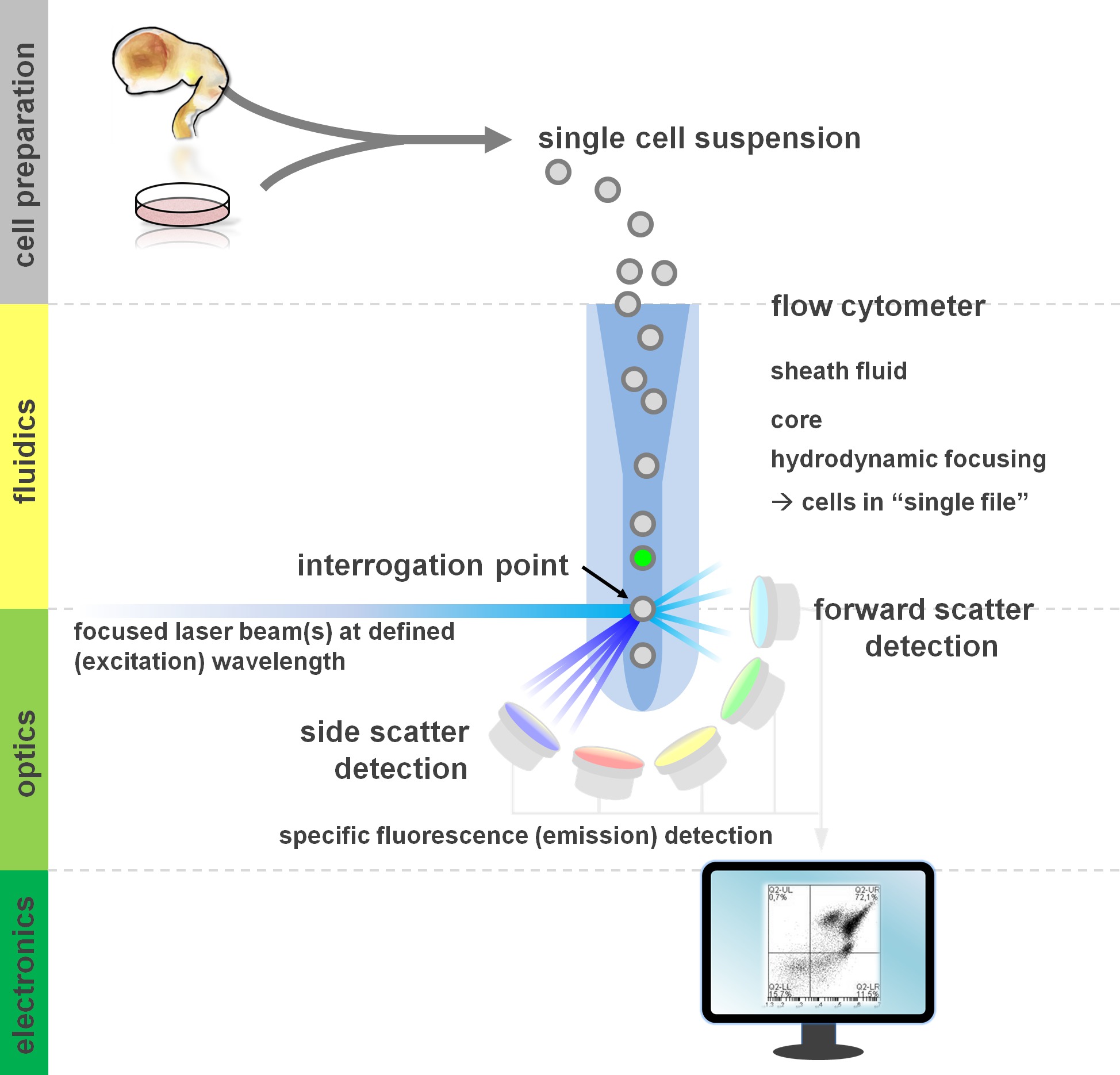
. Figur 1. Prinsipp for flowcytometrisk analyse og komponenter av et flowcytometer flowcytometere består av tre hovedsystemer: fluidics, optikk og elektronikk. En strømlinjeformet strøm av celler i suspensjon (fremstilt fra primært eller vev in vitro kultur) oppnås ved kappen fluid via hydrodynamisk fokusering, begrenser prøven til dets midtkjernen. De optiske deler er sammensatt av lasere som belyser strømmen av celler og optiske filtre som styrer signalet til de passende detektorer. Lyssignalene oppdaget konverteres til elektroniske signaler, deretter behandles av en datamaskin og visualisert på en monitor for dataanalyse og gating. Klikk her for å se en større versjon av dette tallet.
Brukere av strømningscytometriske metoder overskudd fra minst en grunnleggende forståelse av de underliggende fundamentale forhold, inkludert en cytometer byggesteiner (for oversikt se 12,13, se også figur 1). En laserstråle skjærer med en hydrodynamisk fokusert fluidstrømmen som inneholder de celler i suspensjonen, som i sin tur passerer gjennom laserstrålen i 'enkelt fil' etter hverandre. Den interceptipå i en celle (eller enhver annen partikkel, for den saks skyld) med laser resulterer i spredning av lyset fra denne utspørringspunktet. Spredt lys kan detekteres i fortsettelse av laserretningen (forover spredning, forbundet med størrelsen av partikkelen), samt vinkelrett på retningen (side scatter; reflekterer granulosity av partikkel / celle). Disse nevnte spredningsegenskaper ikke krever spesiell merking, noe som er grunnen til at en umerket prøve (eller også mobilnettet rusk, luftbobler, etc.) vil generere et signal (hendelse) på bivariate fremover scatter versus side spredningsdiagram som vanligvis brukes til innledende gating. Ved å bruke de passende lasere og filtre som er spesifikke for den tilhørende eksitasjon og emisjonsspektra, kan en celle bli analysert for sin positivitet, nivå av intensitet eller fravær av fluorescerende markører. Flertallet av strømningscytometriske applikasjoner har fokusert på karakterisering via celleoverflateantigener. I motsetning til blodkreft lineage har nevrale avstamning forble mindre omfattende definert i henhold til overflaten epitope uttrykk mønstre fem. En fordel med å utnytte overflateantigener er at levende celler kan utsettes for cellesortering paradigmer som FACS. I kontrast, krever intracellulær antigen flekker fiksering og permeabilization skritt for å mekle epitopet-antistoff samhandling, utelukker nedstrøms applikasjoner som krever levedyktige celler. Av notatet, slike tilnærminger fortsatt tillate for mange kvantitative analyser 14 samt nedstrøms analyser for RNA og protein uttrykk 15. Hematologi, immunologi og onkologi har ofte brukt mer enn et dusin markører i forbindelse å definere bestemte subpopulasjoner 16. Dessuten kan massen cytometri eller CyTOF nå bli brukt til å analysere opptil 30 parametere samtidig, 17,18.
For nevrale stamcelle applikasjoner samt primærkulturer 14,19,20 den heterogenitet av celler ivitro er et vanlig fenomen 21-23. Cellene ikke representerer målgruppen av interesse legemliggjøre et potensielt problemfaktor for eksperimentell avlesning 24,25. Hensiktsmessig de forskjellige cellulære undersett som er tilstede i en heterogen cellesuspensjon bærer distinkte (som er kjent eller som vil bli tydet) antigen ekspresjon profiler, som kan benyttes for å definere disse forskjellige populasjonene. Flowcytometri kan dermed spille en avgjørende rolle i å løse cellulære heterogenitet og dermed legge til rette for biomedisinske applikasjoner (in vitro, celleterapi) og optimalisere kvantitativ avlesning ved å fokusere på den mest relevante undergruppe 24,26. Forskjellige overflate antigen kombinasjoner er blitt identifisert i løpet av de siste årene for å tillate kvantitering og isolering av bestemte neurale celletyper. Dette omfatter CD133 for anriking av nevrale stamceller 27, slik at kombinasjonen av de CD15 / CD24 / CD29-overflateantigener for isolering av NSC, differentiated nevron og neural crest celler 28 eller CD15 / CD24 / CD44 / CD184 / CD271 å isolere nevrale og gliaceller undergrupper 25, blant andre signaturer 29,30. Utover nevroner, gliaceller markører A2B5 31, CD44 25, NG2 32 og GLAST 33. En fersk publikasjon har utnyttet den midthjernen gulv forløper markør CORIN 34,35 å berike for dopaminerge forløpere i Parkinson celletransplantasjon paradigmer 36. CD-molekyler er ikke bare markører, men funksjonelt relevante mediatorer av celle-celle interaksjoner og i en celle evne til å svare på signaler fra ekstracellulære matrise molekyler og vekstfaktorer 37. En strategi for ytterligere styrking av arsenal av kombinatoriske CD antigener å karakter nevrale avstamning utvikling er å bruke kjente intracellulære markører for å screene for og definere CD antigen kombinasjoner for en bestemt celletype av interesse. Vi har nylig utnyttes slik tilnærming og identifisert CD49f – / CD200 høye kombinatoriske uttrykk mønstre som en ny tilnærming for berikende nevronale undergrupper fra nevralt differensierte indusert pluripotente stamceller kultursystemer 38. Her inkluderer vi diskutere og den sistnevnte protokoll (og eventuelle variasjoner derav), hvor overflatefarging og intracellulær farging kan brukes samtidig for å definere nervecellepopulasjoner ved strømningscytometri.

Figur 2 viser et flytdiagram av eksperimentelle protokoll alternativer. Figuren viser en skjematisk fremstilling av de viktigste trinnene involvert i protokollen. Valgfritt trinn (CFSE dye eller intracellulær antigen merking) er angitt med lys grå ruter. Etter høsting, er det viktig å vurdere levedyktigheten og celleantallet av nervecellesuspensjoner før celleoverflatefarging. Positiv somvel som negative kontroller trenger å være inkludert i tillegg til prøvene av interesse. Prøvene kan analyseres ved flowcytometrisk analyse og / eller brukes i celle sortering paradigmer. Klikk her for å se en større versjon av dette tallet.
Mens vi tidligere har brukt primært antistoff i kombinasjon med sekundært antistoff for intracellulær farging 38, introduserer vi nå ikke-kovalent merking av det primære antistoff via fluorescerende Fab-fragmenter (Zenon merking) som en svak variant, for derved å redusere de trinn celle 39 manipulasjon. Videre, som et ytterligere eksempel på protokoll allsidighet, anvender vi en eventuell merking av en eksperimentell undergruppe av karboksyfluorescein succinimidylester (CFSE) før overflateantigen farging. Slike CFSE pre-merking muliggjør umiddelbar direkte sammenligning av to cellelinjer eller eksperimentelle betingelser (CFSE-merket vs. umerket) i et enkelt prøverør, redusere avviket eller små forskjeller i inkubasjonstid og lagring av antistoff. CFSE er en etablert fluorescerende fargestoff som vanligvis brukes for celle sporing 40, i sprednings 41,42 og strekkoding eksperimenter 43,44. Til slutt, mens selve sorterings trinn (FACS, immunomagnetisk Celleseparasjonsanordningene eller immunopanning) er ikke en del av denne protokollen, i prinsippet, slakteriene og merking prosedyrene som er beskrevet her gjør avkastning prøver som kan utsettes til overflaten antigen eller intracellulære merking basert sortering applikasjoner 15 25,28.
Med denne artikkelen, vi tar sikte på å: oppsummere en levedyktig overflateantigen farging protokollen 25,28, oppsummere en protokoll for påvisning av intracellulære mål samt kombinert overflate og intracellulær antigen analyse 38, presentere en intracellulær CFSE fargestoff merking steg 41,45 som en eksperimentell alternativ for comkomparative analyser av nervecellepopulasjoner, og oppsummere tilnærminger til flowcytometri analyse (hensiktsmessige kontroller 13,46, gating strategi og datapresentasjon 47).
Protocol
Representative Results
Discussion
Protokollen som presenteres her er vel etablert for neural cellekulturer avledet fra humane stamceller, men kan like anvendes på andre neurale cellekilder, inkludert primære neural vev eller cellelinjer. I tillegg til embryonale kilder, kan neurale stamceller og forløperceller ekstraheres fra den nevrogene regioner av voksen hjerne 27. Videre flow cytometri og FACS kan utnyttes til å kvantifisere, analysere og isolere forskjellige cellepopulasjoner, inkludert moden nerveceller 54, 33, astroglia…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Our research program is funded through the Emmy Noether-Program of the German Research Foundation (DFG), grant PR1132/3-1. Further support by the Müller-Fahnenberg Foundation of the University of Freiburg is gratefully acknowledged. This study was supported in part by the Excellence Initiative of the German Research Foundation (GSC-4, Spemann Graduate School).
Materials
| DMEM/F12 (1:1) (Dulbecco's Modified Eagle Medium/Nutrient Mixture F-12) | Life Technologies | 11330057 | www.lifetechnologies.com | |
| DPBS without Ca2+ Mg2+ | Life Technologies | 14190169 | www.lifetechnologies.com | |
| Fetal bovine serum, qualified, E.U.-approved, South America origin (FBS) | Life Technologies | 10270-106 | www.lifetechnologies.com | |
| MEM Non-essential amino acids (100 x) | Life Technologies | 11140035 | www.lifetechnologies.com | |
| TrypLE Express | Life Technologies | 12604013 | www.lifetechnologies.com | |
| Trypan blue solution, 0.4% | Life Technologies | 15250061 | www.lifetechnologies.com | |
| Paraformaldehyde | Carl Roth | 335.3 | www.carlroth.com | |
| Bovine serum albumin (BSA) Fraction V | PAA Laboratories, Coelbe | K41-001 | www.gelifesciences.com | |
| Tween-20 Detergent | Calbiochem | 655205 | www.merckmillipore.de | |
| Carboxyfluorescein succinimidyl ester (CFSE) | eBioscience | 65-0850-84 | www.ebioscience.com | |
| DMSO | AppliChem | A1584 | www.applichem.com | |
| Bottle top filters express plus 0.22 µm, 250 ml | Millipore | SCGPU02RE | www.millipore.com | |
| Cell culture treated flasks (T 25) | NUNC | 156367 | www.thermoscientific.com | |
| Cell culture treated flasks (T 75) | NUNC | 156499 | www.thermoscientific.com | |
| Conical tubes (15 ml) | Greiner Bio-One | 188271 | www.greinerbioone.com | |
| Conical tubes (50 ml) | Greiner Bio-One | 227261 | www.greinerbioone.com | |
| Pasteur pipet, glass (150 mm) | STEIN Labortechnik, Remchingen | S03710150 | www.stein-labortechnik.de | |
| Pipet tips (0.1-10 µl) | Corning | 4125 | www.corning.com | |
| Pipet tips (1-200 µl) | Corning | 4126 | www.corning.com | |
| Pipet tips (100-1000 µl) | Corning | 4129 | www.corning.com | |
| Serological pipets, 5 ml | Corning | 4051 | www.corning.com | |
| Serological pipets, 10 ml | Corning | 4101 | www.corning.com | |
| Serological pipets, 25 ml | Corning | 4251 | www.corning.com | |
| Microcentrifuge tubes (0.5 ml) | Sarstedt | 72,699 | www.sarstedt.com | |
| Microcentrifuge tubes (1.5 ml) | Greiner Bio-One | 616201 | www.greinerbioone.com | |
| Microcentrifuge tubes (2.0 ml) | Sarstedt | 72,695,500 | www.sarstedt.com | |
| Anti-Human CD24 APC monoclonal antibody | eBioscience | 17-0247-42 | www.ebioscience.com Working dilution 1:50 |
|
| Anti-Human CD54 PE monoclonal antibody | eBioscience | 12-0549-42 | www.ebioscience.com Working dilution 1:50 |
|
| Neuronal Class III β-Tubulin (Tuj1) polyclonal antibody | Covance | PRB-435P | www.covance.com Working dilution 1:2000 |
|
| Alexa Fluor 488 Donkey anti Rabbit | Life Technologies | A21206 | www.lifetechnologies.com Working dilution 1:2000 |
|
| Zenon® Fluorescein Rabbit IgG Labeling Kit | Life Technologies | Z-25342 | www.lifetechnologies.com | |
| Neubauer-Improved counting chamber | Marienfeld | 0640010 | www.marienfeld-superior.com | |
| Vortex | Scientific Industries | G560E | www.scientificindustries.com | |
| Thermomixer comfort | Eppendorf | 5355 000.001 | www.eppendorf.com | |
| Accuri C6 flow cytometer | Becton Dickinson (BD) | 653118 | www.bdbiosciences.com/instruments/accuri | |
| Microcentrifuge refrigerated, PerfectSpin 24 R | Peqlab | 91-PSPIN-24R | www.peqlab.de | |
| Orbital shaker, Unimax 1010 | Heidolph | 543-12310-00 | www.heidolph-instruments.de | |
| Centrifuge refrigerated, Rotanta 96 RC | Hettich | 4480-50 | www.hettichlab.com | |
| Class II Biological safety cabinet Safe 2020 | Thermo Scientific | 51026640 | www.thermoscientific.com | |
| CO2 Incubator, Heracell 240i | Thermo Scientific | 51026331 | www.thermoscientific.com | |
| Vacuum system, Vacusafe comfort | Integra Biosciences | 158320 | www.integra-biosciences.de | |
| Microscope, Axiovert 40 CFL | Zeiss | 451212 | www.zeiss.de | |
| Pipet controller, accu-jet pro | Brand | 26303 | www.brand.de | |
| Micropipet, Pipetman neo P20N (2-20 µl) | Gilson | F144563 | www.gilson.com | |
| Micropipet, Pipetman neo P200N (20-200 µl) | Gilson | F144565 | www.gilson.com | |
| Micropipet, Pipetman neo P1000N (100-1000 µl) | Gilson | F144566 | www.gilson.com |
References
- Herzenberg, L. A., et al. The History and Future of the Fluorescence Activated Cell Sorter and Flow Cytometry: A View from. 48 (10), 1819-1827 (2002).
- Chattopadhyay, P. K., Roederer, M. Cytometry: today’s technology and tomorrow’s horizons. Methods (San Diego, Calif). 57 (3), 251-258 (2012).
- Jaye, D. L., Bray, R. A., Gebel, H. M., Harris, W. A. C., Waller, E. K. Translational applications of flow cytometry in clinical practice). J. Immunol. 188 (10), 4715-4719 (2012).
- Henel, G., Schmitz, J. Basic Theory and Clinical Applications of Flow Cytometry. Lab Med. 38 (7), 428-436 (2007).
- Seita, J., Weissman, I. L. Hematopoietic stem cell: self-renewal versus differentiation. Wiley Interdiscip. Rev. Syst. Biol. Med. 2 (6), 640-653 (2010).
- Ulrich, H., Bocsi, J. Phenotypes of stem cells from diverse origin. Cytometry. A. 77 (1), 6-10 (2010).
- Panchision, D. M., et al. Optimized flow cytometric analysis of central nervous system tissue reveals novel functional relationships among cells expressing CD133, CD15, and CD24. Stem cells. 25 (6), 1560-1570 (2007).
- Meyer, R. A., Zaruba, M. E., McKhann, G. M. Flow cytometry of isolated cells from the brain. Anal. Quant. Cytol. 2 (1), 66-74 (1980).
- Junger, H., Junger, W. G. CNTF and GDNF, but not NT-4, support corticospinal motor neuron growth via direct mechanisms. Neuroreport. 9 (16), 3749-3754 (1998).
- McLaren, F. H., Svendsen, C. N., Vander Meide, P., Joly, E. Analysis of neural stem cells by flow cytometry: cellular differentiation modifies patterns of MHC expression. J. Neuroimmunol. 112 (1-2), 35-46 (2001).
- Wang, S., Roy, N. S., Benraiss, A., Goldman, S. A. Promoter-based isolation and fluorescence-activated sorting of mitotic neuronal progenitor cells from the adult mammalian ependymal/subependymal. 22 (1-2), 167-176 (2000).
- Tanke, H. J., vander Keur, M. Selection of defined cell types by flow-cytometric cell sorting. Trends Biotechnol. 11 (2), 55-62 (1993).
- Baumgarth, N., Roederer, M. A practical approach to multicolor flow cytometry for immunophenotyping. J. Immunol. Methods. 243 (1-2), 77-97 (2000).
- Sergent-Tanguy, S., Chagneau, C., Neveu, I., Naveilhan, P. Fluorescent activated cell sorting (FACS): a rapid and reliable method to estimate the number of neurons in a mixed population. J. Neurosci. Methods. 129 (1), 73-79 (2003).
- Ernst, A., et al. Neurogenesis in the striatum of the adult human brain. Cell. 156 (5), 1072-1083 (2014).
- Perfetto, S. P., Chattopadhyay, P. K., Roederer, M. Seventeen-colour flow cytometry: unravelling the immune system. Nat. Rev. Immunol. 4 (8), 648-655 (2004).
- Bandura, D. R., et al. Mass cytometry: technique for real time single cell multitarget immunoassay based on inductively coupled plasma time-of-flight mass spectrometry. Anal. Chem. 81 (16), 6813-6822 (2009).
- Bendall, S. C., et al. Single-cell mass cytometry of differential immune and drug responses across a human hematopoietic continuum. Science. 332 (6030), 687-696 (2011).
- Neveu, I., Rémy, S., Naveilhan, P. The neuropeptide Y receptors, Y1 and Y2, are transiently and differentially expressed in the developing cerebellum. Neuroscience. 113 (4), 767-777 (2002).
- Pruszak, J., Just, L., Isacson, O., Nikkhah, G. Isolation and culture of ventral mesencephalic precursor cells and dopaminergic neurons from rodent brains. Curr. Protoc. Stem Cell Biol. 2 (Unit 2D.5), (2009).
- Suslov, O. N., Kukekov, V. G., Ignatova, T. N., Steindler, D. A. Neural stem cell heterogeneity demonstrated by molecular phenotyping of clonal neurospheres. Proc. Natl. Acad. Sci. U.S.A. 99 (22), 14506-14511 (2002).
- Bez, A., et al. Neurosphere and neurosphere-forming cells: morphological and ultrastructural characterization. Brain Res. 993 (1-2), 18-29 (2003).
- Pruszak, J., Isacson, O. Molecular and cellular determinants for generating ES-cell derived dopamine neurons for cell therapy. Adv. Exp. Med. Biol. 651, 112-123 (2009).
- Carson, C. T., Aigner, S., Gage, F. H. Stem cells: the good, bad and barely in control. Nat. Med. 12 (11), 1237-1238 (2006).
- Yuan, S. H., et al. Cell-surface marker signatures for the isolation of neural stem cells, glia and neurons derived from human pluripotent stem cells. PloS One. 6 (3), e17540 (2011).
- Roy, N. S., Cleren, C., Singh, S. K., Yang, L., Beal, M. F., Goldman, S. Functional engraftment of human ES cell-derived dopaminergic neurons enriched by coculture with telomerase-immortalized midbrain astrocytes. Nat. Med. 12 (11), 1259-1268 (2006).
- Uchida, N., et al. Direct isolation of human central nervous system stem cells. Proc. Natl. Acad. Sci. U. S. A. 97 (26), 14720-14725 (2000).
- Pruszak, J., Ludwig, W., Blak, A., Alavian, K., Isacson, O. CD15, CD24, and CD29 define a surface biomarker code for neural lineage differentiation of stem cells. Stem Cells. 27 (12), 2928-2940 (2009).
- Peh, G. S. -. L., Lang, R. J., Pera, M. F., Hawes, S. M. CD133 expression by neural progenitors derived from human embryonic stem cells and its use for their prospective isolation. Stem Cells Dev. 18 (2), 269-282 (2009).
- Golebiewska, A., Atkinson, S. P., Lako, M., Armstrong, L. Epigenetic landscaping during hESC differentiation to neural cells. Stem Cells. 27 (6), 1298-1308 (2009).
- Dietrich, J., Noble, M., Mayer-Proschel, M. Characterization of A2B5+ glial precursor cells from cryopreserved human fetal brain progenitor cells. Glia. 40 (1), 65-77 (2002).
- Nishiyama, A. NG2 cells in the brain: a novel glial cell population. Hum. Cell. 14 (1), 77-82 (2001).
- Jungblut, M., et al. Isolation and characterization of living primary astroglial cells using the new GLAST-specific monoclonal antibody ACSA-1. Glia. 60 (6), 894-907 (2012).
- Ono, Y., et al. Differences in neurogenic potential in floor plate cells along an anteroposterior location: midbrain dopaminergic neurons originate from mesencephalic floor plate cells. Development. 134 (17), 3213-3225 (2007).
- Chung, S., et al. ES cell-derived renewable and functional midbrain dopaminergic progenitors. Proc. Natl. Acad. Sci. U.S.A. 108 (23), 9703-9708 (2011).
- Doi, D., et al. Isolation of Human Induced Pluripotent Stem Cell-Derived Dopaminergic Progenitors by Cell Sorting for Successful Transplantation. Stem Cell Reports. 2 (3), 337-350 (2014).
- Solozobova, V., Wyvekens, N., Pruszak, J. Lessons from the embryonic neural stem cell niche for neural lineage differentiation of pluripotent stem cells. Stem Cell Rev. 8 (3), (2012).
- Turaç, G., et al. Combined flow cytometric analysis of surface and intracellular antigens reveals surface molecule markers of human neuropoiesis. PloS One. 8 (6), e68519 (2013).
- Buchwalow, I. B., Böcker, W. Chapter 2. Immunohistochemistry: Basics and Methods. , 9-17 (2010).
- Tario, J. D., et al. Optimized staining and proliferation modeling methods for cell division monitoring using cell tracking dyes. J. Vis. Exp. (70), e4287 (2012).
- Lyons, A. B., Parish, C. R. Determination of lymphocyte division by flow cytometry. J. Immunol. Methods. 171 (1), 131-137 (1994).
- Hawkins, E. D., et al. Measuring lymphocyte proliferation, survival and differentiation using CFSE time-series data. Nat. Protoc. 2 (9), 2057-2067 (2007).
- Quah, B. J. C., Parish, C. R. The use of carboxyfluorescein diacetate succinimidyl ester (CFSE) to monitor lymphocyte proliferation. J. Vis. Exp. 44, (2010).
- Sukhdeo, K., et al. Multiplex flow cytometry barcoding and antibody arrays identify surface antigen profiles of primary and metastatic colon cancer cell lines. PloS One. 8 (1), e53015 (2013).
- Jiang, L., et al. Daucosterol promotes the proliferation of neural stem cells. The J. Steroid Biochem. Mol. Biol. 140, 90-99 (2014).
- Hulspas, R., et al. Considerations for the control of background fluorescence in clinical flow cytometry. Cytometry. B. 76 (6), 355-364 (2009).
- Moloney, M., Shreffler, W. G. Basic science for the practicing physician: flow cytometry and cell sorting. Annals of Allergy, Asthm., & Immunology: Official Publication of the American College of Allergy, Asthma., & Immunology. 101 (5), 544-549 (2008).
- Siebzehnrubl, F. A., et al. Isolation and characterization of adult neural stem cells. Methods Mol. Biol. 750, 61-77 (2011).
- Guez-Barber, D., et al. FACS purification of immunolabeled cell types from adult rat brain). J. Neurosci. Methods. 203 (1), 10-18 (2012).
- Tham, C. -. S., Lin, F. -. F., Rao, T. S., Yu, N., Webb, M. Microglial activation state and lysophospholipid acid receptor expression. Int. J. Dev. Neurosci. 21 (8), 431-443 (2003).
- Nguyen, H. X., Beck, K. D., Anderson, A. J. Quantitative assessment of immune cells in the injured spinal cord tissue by flow cytometry: a novel use for a cell purification method. J. Vis. Exp. (50), e2698 (2011).
- Marchenko, S., Flanagan, L. Counting human neural stem cells. J. Vis. Exp. (7), 262 (2007).
- Brunlid, G., Pruszak, J., Holmes, B., Isacson, O., Sonntag, K. C. Immature and neurally differentiated mouse embryonic stem cells do not express a functional Fas/Fas ligand system. Stem Cells. 25 (10), 2551-2558 (2007).
- Brewer, G. J. Isolation and culture of adult rat hippocampal neurons. J. Neurosci. Methods. 71 (2), 143-155 (1997).
- Cardona, A. E., Huang, D., Sasse, M. E., Ransohoff, R. M. Isolation of murine microglial cells for RNA analysis or flow cytometry. Nat. Protoc. 1 (4), 1947-1951 (2006).
- Nielsen, J. A., Maric, D., Lau, P., Barker, J. L., Hudson, L. D. Identification of a novel oligodendrocyte cell adhesion protein using gene expression profiling. J. Neurosci. 26 (39), 9881-9891 (2006).
- Daneman, R., et al. The mouse blood-brain barrier transcriptome: a new resource for understanding the development and function of brain endothelial cells. PloS One. 5 (10), e13741 (2010).
- Gräbner, R., Till, U., Heller, R. Flow cytometric determination of E-selectin, vascular cell adhesion molecule-1, and intercellular cell adhesion molecule-1 in formaldehyde-fixed endothelial cell monolayers. Cytometry. 40 (3), 238-244 (2000).
- Quah, B. J. C., Parish, C. R. New and improved methods for measuring lymphocyte proliferation in vitro and in vivo using CFSE-like fluorescent dyes. J. Immunol. Methods. 379 (1-2), 1-14 (2012).
- Lathia, J. D., et al. High-throughput flow cytometry screening reveals a role for junctional adhesion molecule a as a cancer stem cell maintenance factor. Cell Rep. 6 (1), 117-129 (2014).
- Ganat, Y. M., et al. Identification of embryonic stem cell-derived midbrain dopaminergic neurons for engraftment. J. Clin. Invest. 122 (8), 2928-2939 (2012).
- Hedlund, E., et al. Embryonic stem cell-derived Pitx3-enhanced green fluorescent protein midbrain dopamine neurons survive enrichment by fluorescence-activated cell sorting and function in an animal model of Parkinson’s disease. Stem Cells. 26 (6), 1526-1536 (2008).
- Maroof, A. M., et al. Directed differentiation and functional maturation of cortical interneurons from human embryonic stem cells. Cell Stem Cell. 12 (5), 559-572 (2013).
- Chivet, M., Hemming, F., Pernet-Gallay, K., Fraboulet, S., Sadoul, R. Emerging role of neuronal exosomes in the central nervous system. Front. Physiol. 3, 145 (2012).
- Graner, M. W., et al. Proteomic and immunologic analyses of brain tumor exosomes. FASEB J. 23 (5), 1541-1557 (2009).
- Eldh, M., Lötvall, J. Isolation and characterization of RNA-containing exosomes. J. Vis. Exp. (59), e3037 (2012).
- Capela, A., Temple, S. LeX is expressed by principle progenitor cells in the embryonic nervous system, is secreted into their environment and binds Wnt-1. Dev. Biol. 291 (2), 300-313 (2006).
- Nieoullon, V., Belvindrah, R., Rougon, G., Chazal, G. mCD24 regulates proliferation of neuronal committed precursors in the subventricular zone. Mol. Cell. Neurosci. 28 (3), 462-474 (2005).
- Nagato, M., et al. Prospective characterization of neural stem cells by flow cytometry analysis using a combination of surface markers. J. Neurosci. Res. 80 (4), 456-466 (2005).
- Hall, P. E., Lathia, J. D., Miller, N. G. A., Caldwell, M. A., French-Constant, C. Integrins are markers of human neural stem cells. Stem Cells. 24 (9), 2078-2084 (2006).
- Hargus, G., et al. Differentiated Parkinson patient-derived induced pluripotent stem cells grow in the adult rodent brain and reduce motor asymmetry in Parkinsonian rats. Proc. Natl. Acad. Sci. U.S.A. 107 (36), 15921-15926 (2010).
- Elkabetz, Y., et al. Human ES cell-derived neural rosettes reveal a functionally distinct early neural stem cell stage. Genes Dev. 22 (2), 152-165 (2008).

