Sinir Hücresi Tipleri Yüzey Akış Sitometri Protokolleri ve Hücre içi Antijen Analizleri
Summary
We provide a detailed description of a protocol for flow cytometric analysis of surface antigens and/or intracellular antigens in neural cell types. Critical aspects of experimental planning, step-by-step methodological procedures, and fundamental principles of flow cytometry are explained in order to enable neurobiologists to exploit this powerful technology.
Abstract
Flow cytometry has been extensively used to define cell populations in immunology, hematology and oncology. Here, we provide a detailed description of protocols for flow cytometric analysis of the cluster of differentiation (CD) surface antigens and intracellular antigens in neural cell types. Our step-by-step description of the methodological procedures include: the harvesting of neural in vitro cultures, an optional carboxyfluorescein succinimidyl ester (CFSE)-labeling step, followed by surface antigen staining with conjugated CD antibodies (e.g., CD24, CD54), and subsequent intracellar antigen detection via primary/secondary antibodies or fluorescently labeled Fab fragments (Zenon labeling). The video demonstrates the most critical steps. Moreover, principles of experimental planning, the inclusion of critical controls, and fundamentals of flow cytometric analysis (identification of target population and exclusion of debris; gating strategy; compensation for spectral overlap) are briefly explained in order to enable neurobiologists with limited prior knowledge or specific training in flow cytometry to assess its utility and to better exploit this powerful methodology.
Introduction
Akım sitometri yoğun içsel dağılım özellikleri, hücre yüzey antijeni ifade ve diğer floresan parametreleri 1-3 vasıtasıyla hücre popülasyonlarının tanımlamak için immünoloji, hematoloji ve onkoloji istismar edilmiştir. Kan soy geliştirme ve hastalık halinde bizim anlayışlar ilk uygulama 4,5'ten sonra bu metodolojinin sürekli arıtma önemli ölçüde bir sonucudur. Akış nicel ve genel analitik potansiyeli artan farkındalık sitometri son zamanlarda kök hücre araştırmalarında da daha yaygın kullanımını teşvik etmiştir ve kısa bir zaman dilimi 6 benzer derin ilerleme sağlayabilir. Ancak, özellikle nöral popülasyonları analiz ve izole etmek için akış sitometri uygulaması uzun zorlu olarak algılanmıştır. Doğal olarak süspansiyonda mevcut hematopoietik hücrelerin aksine, sinir hücresi tipleri, tipik olarak glia ve çeşitli o içerebilir aşırı derecede karmaşık kaynaklardan toplanırTher çevreleyen hücreleri ve aynı zamanda işlem taşıyan nöronların karmaşık bir ağdır. Sonuç olarak, nörobiyoloji günlük araştırma rutinleri onun tam potansiyeline flow sitometri çok yönlülüğünü uygulamak için henüz. Ancak nörobiyolojisinde analitik repertuarın değerli unsuru olarak kabul edilebilir olduğu sürece uygun bir tek hücre süspansiyonu elde edilebilir (ve protokoller bu amaçla 7 için tasarlanmış ve optimize edilmiş) halinde, akış sitometrisi ve floresans ile aktive edilen hücre çeşitleme (FACS) 8-11.
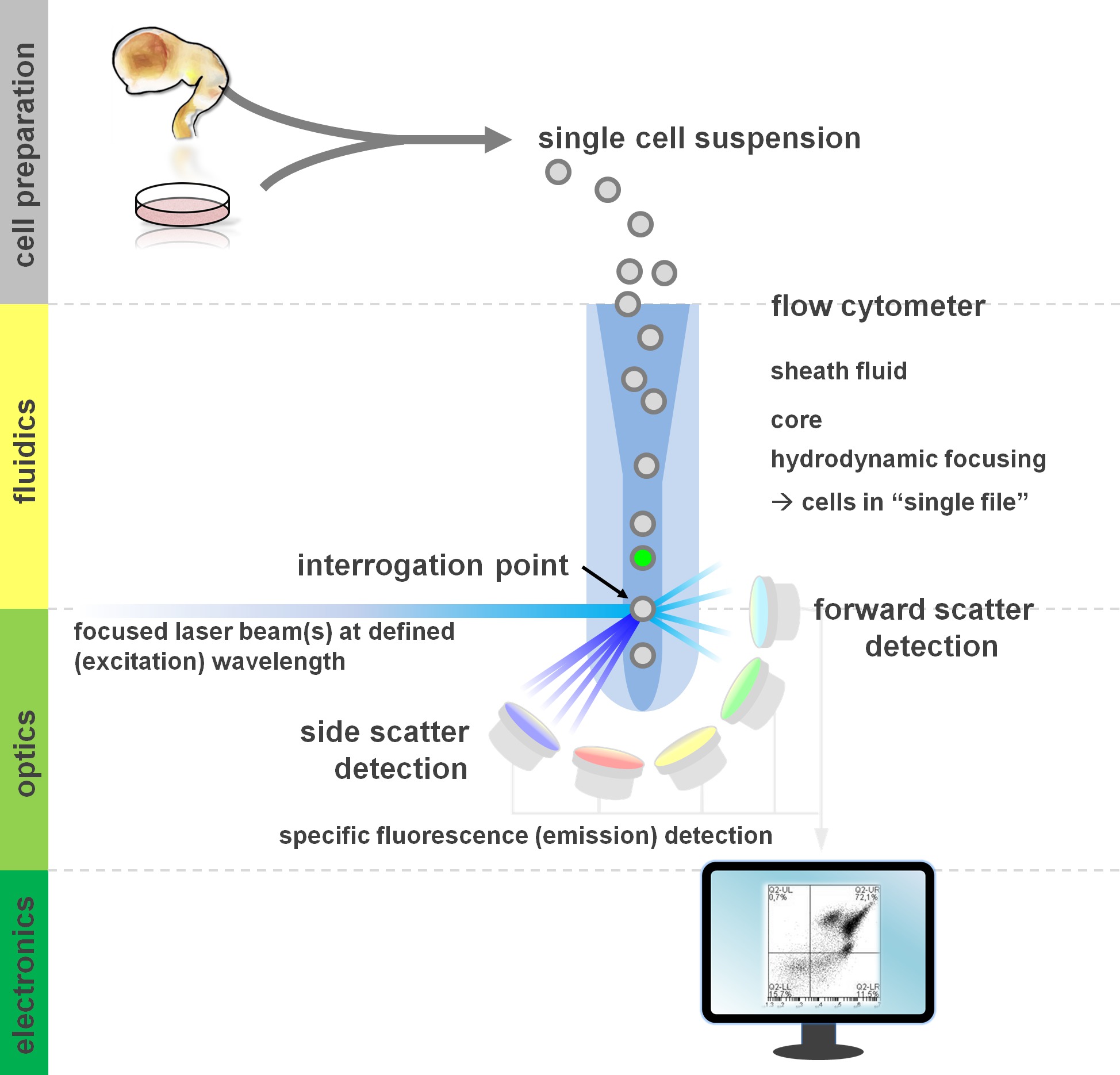
. Fluidik, optik ve elektronik: akım sitometri analizi ve bir akış sitometresinde bileşenlerinin Şekil 1. İlke akış sitometrelerinde üç ana sistemleri içermektedir. Süspansiyon içinde bulunan hücrelerin bir akıcı akış kılıf flui ile gerçekleştirilir (birincil doku ya da in vitro kültürü hazırlanmış)hidrodinamik yoluyla d merkez çekirdek örneği kısıtlayan, odaklama. Optik parçalar uygun dedektör sinyal doğrudan hücrelere ve optik filtrelerin akışı aydınlatmak lazerler oluşmaktadır. elektronik sinyaller, daha sonra bir bilgisayar tarafından işlenir ve veri analizi ve yolluk için bir monitörde görüntülenebilir dönüştürülür tespit ışık sinyalleri. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
Bir sitometresinin yapı blokları dahil altta yatan temelleri en azından temel bir anlayış akış sitometri yöntemleri kar Kullanıcılar (inceleme için 12,13 görüyorum; ayrıca bakınız Şekil 1). Bir lazer ışını da 'tek dosya' birbiri ardına lazer ışınının geçmesine süspansiyon hücreleri içeren bir hidrodinamik odaklı akışkan akışı ile kesişir. interceptiBu sorgulama alanına ışık saçılması lazer sonuçları ile hücre (veya bu konuda herhangi bir diğer parçacık, sırasıyla) ile. (Parçacık / hücre granulosity yansıtan tarafında dağılım) Dağınık ışık, hem de dik olan doğrultu (parçacık boyutu ile ilişkili ileri dağılım, hem) lazer yönünde devamında tespit edilebilir. Bu Anılan dağılım özellikleri (aynı zamanda veya hücresel enkaz, hava kabarcıkları, vb) bir etiketsiz örnek yaygın ilk yolluk için kullanılan yan dağılım grafiği iki değişkenli ileri saçılma bir sinyal (olay) üretecektir neden özel etiketleme, gerekmez. Uygun lazerler ve karşılık gelen uyarma ve emisyon spektrumu için özel filtreler kullanılarak, bir hücrenin pozitiflik, yoğunluk seviyesinde veya flüoresan işaretler yokluğu için analiz edilebilir. Akış sitometrik uygulamalarının çoğunluğu hücre yüzey antijenleri üzerinden karakterizasyonu üzerine odaklanmıştır. Hematopoietik lineag aksineE, sinir soy yüzey epitop ifade desenleri 5'e göre daha az kapsamlı tanımlanmış kalmıştır. Yüzey antijenleri istismar bir avantajı, canlı hücreler, FACS gibi sıralama paradigmalar hücre tabi olmasıdır. Buna karşılık, hücre içi antijen boyama canlı hücreler gerektiren mansap uygulamaları engelleyen, epitop-antikor etkileşimi aracılık tespit ve permeabilization adımları gerektirir. Dikkat çekici bir şekilde, bu tür yaklaşımlar yine çok nicel deneyleri 14 yanı sıra, RNA ve protein ekspresyonu 15 alt baş analizler için izin verir. Hematoloji, immünoloji ve onkoloji genellikle belirli alt popülasyonlar 16 tanımlamak için birlikte bir düzineden fazla belirteçleri kullandık. Ayrıca, kitle sitometri veya CyTOF geç 30 parametreleri aynı anda 17,18 kadar analiz etmek için kullanılabilir.
Nöral kök hücre uygulamaları yanı sıra birincil kültürlerin 14,19,20 hücrelerin heterojen olarak içinIn vitro ortak bir olgudur 21-23 olduğunu. ilgi hedef kitleyi temsil etmeyen hücreler deneysel okuma 24,25 için bir potansiyel karıştırıcı faktör somutlaştırmak. Uygun, heterojen bir hücre süspansiyonu içinde bulunan farklı hücresel alt kümeleri bu çeşitli popülasyonları tanımlamak için kullanılabilir farklı (bilinen veya henüz deşifre edilecek) antijen ifade profilleri, ayı. Biyomedikal uygulamaları kolaylaştırmak, dolayısıyla böylece, hücresel heterojenite çözümünde önemli bir rol oynayabilir ve Flow sitometri (in vitro deneyler, hücre tedavisi) ve en alakalı alt kümesi 24,26 odaklanarak kantitatif okuma optimize. Çeşitli yüzey antijen kombinasyonları özel nöral hücre tiplerinin kantitatif ve izole izin vermek için son birkaç yıl içinde tespit edilmiştir. Bu nöral kök hücreler 27 NSC izolasyonu için CD15 / CD24 / CD29 yüzey antijenlerinin kombinasyonu, differentia zenginleştirilmesi için CD133 içerirTed nöron ve nöral krest hücreleri 28 veya CD15 / CD24 / CD44 / CD184 / CD271, diğer imzalar 29,30 arasında nöral ve glial alt kümeleri 25, izole etmek. Nöronlar ötesinde, gliyal belirteçler A2B5 31, CD44, 25 NG2 32 ve GLAST 33 içerir. Son zamanlarda yayın Parkinson hücre nakli dopaminerjik öncüleri zenginleştirmek için orta beyin tabanının habercisi işaretleyici CORIN 34,35 36 paradigmalar istismar etmiştir. CD molekülleri sadece belirteçler değil, hücre-hücre etkileşimleri ve hücrenin yeteneği fonksiyonel ilgili arabulucular dışı matriks molekülleri ipuçlarını cevap ve büyüme faktörleri 37. Ayrıca sinir soy gelişimini karakterize etmek için kombinasyon CD antijenlerinin cephanelik arttırıcı bir strateji, söz konusu özel bir hücre tipi için bir CD antijeni kombinasyonu için taranması ve tanımlamak için bilinen hücre içi belirteçler kullanmaktır. Biz son zamanlarda böyle bir yaklaşım sömürülen ve CD4 belirledik9f – / CD200 nöral ayırt uyarılmış pluripotent kök hücre kültürü sistemleri 38 nöronal alt kümelerini zenginleştirmek için yeni bir yaklaşım olarak yüksek birleştirici ifade desenleri. Burada, içerir ve ikinci protokolü (ve bunların isteğe bağlı varyasyonlar) 'in yüzey boyama ve hücre içi boyama akış sitometrisi ile nöral hücre alt-popülasyonunu tanımlamak için aynı anda kullanılabilir tartışır.

Deneysel protokol seçenekleri Şekil 2. akış diyagramı. Şekil protokolde yer alan önemli adımlardan şematik bir temsilini tasvir etmektedir. İsteğe bağlı adımlar (KAKE boya veya hücre içi antijen etiketleme) açık gri kutular ile gösterilir. Hasattan sonra, bu hücre yüzey boyamadan önce nöral hücre süspansiyonlarının yaşayabilirliği ve hücre sayısını belirlemek için gereklidir. Pozitif olarakde negatif kontroller olarak ilgi örneklere ek olarak dahil edilmesi gerekir. Numuneler akım sitometri ile analiz ve / veya hücre sıralama paradigmalar kullanılabilir. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
Daha önce hücre içi boyama 38 için ikincil bir antikor ile kombinasyon halinde birincil antikor kullanmış iken, şimdi, böylece hücre manipülasyonu 39 aşamaları azaltarak küçük bir değişikliği gibi floresan Fab parçaları (Zenon etiketleme) yoluyla birincil antikor kovalent olmayan etiketleme getirmektedir. Ayrıca, protokolün çok yönlü bir başka örnek olarak, antijen lekeleme yüzey önce süksinimidil ester (CFSE) karboksifloresan ile bir deney alt-grubun isteğe bağlı bir etiketleme kullanır. Böyle KAKE ön-etiketleme, iki hücre hatları ya da deneysel koşullar hemen doğrudan karşılaştırma (sağlarVs KAKE-etiketli. Tek bir örnek tüpü, değişiklik veya inkübasyon süresi ince farklılıkların azaltılması ve antikor tasarruf içinde) etiketsiz. CFSE, yaygın üreme 41,42 ve Barkod deneylerde 43,44, hücre takibi 40 için kullanılan kurulu bir floresan boya olan. Gerçek sıralama adımlar (FACS, immünomanyetik hücre ayırma veya immunopanning) Bu protokolün bir parçası değil ise Nihayet, prensip olarak, burada açıklanan hasat ve etiketleme işlemleri antijen ya da hücre içi etiketleme-tabanlı uygulamaları sıralama yüzey tabi olabilir verim örnekleri yapmak 15 25,28.
Bu makale ile, biz hedefliyoruz: bir olarak hücre içi KAKE boya etiketleme adım 41,45 sunmak, bir hücre içi hedeflerin tespiti için protokol yanı sıra kombine yüzeyi ve hücre içi antijen analizi 38 özetlemek, geçerli bir yüzey antijeni boyama protokolü 25,28 özetlemek com için deneysel seçenekkarşılaştırmalı nöral hücre popülasyonlarının analizleri ve sitometrik analizi (strateji ve veri sunumu 47 yolluk uygun kontrolleri 13,46) akış yaklaşımları özetlemek.
Protocol
Representative Results
Discussion
Burada sunulan protokol, insan kök hücrelerinden elde edilen nöral hücre kültürleri için oluşturulmuş, ancak aynı derecede birincil doku ya da nöral hücre hatları dahil olmak üzere, diğer nöral hücre kaynaklarına uygulanabilir. Embriyonik kaynaklardan ek olarak, nöral kök veya progenitor hücreler yetişkin beyin 27 nörojenik bölgelerinden elde edilebilir. Ayrıca, akım sitometri ve FACS olgun nöronlar 54, astroglial 33, mikrogliyal 55, oligodendrositle…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Our research program is funded through the Emmy Noether-Program of the German Research Foundation (DFG), grant PR1132/3-1. Further support by the Müller-Fahnenberg Foundation of the University of Freiburg is gratefully acknowledged. This study was supported in part by the Excellence Initiative of the German Research Foundation (GSC-4, Spemann Graduate School).
Materials
| DMEM/F12 (1:1) (Dulbecco's Modified Eagle Medium/Nutrient Mixture F-12) | Life Technologies | 11330057 | www.lifetechnologies.com | |
| DPBS without Ca2+ Mg2+ | Life Technologies | 14190169 | www.lifetechnologies.com | |
| Fetal bovine serum, qualified, E.U.-approved, South America origin (FBS) | Life Technologies | 10270-106 | www.lifetechnologies.com | |
| MEM Non-essential amino acids (100 x) | Life Technologies | 11140035 | www.lifetechnologies.com | |
| TrypLE Express | Life Technologies | 12604013 | www.lifetechnologies.com | |
| Trypan blue solution, 0.4% | Life Technologies | 15250061 | www.lifetechnologies.com | |
| Paraformaldehyde | Carl Roth | 335.3 | www.carlroth.com | |
| Bovine serum albumin (BSA) Fraction V | PAA Laboratories, Coelbe | K41-001 | www.gelifesciences.com | |
| Tween-20 Detergent | Calbiochem | 655205 | www.merckmillipore.de | |
| Carboxyfluorescein succinimidyl ester (CFSE) | eBioscience | 65-0850-84 | www.ebioscience.com | |
| DMSO | AppliChem | A1584 | www.applichem.com | |
| Bottle top filters express plus 0.22 µm, 250 ml | Millipore | SCGPU02RE | www.millipore.com | |
| Cell culture treated flasks (T 25) | NUNC | 156367 | www.thermoscientific.com | |
| Cell culture treated flasks (T 75) | NUNC | 156499 | www.thermoscientific.com | |
| Conical tubes (15 ml) | Greiner Bio-One | 188271 | www.greinerbioone.com | |
| Conical tubes (50 ml) | Greiner Bio-One | 227261 | www.greinerbioone.com | |
| Pasteur pipet, glass (150 mm) | STEIN Labortechnik, Remchingen | S03710150 | www.stein-labortechnik.de | |
| Pipet tips (0.1-10 µl) | Corning | 4125 | www.corning.com | |
| Pipet tips (1-200 µl) | Corning | 4126 | www.corning.com | |
| Pipet tips (100-1000 µl) | Corning | 4129 | www.corning.com | |
| Serological pipets, 5 ml | Corning | 4051 | www.corning.com | |
| Serological pipets, 10 ml | Corning | 4101 | www.corning.com | |
| Serological pipets, 25 ml | Corning | 4251 | www.corning.com | |
| Microcentrifuge tubes (0.5 ml) | Sarstedt | 72,699 | www.sarstedt.com | |
| Microcentrifuge tubes (1.5 ml) | Greiner Bio-One | 616201 | www.greinerbioone.com | |
| Microcentrifuge tubes (2.0 ml) | Sarstedt | 72,695,500 | www.sarstedt.com | |
| Anti-Human CD24 APC monoclonal antibody | eBioscience | 17-0247-42 | www.ebioscience.com Working dilution 1:50 |
|
| Anti-Human CD54 PE monoclonal antibody | eBioscience | 12-0549-42 | www.ebioscience.com Working dilution 1:50 |
|
| Neuronal Class III β-Tubulin (Tuj1) polyclonal antibody | Covance | PRB-435P | www.covance.com Working dilution 1:2000 |
|
| Alexa Fluor 488 Donkey anti Rabbit | Life Technologies | A21206 | www.lifetechnologies.com Working dilution 1:2000 |
|
| Zenon® Fluorescein Rabbit IgG Labeling Kit | Life Technologies | Z-25342 | www.lifetechnologies.com | |
| Neubauer-Improved counting chamber | Marienfeld | 0640010 | www.marienfeld-superior.com | |
| Vortex | Scientific Industries | G560E | www.scientificindustries.com | |
| Thermomixer comfort | Eppendorf | 5355 000.001 | www.eppendorf.com | |
| Accuri C6 flow cytometer | Becton Dickinson (BD) | 653118 | www.bdbiosciences.com/instruments/accuri | |
| Microcentrifuge refrigerated, PerfectSpin 24 R | Peqlab | 91-PSPIN-24R | www.peqlab.de | |
| Orbital shaker, Unimax 1010 | Heidolph | 543-12310-00 | www.heidolph-instruments.de | |
| Centrifuge refrigerated, Rotanta 96 RC | Hettich | 4480-50 | www.hettichlab.com | |
| Class II Biological safety cabinet Safe 2020 | Thermo Scientific | 51026640 | www.thermoscientific.com | |
| CO2 Incubator, Heracell 240i | Thermo Scientific | 51026331 | www.thermoscientific.com | |
| Vacuum system, Vacusafe comfort | Integra Biosciences | 158320 | www.integra-biosciences.de | |
| Microscope, Axiovert 40 CFL | Zeiss | 451212 | www.zeiss.de | |
| Pipet controller, accu-jet pro | Brand | 26303 | www.brand.de | |
| Micropipet, Pipetman neo P20N (2-20 µl) | Gilson | F144563 | www.gilson.com | |
| Micropipet, Pipetman neo P200N (20-200 µl) | Gilson | F144565 | www.gilson.com | |
| Micropipet, Pipetman neo P1000N (100-1000 µl) | Gilson | F144566 | www.gilson.com |
References
- Herzenberg, L. A., et al. The History and Future of the Fluorescence Activated Cell Sorter and Flow Cytometry: A View from. 48 (10), 1819-1827 (2002).
- Chattopadhyay, P. K., Roederer, M. Cytometry: today’s technology and tomorrow’s horizons. Methods (San Diego, Calif). 57 (3), 251-258 (2012).
- Jaye, D. L., Bray, R. A., Gebel, H. M., Harris, W. A. C., Waller, E. K. Translational applications of flow cytometry in clinical practice). J. Immunol. 188 (10), 4715-4719 (2012).
- Henel, G., Schmitz, J. Basic Theory and Clinical Applications of Flow Cytometry. Lab Med. 38 (7), 428-436 (2007).
- Seita, J., Weissman, I. L. Hematopoietic stem cell: self-renewal versus differentiation. Wiley Interdiscip. Rev. Syst. Biol. Med. 2 (6), 640-653 (2010).
- Ulrich, H., Bocsi, J. Phenotypes of stem cells from diverse origin. Cytometry. A. 77 (1), 6-10 (2010).
- Panchision, D. M., et al. Optimized flow cytometric analysis of central nervous system tissue reveals novel functional relationships among cells expressing CD133, CD15, and CD24. Stem cells. 25 (6), 1560-1570 (2007).
- Meyer, R. A., Zaruba, M. E., McKhann, G. M. Flow cytometry of isolated cells from the brain. Anal. Quant. Cytol. 2 (1), 66-74 (1980).
- Junger, H., Junger, W. G. CNTF and GDNF, but not NT-4, support corticospinal motor neuron growth via direct mechanisms. Neuroreport. 9 (16), 3749-3754 (1998).
- McLaren, F. H., Svendsen, C. N., Vander Meide, P., Joly, E. Analysis of neural stem cells by flow cytometry: cellular differentiation modifies patterns of MHC expression. J. Neuroimmunol. 112 (1-2), 35-46 (2001).
- Wang, S., Roy, N. S., Benraiss, A., Goldman, S. A. Promoter-based isolation and fluorescence-activated sorting of mitotic neuronal progenitor cells from the adult mammalian ependymal/subependymal. 22 (1-2), 167-176 (2000).
- Tanke, H. J., vander Keur, M. Selection of defined cell types by flow-cytometric cell sorting. Trends Biotechnol. 11 (2), 55-62 (1993).
- Baumgarth, N., Roederer, M. A practical approach to multicolor flow cytometry for immunophenotyping. J. Immunol. Methods. 243 (1-2), 77-97 (2000).
- Sergent-Tanguy, S., Chagneau, C., Neveu, I., Naveilhan, P. Fluorescent activated cell sorting (FACS): a rapid and reliable method to estimate the number of neurons in a mixed population. J. Neurosci. Methods. 129 (1), 73-79 (2003).
- Ernst, A., et al. Neurogenesis in the striatum of the adult human brain. Cell. 156 (5), 1072-1083 (2014).
- Perfetto, S. P., Chattopadhyay, P. K., Roederer, M. Seventeen-colour flow cytometry: unravelling the immune system. Nat. Rev. Immunol. 4 (8), 648-655 (2004).
- Bandura, D. R., et al. Mass cytometry: technique for real time single cell multitarget immunoassay based on inductively coupled plasma time-of-flight mass spectrometry. Anal. Chem. 81 (16), 6813-6822 (2009).
- Bendall, S. C., et al. Single-cell mass cytometry of differential immune and drug responses across a human hematopoietic continuum. Science. 332 (6030), 687-696 (2011).
- Neveu, I., Rémy, S., Naveilhan, P. The neuropeptide Y receptors, Y1 and Y2, are transiently and differentially expressed in the developing cerebellum. Neuroscience. 113 (4), 767-777 (2002).
- Pruszak, J., Just, L., Isacson, O., Nikkhah, G. Isolation and culture of ventral mesencephalic precursor cells and dopaminergic neurons from rodent brains. Curr. Protoc. Stem Cell Biol. 2 (Unit 2D.5), (2009).
- Suslov, O. N., Kukekov, V. G., Ignatova, T. N., Steindler, D. A. Neural stem cell heterogeneity demonstrated by molecular phenotyping of clonal neurospheres. Proc. Natl. Acad. Sci. U.S.A. 99 (22), 14506-14511 (2002).
- Bez, A., et al. Neurosphere and neurosphere-forming cells: morphological and ultrastructural characterization. Brain Res. 993 (1-2), 18-29 (2003).
- Pruszak, J., Isacson, O. Molecular and cellular determinants for generating ES-cell derived dopamine neurons for cell therapy. Adv. Exp. Med. Biol. 651, 112-123 (2009).
- Carson, C. T., Aigner, S., Gage, F. H. Stem cells: the good, bad and barely in control. Nat. Med. 12 (11), 1237-1238 (2006).
- Yuan, S. H., et al. Cell-surface marker signatures for the isolation of neural stem cells, glia and neurons derived from human pluripotent stem cells. PloS One. 6 (3), e17540 (2011).
- Roy, N. S., Cleren, C., Singh, S. K., Yang, L., Beal, M. F., Goldman, S. Functional engraftment of human ES cell-derived dopaminergic neurons enriched by coculture with telomerase-immortalized midbrain astrocytes. Nat. Med. 12 (11), 1259-1268 (2006).
- Uchida, N., et al. Direct isolation of human central nervous system stem cells. Proc. Natl. Acad. Sci. U. S. A. 97 (26), 14720-14725 (2000).
- Pruszak, J., Ludwig, W., Blak, A., Alavian, K., Isacson, O. CD15, CD24, and CD29 define a surface biomarker code for neural lineage differentiation of stem cells. Stem Cells. 27 (12), 2928-2940 (2009).
- Peh, G. S. -. L., Lang, R. J., Pera, M. F., Hawes, S. M. CD133 expression by neural progenitors derived from human embryonic stem cells and its use for their prospective isolation. Stem Cells Dev. 18 (2), 269-282 (2009).
- Golebiewska, A., Atkinson, S. P., Lako, M., Armstrong, L. Epigenetic landscaping during hESC differentiation to neural cells. Stem Cells. 27 (6), 1298-1308 (2009).
- Dietrich, J., Noble, M., Mayer-Proschel, M. Characterization of A2B5+ glial precursor cells from cryopreserved human fetal brain progenitor cells. Glia. 40 (1), 65-77 (2002).
- Nishiyama, A. NG2 cells in the brain: a novel glial cell population. Hum. Cell. 14 (1), 77-82 (2001).
- Jungblut, M., et al. Isolation and characterization of living primary astroglial cells using the new GLAST-specific monoclonal antibody ACSA-1. Glia. 60 (6), 894-907 (2012).
- Ono, Y., et al. Differences in neurogenic potential in floor plate cells along an anteroposterior location: midbrain dopaminergic neurons originate from mesencephalic floor plate cells. Development. 134 (17), 3213-3225 (2007).
- Chung, S., et al. ES cell-derived renewable and functional midbrain dopaminergic progenitors. Proc. Natl. Acad. Sci. U.S.A. 108 (23), 9703-9708 (2011).
- Doi, D., et al. Isolation of Human Induced Pluripotent Stem Cell-Derived Dopaminergic Progenitors by Cell Sorting for Successful Transplantation. Stem Cell Reports. 2 (3), 337-350 (2014).
- Solozobova, V., Wyvekens, N., Pruszak, J. Lessons from the embryonic neural stem cell niche for neural lineage differentiation of pluripotent stem cells. Stem Cell Rev. 8 (3), (2012).
- Turaç, G., et al. Combined flow cytometric analysis of surface and intracellular antigens reveals surface molecule markers of human neuropoiesis. PloS One. 8 (6), e68519 (2013).
- Buchwalow, I. B., Böcker, W. Chapter 2. Immunohistochemistry: Basics and Methods. , 9-17 (2010).
- Tario, J. D., et al. Optimized staining and proliferation modeling methods for cell division monitoring using cell tracking dyes. J. Vis. Exp. (70), e4287 (2012).
- Lyons, A. B., Parish, C. R. Determination of lymphocyte division by flow cytometry. J. Immunol. Methods. 171 (1), 131-137 (1994).
- Hawkins, E. D., et al. Measuring lymphocyte proliferation, survival and differentiation using CFSE time-series data. Nat. Protoc. 2 (9), 2057-2067 (2007).
- Quah, B. J. C., Parish, C. R. The use of carboxyfluorescein diacetate succinimidyl ester (CFSE) to monitor lymphocyte proliferation. J. Vis. Exp. 44, (2010).
- Sukhdeo, K., et al. Multiplex flow cytometry barcoding and antibody arrays identify surface antigen profiles of primary and metastatic colon cancer cell lines. PloS One. 8 (1), e53015 (2013).
- Jiang, L., et al. Daucosterol promotes the proliferation of neural stem cells. The J. Steroid Biochem. Mol. Biol. 140, 90-99 (2014).
- Hulspas, R., et al. Considerations for the control of background fluorescence in clinical flow cytometry. Cytometry. B. 76 (6), 355-364 (2009).
- Moloney, M., Shreffler, W. G. Basic science for the practicing physician: flow cytometry and cell sorting. Annals of Allergy, Asthm., & Immunology: Official Publication of the American College of Allergy, Asthma., & Immunology. 101 (5), 544-549 (2008).
- Siebzehnrubl, F. A., et al. Isolation and characterization of adult neural stem cells. Methods Mol. Biol. 750, 61-77 (2011).
- Guez-Barber, D., et al. FACS purification of immunolabeled cell types from adult rat brain). J. Neurosci. Methods. 203 (1), 10-18 (2012).
- Tham, C. -. S., Lin, F. -. F., Rao, T. S., Yu, N., Webb, M. Microglial activation state and lysophospholipid acid receptor expression. Int. J. Dev. Neurosci. 21 (8), 431-443 (2003).
- Nguyen, H. X., Beck, K. D., Anderson, A. J. Quantitative assessment of immune cells in the injured spinal cord tissue by flow cytometry: a novel use for a cell purification method. J. Vis. Exp. (50), e2698 (2011).
- Marchenko, S., Flanagan, L. Counting human neural stem cells. J. Vis. Exp. (7), 262 (2007).
- Brunlid, G., Pruszak, J., Holmes, B., Isacson, O., Sonntag, K. C. Immature and neurally differentiated mouse embryonic stem cells do not express a functional Fas/Fas ligand system. Stem Cells. 25 (10), 2551-2558 (2007).
- Brewer, G. J. Isolation and culture of adult rat hippocampal neurons. J. Neurosci. Methods. 71 (2), 143-155 (1997).
- Cardona, A. E., Huang, D., Sasse, M. E., Ransohoff, R. M. Isolation of murine microglial cells for RNA analysis or flow cytometry. Nat. Protoc. 1 (4), 1947-1951 (2006).
- Nielsen, J. A., Maric, D., Lau, P., Barker, J. L., Hudson, L. D. Identification of a novel oligodendrocyte cell adhesion protein using gene expression profiling. J. Neurosci. 26 (39), 9881-9891 (2006).
- Daneman, R., et al. The mouse blood-brain barrier transcriptome: a new resource for understanding the development and function of brain endothelial cells. PloS One. 5 (10), e13741 (2010).
- Gräbner, R., Till, U., Heller, R. Flow cytometric determination of E-selectin, vascular cell adhesion molecule-1, and intercellular cell adhesion molecule-1 in formaldehyde-fixed endothelial cell monolayers. Cytometry. 40 (3), 238-244 (2000).
- Quah, B. J. C., Parish, C. R. New and improved methods for measuring lymphocyte proliferation in vitro and in vivo using CFSE-like fluorescent dyes. J. Immunol. Methods. 379 (1-2), 1-14 (2012).
- Lathia, J. D., et al. High-throughput flow cytometry screening reveals a role for junctional adhesion molecule a as a cancer stem cell maintenance factor. Cell Rep. 6 (1), 117-129 (2014).
- Ganat, Y. M., et al. Identification of embryonic stem cell-derived midbrain dopaminergic neurons for engraftment. J. Clin. Invest. 122 (8), 2928-2939 (2012).
- Hedlund, E., et al. Embryonic stem cell-derived Pitx3-enhanced green fluorescent protein midbrain dopamine neurons survive enrichment by fluorescence-activated cell sorting and function in an animal model of Parkinson’s disease. Stem Cells. 26 (6), 1526-1536 (2008).
- Maroof, A. M., et al. Directed differentiation and functional maturation of cortical interneurons from human embryonic stem cells. Cell Stem Cell. 12 (5), 559-572 (2013).
- Chivet, M., Hemming, F., Pernet-Gallay, K., Fraboulet, S., Sadoul, R. Emerging role of neuronal exosomes in the central nervous system. Front. Physiol. 3, 145 (2012).
- Graner, M. W., et al. Proteomic and immunologic analyses of brain tumor exosomes. FASEB J. 23 (5), 1541-1557 (2009).
- Eldh, M., Lötvall, J. Isolation and characterization of RNA-containing exosomes. J. Vis. Exp. (59), e3037 (2012).
- Capela, A., Temple, S. LeX is expressed by principle progenitor cells in the embryonic nervous system, is secreted into their environment and binds Wnt-1. Dev. Biol. 291 (2), 300-313 (2006).
- Nieoullon, V., Belvindrah, R., Rougon, G., Chazal, G. mCD24 regulates proliferation of neuronal committed precursors in the subventricular zone. Mol. Cell. Neurosci. 28 (3), 462-474 (2005).
- Nagato, M., et al. Prospective characterization of neural stem cells by flow cytometry analysis using a combination of surface markers. J. Neurosci. Res. 80 (4), 456-466 (2005).
- Hall, P. E., Lathia, J. D., Miller, N. G. A., Caldwell, M. A., French-Constant, C. Integrins are markers of human neural stem cells. Stem Cells. 24 (9), 2078-2084 (2006).
- Hargus, G., et al. Differentiated Parkinson patient-derived induced pluripotent stem cells grow in the adult rodent brain and reduce motor asymmetry in Parkinsonian rats. Proc. Natl. Acad. Sci. U.S.A. 107 (36), 15921-15926 (2010).
- Elkabetz, Y., et al. Human ES cell-derived neural rosettes reveal a functionally distinct early neural stem cell stage. Genes Dev. 22 (2), 152-165 (2008).

