Summary
Heri, rapporterer vi syntese og krystallisering af 3,5-lutidine N -oxid dehydrere ved en enkel protokol, der adskiller sig fra den klassiske syntese af pyridin N-oxid. Denne protokol udnytter forskellige udgangsmaterialet og indebærer mindre reaktion tid at give en ny solvated Supramolekylær struktur, som udkrystalliserer under langsom fordampning.
Abstract
Syntesen af 3,5-lutidine N -oxid dehydrere, 1, blev opnået i ruten syntese af 2-amino-pyridin-3,5-dicarboxylsyrer syre. Ochiai først brugt metoden for ikke-substituerede pyridines i 1957 i en proces, 12 h, men ingen X-ray egnet krystaller blev indhentet. Den substituerede ring brugt i den metode, der præsenteres her klart påvirket tilsætning af vandmolekyler i den asymmetriske enhed, som giver en anderledes nukleofil styrke i 1. X-ray egnet krystal sammensatte 1 var muligt på grund af en stabilisering af den negative ladning i ilt ved tilstedeværelsen af to vandmolekyler hvor brintatomer donerer positiv ladning ind i ringen; sådanne vandmolekyler tjene godt at konstruere en Supramolekylær interaktion. Hydreret molekyler kan være muligt for den alkaliske system, der er opnået ved at justere pH-værdien til 10. Vigtigere er, den dobbelt methyl substituerede ring og en reaktionstid på 5 h, gør det til en mere alsidig metode og med bredere kemiske applikationer for fremtidige ring indsættelser.
Introduction
I dag er har forskere rundt om i verden investeret ressourcer i udviklingen af nye syntetiske ruter for functionalization af aromatiske grupper, som er kendt for lave reaktivitet front til tilføjelse reaktioner1,2, 3. Pyridin, hvor en nitrogen atom erstatter et kulstofatom, præsenterer en lignende kemisk reaktivitet til analog ringe består udelukkende af kulstof atomer3, og det gennemgår normalt en substitution mekanisme i stedet for tilsætning. N-oxider er karakteristisk ved tilstedeværelsen af en donor bånd mellem kvælstof og ilt dannet af overlapningen af den nonbonding elektron-par på kvælstof med en tom orbital på ilt atom3. Især pyridin N-oxider er Lewis baser, fordi deres N-O gruppe kan fungere som en elektron donor, og de kan kombinere med Lewis syrer danner de tilsvarende Lewis syre-basepar. Denne ejendom har en afgørende kemiske konsekvens, fordi det kan øge nucleophilicity af Lewis syre mod potentielle electrophiles og således give dem til at reagere på betingelser, hvor normalt reaktionen ikke ville forekomme. Sandsynligvis er den mest hyppige brug af sådanne forbindelser i forskellige oxidation reaktioner hvor de fungerer som oxidanter4. Pyridin N-oxider og mange af deres ring-functionalized derivater er tilbagevendende molekyler af biologisk aktive og farmakologiske agenter5, og en klart geografiske fordeling af forskellige spektroskopiske værktøjer er blevet etableret for nogle af dem6,7. I forskning på knyttet forskellige grupper til pyridin ring, har forskerne testet forskellige metoder til at producere en nem og konventionelle metode, da isoxazolines kræver en katalytisk base som DBU i kogende xylen til form 6- substitueret-2-aminopyridine N-oxider8,9. En bred vifte af pyridin derivater blev omdannet til deres tilsvarende N-oxider i overværelse af en katalytisk mængden af mangan tetrakis(2,6-diclorophenyl) porfyrin og ammonium acetat i CH2Cl2/CH3 KN-8,10. Andre pyridines er oxideret til deres oxider, ved hjælp af H2O2 i tilstedeværelsen af katalytiske mængder af methyltrioxorhenium8,11, eller ved tilsætning af overskydende dimethyldioxirane i CH2Cl2 ved 0 ° C, hvilket fører til den tilsvarende N-oxider8,12,13,14. Bis (trimethylsilyl) peroxid i overværelse af trioxorhenium i CH2Cl2 har været brugt til syntese af pyridin N-oxider8,11. Syntesen af aminopyridine N-oxider involverer acylation ved hjælp af caros syre (peroxomonosulfuric syre) har også været rapporteret8. Ikke desto mindre, den metode, der er rapporteret her, og som bruger en del af den metode, som rapporteret af Ochiai1, giver meget gode resultater med anvendelse af billigere og tilgængelige reagenser, H2O2 og iseddike. Denne praksis er mere egnet til brug i stor skala præparater, der fungerer på tertiære aminer, det producerer gode udbytter i en reaktion, der kun kræver 30% hydrogenperoxid og iseddike i en temperatur mellem 70-80 ° C, og det bruger en rensningsproces der er tilgængelig i de fleste syntese laboratorier som destillation, uden brug af katalysator eller dyrere reagenser1. Litteraturen rapporterer, at andre metoder også ofte involverer tidsrammer fra 10-24 h og temperaturer over 100 ° C 4,8, og udbyttet af velformede krystaller X-ray analyser er sjældent rapporteret.
Reaktivt, bruges forskellige N -oxid derivater til at aktivere tilstrækkeligt lutidine ring, i enten en nukleofil eller elektrofil måde. Den nukleofil eller elektrofil faktor er påvirket af substituenterne. Med pyridin ring bliver de fratagelse af elektron grupper, er den vigtigste faktor den nukleofil karakteristiske1. Den gratis N-oxid forbindelser er sjældent isoleret som egnet krystaller for X-ray analyse på grund af den delocalized afgift i de aromatiske ring. Solvation faktoren er imidlertid afgørende at stabilisere den negative tæthed af ilt15.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1. reaktion
- Anbringes i et stinkskab en åbnet runde 100 mL kolbe med 0,5 mol (29.8 mL) iseddike og tilføje 0.051 mol (5.82 mL) af 3,5-dimethylpyridine og 5 mL af H2O2 (35%). Holde blanding reaktionen under konstant magnetiske omrøring, ved en indre temperatur på 80 ° C i 5 h.
- Efter reaktionstid, afkøles kolben til 24 ° C med ice (ikke eksponere eddikesyren gasser til isen), og Tilslut det til en høj vakuumdestillation enhed for 90-120 min. til at fjerne overskydende eddikesyre.
Forsigtig: Brug ikke varmt materiale. Vent indtil glasvarer når en håndterbar temperatur. Dette vil også undgå dampe ind i toppen af destillation enhed. - Tilføj destilleret vand (10 mL) to gange for at sikre fjernelse af spor af eddikesyre og at koncentrere blandingen meget som muligt.
2. baser justering og udvinding
- Opløses i bi-distillated vand isolerede tyktflydende og gennemsigtigt produktet og bruge et potentiometer til pH indstilles til 10 med ren solid Na2CO3.
- Læg forsigtigt løsningen i en 250 mL skilletragt og uddrag sig 5 gange med 250 mL af CHCl3 til at forbedre udbyttet. Genskab de organiske lag og tør det over solid Na2så4 for 30 min maksimale, som indeholder produktet. Hvis nødvendigt, igen uddrag den vandige fase med den ønskede mængde af CHCl3.
Forsigtig: CHCl3 kan give sløvhed og svimmelhed; håndterer med omhu og inde i et stinkskab. - Fjerne opløsningsmiddel under reduceret tryk med en høj vakuumdestillation enhed, indtil dannelsen af et meget hygroskopisk klart beige krystallinsk pulver (70%).
3. krystallisering processen
- 4,3 g af krystallinsk pulver i 50 mL koldt høj udført væskekromatografi (HPLC) grade dietylaeter opløses. Vakuum filter løsning til at fjerne ethvert spor af solid råvare eller endda støv. Hæld filtratet i et glas petriskål, overlader det til langsomt fordamper ved 4 ° C i et laboratorium køleskab.
- Sikre, at efter to dage, klare farveløse krystaller er fremstillet. Derefter mål smeltepunkt, som bør være i rækken af 310 311 K.
4. analyse af 3,5-Lutidine N -oxid Dehydrate
- Fjern de krystaller, der er dannet af prismatiske form og farveløs, ved dekantering af kolbens vægge for yderligere X-ray analyse. Hvis ikke straks bruges, skal du holde krystaller i diethylether at undgå krystal hydrering.
- Opløse 0.010 g 3,5-lutidine N -oxid dehydrere i 0,4 mL af CDCl3 til at udføre NMR H1 og C13 analyse at bevise effektiviteten af proceduren.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
Protokollen er det væsentlige en forlængelse af Ochiais teknik1. Dog anvendes lavere temperatur og mindre tid. Denne enkle metode kan bruges til at få en alsidig ligand, som er en substitueret pyridin N-oxid afledte. For at bekræfte dannelsen af 1, er NMR 1H og 13C analyse foretrukket at teste effektiviteten af proceduren.
De kemiske Skift viser dannelsen af 1. Signal på 2.28 ppm (dele pr. million) svarer til de seks tilsvarende brintatomer i de to methylgrupper i 3 og 5 positioner, som opfatter det magnetiske felt i mindre andel end permanent magnetiske. Der er to sæt af septuplets: en tilhører proton i positionen c på 7.9, hvilke fordobler størrelsen af andre signalet på 6,9, der tilhører proton i position a. figur 1 viser de kemiske Skift provokeret af tilstedeværelsen af ilt atom bonde d at nitrogen atom af pyridin ring. Ilt atomet er fratagelse af electro og tættere brintatomer til iltatom (c og a) Vis forskydning til en højere frekvens end for methyl brintatomer (b).
Den samme proces er afbildet for NMR 13C spektrum, figur 2, hvor signaler til de tættere kulstofatomer til iltatom (c og en) Vis frekvens adskillelse mellem deres signaler Δc = 1.300 Hz og Δen = 200 Hz. Methyl kulstofatomer viser endnu en gang ikke nogen forandring. IR-spektrum kan bruges til at se succesen af metoden.
ORTEP-diagrammet, figur 4, viser tilstedeværelsen af to molekyler af vand omkring den asymmetriske molekyle. Disse molekyler menes at stabilisere N-O bindingen. I lignende sager, det er blevet beskrevet for pyridin N-oxid og relaterede aromatiske oxider. Der er en betydelig stabiliserende π-type O→N back-donation, afspejles i en beregnede obligation order højere end 1 og en række elektron enlige par på O atom lavere end 36.
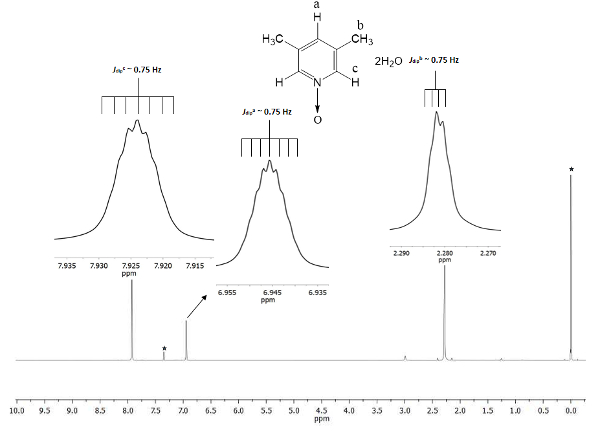
Figur 1 . TMS henvises til CDCl3 500 MHz NMR 1H spektrum af 1. Integrationer og kemiske forskydninger af de tre signaler er enig med tre forskellige typer af brintatomer i lutine N-oxid. Venligst klik her for at se en større version af dette tal.
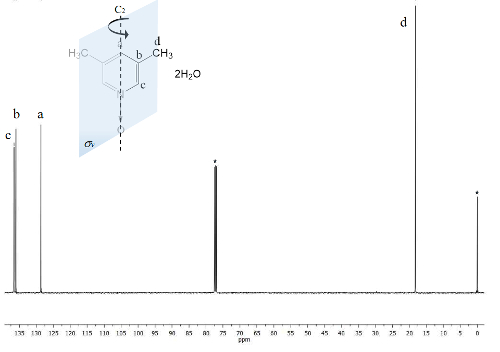
Figur 2 . TMS henvises til CDCl3 100 MHz NMR 13C spektrum af 1. Tre signaler er observeret for de fem aromatiske kulstofatomer og én for de to methylgrupper. Venligst klik her for at se en større version af dette tal.
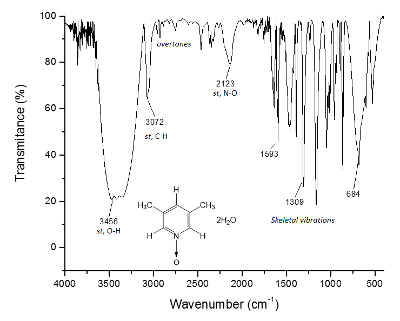
Figur 3 . IR spektrum af 1. O-H obligationer frem af 3.300 cm-1, er ansvarlige for Supramolekylær struktur dannelse og krystal formation. Venligst klik her for at se en større version af dette tal.

Figur 4 . ORTEP diagram 1 hvor to molekyler af H2O forms broen hydrogenbindinger med lutidine's ilt, køre deres brintatomer mod ilt atomet. Dette tal er blevet ændret fra Merino García et al. 12 Venligst klik her for at se en større version af dette tal.

Figur 5 . Billeder af egnet røntgen diffraktion krystaller af 1 i diethylether (øverst) og på friland (nederst). En af disse krystaller blev bekræftet i X-ray diffractometer og viste en diffraktion sti af X-ray, som blev bagtalt og raffineret af særlige beregningsmæssige programmer i en molekylær og krystallinsk struktur24,25, 26,27,28. Venligst klik her for at se en større version af dette tal.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
Protokollen præsenteres her er en konventionel metode til at sammenkæde et iltatom med nitrogen atom af 3,5-lutidine som en functionalization metode til substrater. Denne teknik er også veletableret at give X-ray egnet dehydreret krystaller (figur 5, billeder taget med et Sony DSC-HX300 Cyber-skud kamera). Så vidt vi er bekymrede, har ikke mange rapporter beskrevet produktionen af sådanne krystaller16. Mange forbindelser vokse ideelle krystaller for X-ray analyse, når de er chelateret med forskellige metaller17,18,19,20. Når den krystallinsk pulver er dannet, er det vigtigt at udtrække det fra deres moderlud, ved hjælp af en Kitasato kolbe og en Buchner tragt. Bruger gummi slanger, Kitasato kolben forbindes med en vakuum linje og på toppen af det Buchner tragt er placeret med et filtrerpapir. Når vakuum har været tændt, fugtet filter papir med en lille mængde opløsningsmiddel, hvorfra produktet krystalliseret. Dette forhindrer den krystallinsk pulver rislende i Buchner tragt af vakuum-effekt. Efter at sikre filtrerpapir, er den løsning, der indeholder den krystallinsk pulver rystet for at sikre, at alle de krystallinsk pulver er filtreret, og ingen er stadig i bunden af kolben. Opløsningen hældes hurtigt over Buchner tragten. Krystallinsk pulver fremstillet er tilbage i ca 10 min på filtrerpapir, og derefter vakuum er slukket og krystallinsk pulver er løsrevet fra papiret og gemt i en uigennemsigtig hætteglasset, mærket med sin kode og opbevares ved 4 ° C indtil yderligere analyse. Filtrated væsken hældes i et glas petriskål, overlader det til langsomt fordampning ved 4 ° C for at forbedre dannelsen af passende krystaller for X-ray analyse.
Det er vigtigt at bemærke, at denne protokol bruger opløsningsmidler og materialer, der let kan indhentes og generelt findes på enhver forskningslaboratorium. PH justering ved tilsætning af Na2CO3 og konsekvent magnetiske omrøring er afgørende for udbyttet af det endelige produkt. Det er dog vigtigt at være ekstra omhyggelig opmærksomhed i alle procestrin, især i ekstraktionen hvor ingen spor af starter materiale skal være til stede til at råd til dannelsen af krystallinsk pulver og efterfølgende krystaller. Således, denne udvinding/rensning fase kan overvåges af enten NMR eller IR-spektroskopi til at sikre kvaliteten af produktet.
For at sikre reproducerbarheden af denne protokol, er NMR et fremragende værktøj. Selv fine detaljer er synlige i spektret. Alle signaler er vist som mellemværker i figur 1. Disse mellemværker skildrer helt klart et split, nemlig mangfoldigheden af alle signaler. Eksempelvis protoner b (Jdukkertb ~ 0.75 Hz) viser fire toppe på toppen af signal med en adskillelse mellem dem (Δpeak-peak) utilpas konstant af ~ 0,0075 ppm. 0,0075 ppm kan blive omdannet til energi ved hjælp af følgende ligning21
 Ligning 1
Ligning 1

Transformationen anbefales fordi signalerne udfoldning kommer fra dipolære rumlige samspillet mellem de tre brintatomer kerner af methylgruppe, og selvom de er længere end de 4 enkeltbindinger med protoner c og a, de er i stand til at opfatte deres dipolære magnetiske momentum interaktioner22. Derudover tillader gratis sigma limning rotation i gruppen methyl super hyperfine proton-proton interaktion kan ses i mangfoldigheden af signalet. Septuplets af protoner en og c på 6,9 og 7,9 ppm, henholdsvis er afledt af den samme dipolære karakter fænomen. I disse tilfælde, protoner en og c kan skelne protoner i methylgruppe til samme rotation dynamisk. Sidst, som forventet, den beregnede Jørgensendukkert for a, b og c har næppe den samme værdi, ~ 0.75 Hz. Disse mængder af interaktioner bekræfte brint kerner rumlige arrangement gennem hele den magnetiske anisotropy.
På den anden side gør C2v symmetri af 1 tilsvarende kulstofatomer23. 13C spektrum, figur 2, viser den typiske signal for methylgrupper knyttet til aromatiske ringe, kulstofatomer d 18 ppm. Desuden et signal på 129 ppm er synlig på dette område på grund af den mindre elektronegative element påvirket carbon en. Ved høje frekvenser signal for de mere udsatte kulstofatomer kerner til det magnetiske felt er præsenteret på 137 ppm22.
De præsenterede metoder er meget nyttigt for syntesen af pyridin N-oxider, giver gode udbytter, i rimelig tid med bløde reaktionsbetingelser og billige og let tilgængelige reagenser, der ikke kræver yderligere katalysatorer. Disse betingelser kan bruges til det videnskabelige og uddannelsesmæssige samfund til at opnå en bred vifte af pyridines N-oxider som forløbere for andre molekyler af interesse. Den egnede metode giver mulighed for at erhverve grundlæggende eksperimentelle og begrebsmæssige redskaber i pædagogiske laboratorier for studerende, at bevise en vellykket syntese af forbindelser og lykken at se dannelsen af krystaller. Det er dog vigtigt at understrege, at ligesom enhver kemisk reaktion, er det nødvendigt at tage alle forholdsregler, da generelt de reagenser er farlige.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Alle forfattere erklære nogen interessekonflikt.
Acknowledgments
Det nuværende arbejde er blevet understøttet af Vicerrectoría de Investigación y Estudios de Posgrado fra BUAP, udbredelse af videnskab og projekter nr. REOY-NAT14, 15, 16-G. HEAS-NAT17. RMG tak CONACyT (Mexico) for stipendium 417887.
Materials
| Name | Company | Catalog Number | Comments |
| 3,5-lutidine | Sigma-Aldrich | L4206-500ML | |
| Glacial acetic acid | Fermont | 3015 | |
| Hidrogen peroxide (35%) | Sigma-Aldrich | 349887-500ML | |
| Na2CO3 anhydrous | Productos Químicos Monterrey | 1792 | |
| Na2SO4 anhydrous | Alfa reactivos | 25051-C | |
| CHCl3 | Fermont | 6205 | |
| Ethyl eter | Mercury Chemist | QME0309 | |
| Distilled water | Comercializadora Química Poblana | not-existent |
References
- Ochiai, E. Recent Japanese work on the chemistry of pyridine 1-oxide and related compounds. J. Org. Chem. 18 (5), 534-551 (1953).
- Solomons, T. W. G. Organic Chemistry 2nd Edition. , John Wiley & Sons. 1110 (1976).
- Albini, A., Pietra, S. Heterocyclic N-Oxides. , CRC Press. ISBN: 0849345529 328 (1991).
- Koukal, P., Ulc, J., Necas, D., Kotora, Heterocyclic N.-Oxides. Topics in Heterocyclic Chemistry. 53, 29-58 (2017).
- Wen-Man, Z., Jian-Jun, D., Xu, J., Jun, X., Huan-Jian, X. Visible-Light-Induced C2 alkylation of pyridine N.-oxides. J. Org. Chem. 82 (4), 2059-2066 (2017).
- Merino García, M. R., Ríos-Merino, F. J., Bernès, S., Reyes-Ortega, Y. Crystal structure of 3,5-dimethylpyridine N-oxide dihydrate. Acta Cryst. 72 (12), 1687-1690 (2016).
- Sarma, R., Karmakar, A., Baruah, J. B. N-Oxides in Metal-Containing Multicomponent Molecular Complexes. Inorg. Chem. 47 (3), 763-765 (2008).
- Youssif, S. Recent trends in the chemistry of pyridine N-oxides. ARKIVOC. 2001, 242-268 (2001).
- Chucholowski, A. W., Uhlendorf, S. Base catalyzed rearrangement of 5-cyanomethyl-2-isoxazolines; novel pathway for the formation of 2-aminopyridine N-oxides. Tetrahedron Lett. 31 (14), 1949-1952 (1990).
- Thellend, A., Battioni, P., Sanderson, W., Mansuy, D. Oxidation of N-Heterocycles by H2O2 Catalyzed by a Mn-Porphyrin: An Easy Access to N-Oxides Under Mild Conditions. Synthesis. 1997 (12), 1387-1388 (1997).
- Copéret, C., Adolfson, H., Tinh-Alfredo, V. K. h, Yudin, A. K., Sharpless, K. B. A simple and Efficient Method for the Preparation of Pyridine N-Oxides. J. Org. Chem. 63 (5), 1740-1741 (1998).
- Ferrer, M., Sánchez-Baeza, F., Messeguer, A. On the preparation of amine N-oxides by using dioxiranes. Tetrahedron. 53 (46), 15877-15888 (1997).
- Adam, W., Briviba, K., Duschek, F., Golsch, D., Kiefer, W., Sies, H. Formation of singlet oxygen in the deoxygenation of heteroarene N-oxides by dimethyldioxirane. J. Chem. Soc. Chem. Commun. 1995 (18), 1831-1832 (1995).
- Murray, R. W., Singh, M. A Facile One-Step Synthesis of C-Arylnitrones Using Dimethyldioxirane. J.Org.Chem. 55 (9), 2954-2957 (1990).
- Kim, S. W., Um, T., Shin, S. Brønsted acid-catalyzed α-halogenation of ynamides from halogenated solvents and pyridine-N-oxides. Chem. Commun. 53 (18), 2733-2736 (2017).
- Campeau, L., Rousseaux, R., Fagnou, K. A solution to the 2-pyridyl organometallic cross-coupling problem: regioselective catalytic direct arylation of pyridine N-oxides. J. Am. Chem. Soc. 127 (51), 18020-18021 (2005).
- Gang, L., et al. Metal-free methylation of a pyridine N-oxide C-H bond by using peroxides. Org. Biomol. Chem. 13 (46), 11184-11188 (2015).
- May, D., Nyman,, Hampden-Smith, M. J., Duesler, E. N. Synthesis, characterization, and reactivity of group 12 metal thiocarboxylates M(SOCR)2Lut2[M) Cd, Zn; R ) CH3, C(CH3)3; Lut ) 3,5-Dimethylpyridine (Lutidine)]. Inorg. Chem. 36 (10), 2218-2224 (1997).
- Cho, S. H., Hwang, S. J., Chang, S. Palladium-Catalyzed C-H Functionalization of Pyridine N-Oxides: Highly Selective Alkenylation and Direct Arylation with Unactivated Arenes. J. Am. Chem. Soc. 130 (29), 9254-9256 (2008).
- Ide, Y., et al. Spin-crossover between high-spin (S = 5/2) and low-spin (S = 1/2) states in six-coordinate iron(III) porphyrin complexes having two pyridine-N. oxide derivatives. Dalton Trans. 46 (1), 242-249 (2017).
- Drago, R. S. Physical Methods in Chemistry. , Saunders College Publishing USA. 750 (1977).
- Cervantes-Mejía, V., et al. Branched Polyamines Functionalized with Proposed Reaction Pathways Based on 1H-NMR, Atomic Absorption and IR Spectroscopies. American Journal of Analytical Chemistry. 5 (16), 1090-1101 (2014).
- Huheey, J. E., Keiter, E. A., Keiter, R. L. Inorganic Chemistry: Principles of Structure and Reactivity, 4th Edition. , Oxford University Press. Mexico. ISBN: 9706131620 1023 (1997).
- Rigaku, CrysAlisPRO. , (2013).
- Sheldrick, G. M. SHELXT - Integrated space-group and crystal-structure determination. Acta Cryst. 71 (1), 3-8 (2015).
- Sheldrick, G. M. Crystal structure refinement with SHELXL. Acta Cryst. 71 (1), 3-8 (2015).
- Sheldrick, G. M. A short history of SHELX. Acta Cryst. 64 (1), 112-122 (2008).
- Macrae, C. F., et al. Mercury CSD 2.0 - new features for the visualization and investigation of crystal structures. J. Appl. Cryst. 41 (2), 466-470 (2008).
- ChemBioDraw Ultra 13. , PerkinElmer. (2013).



