증기-액체 평형
English
Share
Overview
출처: 마이클 G. 벤턴과 케리 M. 둘리,화학 공학부, 루이지애나 주립 대학, 배턴 루지, LA
증기 액체 평형은 증류, 환경 모델링 및 일반 공정 설계와 같은 엔지니어링 응용 분야에서 가장 중요합니다. 혼합물에서 구성 요소의 상호 작용을 이해하는 것은 이러한 분리기를 설계, 작동 및 분석하는 데 매우 중요합니다. 활성 계수는 분자 상호 작용을 혼합물 조성에 관련시키기위한 훌륭한 도구입니다. 분자 상호 작용 매개 변수를 찾는 것은 모델을 사용하여 혼합물에 대한 활성 계수의 미래 예측을 가능하게 한다.
증기 액체 평형은 증류와 같은 화학 산업에서 일반적인 공정에서 중요한 요소입니다. 증류는 액체를 비등점으로 분리하는 과정입니다. 액체 혼합물은 증류 장치 또는 기둥으로 공급한 다음 끓입니다. 증기 액체 평형 데이터는 액체 혼합물이 어떻게 분리되는지 결정하는 데 유용합니다. 액체는 다른 비등점을 가지고 있기 때문에, 하나의 액체는 증기로 끓고 기둥에서 상승하고, 다른 하나는 액체로 유지하고 단위를 통해 배수됩니다. 이 과정은 다양한 산업에서 매우 중요합니다.
본 실험에서, 메탄올, 이소프로판올 및 탈이온화된 물의 다양한 조성물의 혼합물의 활성 계수는 증기액체 평형 장치 및 가스 크로마토그래프를 사용하여 수득될 것이다. 또한 시스템의 이진 상호 작용 매개 변수는 Wilson의 방정식 및 활동 계수를 사용하여 결정됩니다.
Principles
증기-액체 평형은 순수 성분 또는 혼합물이 액체 및 증기 상에 존재하는 상태이며, 기계적 및 열 평형과 두 단계 사이의 순 질량 전달이 없습니다. 증기와 액체는 중력과 열에 의해 분리됩니다 (그림 1). 액체 혼합물은 진공 펌프와 진공 상태로 넣어 시스템에 삽입됩니다. 증기는 응축되고 액체와 섞이기 위해 반환되며, 그 다음 다시 끓는 챔버로 전달됩니다. 비등점의 차이는 혼합물의 일부 분리를 초래한다. 물의 비등점은 추가된 성분보다 높기 때문에 휘발성 성분이 증발하기 시작합니다.
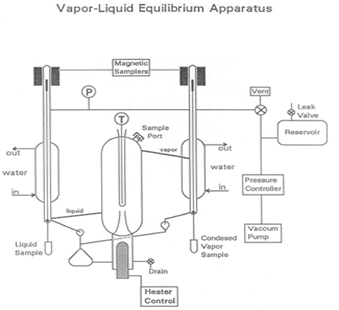
도 1: 장치의 묘사
활동 계수는 동일한 조성물의 이상적인 용액의 fugacity에 대한 실제 혼합물에서 성분의 해가성의 비율로 정의된다. Fugacity는 표준 상태에서 화학 적 잠재력 사이의 차이를 표시하는 데 사용되는 속성입니다. 증기상 fugacities는 해가시티 계수의 관점에서 발현될 수 있다 [φ: fiV = φi f i0V], yi = 몰 분획i와 함께 증기상에서 i의, fi0V = 증기 표준 상태 fugacity (T 및 P에서 순수 성분 증기의 fugacity). 저압의 경우, 이 실험에서와같이, φi = 1 및 fi0V = P. 액체 상 fugacities는 활성 계수 γi: fiL = γi x i fi 0L, xi = 몰 분획으로 액체 상에서 i0L= 액체 표준 상태 fugacity의 관점에서 발현될 수 있다.
이 T의 포화 압력(Pis)에서순수한 성분의 액체 fugacity는 순수한 증기와 액체가 평형에 있기 때문에 Pis가될 것입니다. 액체 fugacity는 압력의 약한 기능이기 때문에, 우리는 Pis와 P의 차이가 크지 않는 한, Pis로T와P (fi0L)에서순수한 성분 액체 fugacity를 근사할 수 있습니다. 이 근사치는 일반적으로 “포인팅 보정을 무시”라고합니다. 실험자가 VLE 장치를 사용하여 평형에 있는 증기 및 액체의 조성물을 측정하는 경우, 실험자는 P와 T.T를 측정하기 위해 제공된 활성 계수를 직접 계산할 수 있어 모든 i에 대해 PiS를 결정하도록 측정되어야 한다.
혼합물의 조성물을 결정하는 데 사용되는 VLE 장치의 핵심은 비열한 평형 챔버로 끓는 액체를 “스피”하는 Cottrell 펌프입니다. 두 개의 자기 조작 샘플링 밸브는 액체 및 응축 증기 시료를 인출할 수 있습니다. 대형 저수지는 온오프 제어 밸브 스위치와 Cottrell 펌프로 인한 변동으로 인해 시스템의 압력 펄스를 약화시키는 데 도움이 됩니다. 느린 누출은 필요한 경우 일정한 압력을 유지하기 위해 공기 철수 속도와 공기 입력 속도 사이의 균형을 만드는 데 사용할 수 있습니다.
증기 액체 평형을 해결하기위한 유사한 방법은 다양한 모델을 사용하는 것입니다. 라울트의 법칙, 달튼의 법칙, 헨리의 법칙은 증기 액체 평형 농도 데이터를 찾을 수있는 모든 이론적 모델입니다. 세 가지 모델은 모두 부분 압력의 비례성, 총 압력 및 물질의 두더지 분수와 관련이 있습니다. 윌슨의 방정식은 지나치게 복잡하지는 않지만 잘못된 액체에 대해 정확하다는 것이 입증되었습니다. 또한 Wilson의 모델에는 활동 계수가 통합되어 이상적인 값과 의 편차를 고려합니다.
Procedure
Results
The activity coefficients of the data do not show significant deviations from a mean value for each component (Table 1). This is as expected because for intermediate component compositions there are not large variations. However, components near 1 have γ's near 1. Low composition components have high γ's. Components highest in concentration in a mixture which will have a reduced deviation, therefore it will be closer to ideal (γ = 1). Components with lower concentrations in a mixture will have higher deviations, so their γ's will be greater than 1.

Table 1: Results of each sampling of the experimental data.
The data were fit to Wilson model parameters and the coefficients were calculated (Table 2). A simple reduction in the sum of squared residuals between experimental and Wilson equation (1) activity coefficients was used. This was achieved using Excel's solver function. The parity plot shown relates the Wilson's Equation model activity coefficients to the experimentally found activity coefficients. The experimental activity coefficients were calculated and graphically compared to the calculated model coefficients.

Table 2: Results of fitting the data to the Wilson model parameters.
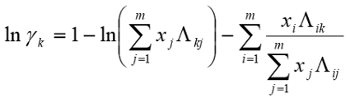 (1)
(1)
The parameter values found were the best fit (Table 3). Ideally the correlation is along the y=x line; however, a significant correlation resembling the ideal scenario was found (Figure 2). The activity coefficients of the data did not show significant deviations from a mean value for each component, as expected. A reduction in the sum of squared residuals between experimental and Wilson equation activity coefficients was used with Excel's solver function. The parity plot relates the Wilson's Equation model activity coefficients to the experimentally found activity coefficients.

Table 3: Model parameters with water (a), MeOH (b), and IPA (c). The experimental values are compared to expected values.
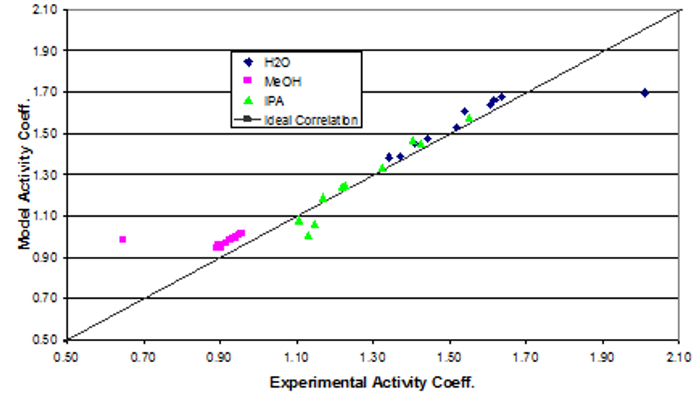
Figure 2: Depiction of the correlation between the experimental activity coefficients and the model activity coefficients.
Applications and Summary
This experiment demonstrated the equilibration of methanol – isopropanol – water vapor-liquid mixtures at a constant P = 700 mm Hg and how to measure temperature and composition and calculate activity coefficients. The activity coefficients of the data did not significantly deviate from a mean value for each component, as expected. A reduction in the sum of squared residuals between experimental and Wilson equation activity coefficients was used with Excel's solver function. The parity plot relates the Wilson's Equation model activity coefficients to the experimentally found activity coefficients.
In the petroleum industry, distillation is the primary process for separation of petroleum products. Many oil refineries use distillation for crude oil1. Light hydrocarbons are separated from heavier particles, separating based on boiling points1. Heavy materials like gas oils collect in the lower plates, while light materials like propane and butane rise up1. Hydrocarbons, such as gasoline, jet, and diesel fuels, are separated1. This process is often repeated many times to fully separate and refine the products1. Refineries run these processes at steady state, constantly creating new products at maximum capacity, so efficiency is key1. Chemical engineers working on these processes focus on optimizing the efficiency of the production1.
Tray distillation columns are also used to separate a variety of chemical products. Ethanol is one such product. Through closely related processes, a variety of products such as fuel-grade ethanol, beer, and liquor can all be distilled2. Specific amounts of alcohol can be separated from water in order to create a specific proof2. This process is limited to reducing the percentage of water in the product, but cannot completely eliminate it2. In order to remove water completely, azeotropic distillation is required, which uses extractor chemicals to separate water from ethanol2.
References
- About the Refinery." Processing & Refining Crude Oil. Chevron.com, n.d. Web. 17 Nov. 2016.
- Madson, PW. Ethanol Distillation: The Fundamentals. Cincinnati: Katzen International, n.d. Print. Accessed from Web. 01 Oct. 2016.
Transcript
Understanding the distribution of chemical components in both the vapor and liquid phase, called vapor-liquid equilibrium is essential to the design, operation, and analysis of many engineering processes. Vapor-liquid equilibrium or VLE is a state at which a pure component or mixture exists in both the liquid and vapor phases. The phases are at equilibrium meaning that there were no changes in the macroscopic properties of the system over time. Single component VLE is simple to visualize. Take for example water which is at equilibrium in the vapor and liquid phase at 100 degrees Celsius and one atm. Above this temperature water is a vapor. Below it, water is a liquid. However, engineers generally encounter processes with mixtures in equilibrium making the analysis of VLE more complex and therefore essential to process design. This video will illustrate the principles behind vapor-liquid equilibrium of mixtures and demonstrate how to analyze the VLE of a mixture in the laboratory. Finally, some applications of VLE in the chemical engineering field will be introduced.
When a heated mixture is in a vapor-liquid equilibrium, the vapor and liquid phases generally do not have the same composition. The substance with the lower boiling point will have a higher concentration in the vapor than the substance with the higher boiling point. Thus, engineers refer to components in each phase by their mole fraction where xi is the mole fraction of species i in the liquid and yi is the mole fraction of species i in the vapor phase. This relationship is often depicted using an xy curve like the one shown here for a mixture of two components which illustrates the relationship between each component in each phase. A starting point for all VLE calculations is the simple equilibrium criterion where the fugacity of the species in the vapor equals the fugacity of the species in the liquid. Fugacity is a property related to the exponential difference between the real and ideal gas Gibbs energies. The vapor phase fugacity is equal to the mole fraction of species i in the vapor phase times the pure component vapor fugacity. The expression can be simplified as the pure component vapor fugacity is approximately equal to pressure at low pressure. Liquid phase fugacities are expressed in terms of an activity coefficient, gamma. The activity coefficient is defined as the ratio of a component’s fugacity in an actual mixture to the fugacity of an ideal solution of the same composition. At the saturation vapor pressure the pure component liquid fugacity would equal the saturation vapor pressure because the pure vapor and liquid are in equilibrium there. Finally, since the liquid and vapor fugacities are equal, we can further simplify the relationship as shown which is also known as Raoult’s law. The saturation vapor pressure is often calculated using the Antoine equation where the constants A, B, and C are species-specific and can be found in the literature. Thus, if we measure the compositions of the vapor and liquid which are in equilibrium, we can directly calculate the activity coefficients by measuring temperature and pressure and therefore the saturation vapor pressure. In this experiment a ternary mixture of methanol, isopropyl alcohol and water will be investigated. Various compositions of the mixture are boiled in a VLE apparatus and the lower boiling point components vaporize and are collected in a separate container while the liquid gathers back into the initial sample vessel. Once equilibrium is reached, the liquid and condensed vapor fractions are collected and analyzed with gas chromatography. Using temperature and the liquid and vapor mole fractions the activity coefficients can be calculated. Now that you’ve been introduced to the concepts of VLE and the testing apparatus, let’s see how to carry out the experiment in the laboratory.
To start, drain any liquid out of the system into a waste flask. Keep in mind that the liquid may not completely drain. For the first run add a mixture of 50% methanol, 30% IPA and 20% water through the opening at the top. After filling the mixture, turn on the heater power and condenser water. The apparatus will require roughly 20 minutes to approach equilibrium. The system is now ready to begin the experiment.
When the sample begins boiling, release the stopper to vent the inert outlet of the system. Condensed vapor will start collecting. When equilibrium is reached, steady drips of condensed vapor and returns liquid should be observed. With the temperature stable to within 0.3 degrees for 10 minutes, collect about 1/2 milliliter of liquid in sample vials from both the condensed vapor and the boiling liquid. Drain the condensed vapor from the last sample. Then add a new sample consisting of either 20 milliliters of pure methanol or 50-50 methanol-isopropanol through the sample port. This will give a new overall composition. Reestablish the equilibrium as performed before, however expect a temperature difference from the previous sample. Repeat the equilibration and sampling procedure as before, and then collect the sample to be analyzed. Continue the experiment using different mixtures of the three components. 12 points are sufficient to determine the activity coefficients and the binary interaction coefficients. When all the mixtures have been run, shut down the system by turning off the heaters. When the apparatus begins to cool, shut off the condenser water. Finally measure the composition of each liquid and vapor sample with the gas chromatograph or GC.
Using the system temperature and the liquid and vapor mole fractions acquired from GC, calculate the activity coefficients. This first requires that the saturation pressure is calculated using the Antoine equation where the constants A, B and C for each component can be found in the literature. Now we can use the calculated activity coefficients to correlate the data to a model. We will use the Wilson equation for a ternary mixture which accounts for deviations from ideality in a mixture. The nine lambda constants are the Wilson constants which equal one when i equals j. For each ij pair, there are two different constants. Use a nonlinear regression and a standard sum of squares residual function to determine the six remaining Wilson constants using the mole fraction data from the experiment. The Wilson constants are then used to determine the expected activity coefficients for each component of each sample. Here we show the modeled activity coefficient plotted against the experimental activity coefficients. Ideally, the modeled and experimental activity coefficients would fall along the y equals x line. As you can see in general, the modeled and experimental values fit along this line showing that the model is a good fit to the real system.
Understanding and manipulating the vapor-liquid equilibrium of mixtures is a vital component to a range of processes especially separations. Distillation columns separate mixtures based on their volatility with different compositions of each component in the liquid and vapor phrases on each tray. The more volatile component is vaporized and collected at the top of the column, while the less volatile component remains liquid and is collected at the bottom. VLE data of the components of the mixture is used to determine the number of trays needed to achieve separation in a distillation column. This helps engineers optimize the separation process while keeping operating costs low. Another valuable separation technique using VLE is flash separation. Flash separation is based on the fact that a liquid at a pressure equal to or greater than its bubble point pressure flashes meaning that it partially evaporates when the pressure is reduced. The feed is preheated thus consisting of some liquid and some vapor in equilibrium. It then flows through a pressure reducing valve into the separator. The degree of vaporization and therefore the amount of the solute in the vapor or liquid phases depends on the initial state of the feed stream.
You’ve just watched Jove’s introduction to vapor-liquid equilibrium. You should now understand the concepts behind VLE, how it’s measured in the laboratory, and some of its uses in engineering processes. Thanks for watching.
