Flowcytometrie Protocollen voor Surface en intracellulaire Antigen Analyses van Neural Cell Types
Summary
We provide a detailed description of a protocol for flow cytometric analysis of surface antigens and/or intracellular antigens in neural cell types. Critical aspects of experimental planning, step-by-step methodological procedures, and fundamental principles of flow cytometry are explained in order to enable neurobiologists to exploit this powerful technology.
Abstract
Flow cytometry has been extensively used to define cell populations in immunology, hematology and oncology. Here, we provide a detailed description of protocols for flow cytometric analysis of the cluster of differentiation (CD) surface antigens and intracellular antigens in neural cell types. Our step-by-step description of the methodological procedures include: the harvesting of neural in vitro cultures, an optional carboxyfluorescein succinimidyl ester (CFSE)-labeling step, followed by surface antigen staining with conjugated CD antibodies (e.g., CD24, CD54), and subsequent intracellar antigen detection via primary/secondary antibodies or fluorescently labeled Fab fragments (Zenon labeling). The video demonstrates the most critical steps. Moreover, principles of experimental planning, the inclusion of critical controls, and fundamentals of flow cytometric analysis (identification of target population and exclusion of debris; gating strategy; compensation for spectral overlap) are briefly explained in order to enable neurobiologists with limited prior knowledge or specific training in flow cytometry to assess its utility and to better exploit this powerful methodology.
Introduction
Flowcytometrie is uitgebreid in de immunologie, hematologie en oncologie benut om celpopulaties te definiëren via intrinsieke scatter eigenschappen, celoppervlakantigeen expressie en andere fluorescentie parameters 1-3. Het inzicht in bloedlijn ontwikkeling en ziekte resultaat in belangrijke mate van de continue verfijning van deze methode na de eerste uitvoering 4,5. Toegenomen bewustzijn van de kwantitatieve en de algemene analytische mogelijkheden van flowcytometrie heeft onlangs haar meer wijdverspreid gebruik in stamcelonderzoek aangemoedigd en kan op dezelfde diepe vooruitgang in een korter tijdsbestek 6 mogelijk te maken. De toepassing van flowcytometrie specifiek analyseren en te isoleren neurale populaties is lang beschouwd als een uitdaging. In tegenstelling tot hematopoëtische cellen die van nature voorkomen in suspensie worden neurale celtypes typisch geoogst uit te ingewikkelde bronnen kunnen glia en diverse oTher omringende cellen en een ingewikkeld netwerk van proces dragende neuronen. Bijgevolg neurobiologie heeft nog tot uitvoering van de veelzijdigheid van flowcytometrie om zijn volledige potentieel in de dagelijkse routines onderzoek. Zolang echter als een levensvatbare enkele celsuspensie kan worden gegenereerd (en protocollen ontwikkeld en geoptimaliseerd daartoe 7), flowcytometrie en fluorescentie-geactiveerde celsortering (FACS) kan worden beschouwd als een waardevol bestanddeel van de analytische repertoire neurobiologie 8-11.
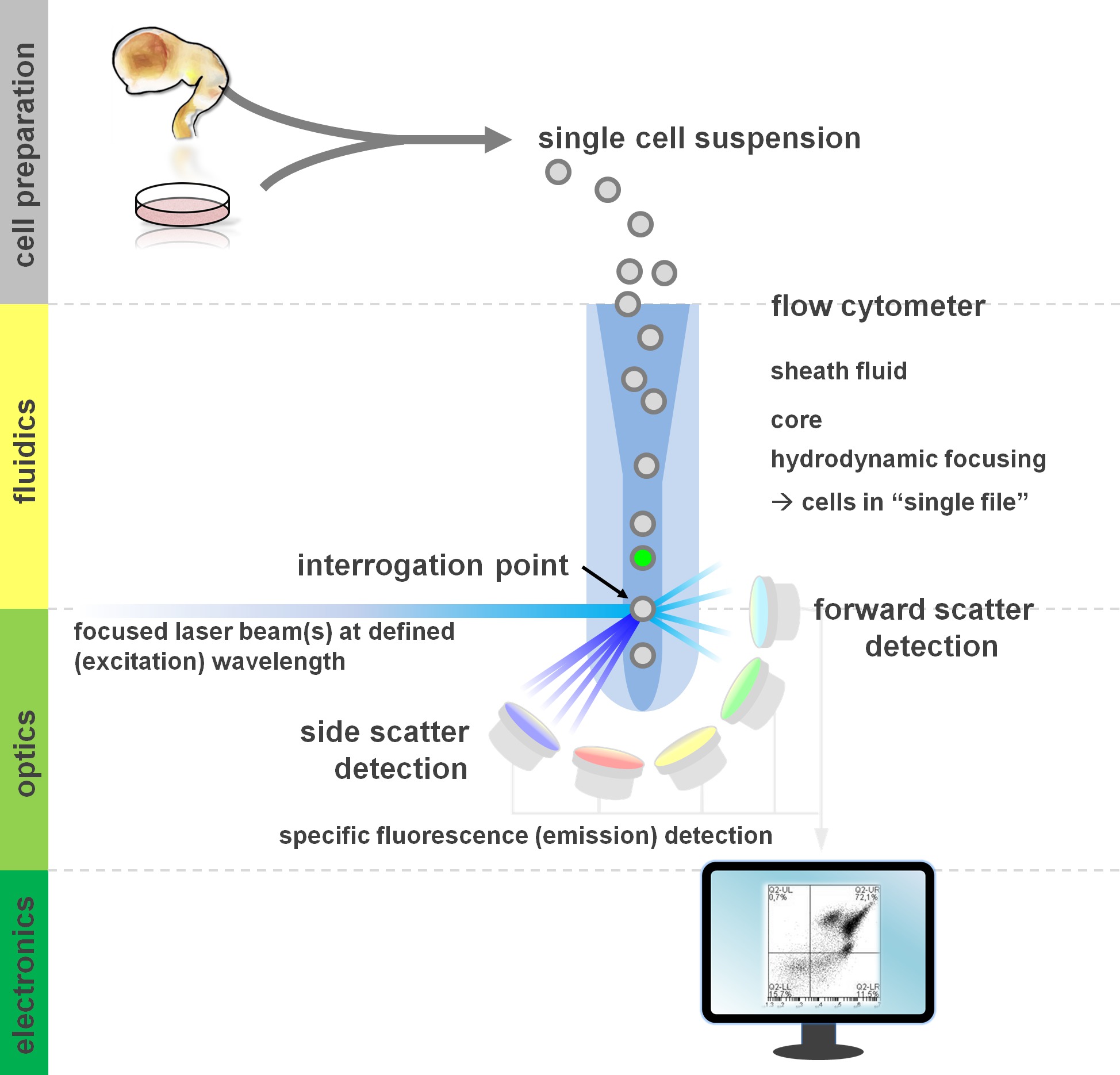
. Figuur 1. Principe van flowcytometrische analyse en componenten van een stromingscytometer flowcytometers bestaan uit drie belangrijke systemen: fluïdica, optica en elektronica. Een gestroomlijnde stroming van cellen in suspensie (bereid uit primair weefsel of in vitro kweek) wordt bewerkstelligd door de huls fluid via hydrodynamische focussen, het beperken van het monster naar het centrum kern. De optische onderdelen zijn samengesteld uit lasers die de stroom van cellen en optische filters die het signaal naar de geschikte detectoren direct verlichten. De lichtsignalen gedetecteerd worden omgezet naar elektronische signalen, vervolgens verwerkt door een computer en gevisualiseerd op een monitor voor data-analyse en gating. Klik hier om een grotere versie van deze afbeelding te bekijken.
Gebruikers van stromingscytometrische methoden winst van ten minste een basiskennis van de onderliggende fundamentals waaronder bouwstenen van een cytometer's (zie voor een overzicht 12,13; zie ook figuur 1). Een laserstraal snijdt een hydrodynamisch gerichte vloeibare stroom die de cellen in suspensie, waardoor pass laserstraal 'bestand' achter elkaar bevat. De interceptiop een cel (of een ander deeltje, wat dat betreft) met de laser resulteert in de verstrooiing van licht van deze ondervragingspunt. Strooilicht kan worden gedetecteerd in het verlengde van de laser richting (voorwaartse verstrooiing, die bij de omvang van het deeltje), alsmede loodrecht op de richting (zijwaartse verstrooiing, die de granulosity van de deeltjes / cel). Deze voornoemde scatter eigenschappen geen specifieke etikettering, dat is de reden waarom een ongemerkt monster (of ook cellulaire puin, luchtbellen, enz.) Een signaal (event) op de bivariate voorwaartse verstrooiing versus kant scatterplot vaak gebruikt voor de initiële venstertijd zal genereren vereisen. Door de geschikte lasers en filters specifiek voor de overeenkomstige excitatie en emissie spectra kan een cel worden geanalyseerd op positiviteit, intensiteit of afwezigheid van fluorescente merkers. De meeste flowcytometrische toepassingen gericht op de karakterisering via celoppervlakte antigenen. In tegenstelling tot de hematopoietische lineage is de neurale stam bleef minder uitgebreid gedefinieerd volgens oppervlak epitoop expressiepatronen 5. Een voordeel exploiteren oppervlakteantigenen is dat levende cellen kunnen worden gesorteerd paradigma zoals FACS cel. In tegenstelling, intracellulaire antigeen kleuring vereist fixatie en permeabilisatie stappen om de epitoop-antilichaam interactie bemiddelen, zich verzet tegen downstream toepassingen die levensvatbare cellen nodig. Van de nota, dergelijke benaderingen nog steeds de mogelijkheid voor tal van kwantitatieve assays 14 als downstream analyses voor RNA en eiwit expressie 15. Hematologie, immunologie en oncologie zijn vaak meer dan een dozijn markers in samenhang met bepaalde subpopulaties 16 definiëren. Daarnaast kan de massa cytometrie of CyTOF nu worden gebruikt voor het analyseren tot 30 parameters tegelijkertijd 17,18.
Voor neurale stamcellen aanvragen evenals primaire culturen 14,19,20 de heterogeniteit van cellen invitro is een veel voorkomend verschijnsel 21-23. De cellen die geen deel uitmaken van de doelgroep van belang belichamen een potentieel verstorende factor voor experimentele uitlezing 24,25. Op geschikte wijze de verschillende cellulaire subsets aanwezig in een heterogene celsuspensie aangebracht onderscheiden (bekend of nog te ontcijferd) antigeen expressie profielen die kunnen worden gebruikt om deze verschillende populaties te definiëren. Flowcytometrie kan dus een cruciale rol spelen bij het oplossen van de cellulaire heterogeniteit en, daardoor, biomedische toepassingen te vergemakkelijken (in vitro testen, celtherapie) en optimaliseren van kwantitatieve uitlezing door te focussen op de meest relevante subset 24,26. Diverse oppervlakte-antigeen combinaties zijn geïdentificeerd in de afgelopen jaren aan de kwantificering en isolatie van specifieke neurale celtypes mogelijk te maken. Dit omvat CD133 voor de verrijking van neurale stamcellen 27, een combinatie van de CD15 / CD24 / CD29 oppervlakte-antigenen voor de isolatie van NSC, differentiated neuron en de neurale lijst cellen 28 of CD15 / CD24 / CD44 / CD184 / CD271 om neurale en gliale subsets 25, onder andere handtekeningen 29,30 isoleren. Beyond neuronen, gliale merkers omvatten A2B5 31, CD44 25, NG2 32 en GLAST 33. Een recente publicatie is gebruik gemaakt van de middenhersenen vloerplaat voorloper marker CORIN 34,35 te verrijken voor dopaminerge voorlopers in Parkinson celtransplantatie paradigma 36. CD moleculen niet alleen markers, maar functioneel relevante mediatoren van cel-cel interacties en het vermogen van een cel om te reageren op signalen van extracellulaire matrix moleculen en groeifactoren 37. Een strategie voor verdere verbetering van de arsenaal van combinatorische CD antigenen neurale stam ontwikkeling karakteriseren bekende intracellulaire merkers gebruikt voor het screenen en bepalen CD antigeen combinaties voor een bepaald celtype. We hebben onlangs uitgebuit een dergelijke aanpak en geïdentificeerd CD49f – / CD200 hoge combinatorische expressie patronen als een nieuwe benadering voor het verrijken van neuronale subsets van neuraal gedifferentieerde geïnduceerde pluripotente stamcellen kweeksystemen 38. Hier nemen we bespreken laatstgenoemde protocol (en optioneel variaties daarvan), waarbij het oppervlak kleuring en intracellulaire kleuring gelijktijdig worden gebruikt voor het definiëren neurale celtypes door flowcytometrie.

Figuur 2. Stroomdiagram van experimentele protocolopties. De figuur toont een schematische weergave van de belangrijkste stappen van het protocol. Optionele stappen (CFSE kleurstof of intracellulaire antigeen etikettering) zijn aangegeven met licht grijze vakken. Na oogsten, is het essentieel om de levensvatbaarheid en aantal cellen van neurale celsuspensies voor celoppervlak kleuring beoordelen. Positiefen negatieve controles dienen te worden opgenomen naast de interessante monsters. Monsters kunnen worden geanalyseerd door flowcytometrische analyse en / of worden gebruikt in cel sortering paradigma's. Klik hier om een grotere versie van deze afbeelding te bekijken.
Hoewel we eerder gebruik primair antilichaam in combinatie met secundaire antilichaam voor intracellulaire kleuring 38, is er nu niet covalente labeling van het primaire antilichaam fluorescente Fab fragmenten (Zenon etikettering) als een lichte variatie, waardoor de stappen celmanipulatieniveau 39 verminderen. Bovendien, als een ander voorbeeld van de veelzijdigheid van het protocol, in dienst nemen we een facultatieve etikettering van een experimentele deelverzameling door carboxyfluoresceïne succinimidylester (CFSE) voorafgaand aan het antigeen kleuring oppervlak. Dergelijke CFSE pre-labeling kan de onmiddellijke directe vergelijking van twee cellijnen of experimentele condities (CFSE-gelabelde vs. ongelabelde) binnen een enkel monster buis, het verminderen van variantie of subtiele verschillen in incubatietijd en opslaan antilichaam. CFSE is een gevestigde fluorescerende kleurstof die vaak wordt gebruikt voor het cell tracking 40, in proliferatie 41,42 en barcoding experimenten 43,44. Tot slot, terwijl de werkelijke sorteer- stappen (FACS, immunomagnetische celscheiding of immunopanning) maken geen deel uit van dit protocol, in principe, de oogst en de etikettering procedures hier beschreven doen opbrengst monsters die kunnen worden onderworpen aan antigeen of intracellulaire-etikettering gebaseerd sorteren toepassingen oppervlak 15 25,28.
Met dit artikel willen we: samenvatten een levensvatbare oppervlakte-antigeen kleuringsprotocol 25,28, vatten een protocol voor de detectie van intracellulaire targets alsmede gecombineerd oppervlak en intracellulaire antigeen analyse 38, presenteren een intracellulaire CFSE kleurstof etikettering stap 41,45 als een experimentele optie voor comvergelijkende analyses van neurale celpopulaties, en samenvatten benaderingen cytometrieanalyse (passende controles 13,46, gating strategie en presentatie van gegevens 47) stromen.
Protocol
Representative Results
Discussion
De hier gepresenteerde protocol is goed vastgesteld voor neurale celculturen afkomstig van menselijke stamcellen, maar ook kan worden toegepast op andere neurale cel bronnen primaire weefsel of neurale cellijnen. Naast embryonale bronnen, kunnen neurale stamcellen of voorlopercellen worden gewonnen uit de neurogene gebieden van volwassen hersenen 27. Bovendien flowcytometrie en FACS kan worden benut om te kwantificeren, te analyseren en te isoleren diverse celpopulaties waaronder volwassen neuronen 54,</…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Our research program is funded through the Emmy Noether-Program of the German Research Foundation (DFG), grant PR1132/3-1. Further support by the Müller-Fahnenberg Foundation of the University of Freiburg is gratefully acknowledged. This study was supported in part by the Excellence Initiative of the German Research Foundation (GSC-4, Spemann Graduate School).
Materials
| DMEM/F12 (1:1) (Dulbecco's Modified Eagle Medium/Nutrient Mixture F-12) | Life Technologies | 11330057 | www.lifetechnologies.com | |
| DPBS without Ca2+ Mg2+ | Life Technologies | 14190169 | www.lifetechnologies.com | |
| Fetal bovine serum, qualified, E.U.-approved, South America origin (FBS) | Life Technologies | 10270-106 | www.lifetechnologies.com | |
| MEM Non-essential amino acids (100 x) | Life Technologies | 11140035 | www.lifetechnologies.com | |
| TrypLE Express | Life Technologies | 12604013 | www.lifetechnologies.com | |
| Trypan blue solution, 0.4% | Life Technologies | 15250061 | www.lifetechnologies.com | |
| Paraformaldehyde | Carl Roth | 335.3 | www.carlroth.com | |
| Bovine serum albumin (BSA) Fraction V | PAA Laboratories, Coelbe | K41-001 | www.gelifesciences.com | |
| Tween-20 Detergent | Calbiochem | 655205 | www.merckmillipore.de | |
| Carboxyfluorescein succinimidyl ester (CFSE) | eBioscience | 65-0850-84 | www.ebioscience.com | |
| DMSO | AppliChem | A1584 | www.applichem.com | |
| Bottle top filters express plus 0.22 µm, 250 ml | Millipore | SCGPU02RE | www.millipore.com | |
| Cell culture treated flasks (T 25) | NUNC | 156367 | www.thermoscientific.com | |
| Cell culture treated flasks (T 75) | NUNC | 156499 | www.thermoscientific.com | |
| Conical tubes (15 ml) | Greiner Bio-One | 188271 | www.greinerbioone.com | |
| Conical tubes (50 ml) | Greiner Bio-One | 227261 | www.greinerbioone.com | |
| Pasteur pipet, glass (150 mm) | STEIN Labortechnik, Remchingen | S03710150 | www.stein-labortechnik.de | |
| Pipet tips (0.1-10 µl) | Corning | 4125 | www.corning.com | |
| Pipet tips (1-200 µl) | Corning | 4126 | www.corning.com | |
| Pipet tips (100-1000 µl) | Corning | 4129 | www.corning.com | |
| Serological pipets, 5 ml | Corning | 4051 | www.corning.com | |
| Serological pipets, 10 ml | Corning | 4101 | www.corning.com | |
| Serological pipets, 25 ml | Corning | 4251 | www.corning.com | |
| Microcentrifuge tubes (0.5 ml) | Sarstedt | 72,699 | www.sarstedt.com | |
| Microcentrifuge tubes (1.5 ml) | Greiner Bio-One | 616201 | www.greinerbioone.com | |
| Microcentrifuge tubes (2.0 ml) | Sarstedt | 72,695,500 | www.sarstedt.com | |
| Anti-Human CD24 APC monoclonal antibody | eBioscience | 17-0247-42 | www.ebioscience.com Working dilution 1:50 |
|
| Anti-Human CD54 PE monoclonal antibody | eBioscience | 12-0549-42 | www.ebioscience.com Working dilution 1:50 |
|
| Neuronal Class III β-Tubulin (Tuj1) polyclonal antibody | Covance | PRB-435P | www.covance.com Working dilution 1:2000 |
|
| Alexa Fluor 488 Donkey anti Rabbit | Life Technologies | A21206 | www.lifetechnologies.com Working dilution 1:2000 |
|
| Zenon® Fluorescein Rabbit IgG Labeling Kit | Life Technologies | Z-25342 | www.lifetechnologies.com | |
| Neubauer-Improved counting chamber | Marienfeld | 0640010 | www.marienfeld-superior.com | |
| Vortex | Scientific Industries | G560E | www.scientificindustries.com | |
| Thermomixer comfort | Eppendorf | 5355 000.001 | www.eppendorf.com | |
| Accuri C6 flow cytometer | Becton Dickinson (BD) | 653118 | www.bdbiosciences.com/instruments/accuri | |
| Microcentrifuge refrigerated, PerfectSpin 24 R | Peqlab | 91-PSPIN-24R | www.peqlab.de | |
| Orbital shaker, Unimax 1010 | Heidolph | 543-12310-00 | www.heidolph-instruments.de | |
| Centrifuge refrigerated, Rotanta 96 RC | Hettich | 4480-50 | www.hettichlab.com | |
| Class II Biological safety cabinet Safe 2020 | Thermo Scientific | 51026640 | www.thermoscientific.com | |
| CO2 Incubator, Heracell 240i | Thermo Scientific | 51026331 | www.thermoscientific.com | |
| Vacuum system, Vacusafe comfort | Integra Biosciences | 158320 | www.integra-biosciences.de | |
| Microscope, Axiovert 40 CFL | Zeiss | 451212 | www.zeiss.de | |
| Pipet controller, accu-jet pro | Brand | 26303 | www.brand.de | |
| Micropipet, Pipetman neo P20N (2-20 µl) | Gilson | F144563 | www.gilson.com | |
| Micropipet, Pipetman neo P200N (20-200 µl) | Gilson | F144565 | www.gilson.com | |
| Micropipet, Pipetman neo P1000N (100-1000 µl) | Gilson | F144566 | www.gilson.com |
References
- Herzenberg, L. A., et al. The History and Future of the Fluorescence Activated Cell Sorter and Flow Cytometry: A View from. 48 (10), 1819-1827 (2002).
- Chattopadhyay, P. K., Roederer, M. Cytometry: today’s technology and tomorrow’s horizons. Methods (San Diego, Calif). 57 (3), 251-258 (2012).
- Jaye, D. L., Bray, R. A., Gebel, H. M., Harris, W. A. C., Waller, E. K. Translational applications of flow cytometry in clinical practice). J. Immunol. 188 (10), 4715-4719 (2012).
- Henel, G., Schmitz, J. Basic Theory and Clinical Applications of Flow Cytometry. Lab Med. 38 (7), 428-436 (2007).
- Seita, J., Weissman, I. L. Hematopoietic stem cell: self-renewal versus differentiation. Wiley Interdiscip. Rev. Syst. Biol. Med. 2 (6), 640-653 (2010).
- Ulrich, H., Bocsi, J. Phenotypes of stem cells from diverse origin. Cytometry. A. 77 (1), 6-10 (2010).
- Panchision, D. M., et al. Optimized flow cytometric analysis of central nervous system tissue reveals novel functional relationships among cells expressing CD133, CD15, and CD24. Stem cells. 25 (6), 1560-1570 (2007).
- Meyer, R. A., Zaruba, M. E., McKhann, G. M. Flow cytometry of isolated cells from the brain. Anal. Quant. Cytol. 2 (1), 66-74 (1980).
- Junger, H., Junger, W. G. CNTF and GDNF, but not NT-4, support corticospinal motor neuron growth via direct mechanisms. Neuroreport. 9 (16), 3749-3754 (1998).
- McLaren, F. H., Svendsen, C. N., Vander Meide, P., Joly, E. Analysis of neural stem cells by flow cytometry: cellular differentiation modifies patterns of MHC expression. J. Neuroimmunol. 112 (1-2), 35-46 (2001).
- Wang, S., Roy, N. S., Benraiss, A., Goldman, S. A. Promoter-based isolation and fluorescence-activated sorting of mitotic neuronal progenitor cells from the adult mammalian ependymal/subependymal. 22 (1-2), 167-176 (2000).
- Tanke, H. J., vander Keur, M. Selection of defined cell types by flow-cytometric cell sorting. Trends Biotechnol. 11 (2), 55-62 (1993).
- Baumgarth, N., Roederer, M. A practical approach to multicolor flow cytometry for immunophenotyping. J. Immunol. Methods. 243 (1-2), 77-97 (2000).
- Sergent-Tanguy, S., Chagneau, C., Neveu, I., Naveilhan, P. Fluorescent activated cell sorting (FACS): a rapid and reliable method to estimate the number of neurons in a mixed population. J. Neurosci. Methods. 129 (1), 73-79 (2003).
- Ernst, A., et al. Neurogenesis in the striatum of the adult human brain. Cell. 156 (5), 1072-1083 (2014).
- Perfetto, S. P., Chattopadhyay, P. K., Roederer, M. Seventeen-colour flow cytometry: unravelling the immune system. Nat. Rev. Immunol. 4 (8), 648-655 (2004).
- Bandura, D. R., et al. Mass cytometry: technique for real time single cell multitarget immunoassay based on inductively coupled plasma time-of-flight mass spectrometry. Anal. Chem. 81 (16), 6813-6822 (2009).
- Bendall, S. C., et al. Single-cell mass cytometry of differential immune and drug responses across a human hematopoietic continuum. Science. 332 (6030), 687-696 (2011).
- Neveu, I., Rémy, S., Naveilhan, P. The neuropeptide Y receptors, Y1 and Y2, are transiently and differentially expressed in the developing cerebellum. Neuroscience. 113 (4), 767-777 (2002).
- Pruszak, J., Just, L., Isacson, O., Nikkhah, G. Isolation and culture of ventral mesencephalic precursor cells and dopaminergic neurons from rodent brains. Curr. Protoc. Stem Cell Biol. 2 (Unit 2D.5), (2009).
- Suslov, O. N., Kukekov, V. G., Ignatova, T. N., Steindler, D. A. Neural stem cell heterogeneity demonstrated by molecular phenotyping of clonal neurospheres. Proc. Natl. Acad. Sci. U.S.A. 99 (22), 14506-14511 (2002).
- Bez, A., et al. Neurosphere and neurosphere-forming cells: morphological and ultrastructural characterization. Brain Res. 993 (1-2), 18-29 (2003).
- Pruszak, J., Isacson, O. Molecular and cellular determinants for generating ES-cell derived dopamine neurons for cell therapy. Adv. Exp. Med. Biol. 651, 112-123 (2009).
- Carson, C. T., Aigner, S., Gage, F. H. Stem cells: the good, bad and barely in control. Nat. Med. 12 (11), 1237-1238 (2006).
- Yuan, S. H., et al. Cell-surface marker signatures for the isolation of neural stem cells, glia and neurons derived from human pluripotent stem cells. PloS One. 6 (3), e17540 (2011).
- Roy, N. S., Cleren, C., Singh, S. K., Yang, L., Beal, M. F., Goldman, S. Functional engraftment of human ES cell-derived dopaminergic neurons enriched by coculture with telomerase-immortalized midbrain astrocytes. Nat. Med. 12 (11), 1259-1268 (2006).
- Uchida, N., et al. Direct isolation of human central nervous system stem cells. Proc. Natl. Acad. Sci. U. S. A. 97 (26), 14720-14725 (2000).
- Pruszak, J., Ludwig, W., Blak, A., Alavian, K., Isacson, O. CD15, CD24, and CD29 define a surface biomarker code for neural lineage differentiation of stem cells. Stem Cells. 27 (12), 2928-2940 (2009).
- Peh, G. S. -. L., Lang, R. J., Pera, M. F., Hawes, S. M. CD133 expression by neural progenitors derived from human embryonic stem cells and its use for their prospective isolation. Stem Cells Dev. 18 (2), 269-282 (2009).
- Golebiewska, A., Atkinson, S. P., Lako, M., Armstrong, L. Epigenetic landscaping during hESC differentiation to neural cells. Stem Cells. 27 (6), 1298-1308 (2009).
- Dietrich, J., Noble, M., Mayer-Proschel, M. Characterization of A2B5+ glial precursor cells from cryopreserved human fetal brain progenitor cells. Glia. 40 (1), 65-77 (2002).
- Nishiyama, A. NG2 cells in the brain: a novel glial cell population. Hum. Cell. 14 (1), 77-82 (2001).
- Jungblut, M., et al. Isolation and characterization of living primary astroglial cells using the new GLAST-specific monoclonal antibody ACSA-1. Glia. 60 (6), 894-907 (2012).
- Ono, Y., et al. Differences in neurogenic potential in floor plate cells along an anteroposterior location: midbrain dopaminergic neurons originate from mesencephalic floor plate cells. Development. 134 (17), 3213-3225 (2007).
- Chung, S., et al. ES cell-derived renewable and functional midbrain dopaminergic progenitors. Proc. Natl. Acad. Sci. U.S.A. 108 (23), 9703-9708 (2011).
- Doi, D., et al. Isolation of Human Induced Pluripotent Stem Cell-Derived Dopaminergic Progenitors by Cell Sorting for Successful Transplantation. Stem Cell Reports. 2 (3), 337-350 (2014).
- Solozobova, V., Wyvekens, N., Pruszak, J. Lessons from the embryonic neural stem cell niche for neural lineage differentiation of pluripotent stem cells. Stem Cell Rev. 8 (3), (2012).
- Turaç, G., et al. Combined flow cytometric analysis of surface and intracellular antigens reveals surface molecule markers of human neuropoiesis. PloS One. 8 (6), e68519 (2013).
- Buchwalow, I. B., Böcker, W. Chapter 2. Immunohistochemistry: Basics and Methods. , 9-17 (2010).
- Tario, J. D., et al. Optimized staining and proliferation modeling methods for cell division monitoring using cell tracking dyes. J. Vis. Exp. (70), e4287 (2012).
- Lyons, A. B., Parish, C. R. Determination of lymphocyte division by flow cytometry. J. Immunol. Methods. 171 (1), 131-137 (1994).
- Hawkins, E. D., et al. Measuring lymphocyte proliferation, survival and differentiation using CFSE time-series data. Nat. Protoc. 2 (9), 2057-2067 (2007).
- Quah, B. J. C., Parish, C. R. The use of carboxyfluorescein diacetate succinimidyl ester (CFSE) to monitor lymphocyte proliferation. J. Vis. Exp. 44, (2010).
- Sukhdeo, K., et al. Multiplex flow cytometry barcoding and antibody arrays identify surface antigen profiles of primary and metastatic colon cancer cell lines. PloS One. 8 (1), e53015 (2013).
- Jiang, L., et al. Daucosterol promotes the proliferation of neural stem cells. The J. Steroid Biochem. Mol. Biol. 140, 90-99 (2014).
- Hulspas, R., et al. Considerations for the control of background fluorescence in clinical flow cytometry. Cytometry. B. 76 (6), 355-364 (2009).
- Moloney, M., Shreffler, W. G. Basic science for the practicing physician: flow cytometry and cell sorting. Annals of Allergy, Asthm., & Immunology: Official Publication of the American College of Allergy, Asthma., & Immunology. 101 (5), 544-549 (2008).
- Siebzehnrubl, F. A., et al. Isolation and characterization of adult neural stem cells. Methods Mol. Biol. 750, 61-77 (2011).
- Guez-Barber, D., et al. FACS purification of immunolabeled cell types from adult rat brain). J. Neurosci. Methods. 203 (1), 10-18 (2012).
- Tham, C. -. S., Lin, F. -. F., Rao, T. S., Yu, N., Webb, M. Microglial activation state and lysophospholipid acid receptor expression. Int. J. Dev. Neurosci. 21 (8), 431-443 (2003).
- Nguyen, H. X., Beck, K. D., Anderson, A. J. Quantitative assessment of immune cells in the injured spinal cord tissue by flow cytometry: a novel use for a cell purification method. J. Vis. Exp. (50), e2698 (2011).
- Marchenko, S., Flanagan, L. Counting human neural stem cells. J. Vis. Exp. (7), 262 (2007).
- Brunlid, G., Pruszak, J., Holmes, B., Isacson, O., Sonntag, K. C. Immature and neurally differentiated mouse embryonic stem cells do not express a functional Fas/Fas ligand system. Stem Cells. 25 (10), 2551-2558 (2007).
- Brewer, G. J. Isolation and culture of adult rat hippocampal neurons. J. Neurosci. Methods. 71 (2), 143-155 (1997).
- Cardona, A. E., Huang, D., Sasse, M. E., Ransohoff, R. M. Isolation of murine microglial cells for RNA analysis or flow cytometry. Nat. Protoc. 1 (4), 1947-1951 (2006).
- Nielsen, J. A., Maric, D., Lau, P., Barker, J. L., Hudson, L. D. Identification of a novel oligodendrocyte cell adhesion protein using gene expression profiling. J. Neurosci. 26 (39), 9881-9891 (2006).
- Daneman, R., et al. The mouse blood-brain barrier transcriptome: a new resource for understanding the development and function of brain endothelial cells. PloS One. 5 (10), e13741 (2010).
- Gräbner, R., Till, U., Heller, R. Flow cytometric determination of E-selectin, vascular cell adhesion molecule-1, and intercellular cell adhesion molecule-1 in formaldehyde-fixed endothelial cell monolayers. Cytometry. 40 (3), 238-244 (2000).
- Quah, B. J. C., Parish, C. R. New and improved methods for measuring lymphocyte proliferation in vitro and in vivo using CFSE-like fluorescent dyes. J. Immunol. Methods. 379 (1-2), 1-14 (2012).
- Lathia, J. D., et al. High-throughput flow cytometry screening reveals a role for junctional adhesion molecule a as a cancer stem cell maintenance factor. Cell Rep. 6 (1), 117-129 (2014).
- Ganat, Y. M., et al. Identification of embryonic stem cell-derived midbrain dopaminergic neurons for engraftment. J. Clin. Invest. 122 (8), 2928-2939 (2012).
- Hedlund, E., et al. Embryonic stem cell-derived Pitx3-enhanced green fluorescent protein midbrain dopamine neurons survive enrichment by fluorescence-activated cell sorting and function in an animal model of Parkinson’s disease. Stem Cells. 26 (6), 1526-1536 (2008).
- Maroof, A. M., et al. Directed differentiation and functional maturation of cortical interneurons from human embryonic stem cells. Cell Stem Cell. 12 (5), 559-572 (2013).
- Chivet, M., Hemming, F., Pernet-Gallay, K., Fraboulet, S., Sadoul, R. Emerging role of neuronal exosomes in the central nervous system. Front. Physiol. 3, 145 (2012).
- Graner, M. W., et al. Proteomic and immunologic analyses of brain tumor exosomes. FASEB J. 23 (5), 1541-1557 (2009).
- Eldh, M., Lötvall, J. Isolation and characterization of RNA-containing exosomes. J. Vis. Exp. (59), e3037 (2012).
- Capela, A., Temple, S. LeX is expressed by principle progenitor cells in the embryonic nervous system, is secreted into their environment and binds Wnt-1. Dev. Biol. 291 (2), 300-313 (2006).
- Nieoullon, V., Belvindrah, R., Rougon, G., Chazal, G. mCD24 regulates proliferation of neuronal committed precursors in the subventricular zone. Mol. Cell. Neurosci. 28 (3), 462-474 (2005).
- Nagato, M., et al. Prospective characterization of neural stem cells by flow cytometry analysis using a combination of surface markers. J. Neurosci. Res. 80 (4), 456-466 (2005).
- Hall, P. E., Lathia, J. D., Miller, N. G. A., Caldwell, M. A., French-Constant, C. Integrins are markers of human neural stem cells. Stem Cells. 24 (9), 2078-2084 (2006).
- Hargus, G., et al. Differentiated Parkinson patient-derived induced pluripotent stem cells grow in the adult rodent brain and reduce motor asymmetry in Parkinsonian rats. Proc. Natl. Acad. Sci. U.S.A. 107 (36), 15921-15926 (2010).
- Elkabetz, Y., et al. Human ES cell-derived neural rosettes reveal a functionally distinct early neural stem cell stage. Genes Dev. 22 (2), 152-165 (2008).

