This content is Free Access.
JoVE Journal
Medicine
Surgical Procedures for a Rat Model of Partial Orthotopic Liver Transplantation with Hepatic Arterial Reconstruction
Chapters
- 00:05Title
- 01:07Donor Operation
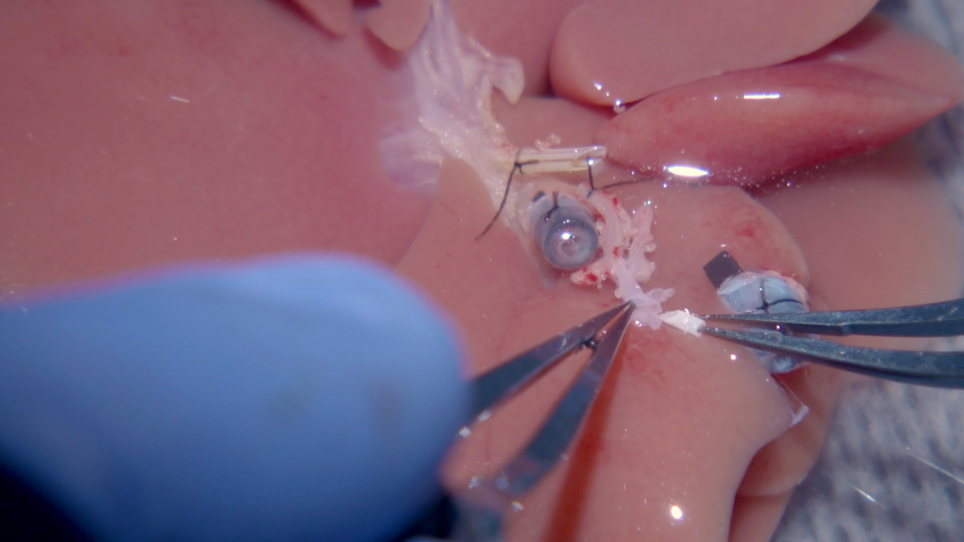
- 06:30Ex vivo Graft Preparation
- 10:02Recipient Operation
- 17:46Results: Survival of Recipient Rats and Hepatocellular Damage to the Liver Grafts
- 18:24Conclusion
Orthotopic liver transplantation in rats is an indispensable experimental model for biomedical research. Here we present our surgical procedures for orthotopic rat liver transplantation with hepatic arterial reconstruction using a 50% partial graft.
Tags
Surgical ProceduresRat ModelPartial Orthotopic Liver TransplantationHepatic Arterial ReconstructionTransplantation ResearchGraft PreservationIschemia-reperfusion InjuryImmunological ResponsesHemodynamicsSmall-for-size SyndromeDifficult Animal ModelMicrosurgical SkillsReliabilityReproducibilityStandardized ProceduresSophisticated ProceduresHepatic Arterial Reconstruction EliminationCuff Anastomosis TechniqueKamada Et Al.Hepatic Rearterialization Elimination