A subscription to JoVE is required to view this content. Sign in or start your free trial.
JoVE Journal
Biology
Methods for Patch Clamp Capacitance Recordings from the Calyx
Chapters
- 00:00Introduction
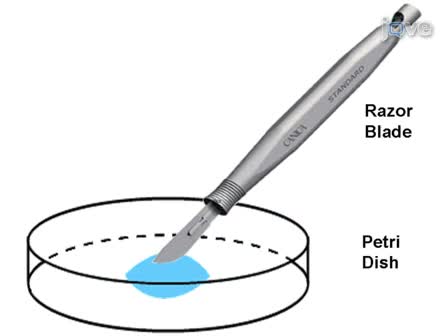
- 00:25Dissection Overview
- 02:00Dissection of Brain
- 05:52Physiology Experiments
- 11:34Locating an Accessible Calyx
- 12:16After Some Searching
- 14:04Conclusion
- 14:48Credits
We demonstrate the basic techniques for presynaptic patch clamp recording at the calyx of Held, a mammalian central nervous system nerve terminal.
Tags
Patch ClampCapacitance RecordingsCalyx Of HeldPresynaptic TerminalAction PotentialsCalcium Channel CurrentsVesicle FusionExocytosisMembrane UptakeEndocytosisCell MembraneNeurotransmitterCapacitance IncreaseCapacitance ReductionVesicular ReleaseMammalian CNS Nerve TerminalPostsynaptic ActivitySlice PreparationMorphological FeaturesPatch Clamping Techniques