Summary
이 문서에는 유리한 줄기 세포 재산으로 다층된 줄기 세포 시트를 건설 하기 위한 효율적이 고 실현 가능한 방법을 제공 합니다.
Abstract
줄기 세포 치료 보여줍니다 유망한 재생성 하는 손상 된 장기 및 조직, 미래 및 셀 시트 기술 낮은 세포 보존 및 대상 영역 내에서 가난한 생존을 향상 시키기 위해 개발 되었습니다. 그러나, 생체 외에서 건설 과정 중 줄기 세포 bioactivity를 유지 하 고 셀 시트 내의 셀 금액 증가 대 한 솔루션은 절실히 필요 합니다. 여기,이 프로토콜은 유리한 줄기 세포 bioactivity와 최적의 운용성 다층된 셀 시트를 만들기 위한 메서드를 제공 합니다. Decellularized 돼지 심장 (DPP) 셀 시트 발판으로2 (PLA2) decellularization 메서드 phospholipase에 의해 준비 되 고 쥐 골 수 중간 엽 줄기 세포 (BMSCs) 절연 및 시드 셀으로 확장. 임시 다층된 셀 시트 구조는 RAD16를 사용 하 여 건설-나 펩타이드 하이드로 겔. 마지막으로, 셀 시트 동적 관류 시스템을 3 차원 (3D) 구조를 안정화할와 교양 그리고 셀 시트는 48 시간 문화에 체 외에얻을 수 있었습니다. 이 프로토콜 다층된 줄기 세포 시트를 건설 하기 위한 효율적이 고 실현 가능한 방법을 제공 하 고 셀 시트 유리한 줄기 세포 치료 제품으로 미래에 개발 될 수 있습니다.
Introduction
줄기 세포 치료; 많은 질병에 대 한 효과적인 치료로 보고 되었습니다. 그러나, 낮은 세포 보존 및 대상 영역 내에서 가난한 생존 기존의 줄기 세포 주입을 다음과 같은 중요 한 문제 남아 있다. 이 문제를 해결 하려면 조직 공학 과학자 셀 시트 기술 개발. 그대로 세포 외 매트릭스 monolayered 셀 시트 온도 응답 문화 접시1을 사용 하 여 첫째로 준비 되었다 그리고 그것의 후속 연구 보고 줄기 세포 보존 및 infarcted는 내 생존의 중요 한 개선 지역2,3. 방법 중에서 다층된 셀 시트 구성 보고 되었습니다 셀 생존과 셀 시트 치료 효과3,4를 개선 하기 위한 효과적인 전략으로. 그 이후, 과학자 들은 셀 금액, 줄기 세포 속성 및 셀 시트의 기계적 성질을 향상 시키기 위해 다른 셀 시트 공법을 개발 했습니다. 지금까지 특정 유형의 셀 시트 건설 되 고 심근 경색5, 연골 부상6, 치료에서 공부 하 고 피부 상처7.
줄기 세포 이식 전에 bioactivity 손상된 조직 재생에 새로운 영향 그리고 다른 셀 시트 건설 전략 줄기 세포에 다른 효과가지고. 한 손으로, confluent 셀 시트, 고밀도 줄기 세포만 이루어져 고 자연 세포 외 매트릭스 스태킹 monolayered 셀 시트8 하거나 자기 조직 공학 기법9를 사용 하 여 얻을 수 있습니다. 다른 한편으로, 연구원은 적절 한 기계적 강도 제공 하 여 세포 성장10,11,12, 허용 되도록 영양 밀도 시드 낮은 줄기 세포 지원 다른 건설 기계 개발 공급. 그러나, 이러한 방법에도 불구 하 고 다층된 셀 시트 구조 내에서 낮은 효율적인 영양 공급 체 외에 건설 기간 동안 주요 관심사 남아 있습니다. 따라서, 효율적이 고 실현 가능한 셀 시트 건설 시스템이 급히 필요 합니다.
이 프로토콜 multilayeredmesenchymal 줄기 세포 (MSC) 셀 시트를 준비 하는 단계를 설명 합니다. 이 건설 시스템에서 셀 시트 기계적 강도 DPP에 의해 제공 됩니다. 이 비 계에 따라, 3D 셀 구조 건설 수 있습니다 신속 하 게 RAD16와 함께-난 펩 티 드 히드로, 동적 관류 시스템 문화 다층된 셀 시트 3D 셀 시트 구조를 안정화 하 고 충분 한 영양을 제공 하기 위해 사용 된다 셀에 대 한 공급입니다. 이 시스템을 사용 하 여, 다층된 BMSC 시트 성공적으로 준비 하 고 쥐 심근 경색 모델13에 대 한 최적의 치료 효과 전시.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
모든 줄기 세포 및 동물 실험 절차 관리 및 실험 동물의 사용에 대 한 국가 가이드의 윤리 지침에 따라 실시 되었고 제 남 대학교 동물 관리 및 사용 위원회 (광저우, 중국)에 의해 승인.
1. PLA2 Decellularization와 DPP 발판의 준비 방법14
주: PLA2 decellularization 방법의 회로도 대 한 그림 1A 를 참조 하십시오.
- 100 mL 200 U/mL PLA2 솔루션의 준비. 탄산 버퍼 솔루션의 198 mL에 0.5 g의 나트륨 deoxycholate 및 PLA2 의 2 개 mL를 추가 합니다. 이 솔루션의 준비 후 24 시간 안에 사용 되어야 한다.
- 도살에서 신선한 돼지 심장 막 (FPP)을 얻습니다 그리고 1 시간 이내 실험실 돌아갑니다.
참고:는 FPP 저장 되어야 한다 4 ° C에서 수송 하는 동안. 단계 1.2 1.10 온도 제어 물 욕조에 지속적인 동요와 함께 실시 한다. - 철저 하 게 세척 1% 페니실린-스 10 ° Cfor 10 분에 500 mL 비 커에 포함 된 인산 염 버퍼 솔루션 (PBS)의 200 mL와 FPP 2 x이이 단계를 반복 합니다.
- FPP는 2 개의 층으로 분할 하 고 집게와가 위 지방 조직 제거 합니다.
참고: 모든 20 분의 지방 조직을 제거 하는 동안 PBS의 50 mL를 추가 하 여 젖은 FPP 유지. - 가 위는 FPP 10 x 10 cm2 조각으로 모양. 워시 200ml 탄산 버퍼 솔루션 (CBS)의 2 배가이 단계를 반복 하는 10 분에 대 한 1% 페니실린-10 ° C에서 500 mL 비 커에 스를 포함와 FPP.
- 순수한 물에는 FPP를 전송 하 고 12 h 10 ° C에서 그것을 담가.
- 200 U/mL PLA2 와 6 h 37 ° C에서 0.5% (w/v) 나트륨 deoxycholate 솔루션을 포함 하는 CBS의 50 mL 10 x 10 cm2 샘플을 담근 다.
- 이 단계 2 x 10 분 반복 10 ° C에서 1% 페니실린-스를 포함 하는 CBS와 샘플을 씻으십시오.
- 200 U/mL PLA2 , 2 h 37 ° C에서 0.5% (w/v) 나트륨 deoxycholate 솔루션을 포함 하는 CBS의 50 mL에 각 샘플을 담근 다.
- 워시 샘플 2 h. 반복 10 ° C에서 1% 페니실린-스를 포함 하는 CBS와 10 x에 대 한이 단계 적어도. 샘플 평면 접시에 놓고 55 ° c.에 오븐을 일정 한 온도에서 일정 무게를 건조
참고: 샘플 완전히 건조 해야 합니다. 무게 DPP 샘플 마다 10 분 하 고 반복 하는 3 배 또는 무게까지 더 이상 변경. - 판형으로 각 DPP 샘플 10.5 m m 직경 원형으로 모양. 살 균 밀봉된 봉투에 각 DPP를 팩.
- 감마 방사선 (kGy 25)에 의해 DPP 샘플을 소독. 사용 하기 전에 4 ° C에서 DPP 샘플을 저장.
참고: 모든 샘플은 4 ° c.에 6 달까지 동안 저장 될 수 있다
2. 셀에 대 한 준비 시트 건설
- 오토 클레이 브 모든 악기와 121 ° C에서 조직 캐리어 구성 요소 1.5 mL 원심 튜브, 겸 자를 포함 하 여 30 분, 집게가 위, 이빨에 대 한 흑인 기지 (조직 캐리어 구성 요소), 그리고 백색 긴장 반지 (조직 캐리어 구성 요소).
- 무 균 10% 자당 해결책의 20 mL를 준비 합니다. 자당의 2 세대 무게와 초순 물 18 mL에 자당 분해. 30 분 또는 0.22 μ m 필터 필터 솔루션에 대 한 121 ° C에서 10% 자당 해결책 압력솥.
- 고압 가스를 포함 하 여 30 분 동안 121 ° C에서 동적 관류 시스템 장치 교환 장비, 500ml 유리병, 관류 문화 컨테이너 및 연결 튜브.
- 압력가 마로 소독 기기 및 조직 캐리어 구성 요소를 준비 합니다. 문화 접시에 조직 캐리어의 검은 기본 부분을 넣어.
- 말린된 DPP 비 계를 선택 하 고 검은 기지의 중심에 그것을 넣어. 민 비 계에 흰색 긴장 반지를 넣고 조직 캐리어에 그것을 해결.
참고: 확인 발판은 완전히 조직 캐리어에 고정 블랙 기지와 흰색 긴장 반지 사이 차이가 있다. 그렇지 않다면 조직 캐리어를 분리 하 고 다시 발판을 해결. - 재 위한 DPP 발판에 문화 매체의 100 µ L를 추가 합니다.
참고: 발판 조직 캐리어에 잘 고정 하지 않습니다, 경우 문화 매체 문화 접시에 침투 됩니다. - 37 ° C 배양 기에는 비 계를 넣고 15 분 동안 담가 수 있습니다.
3. 셀 시트 건설에 대 한 셀의 준비
참고:이 프로토콜은 100 mm 접시를 사용 하 여 세포 배양. 다층된 셀 구조 건설의 회로도 그림 1B 를 참조 하십시오.
- BMSCs13를 격리 합니다.
참고:이 메서드는 다중된 MSC 셀 시트를 건설 하기 위한 설계 되었습니다. 쥐 BMSCs이이 프로토콜에 사용 됩니다. BMSCs는 전체 골 부착 방법을 사용 하 여 격리 되며는 BMSCs 확장 된 시험관에 충분 한 셀 크기를.- 고압 121 ° C에서 30 분, 집게,가 위, 이빨된 집게, 등 악기. 2 mL 주입 주사기와 BMSC 문화 매체 (Dulbecco의 수정이 글의 중간 [DMEM], 10% 태아 둔감 한 혈 청, 1% 글루타민, 및 1% 페니실린-스)를 준비 합니다.
- 자 궁 경부 척추 전위에 의해 3 주 된 남성 Sprague-Dawley (SD) 쥐를 안락사. 100 mL 비 커 5 분에 75% 알코올 솔루션의 동물을 담근 다.
- 비 커에서 동물을가지고 고 작업 테이블에 발생 하기 쉬운 장소. 집게와가 위는 동물의 뒷면에 피부를 incise. 피부와 근육 조직을 노출 허벅지 화관을 격리 합니다.
- 허벅지 화관을 분리 하 고 30 mL PBS의 50 mL 원심 분리기 튜브에서에 넣어. 1 개의 관으로 두 허벅지 화관을 놓습니다. 원심 분리기 튜브 조직을 철저 하 게 씻어 소용돌이. 2 x이이 단계를 반복 합니다.
- 가 위는 화관의 양쪽 끝을 잘라 고 골 수 구멍을 노출.
- BMSC 문화 매체의 2 개 mL를 주입 주사기와 발음. 골 수 구멍에 바늘을 삽입 하 고 문화 매체와 골 수 밖으로 플러시. 한 100 m m 문화 접시에 모든 두 허벅지 화관 밖으로 플러시.
- 각 100 m m 문화 요리 문화 접시에 배양의 2 개 mL를 추가 합니다. 문화 요리 72 h에 대 한 정적 문화와 37 ° C 배양 기에 넣어.
- 인큐베이터에서 문화 접시를 꺼내. 신선한 문화 매체의 6 mL에는 상쾌한을 바꿉니다.
- 기본 BMSCs 현미경으로 관찰 합니다. 이것 다음, 모든 5-7 d는 BMSCs 통로.
- 인큐베이터에서 세포를 가져가 라. 현미경으로 세포를 관찰 하 고 셀 시트 건설에 대 한 적합 한 셀을 선택 합니다. BMSCs에 도달 80%-90% 합류, 시드 셀으로 셀을 선택할 수 있습니다.
- 문화 요리에서 문화 매체를 제거 합니다. 부드럽게 따뜻한 PBS의 2 mL로 세포 세척. 문화 요리에서 모든 PBS를 제거 하 고 확실히 더 액체 남아. 접시에 0.25 %trypsin (또는 다른 출신과 솔루션)의 2 개 mL를 추가 하 고 3 분 동안 37 ° C에서 품 어.
- 문화 매체의 2 개 mL를 추가 하 여 트립 신 효과 중지 하 고 부드럽게 씻어 접시에서 셀. 새로운 15ml 원심 분리기 튜브에 세포 현 탁 액을 전송 합니다. Centrifugate 225 x g 5 분에 셀.
- 제거는 상쾌한. 10% (w/v) 자당 솔루션의 3 mL와 함께 셀 resuspend
참고: 다음 단계에서 균일 한 셀-히드로 혼합물을 얻기 위하여 세포를 씻어 10% (w/v) 자당 솔루션 사용 됩니다. - 세포 현 탁 액의 10 µ L 발음과 hemocytometer와 셀 번호. 다음 단계에 필요한 볼륨을 계산 합니다. 한 셀 시트, 3 백만 BMSCs 사용 됩니다.
- 3 백만 세포를 추출 하 고 새로운 15ml 원심 관으로 그들을 전송. 5 분에 대 한 225 x g 에서 셀 원심
- 제거는 상쾌한. 10% (w/v) 자당 해결책의 1 mL와 함께 셀 resuspend 1.5 mL 원심 분리기 튜브에 세포 현 탁 액을 전송 합니다.
참고: 셀 하이드로 겔 혼합물을 준비 도움이 됩니다 1.5 mL 원심 튜브를 사용 하 여. - 원심 260 xg 에서 셀에 대 일 분 완전히 제거는 상쾌한 셀 앙금을 얻을.
4. 준비는 BMSCs는 RAD16의-나 펩 티 드 히드로 혼합물
주: 다층된 셀 구조 건축의 설계도 대 한 그림 1B 를 참조 하십시오.
- 1.5 mL 원심 관에 10% (w/v) 자당 솔루션의 20 µ L를 추가 합니다. 부드럽게 resuspend는 BMSCs 하 고 균일 한 현 탁 액.
참고:는 물의 resuspension 동안 모든 거품을 생성 하지 않습니다. - RAD16의 20 µ L 추가-난 펩 티 드 하이드로 겔 현 탁 액의 상단에. 부드럽게 저 어는 RAD16-나 피 펫 팁과 펩 티 드와 셀 서 스 펜 션. 세포 현 탁 액 및 히드로 함께 혼합 되어, 부드럽게 플라스틱 혼합물 몇 번.
- 조직 캐리어에서 DPP 발판에 밖으로가 고 부드럽게 피 펫 팁 문화 매체를 발음.
주: DPP 비 계는 완전히 셀 하이드로 겔 혼합물을 추가 하기 전에 리하이드레이션 된 확인 하십시오. - 혼합물을 발음 하 고 균등 하 게 DPP 비 계에 그것을 추가.
참고: 혼합물의 전체 볼륨에 대 한 될 것 이라고 40-50 µ L. 발판의 외부에는 센터에서 한 번에 혼합 10 µ L을 추가 하는 것이 좋습니다. - 조직 캐리어의 하단에 문화 매체의 1 mL를 추가 합니다. 5 분 동안 37 ° C 배양 기에서 셀 시트를 넣어.
- 인큐베이터에서 셀 시트를 꺼내. 부드럽게 문화 접시에 배양의 4 mL를 추가 하 고 셀 시트를 담가. 정적 문화의 2 h 37 ° C 배양 기에서 셀 시트를 넣어.
5. 동적 문화 시스템을 사용 하 여 3 차원 다층된 셀 시트의 생체 외에서 문화
참고: 3D 동적 시스템의 회로도 그림 1C 참조.
- 연동 펌프, 가스 교환 장비, 500ml 유리병, 관류 문화 컨테이너 및 연결 튜브를 포함 하 여 동적 관류 시스템을 준비 합니다. 그림 2와 같이 동적 관류 시스템을 조립.
- 문화 매체의 200 mL 소독 유리 병에 추가 합니다. 문화 컨테이너의 챔버에 셀 시트를 삽입 합니다.
참고: 셀 시트의 상부 표면 방향에 주의. - 조직 컨테이너에 문화 매체의 3 개 mL를 추가 하 고 컨테이너를 닫습니다. 인큐베이터에서 동적 관류 시스템을 넣고 펌프를 시작. 연동 펌프의 유량 8 mL/분 문화에로 설정 셀 시트 48 h에 대 한 동적 관류 시스템.
6. 취득 다층된 MSC 셀 시트
- 고압 기기 및 조직 캐리어 구성 요소 1.5 mL 원심 관, 이빨된 집게, 집게, 등 30 분 동안 121 ° C에서.
- 컨테이너에 문화 매체의 공급 중지 유리 병에서 입력된 덕트를 당겨.
참고: 때 문화 컨테이너 비어 연동 펌프를 중지 합니다. - 문화 컨테이너에서 셀 시트를 꺼내와 문화 접시에 그것을 넣어.
- 한 집게를 사용 하 여 조직 캐리어를 고정 하 고 다른 이빨된 집게를 사용 하 여 검은 기지에서 흰색 긴장 반지를 구분. 마지막으로, 다중된 BMSCs 셀 시트를 구하십시오.
- 짧은 보존에 대 한 각 셀 시트는 집게와 원심 1.5 mL 튜브에 전송 수 있습니다. 민 비 계 원심 튜브의 내부 벽에 붙어 있어야 한다 고 셀 시트 전파 한다 원심 분리기 튜브에 가능한 한 많이 밖으로.
- 부드럽게 셀 시트 몰입할 원심 관에 문화 매체의 1 mL를 추가 합니다. 원심 관의 뚜껑을 닫고 4 ° c.에 셀 시트 저장
참고: 셀 시트 이식 하거나 최대한 빨리 분석 되어야 한다. 4 h 이내 셀 시트를 사용 하는 것이 좋습니다.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
다층된 줄기 세포 시트 건설의 회로도 그림 1에 표시 됩니다. PLA2 decellularization 메서드에 의해 셀 시트 발판을 준비 하는 것은 첫 번째 단계입니다. 발판을 바탕으로, RAD16-1 펩 티 드 히드로와 줄기 세포를 혼합 하 여 임시 3D 셀 구조는 건설 한다. 유리한 줄기 세포 bioactivity와 최적의 기계적 강도 다층된 셀 시트를 얻으려면 셀 시트 동적 관류 시스템에 양식입니다. 동적 영양 공급에서 줄기 세포는 증식 하 고 다층된 셀 시트 셀 연락처 설정 허용 되 고 ~ 24-72 최종 안정 다층된 셀 시트 제품을 얻을 수 있습니다-시간 재배.
이 경우에, 셀 시트 발판 DPP PLA2 decellularization 방법에 의해 준비 된다. 말린된 DPP의 외관은 평면, 부드럽고 반투명 (그림 3A). PLA2의 특정 lyse 효과 때문에 이종 세포 제거 될 수 있다 완전히 동안 DPP 비 계 내에서 천연 콜라겐의 열 대권 외 잘 보존 된 (그림 3B), 그리고이 유지 관리 하는 것이 중요 합니다 기계적 강도와 발판의 생체 적합성입니다. 또한, 줄기 세포 성장을 지원 하는 비보에 재생13개선 성장 인자 제어 릴리스 시스템으로는 건설 기계를 수정할 수 있습니다.
줄기 세포 합류 ~ 80%-90%에 도달, 셀 문화 접시에서 격리 되 고 10% 자당 해결책으로 세척. 원심, 후 세포는 RAD16와 함께 혼합-난 펩 티 드 히드로 rehydrated DPP 발판에 추가. 임시 다층된 구조 2 시간 정적 문화를 따라 형성 된다. 마지막으로, 다중된 BMSC 시트 제품 (그림 4) 동적 관류 시스템에서 48 시간 문화에 따라 취득 된다. 민 비의 지원, 셀 시트 겸 자와 함께 쉽게 조작 될 수 있습니다 그리고 그것은 보존 될 수 일시적으로 4 ° C에서 1.5 mL 튜브에 문화 매체에서 4 시간에 대 한 검사 또는 이식 (그림 4) 하기 전에. 면역 형광 검사 결과 쇼를 얼룩이 지는 BMSCs는 CD90 및 CD29 줄기 세포 표식에 대 한 매우 긍정적인. CD29 CD90의 다층된 셀 시트 보기 높은 수준 내에서 BMSCs 셀 시트 시공 후 (그림 5).

그림 1 : 다층된 줄기 세포 시트 건설의 순서도. (A) 자연 세포 외 매트릭스는 DPP 비 계에서 잘 보존 되는 FPP 내의 다른 유형의 셀 파괴 하는 PLA2 decellularized 메서드를 사용 하 여. (B) DPP 비 계에 따라, 임시 다층된 셀 구조는 줄기 세포를 혼합 하 고 각자 펩 티 드 히드로 조립 하 여 건설. (C)에 따라, 셀 시트 3D 동적 시스템에서 경작 하 고 줄기 세포 증식 및 동적 영양 공급에서 셀 연락처 설정 것으로 예상 된다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.

그림 2 : 조직 캐리어 및 동적 관류 시스템. (A)이 패널 쇼는 13 m m 직경 조직 캐리어. (B)이이 패널 동적 관류 시스템의 어셈블리를 보여 줍니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
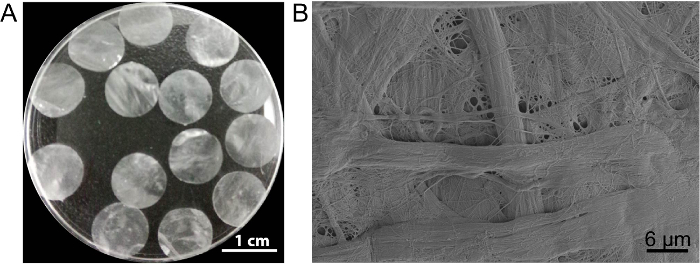
그림 3 : 모양과 DPP의 열 대권 외. (A)이이 패널 10.5 m m 직경 DPP 장비의 외관을 보여줍니다. (B)이이 패널 DPP 발판의 스캐닝 전자 현미경 (SEM) 결과의 대표 이미지를 보여줍니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
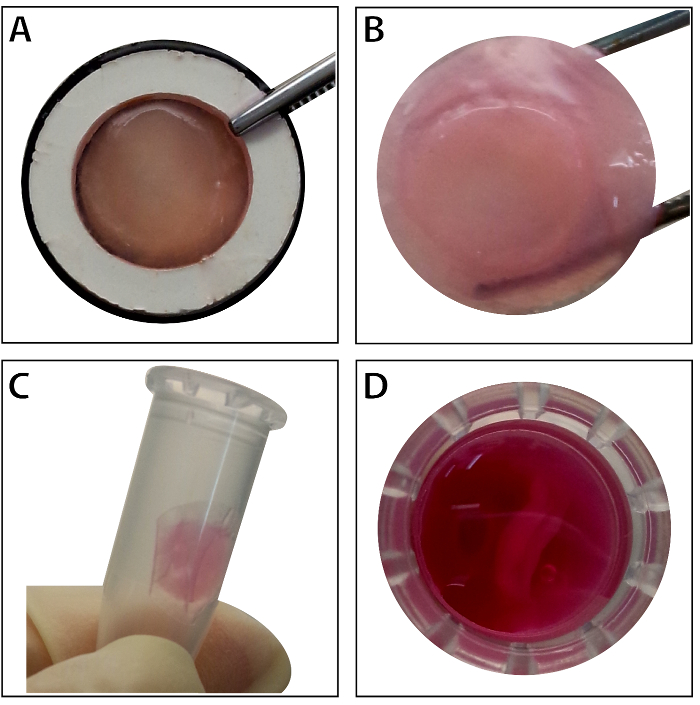
그림 4 : 다층된 BMSC 시트의 모습. (A)이이 패널 표시 다층된 BMSC의 모양을 내 조직 캐리어 시트 합니다. (B) 그대로 다층된 BMSC 시트 겸 자에 의해 개최 됩니다. (C - D) 다층된 셀 시트 사용 하기 전에 1.5 mL 튜브에 일시적으로 보존 될 수 있습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
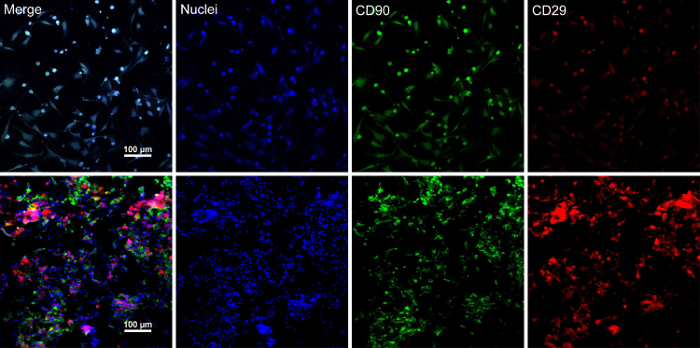
그림 5 : 면역 형광 BMSC 마커 식의 결과 얼룩. (A)이이 패널 쇼 면역 형광 셀 시트 건설 하기 전에 BMSCs의 결과 얼룩이 지기 (B)이이 패널 면역 형광 얼룩 다층된 BMSC 시트 섹션의 결과 보여줍니다. CD90 (녹색) 및 CD29 (빨간) 긍정적으로 BMSCs와 셀 시트에 표현 되었다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
현재 프로토콜 다층된 MSC 시트를 생성 하는 효율적인 방법을 보고 합니다. 이 셀 시트는 최적의 기계적 강도, 높은 셀 시드 밀도, 및 유리한 줄기 세포 bioactivity를 전시 한다. 예를 들어 BMSCs를 사용 하 여, 3 차원 셀 구조는 신속 하 게 구성 RAD16-나 펩타이드 하이드로 겔. 동적 관류 시스템에서 경작 되 고, 후 다층된 BMSC 시트 성공적으로 획득 하 고는 BMSCs 줄기 세포 표식의 높은 식 유지.
임시 다층된 셀 구조를 건설 하는 것은 프로토콜의 중요 한 단계입니다. RAD16-난 상업 히드로 펩 티 드, 그리고 1% 아미노산 및 99% 물으로 구성 됩니다. 여러 연구 보고이 펩 티 드 히드로 ECM 자연을 모방 수 있습니다 줄기 세포 증식과 생존15,,1617에 대 한 도움이 됩니다. 현재 프로토콜 (10% 자당 해결책의 20 µ L)에서 3 백만 MSC 정지 RAD16의 20 µ L를 혼합 했다-난 펩 티 드 하이드로 겔. 세포 현 탁 액 및 펩타이드 하이드로 겔의 볼륨 비율 1:1 이었다. 이 펩 티 드 히드로 환경 pH 값에 민감한 이며 pH 값에서에서 변경 될 때 산 성 중립 펩 티 드 분자 자동으로 3D 네트워크 형성. 세포 표면 입자를 포함 하기 때문에 셀 혼합물에서에서 변경 액체 히드로 영향에는 짧은 시간에도 셀의 혼합. 유리한 셀 하이드로 겔 세포 현 탁 액 및 펩타이드 하이드로 겔의 동등한 혼합물 및 셀 혼합물 균등 하 게 발판에 추가 될 수 있습니다. 연구원은 시드 셀 번호, 자당 솔루션 볼륨, 그리고 그들의 실제 필요에 따라 펩 티 드 히드로 볼륨을 변경 하 여 혼합 상태를 최적화할 수 있습니다. 그것은 가치가 10% 자당 해결책으로 셀을 세척 하는 통지를 그리고 셀 하이드로 겔 혼합물을 균등 하 게 혼합 프로토콜의 중요 한 단계는 고르지 혼합물 큰 셀 손실 및 불안정 한 임시 다층된 구조를 발생할 수 있습니다.
DPP 발판에 셀 하이드로 겔 혼합물을 추가한 후 다층된 셀 시트 구조의 기계적 강도 약한 때문에 펩 티 드 히드로 네트워크 장기 다층된 셀 구조를 유지 하 고 셀에 강하지 않다 연결 및 ECM 분 비 셀 시트의 안정성을 향상 시키기 위해 필요 합니다. 또한, 문화 매체의 동적 침투 줄기 세포 증식 동안 부족 한 영양 공급이 세포 apoptosis를 일으키는 원인이 되며 셀 밀도 줄일 다층된 셀 구조에서 셀 연락처를 구축을 용이 하 게 수 있습니다. 셀의13장. 따라서, 동적 관류 시스템 다층된 셀 시트 구조 안정화에 대 한 중요 하다. 또한, 특정 줄기 세포 유형 및 밀도 시드 셀 문화 매체의 적절 한 흐름 속도 조정 한다. 또한, DPP 비 계 및 다층된 셀 구조 사이 약한 기계적 연결 다층된 세포 층과 발판의 발생할 수 있습니다 현재 공법의 제한 남아 있습니다. 따라서, 추가 연구 필요 3D 하이드로 겔 비 계 및 DPP 비 계의 기계적 생체 적합성을 향상 합니다.
지금까지, 조직 공학 과학자18 세포 내 피 coculturing와 같은 효율적인 영양 공급 시스템에서 생체 외에서설정 하 고 사용 하 여 다공성 비 계19에 집중 되어 있다. 그러나, 3D 구조 내에서 영양 침투성 전통적인 정적 3D 문화 시스템에 낮은 이며 줄기 세포 생존 능력에 크게 영향을 받을 것입니다. 이 경우에 동적 관류 시스템을 사용 하 여 줄기 세포 생존 능력을 유지 하기 위해 충분 한 영양 공급을 제공할 수 있습니다. 이 프로토콜을 사용 하는 다층된 BMSC 시트 개선 심장 기능 및 신생 쥐 심근 경색 모델13에. 높은 셀 부하 및 유리한 줄기 세포 재산 줄기 세포 시트 제품을 구성 하는 것은 조직 재생에 중요 한입니다. 이 효율적인 생성 된 메서드를 사용 하 여 다층된 줄기 세포 시트의 다른 종류는 시드 줄기 세포 유형 상피 줄기 세포 시트, 신경 줄기 세포 시트, 또는 심장 줄기 세포 시트 등을 변경 하 여 건설 수 있습니다. 더 탐험 및 다층된 줄기 세포 시트에 대 한 대안을 더 많은 조직 재생에 대 한 응용 프로그램을 확장으로 예상 된다.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
저자는 공개 없다.
Acknowledgments
이 작품은 국립 자연 과학 재단의 중국 (보조금 번호 31771064);에 의해 지원 되었다 과학 및 기술 계획 프로젝트의 광 동성 (보조금 번호 2013B010404030, 2014A010105029, 및 2016A020214012); 과학 및 기술 계획 프로젝트의 광저우 (보조금 번호 201607010063); 그리고 학부 혁신 및 기업가 정신 교육 프로그램 (보조금 번호 201610559028); 젊은 과학자의 중국 (부여 번호 31800819)는 국립 과학 재단.
Materials
| Name | Company | Catalog Number | Comments |
| Phospholipase A2 | Sigma-Aldrich | P6534 | |
| Sodium deoxycholate | Sigma-Aldrich | D6750-100G | |
| Phosphate buffer | Gibco BRL | 89033 | |
| Penicillin streptomycin / amphotericin | Gibco BRL | 15640055 | |
| Buffer bicarbonate | Sigma-Aldrich | C3041 | |
| Table concentrator | Changzhou Aohua Instrument Co. | KT20183 | |
| Dulbecco's Modified Eagle Medium(DMEM) | Corning Cellgro | 10-014-CVR | |
| South American fetal bovine serum | Gibco BRL | 10270-106/P30-3302 | |
| L-Glutamine | Corning Cellgro | 25-005-CI | |
| 0.25% Trypsin/2.21 mM EDTA | Corning Cellgro | 25-053-CI | |
| Biosafety cabinet | Esco,Singapore | AC2-2S1 | |
| Constant temperature incubator | Esco,Singapore | CLS-170B-8 | |
| Centrifuge tube | Corning | 430790 | |
| EP tube | Axygen | 31617934 | |
| Centrifugal machine | TOMOS | 1-16R | |
| Sucrose | Sigma-Aldrich | S9378-500G | |
| Pura Matrix | BD | 354250 | |
| Dynamic perfusion culture system | Minucells and Minutissue | D-93077 | |
| Peristaltic pump | Ismatec | IPC N8 | |
| Pump tubing | Ismatec | Nr.1306 | |
| MINUSHEET 1300 | Regensburg | tissue carrier components | |
| MINUSHEET | Regensburg | dynamic perfusion system | |
| MINUSHEET 0006 | Regensburg | gas exchange equipment | |
| MINUSHEET 0002 | Regensburg | 500 mL glass bottle | |
| MINUSHEET 1301 | perfusion culture container |
References
- Miyahara, Y., et al. Monolayered mesenchymal stem cells repair scarred myocardium after myocardial infarction. Nature Medicine. 12 (4), 459-465 (2006).
- Narita, T., et al. The use of cell-sheet technique eliminates arrhythmogenicity of skeletal myoblast-based therapy to the heart with enhanced therapeutic effects. International Journal of Cardiology. 168 (1), 261-269 (2013).
- Narita, T., et al. The Use of Scaffold-free Cell Sheet Technique to Refine Mesenchymal Stromal Cell-based Therapy for Heart Failure. Molecular Therapy. 21 (4), 860-867 (2013).
- Matsuo, T., et al. Efficiently Piled-Up Cardiac Tissue-Like Sheets With Pluripotent Stem Cell-Derived Cells Robustly Promotes Cell Engraftment and Ameliorates Cardiac Dysfunction After Myocardial Infarction. Circulation. 128 (22), (2013).
- Alshammary, S., et al. Impact of cardiac stem cell sheet transplantation on myocardial infarction. Surgery Today. 43 (9), 970-976 (2013).
- Chen, G. P., et al. The use of a novel PLGA fiber/collagen composite web as a scaffold for engineering of articular cartilage tissue with adjustable thickness. Journal of Biomedical Materials Research Part A. 67a (4), 1170-1180 (2003).
- Cerqueira, M. T., et al. Human Adipose Stem Cells Cell Sheet Constructs Impact Epidermal Morphogenesis in Full-Thickness Excisional Wounds. Biomacromolecules. 14 (11), 3997-4008 (2013).
- Sasagawa, T., Shimizu, T., Sekiya, S., Yamato, M., Okano, T. Comparison of angiogenic potential between prevascular and non-prevascular layered adipose-derived stem cell-sheets in early post-transplanted period. Journal of Biomedical Materials Research Part A. 102 (2), 358-365 (2014).
- Ishii, M., et al. Multilayered adipose-derived regenerative cell sheets created by a novel magnetite tissue engineering method for myocardial infarction. International Journal of Cardiology. 175 (3), 545-553 (2014).
- Godier-Furnemont, A. F., et al. Composite scaffold provides a cell delivery platform for cardiovascular repair. Proceedings of the National Academy of Sciences of the United States of America. 108 (19), 7974-7979 (2011).
- Liu, Y., et al. Electrospun nanofibrous sheets of collagen/elastin/polycaprolactone improve cardiac repair after myocardial infarction. American Journal of Translational Research. 8 (4), 1678-1694 (2016).
- Arana, M., et al. Epicardial delivery of collagen patches with adipose-derived stem cells in rat and minipig models of chronic myocardial infarction. Biomaterials. 35 (1), 143-151 (2014).
- Wang, Y., et al. Preparation of high bioactivity multilayered bone-marrow mesenchymal stem cell sheets for myocardial infarction using a 3D-dynamic system. Acta Biomaterialia. 72, 182-195 (2018).
- Wu, Z., et al. The use of phospholipase A(2) to prepare acellular porcine corneal stroma as a tissue engineering scaffold. Biomaterials. 30 (21), 3513-3522 (2009).
- Degano, I. R., et al. The effect of self-assembling peptide nanofiber scaffolds on mouse embryonic fibroblast implantation and proliferation. Biomaterials. 30 (6), 1156-1165 (2009).
- Lampe, K. J., Heilshorn, S. C. Building stem cell niches from the molecule up through engineered peptide materials. Neuroscience Letters. 519 (2), 138-146 (2012).
- Cui, X. J., et al. Transplantation of Mesenchymal Stem Cells with Self-Assembling Polypeptide Scaffolds Is Conducive to Treating Myocardial Infarction in Rats. Tohoku Journal of Experimental Medicine. 222 (4), 281-289 (2010).
- Jun, I., et al. Spatially Assembled Bilayer Cell Sheets of Stem Cells and Endothelial Cells Using Thermosensitive Hydrogels for Therapeutic Angiogenesis. Advanced Healthcare Materials. 6 (9), (2017).
- Chen, C. H., et al. Porous tissue grafts sandwiched with multilayered mesenchymal stromal cell sheets induce tissue regeneration for cardiac repair. Cardiovascular Research. 80 (1), 88-95 (2008).



