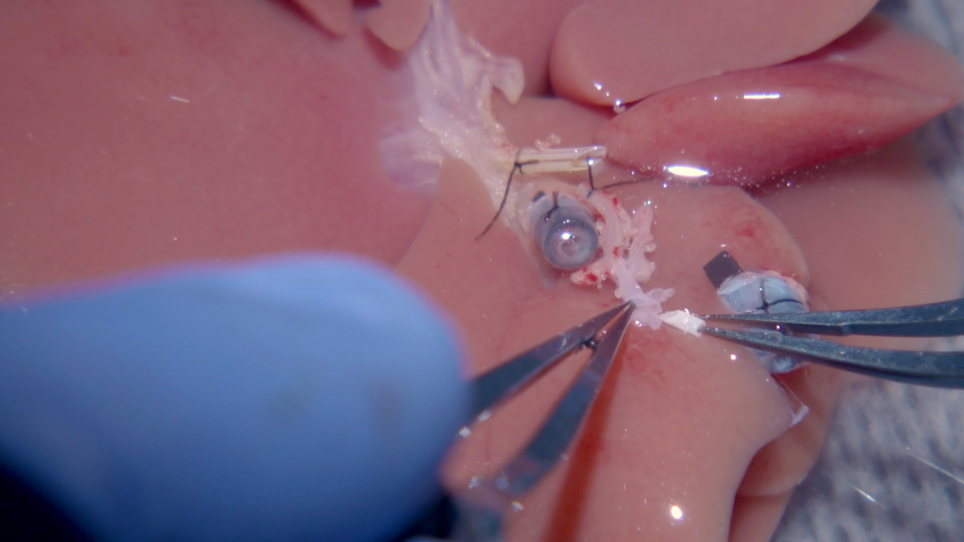
Reducción de las complicaciones después de la reconexión arterial en un modelo de rata de trasplante hepático ortotópico
Summary
El objetivo de este estudio es modificar el modelo de trasplante de hígado ortotópico de rata para representar mejor el trasplante de hígado humano y mejorar la supervivencia del receptor. El método presentado restablece la entrada arterial hepática conectando la arteria hepática común del hígado del donante con la arteria hepática adecuada del hígado receptor.
Abstract
El modelo de trasplante de hígado ortotópico de rata (OLT) es una poderosa herramienta para estudiar el rechazo agudo y crónico. Sin embargo, no es una representación completa del trasplante de hígado humano debido a la ausencia de reconexión arterial. Aquí se describe un procedimiento de trasplante modificado que incluye la incorporación de la reconexión de la arteria hepática (HA), lo que conduce a una marcada mejora en los resultados del trasplante. Con un tiempo anhepático medio de 12 min y 14 s, la reconexión de HA se traduce en una mejor perfusión del hígado trasplantado y un aumento de la supervivencia de los receptores a largo plazo del 37,5% al 88,2%. Este protocolo incluye el uso de puños y soportes impresos en 3D para conectar la vena porta y la vena cava inferior infrahepática. Se puede implementar para el estudio de múltiples aspectos del trasplante de hígado, desde la respuesta inmune y la infección hasta los aspectos técnicos del procedimiento. Al incorporar un método sencillo y práctico para la reconexión arterial mediante una técnica microvascular, este protocolo OLT de rata modificada imita de cerca aspectos del trasplante de hígado humano y servirá como un modelo de investigación valioso y clínicamente relevante.
Introduction
La carga mundial de enfermedad hepática sigue aumentando, con un aumento del 30% en las muertes relacionadas con las enfermedades hepáticas de 2005 a 20131,2. El trasplante de hígado es a menudo el único recurso para los pacientes con enfermedad hepática terminal. El hígado es el segundo órgano sólido trasplantado con más frecuencia, y el número de trasplantes de hígado realizados a nivel mundial aumentó un 7,25% de 2015 a 20161,,2. A pesar de su prevalencia, las tasas de supervivencia post-trasplante se han estancado3,,4,5. Se informa que la tasa de supervivencia de los pacientes a 15 años es del 53%, y la tasa de supervivencia de los pacientes a 20 años puede ser tan baja como 21%3,5. Si bien hay nuevas y emocionantes iniciativas de inmunobiología que pueden conducir a nuevos tratamientos y mejores resultados clínicos, todavía no hay un modelo animal pequeño confiable en el que probarlos.
El modelo de rata OLT ha sido ampliamente utilizado en la investigación del trasplante de hígado, incluyendo el rechazo6,7,8,9,10, tolerancia inmune11, trasplante de isquemia-reperfusión12, inmunosupresión13, y lesión del árbol biliar14,15,16,17. Sin embargo, una desventaja del modelo en su forma actual es su alta morbilidad postoperatoria y mortalidad18,19. Este es un serio inconveniente que está en desacuerdo con la operación humana, y compromete la capacidad de extraer conclusiones clínicamente relevantes del modelo20.
Además, una gran proporción de esta morbilidad se puede atribuir a una reconexión de la arteria hepática ausente o imperfecta (HA)18. Aunque es un paso crítico en el trasplante de hígado humano, las dificultades técnicas tienden a comprometer la reconexión de HA en el modelo OLT de rata. Como resultado, la anastomosis del conducto biliar (BD) es tenue y da lugar a altas tasas de fuga de bilis y necrosis de BD21. Más allá de la alta incidencia de complicaciones biliares22, una ausencia de flujo arterial altera la fisiología del injerto hepático post-trasplante23, con hipoxia en el injerto hepático del donante24 y daño hepático observado en lóbulos inflamados19,,25,,26. Rata OLT sin reconexión arterial también tiende a promover la fibrosis27. El protocolo OLT de rata descrito a continuación aborda estos problemas mediante la incorporación de un sencillo paso de reconstrucción de HA con un método OLT de rata publicado previamente28,lo que resulta en la preservación del parénquima hepático y mejores tasas de supervivencia.
El trasplante de hígado tiene tres fases: (1) extracción del injerto hepático del donante, (2) preparación del injerto hepático del donante y (3) reemplazo del hígado receptor por el injerto hepático. El procedimiento consiste en la manipulación de cinco estructuras anatómicas: la vena cava inferior suprahepática (SHVC), la vena porta (PV), la vena cava inferior infrahepática (IHVC), la arteria hepática (HA) y el conducto biliar (BD).
OLT en la rata fue introducido por primera vez por Lee et al. utilizando anastomosis de microsutura de la SHVC, PV e IHVC, y una técnica de extracción para el BD29. Este modelo fue mejorado más tarde mediante el uso de la técnica de dos puños en 197930. Desde entonces, se han propuesto varias técnicas alternativas, la mayoría centradas en la anastomosis venosa y utilizando una técnica de dos puños con algunas modificaciones31. Aunque la anastomosis HA se ha descrito previamente en el modelo OLT de rata utilizando técnicas tales como microsuture, cuff, y mangas intraluminales26,31,32,33,34, estas técnicas a menudo requieren habilidades microquirúrgicas altamente entrenadas, alterando significativamente la fisiología de la rata, y se ven obstaculizadas por trombosis y / o complicaciones biliares27,35.
Además, la elección del procedimiento quirúrgico también puede influir en el tiempo anhepático (tiempo desde la sujeción fotovoltaica hasta la reperfusión del injerto a través del PV reconstituido), lo que es fundamental para el éxito del trasplante de hígado de rata. Específicamente, se observan altas tasas de supervivencia con tiempos anhepáticos de 15-20 min36,y 30 min es el límite superior para el éxito37,,38. Por lo tanto, el objetivo de este método es implementar un modelo OLT de rata quirúrgica menos invasivo y más fácilmente adoptable que sea capaz de reconectar la arteria hepática, promover la perfusión eficiente del hígado trasplantado, mantener el flujo al conducto biliar receptor y preservar la condición fisiológica del receptor.
Aquí se detallan todos los pasos de este protocolo revisado, incluyendo la manipulación del tronco celíaco del hígado del donante, así como el uso de 1) un stent de 1,5 mm para realizar una conexión de manguito extraluminal con el receptor HA adecuado, 2) una sutura en funcionamiento para la reconstrucción SHVC, 3) dos puños de plástico impresos en 3D para reconstrucción fotovoltaica e IHVC39,40, 4) una reconexión de manguito microvascular para el HA18,27,41 y 5) una técnica de stent BD previamente descrita28. También se incluyen dos pasos adicionales: un lavado en frío a través del PV, y un régimen de antibióticos que se basa en los hallazgos anteriores17. Este protocolo OLT optimizado minimiza las complicaciones perioperatorias y la morbilidad y modela más de cerca el procedimiento quirúrgico de operación empleado en el trasplante de hígado humano.
Protocol
Representative Results
Discussion
Los modelos de trasplante de hígado animal pequeño son importantes para entender la inmunidad del trasplante e identificar nuevas estrategias terapéuticas32. El modelo ideal de trasplante de hígado animal pequeño replica todos los pasos del procedimiento humano, incluida la anastomosis arterial. Puede ser difícil interpretar los resultados del modelo OLT de rata, ya que la mayoría de las versiones no incorporan un paso de anastomosis HA, lo que conduce a mayores tasas de complicaciones y morbilidad42. Algunos procedimientos de reconstrucción han utilizado la arteria renal, que requiere la extirpación del riñón27. Este protocolo evita la extracción de órganos, ya que está más allá de lo que ocurre en el procedimiento humano.
Las reconstrucciones arteriales también se pueden realizar manipulando la aorta de rata31. Sin embargo, estos métodos requieren una amplia disección y sujeción de la aorta. Si el tiempo de abrazadera se prolonga, entonces la rata receptora tendrá malos resultados relacionados con la isquemia distal43. En los seres humanos, una técnica quirúrgica LT implica la ligadura y la división de la arteria gastroduodenal receptora (GDA). Sin embargo, las características fisiológicas y anatómicas de los roedores hacen que el trasplante utilizando esta técnica sea más difícil fisiológicamente y puede conducir a complicaciones (es decir, necrosis del páncreas y del conducto biliar35 y fuga44). La reconexión arterial en este protocolo está destinada a eludir este desafío, mantener el flujo sanguíneo del conducto y mejorar el resultado del receptor.
El uso de una técnica de manga y stent para la reconstrucción de la rata HA se ha descrito previamente27. En esta técnica, se utiliza un stent como guía, y la arteria se reconstruye desde el tronco celíaco del donante hasta el receptor de HA común. A continuación, se disecciona el destinatario de HA común y el GDA receptor está atado27. Como resultado, el suministro de sangre a la parte inferior del receptor BD y la cabeza del páncreas puede verse comprometido. Se cree que la circulación colateral a esta área a menudo proporciona un flujo sanguíneo inadecuado al conducto biliar. Por ejemplo, este protocolo prueba-sujeta el destinatario GDA primero con un clip microvascular y, a continuación, divide el destinatario BD. Con el GDA sujetado, el BD dividido no sangra. Después de retirar la abrazadera GDA, se observa un sangrado rápido del BD. Este protocolo, que mantiene un buen flujo al conducto biliar receptor dividido, protege la fisiología del tejido hepático receptor proporcionando una perfusión adecuada de sangre hepática y previniendo la lesión hepática hipoxica post-OLT.
En el lado del donante, el stent HA se inserta en el tronco celíaco durante la preparación del injerto con facilidad mediante la creación de un parche a partir del tronco celíaco, la arteria gástrica izquierda y la arteria esplénica. El stent se puede insertar a través de la abertura ancha, que es menos difícil que tratar de insertar el stent en el tronco celíaco solo. Se ha encontrado que 24 G es un tamaño ideal para usar para el stent HA. La longitud del stent debe ser de 1,0-1,5 mm de largo, ya que actúa como una puerta abierta para permitir que la HA adecuada del receptor se tire fácilmente en la HA común del donante. Con una cuidadosa atención a donde se coloca la sutura de 10-0 etilon, la sangre que fluye a través de esta conexión nunca tocará el stent directamente, y el HA adecuado del receptor lo protegerá desde el interior, reduciendo el riesgo de complicaciones. Es importante destacar que el HA del donante nunca se sujeta para evitar el vasoespasmo. El éxito de la reconstrucción arterial se evalúa dejando abierto el GDA del donante. La anastomosis exitosa produce un buen flujo sanguíneo del donante GDA una vez completada la reconstrucción.
En este protocolo, similar a otros, la reconexión SHVC es el paso más lento y, en última instancia, dicta la duración de la fase anhepática. A medida que aumenta la duración del tiempo anhepático, el riesgo de lesión isquémica y disfunción hepática aumenta45. Otro componente crítico de los modelos de ratas OLT son los tamaños del injerto, los stents y los puños. Si el injerto es demasiado pequeño, el injerto puede torcer o voltear, obstruyendo las conexiones vasculares. El tamaño de los stents y puños puede requerir ajustes según la edad, el sexo, el peso y la tensión de la rata. El tamaño de los puños utilizados aquí fue elegido como se describió anteriormente28,y se utilizó un tamaño de manguito que controlaba para el tamaño de la rata. No hubo signos de angustia o complicaciones (es decir, congestión hepática, edema, ascitis o esplenomegalia) durante el período de seguimiento (hasta la fecha: mediana de 133 días después de la operación, mínimo 115 días después de la operación, máximo 161 días después de la operación). Se justifican otros estudios para determinar el tamaño adecuado de PV e IHVC para varias cepas de ratas que tienen en cuenta tanto la edad como el sexo.
Este protocolo OLT de rata modificado utiliza puños impresos en 3D para el PV y el IHVC, como se describió anteriormente39,40. Los métodos existentes para conectar el PV y el IHVC incluyen una técnica de microsutura32,técnica de manguito46y técnica de férula temporal microsuture47. La técnica del manguito impreso en 3D fue elegida, ya que permite que el tamaño del manguito se estandarice de acuerdo con la tensión de la rata y sea fácil de preparar y usar. Grandes cantidades de puños con las mismas dimensiones se pueden imprimir a la vez. La superficie exterior del manguito tiene dos ranuras para ayudar con la fijación de lazos y evitar resbalones. Una cola también se incorpora en el diseño del manguito para permitir una manipulación más fácil del manguito. En general, se cree que la incorporación de puños impresos en 3D conduce a altas tasas de éxito y reproducibilidad del procedimiento OLT al acortar el tiempo anhepático. Se determina que esta técnica también acorta la curva de aprendizaje quirúrgico.
En conclusión, el protocolo descrito estableció un modelo que es más similar al trasplante de hígado humano mediante la incorporación de un paso de reconexión arterial. Este protocolo se puede adaptar para estudiar muchos aspectos inmunológicos y quirúrgicos del trasplante de hígado y puede servir como modelo para probar nuevas intervenciones terapéuticas relevantes para el trasplante.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Esta investigación fue financiada a través de fondos del programa de trasplantes Multi-Organ en la UHN y el apoyo de la Fundación General de Toronto y toronto Western Foundation.
Materials
| 10-0 Ethilon | Ethicon | 2830G | 10-0 Ethilon Black 1X5" BV100-4 Taper |
| 10mL Syringe | BD | B302995 | Luer-Lok Tip, Sterile, Disposable |
| 1mL Syringe | BD | B309628 | Luer-Lok Tip, Sterile, Disposable |
| 20mL Syringe | BD | B301031 | Luer-Lok Tip, Sterile, Disposable |
| 3D Printed Cuff for IHVC | Custom | ||
| 3D Printed Cuff for PV | Custom | ||
| 3D Printed Holder for IHVC | Custom | ||
| 3D Printed Holder for PV | Custom | ||
| 3mL Syringe | BD | B309657 | Luer-Lok Tip, Sterile, Disposable |
| 4-0 Sofsilk | Coviden | GS-835 | Wx coded braided silk, 30", Suture 1-Needle 26 mm Length 1/2 Circle Taper Point Needle |
| 5-0 Monocryl | Ethicon | Y433H | Undyed Monofilament 1X27" TF |
| 5mL Syringe | BD | B309646 | Luer-Lok Tip, Sterile, Disposable |
| 7-0 Silk | Teleflex Medical | 103-S | Black |
| 8-0 Prolene | Ethicon | 2775G | 8-0 Prolene Blue 1X24" BV130-5 EVP Double Armed |
| Barraquer Micro Needle Holder Without Catch | Aesculap Surgical Instruments | FD231R | Curved 120 mm, 4 3/4″ |
| Barraquer Needle Holder, Extra Fine Jaws 8.0mm, Curved With Out Lock | Rumex International Co. | 8-025T | Small Size, Titanium |
| Barraquer Needle Holder, Fine Jaws 12.0mm, Curved With Out Lock | Rumex International Co. | 8-021T | Small Size, Titanium |
| BD Insyte Autoguard BC 22 GA x 1.00 IN | BD Angiocath / Autoguard | 382523 | 22 G x 1.00" (0.9 mm x 25 mm) Wingless catheter, 37 mL/min |
| BDPrecisionGlide Single-use Needles: Regular Bevel – Regular Wall. | BD | B305106 | PrecisionGlide stainless-steel needles with translucent, color-coded, polypropylene hubs. 22 G |
| BD Precisionglide Syringe Needle 21G | BD | 305167 | Gauge 21, length 1.5 inch, hypodermic needle |
| BD Precisionglide Syringe Needle 30G | BD | 305128 | Gauge 30, length 1 inch, hypodermic needle |
| Betadine Solution by Purdue Products LP | Purdue Products Lp | 67618-150-17 | 10% povidone–iodine topical solution USP |
| Bupivacaine Injection BP 0.5% | SteriMax Inc. | DIN:02443694 | 0.5% (100mg/20mL) |
| Curved Tying Forceps | Duckworth & Kent | 2-501E | 6mm tying platforms, straight shafts, flat handle, length 88mm |
| DC Temperature Controller | FHC Inc. | 40-90-8D | |
| DK Iris Scissors (Curved) | Duckworth & Kent | 1-211B | Blunt tips, cut length 4mm, tip to pivot length 11mm, round handle, length 107mm |
| Ethanol, 200 proof (100%), USP, Decon Labs | Decon Labs, Inc. | 2716 | Dilute to 70% with d2H2O |
| Fine Adjustable Wire Retractor | Fine Science Tools | 17004-05 | Maximum spread: 3.5cm, Depth 5cm |
| Harvard Apparatus Isoflurane Funnel-Fill Vaporizer | Harvard Appartus Limited | 34-1040SV | |
| Heparin LEO(heparin sodium) | LEO Pharma Inc. | DIN:00453811 | 10,000 i.u./10 mL |
| Ice-Pak | Cryopak | FIP88016 | 4.00 in. x 7.00 in., thickness 1.50 inch |
| Isoflurane United States Pharmacopeia (USP) 99.9% | Piramal Healthcare Limited | DIN: 02231929 | 250 mL, Inhalation Anesthetic, NDC 66794-017-25 |
| Khaw Transconjunctival Adjustable Suture Control Forceps | Duckworth & Kent | 2-502N | 5mm highly polished tying platforms, straight shafts, flat handle, length 84mm |
| Lactate Ringer's Injected USP, 1000mL | Baxter Co. | DIN: 00061085 | JB2324 |
| McPherson Tying Forceps | Duckworth & Kent | 2-500E | 6mm tying platforms, straight shafts, flat handle, length 90mm |
| Metzenbaum Scissors – 14.5 cm | Fine Science Tools | 14024-14 | Straight Sharp/Blunt |
| Micro Kitzmiller Clamp | Scanlan | 3003-630 | Jaw length 23mm, Length 11cm |
| Microscope-Leica M525 F20 | Leica Microsystems | No catalog number | |
| Non-woven Gauze Sponges | Fisherbrand | 22-028-556 | |
| Olsen-Hegar with Suture Cutter | Fine Science Tools | 12002-14 | 15 mm cutting edge, 2mm jaw surface – 14cm |
| OptixCare Eye Lube, 25gm | OptixCare | ES-KE8O-69U1 | Formerly Optixcare Surgical Eye Lubricant |
| Piperacillin sodium salt | Sigma-Aldrich | P8396 | Penicillin analog |
| Puritan 3" Standard Cotton Swab w/Wooden Handle | Puritan Medical Products Company LLC | 803-WC | Regular Cotton Tipped Applicator with Wooden Handle |
| Round Handled Needle Holder Straight w/ Lock | Fine Science Tools | 12075-12 | Round handles allow easy fingertip adjustments – 12.5cm |
| Shea Scissors Curved Blunt | Fine Science Tools | 14105-12 | Transplant scissors with light and delicate pattern – 12cm |
| Stainless Steel Micro Serrefines Curved – 4mm | Fine Science Tools | 18055-06 | Jaw length 4mm, Jaw width 0.75mm, Total length 16mm, Jaw pressure 125g |
| Stainless Steel Micro Serrefines Curved – 6mm | Fine Science Tools | 18055-05 | Jaw length 6mm, Jaw width 1mm, Total length 17mm, Jaw pressure 100g |
| Stainless Steel Micro Serrefines Straight – 6mm | Fine Science Tools | 18055-03 | Jaw length 6mm, Jaw width 1mm, Total length 15mm, Jaw pressure 100g |
| Surgical Platform | Custom, magnetic | ||
| SurgiVet Vaporstick Anesthesia Machine | General Anesthetic Services, Inc | V7015 | |
| T/Pump Localized Therapy | Stryker | TP700 Series | |
| Vacuum-Pressure Pump | Barnant Co. | 400-1901 | |
| Vannas Scissors with Microserrations Straight | Fine Science Tools | 15070-08 | Cutting edge: 5mm, Tip diameter: 0.1mm – 8.5cm |
| Vetergesic Buprenorphine | Ceva Animal Health Ltd | NAC No.:12380352 | 0.324 mg/ml buprenorphine hydochloride Solution for Injection for Dogs and Cats |
| Vetroson V-10 Bipolar Electrosurgical Unit | Summit Hill Laboratories | No catalog number |
References
- Asrani, S. K., Devarbhavi, H., Eaton, J., Kamath, P. S. Burden of liver diseases in the world. Journal of Hepatology. 70 (1), 151-171 (2019).
- Dopazo, C., et al. Analysis of adult 20-year survivors after liver transplantation. Hepatology International. 9 (3), 461-470 (2015).
- Schoening, W. N., et al. Twenty-year longitudinal follow-up after orthotopic liver transplantation: a single-center experience of 313 consecutive cases. American Journal of Transplantation. 13 (9), 2384-2394 (2013).
- Pischke, S., et al. Factors associated with long-term survival after liver transplantation: A retrospective cohort study. World Journal of Hepatology. 9 (8), 427-435 (2017).
- Hamdani, S., et al. Delayed and short course of rapamycin prevents organ rejection after allogeneic liver transplantation in rats. World Journal of Gastroenterology. 23 (38), 6962-6972 (2017).
- Endo, K., et al. Pretransplant replacement of donor liver grafts with recipient Kupffer cells attenuates liver graft rejection in rats. Journal of Gastroenterology and Hepatology. 30 (5), 944-951 (2015).
- Zhao, Z., et al. IL-34 Inhibits Acute Rejection of Rat Liver Transplantation by Inducing Kupffer Cell M2 Polarization. Transplantation. 102 (6), e265-e274 (2018).
- Nagakawa, Y., et al. Over-expression of AIF-1 in liver allografts and peripheral blood correlates with acute rejection after transplantation in rats. American Journal of Transplantation. 4 (12), 1949-1957 (2004).
- Gao, L. H., Zeng, L. X., Chen, H. M., Wan, R. H. Cytomegalovirus infection accelerates the process of chronic rejection in rat liver transplantation. Transplantation Proceedings. 45 (6), 2536-2538 (2013).
- Wu, Y., et al. Effects of combined genes of CTLA4Ig and IDO in post-liver transplantation immune tolerance of rats. Annals of Hepatology. 15 (5), 729-737 (2016).
- He, X. S., et al. Influence of warm ischemia injury on hepatic functional status and survival of liver graft in rats. Hepatobiliary and Pancreatic Diseases International. 2 (4), 504-508 (2003).
- Tamura, A., et al. Combination effect of tacrolimus and FTY720 in liver transplantation in rats. Transplantation Proceedings. 31 (7), 2785-2786 (1999).
- Wang, Z., et al. RhGH attenuates ischemia injury of intrahepatic bile ducts relating to liver transplantation. Journal of Surgical Research. 171 (1), 300-310 (2011).
- Jiang, J. W., et al. Chronic bile duct hyperplasia is a chronic graft dysfunction following liver transplantation. World Journal of Gastroenterology. 18 (10), 1038-1047 (2012).
- Tang, Y., et al. S-Adenosylmethionine attenuates bile duct early warm ischemia reperfusion injury after rat liver transplantation. Molecular Immunology. 95, 83-90 (2018).
- Nosaka, T., Bowers, J. L., Cay, O., Clouse, M. E. Biliary complications after orthotopic liver transplantation in rats. Surgery Today. 29 (9), 963-965 (1999).
- Howden, B., Jablonski, P., Grossman, H., Marshall, V. C. The importance of the hepatic artery in rat liver transplantation. Transplantation. 47 (3), 428-431 (1989).
- Post, S., et al. The impact of arterialization on hepatic microcirculation and leukocyte accumulation after liver transplantation in the rat. Transplantation. 54 (5), 789-794 (1992).
- Hori, T., et al. Impact of hepatic arterial reconstruction on orthotopic liver transplantation in the rat. Journal of Investigative Surgery. 25 (4), 242-252 (2012).
- Zhou, S., et al. New method of stent-facilitated arterial reconstruction for orthotopic mouse liver transplantation. Journal of Surgical Research. 187 (1), 297-301 (2014).
- Noack, K., Bronk, S. F., Kato, A., Gores, G. J. The greater vulnerability of bile duct cells to reoxygenation injury than to anoxia. Implications for the pathogenesis of biliary strictures after liver transplantation. Transplantation. 56 (3), 495-500 (1993).
- Imamura, H., Rocheleau, B., Cote, J., Huet, P. M. Long-term consequence of rat orthotopic liver transplantation with and without hepatic arterial reconstruction: a clinical, pathological, and hemodynamic study. Hepatology. 26 (1), 198-205 (1997).
- Reck, T., et al. Impact of arterialization on hepatic oxygen supply, tissue energy phosphates, and outcome after liver transplantation in the rat. Transplantation. 62 (5), 582-587 (1996).
- Zhao, D., Wheatley, A. M. Orthotopic liver transplantation in the rat: comparison of models with and without rearterialization of the graft. European Surgical Research. 25 (5), 294-302 (1993).
- Chaland, P., et al. Orthotopic liver transplantation with hepatic artery anastomoses. Hemodynamics and response to hemorrhage in conscious rats. Transplantation. 49 (4), 675-678 (1990).
- Liu, X., He, C., Huang, T., Gu, J. Development of a New Technique for Reconstruction of Hepatic Artery during Liver Transplantation in Sprague-Dawley Rat. PLoS One. 10 (12), e0145662 (2015).
- Oldani, G., Lacotte, S., Morel, P., Mentha, G., Toso, C. Orthotopic liver transplantation in rats. Journal of Visualized Experiments. (65), (2012).
- Lee, S., Charters, A. C., Chandler, J. G., Orloff, M. J. A technique for orthotopic liver transplantation in the rat. Transplantation. 16 (6), 664-669 (1973).
- Kamada, N., Calne, R. Y. Orthotopic liver transplantation in the rat. Technique using cuff for portal vein anastomosis and biliary drainage. Transplantation. 28 (1), 47-50 (1979).
- Kashfi, A., et al. A review of various techniques of orthotopic liver transplantation in the rat. Transplantation Proceedings. 37 (1), 185-188 (2005).
- Chong, A. S., Alegre, M. L., Miller, M. L., Fairchild, R. L. Lessons and limits of mouse models. Cold Spring Harbor Perspectives in Medicine. 3 (12), a015495 (2013).
- Hasuike, Y., et al. A simple method for orthotopic liver transplantation with arterial reconstruction in rats. Transplantation. 45 (4), 830-832 (1988).
- Hickman, R., Engelbrecht, G. H., Duminy, F. J. A technique for liver transplantation in the rat. Transplantation. 48 (6), 1080 (1989).
- Steffen, R., Ferguson, D. M., Krom, R. A. A new method for orthotopic rat liver transplantation with arterial cuff anastomosis to the recipient common hepatic artery. Transplantation. 48 (1), 166-168 (1989).
- Shi, Y., et al. Magnetic ring anastomosis of suprahepatic vena cava: novel technique for liver transplantation in rat. Transplant International. 28 (1), 89-94 (2015).
- Dippe, B. E., et al. An improved model for rat liver transplantation including arterial reconstruction and simplified microvascular suture techniques. Journal of Investigative Surgery. 5 (4), 361-373 (1992).
- Kobayashi, E., Kamada, N., Goto, S., Miyata, M. Protocol for the technique of orthotopic liver transplantation in the rat. Microsurgery. 14 (8), 541-546 (1993).
- Oldani, G., et al. Efficient nonarterialized mouse liver transplantation using 3-dimensional-printed instruments. Liver Transplation. 22 (12), 1688-1696 (2016).
- Oldani, G., et al. Manufacturing devices and instruments for easier rat liver transplantation. Journal of Visualized Experiments. (75), e50380 (2013).
- Li, J., et al. Modified sleeve anastomosis for reconstruction of the hepatic artery in rat liver transplantation. Microsurgery. 22 (2), 62-68 (2002).
- Li, G. L., et al. High incidence of biliary complications in rat liver transplantation: can we avoid it?. World Journal of Gastroenterology. 17 (26), 3140-3144 (2011).
- Zammert, M., Gelman, S. The pathophysiology of aortic cross-clamping. Best Practice and Research: Clinical Anaesthesiology. 30 (3), 257-269 (2016).
- Gao, W., Lemasters, J. J., Thurman, R. G. Development of a new method for hepatic rearterialization in rat orthotopic liver transplantation. Reduction of liver injury and improvement of surgical outcome by arterialization. Transplantation. 56 (1), 19-24 (1993).
- Ijtsma, A. J., et al. The clinical relevance of the anhepatic phase during liver transplantation. Liver Transplation. 15 (9), 1050-1055 (2009).
- Miyata, M., Fischer, J. H., Fuhs, M., Isselhard, W., Kasai, Y. A simple method for orthotopic liver transplantation in the rat. Cuff technique for three vascular anastomoses. Transplantation. 30 (5), 335-338 (1980).
- Marni, A., Ferrero, M. E. A four-technique comparative study of orthotopic liver transplantation in the rat. American Journal of Surgery. 156 (3 Pt 1), 209-213 (1988).