This content is Free Access.
JoVE Journal
Medicine
Method of Isolated Ex Vivo Lung Perfusion in a Rat Model: Lessons Learned from Developing a Rat EVLP Program
1Department of Biomedical Engineering,Ohio State University Wexner Medical Center, 2Davis Heart & Lung Research Institute,Ohio State University Wexner Medical Center, 3The Collaboration for Organ Perfusion, Protection, Engineering and Regeneration (COPPER) Laboratory,Ohio State University Wexner Medical Center, 4Division of Cardiac Surgery, Department of Surgery,Ohio State University Wexner Medical Center, 5Departments of Pediatrics and Internal Medicine,Ohio State University, 6Advanced Lung Disease Program, Lung and Heart-Lung Transplant Programs,Nationwide Children’s Hospital, 7Division of Transplantation, Department of Surgery,Ohio State University Wexner Medical Center
Chapters
- 00:05Title
- 01:45Ex Vivo Lung Perfusion (EVLP) Setup
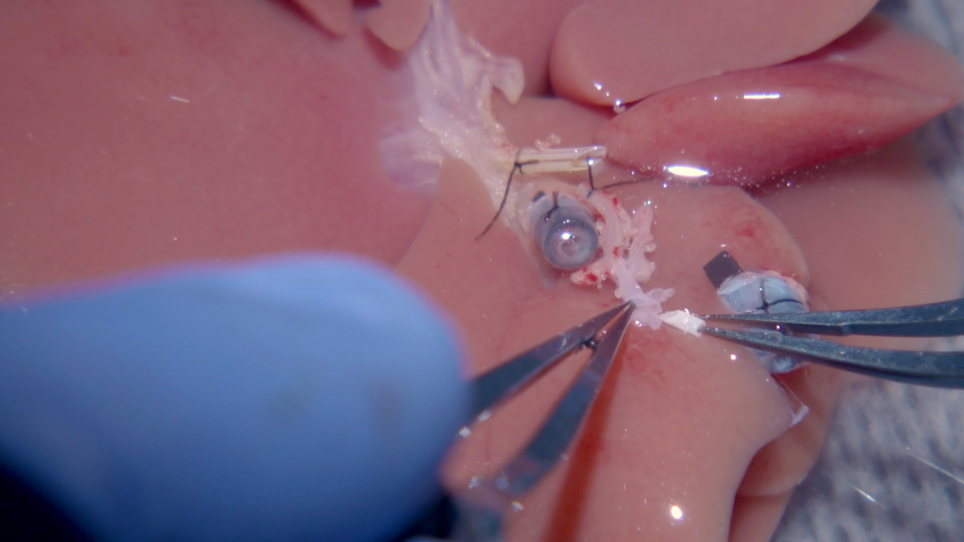
- 02:41Extraction and Initial Ventilation of the Rat Lungs
- 06:11Ex Vivo Perfusion of the Lungs
- 07:51Results: Ex Vivo Lung Perfusion in Rats
- 08:33Conclusion
Ex-Vivo Lung Perfusion (EVLP) has allowed lung transplantation in humans to become more readily available by enabling the ability to assess organs and expand the donor pool. Here, we describe the development of a rat EVLP program and refinements that allow for a reproducible model for future expansion.