Abstract
Yenilenebilir yakıtlar için artan talebi gibi mikroalglerin gibi alternatif feedstocks, fizibilite araştıran araştırmacılar vardır. Kalıtsal avantajlar atık akışları ile potansiyeli yüksek verim olmayan ekilebilir arazi kullanımı ve entegrasyonu yer alıyor. büyük ölçekli mikroalg üretim sisteminin besin gereksinimleri gibi baca gazı ve atık sudan besin karbon dioksit gibi endüstriyel atık kaynakları, yetiştirme sistemleri kaplini gerektirecektir. Bu atıkların mevcut inorganik kirleticiler potansiyel olumsuz verimlilik ve sınırlayıcı uç kullanımını etkileyen mikroalg biyokütle biyolojik birikme yol açabilir. Bu çalışma etkisi deneysel değerlendirilmesi ve Nannochloropsis salina büyüme üzerinde 14 inorganik kirleticiler (As, Cd, Co, Cr, Cu, Hg, Mn, Ni, Pb, Sb, Se, Sn, V ve Zn) kaderi üzerinde duruluyor . Mikroalgler büyüme m pH 7'de 984 ľmol m -2 sn ışıklı fotobiyoreaktörler yetiştirilen -1 ve muhafaza edildiseviyelerde inorganik kirleticiler ile kirlenmiş edia ticari kömür baca gazı sistemlerinde bulunan bileşimine dayalı beklenen. Biyokütle ve 7 gün büyüme dönemi sonunda ortamda bulunan kirleticiler analitik, Hg ve As, Cd, Co, Cr, Cu, Mn, Ni için indüktif eşleşmiş plazma kütle spektrometresi sayesinde soğuk buhar atomik absorpsiyon spektrometresi ile ölçüldü Pb, Sb, Se, Sn, V ve Zn'den en. Sonuçlar N. göstermek salina bu kirleticilerin giriş yieldwith biyokütlesindeki istatistiksel azalma ile çoklu metal çevreye duyarlı bir türdür. Burada sunulan teknikler alg büyümesini miktarının ve inorganik kirleticilerin kaderini belirlemek için yeterli.
Introduction
Geleneksel karasal bitkileri ile karşılaştırıldığında mikroalg doğasında daha yüksek güneş dönüşüm verimliliği 1,2 nedeniyle daha yüksek bir biyokütle ve lipit verimi elde etmek için gösterilmiştir. Yüksek verimlilik oranları microalglerin Yetiştirme harici karbon kaynağı dahil olmak üzere çeşitli besin kaynağı gerektirir. Bu büyük ölçekli büyümesi tesisleri üretim maliyetlerini en aza indirmek için bu tür endüstriyel baca gazı gibi endüstriyel atık akımlarının ile entegre ve aynı zamanda, çevre iyileştirme sağlayabilir olması beklenmektedir. Endüstriyel atık karbon gaz karbondioksit şeklinde tipik ve olumsuz mikroalg üretimi etkileme potansiyeline sahip kirleticiler içerebilir. Spesifik olarak, kömürden türetilmiş baca gazı da dahil olmak üzere kirletici maddelerin çeşitli ancak yanma ürünleri, su ve karbon dioksit gibi sülfür ve nitrojen, ince toz, örneğin dioksin ve furanlar gibi organik kirletici oksitleri ve inorganik con bunlarla sınırlı değildirağır metaller gibi kirleticileri. microalgae verimlilik üzerindeki ağır metaller olarak bilinen bazıları ile inorganiklerin dahil olmak üzere bu kirleticilerin çoğunluğunun etkisi araştırılmış değil. Bu unsurların bazıları, uygun konsantrasyonlarda besin olabilir ancak yüksek konsantrasyonlarda onlar hücre disfonksiyonu ve hatta ölüme 3. üretebilir.
Endüstriyel baca gazıyla mikroalg entegrasyonu doğrudan büyüme ortamı içine inorganik kirletici maddeleri tanıtmak için potansiyele sahiptir. Kömür göre baca gazı, inorganik elementler (örneğin, Cd, Co, Cr, Cu, Hg, Mn, Ni, Pb, Sb, Se, Sn, V ve Zn, As) bazıları, düşük çeşitli konsantrasyonlarda bir çeşitlilik vardır konsantrasyon, mikroalg büyümesi için besin temsil etmektedir. İnorganik kirletici yüksek afiniteli bir mikroalg bağlamak için ve daha fazla besin maddesi taşıyıcıları aracılığıyla dahili emdirilebilecek sahiptir. Bazı inorganik kirletici maddeler (örneğin, Co, Cu, Zn, Mn) içeren enzim parçası besin olanfotosentez, solunum ve diğer fonksiyonlar 3,4 d. Ancak, aşırı metal ve metaloidlerin toksik olabilir. Böyle Pb, Cd, Sn, Sb, Se, As ve Hg gibi diğer unsurlar, herhangi bir konsantrasyonda hücre fonksiyonunu desteklemesi ve olumsuz kültür büyüme 3,5,6 etkileyebilecek olmayan besin metalleri temsil etmek bilinmemektedir. Bu kirletici maddelerin herhangi birinin mevcudiyeti mikroalg hücre fonksiyonu üzerinde olumsuz etkileri üretme potansiyeline sahiptir. Ayrıca, mikroalg ile birden çok metal etkileşimi büyüme dinamiği karmaşık hale getirmekte ve bir büyüme etkisi potansiyeline sahiptir.
Büyük ölçekli ekonomi doğrudan yetiştirme sisteminin 7-19 verimlilik bağlantılı olmuştur. Bu kütlenin 99.9 ve% 99.4'ünü, sırasıyla 20 temsil Dahası, açık kanal havuzlarda (ORP) veya fotobiyoreaktörler biri için mikroalg büyüme sistemi (PBR) orta geri dönüşüm önemlidir. medyada inorganik kirleticilerin varlığı sonuçta m sınırlayabiliricroalgae verimlilik nedeniyle kirletici birikmesi Medyanın geri dönüşüm. Bu çalışma deneysel, (Cd, Co, Cr, Cu, Hg, Mn, Ni, Pb, Sb, Se, Sn, V ve Zn, As) mikroalg yetiştirme sistemlerinin entegrasyonu beklenen konsantrasyonlarda 14 inorganik kirleticilerin etkisini tespit Kömür N. üretkenliğine, baca gazı kaynaklı olan salina airlift PBRs yetişmektedir. Bu çalışmada kullanılan kirletici maddeler yalnızca kömür bazlı baca gazı, ancak belediye atık göre baca gazı, biyolojik katı maddeler bazlı baca gazı, belediye atık su, üretilen suyun, bozulmuş yeraltı suyu ve deniz 21-23 mevcut vermeye gösterilmiştir. Bu çalışmada kullanılan konsantrasyonlar mikroalg büyüme sistemleri ticari PBR sistemleri 20 gösterildiği, bir alım verimle bir kömür bazlı CO2 kaynağı ile entegre takdirde beklenebilecek olana dayanmaktadır. Ağır metaller ve inorganik kirleticilerin konsantrasyonlarının destekleyen detaylı hesaplamalar Napan sunulmuşturve ark., 24 analitik teknikler biyokütle, medya ve ortamda metallerin çoğu dağılımını anlamak için kullanıldı. sunulan yöntemler inorganik kirletici stres ve bitiş kader miktarının altında microalglerin verimlilik potansiyelinin değerlendirilmesini sağladı.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1. Büyüme sistemi

Şekil 1. Mikroalgler büyüme sistemi. (A) Hava rotometre, (B) CO 2 rotometre, solenoid ile (C) pH kontrolörü, (D) data logger, (E)-line hava filtreleri, (F) hava dağılımı başlığı, (G) floresan ışık bankası, (H), pH metre, (I) soğutma sistemi, (J) su banyosu, (K) termokupl teli, (L) hava asansör foto-biyo (M) ısıtıcı, (N) walk-in dumanının davlumbaz, (O) havalandırma, (P) hava teslim kılcal tüp, (Q) hava filtreleri, (R) örnekleme borusu, (S) PBR silikon kapak ve (T)Silikon kapağı pH de. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
- Aşağıdaki microalgae deneysel büyüme sistemi (Şekil 1) oluşturun.
- Cam tüp reaktör çapı 4.5 cm ve silikon kapaklı 1,1 L'lik bir kültür kapasitesi olan yükseklik 80 cm oluşan on iki hava ikmal PBRs elde edin. 10 cm (PBR başına 3) ve uzunluğu 85 cm (PBR başına 1) ve önceden kesilmiş cam kılcal boruları (5 mm'lik dış çapa ve 1 mm iç çap) elde edin.
- -80 ° C derin dondurucuda silikon kapaklarını dondurun. Gliserol ile bir matkap yağlayın ve kapaklar tatbikat havalandırma, numune alma ve gaz iletim kılcal tüpler barındırmak için 3 delik ve 17 mm çapında 1 delik dondurulmuş ise pH probu barındırmak için.
- Pbr altından 2 cm uzayan uzun tüp ile yerine 3 kılcal tüpler yerleştirin. Diğer kılcal tüp içinde bir silikon tüp wi ekleyinarzu edilen bir numune alma noktasına uzanan diğer ucuna bağlı bir kılcal tüp Th. Bir silikon tıpa boyutu 21D ile pH metre deliğini kapatın.
- Su aracılığıyla köpüren ile ortam havasını nemlendirmek ve hava dağıtım başlığına nemlendirilmiş havayı teslim. 0.2 mikron filtre ile gaz Pass ve uzun cam teslim kılcal tüp yoluyla alg süspansiyon teslim.
- Kültür süspansiyon içinde 7.0 ± 0.1 nötr pH değerini muhafaza etmek için, nemlendirilmiş hava akımı içine sıkıştırılmış CO2 sağlayın. Alg kültür pH'ı 7.1 ulaşır ve pH 6.9 de kapandığında manyetik selenoid açan otomatik CO 2 dispanser sistemi (pH kontrolörü) ile CO 2 doğum oranını kontrol edin.
- 984 ľmol m -2 sn -1 açık koşullara zirve benzer bir ortalama aydınlatma sonucu 24 T5 floresan lambalar kullanılarak ışık sağlar.
- M için bir su banyosu içinde PBRs bırakınyaklaşık 25 ° C'lik sabit bir sıcaklıkta AINTAIN. Bir sirkülasyon soğutucu ve otomatik ısıtma sirkülasyon su banyosu ünitesi denetimi kullanarak sistem sıcaklığını kontrol edin.
- Gerçek zamanlı olarak sıcaklık ve pH değeri Monitör ve data logger ile kaydedin.
- Mikroalg büyüme sisteminin tüm bileşenleri düzgün özellikle mikroalg inokulum hasat ya da muhafaza edilemez gibi inorganik kirleticileri hazırlamadan önce, çalıştığından emin olun.
2. Laboratuvar Gereçleri Hazırlanması
- Sabun ve musluk suyu ile hacimsel matara, PBRs, damacanalar ve herhangi kapları, yıkayın. Deiyonize su (DW) ile durulayın.
- Asit inorganik kirletici izlerini ortadan kaldırmak için laboratuar gereçleri yıkayın. Bu iki yoldan biriyle yapılabilir:
- Nefes dumanı, konsantre nitrik asit, bir duman hoo şiddetli yanma ve toksik dumanlar, işi üretebilir Do not: lab eşya O / N% 10 eser metal dereceli nitrik asit (DİKKAT batırınnitril eldiven, gözlük ve laboratuvar önlüğü) ile d.
- % 50 eser metal dereceli nitrik asit içinde 15 dakika boyunca laboratuar gereçleri bekletin.
- DW ile tüm asit kaldırılır emin iyice en az 3 kez laboratuar eşya durulayın. Bu PBRs iyice özellikle örnekleme tüpleri ve kılcal tüpler durulanır önemlidir. Bunun yapılmaması büyüme orta ve olası inhibisyon asitlenmesini üretecek. Tüm asit doğrulamak için durulama suyunun pH test kaldırıldı.
- En az 30 dakika boyunca 120 ° C'de ve standart atmosfer basıncında, onları otoklav ile PBRs, konteyner ve şişeler sterilize edin.
3. N. salina Orta Hazırlık
- Çözelti A'nın Hazırlanması: Kısmi DW ile 1 L'lik bir volumetrik balona doldurmak. Manyetik bir karıştırma çubuğu yerleştirin ve diğer sonra Tablo 1 'de gösterilen bir kimyasal madde ekleyin. Her madde bir sonraki bileşenin eklenmesinden önce çözülür emin olun. Mıknatısı çıkarın ve th doldurmak1 L'lik hacim işaretinin e şişe.
| Bileşen | Eklemek Tutar (g) | Nihai konsantrasyonu (g / l) |
| H 3 BO 3 | 0.900 | 0.900 |
| Na 2 MoO 4 · 2H 2 O | 0.012 | 0.012 |
| MnCl2 · 4H 2 O | 0.300 | 0.300 |
| ZnSO 4 · 7H- 2 O | 0.060 | 0.060 |
| CuSO 4 · 5H 2 O | 0.020 | 0.020 |
Tablo 1:. Çözelti A tarifi Miktarları konsantre çözelti 1 L hazırlanmasında gerekli miktarlardır.
- Vitamin çözeltisinin hazırlanması: Üç ayrı volumetric şişeler steril bir kaba steril 0.2 um şırınga filtre ile Tablo 2'de gösterildiği gibi. vitamin eklemek için, her vitamin çözeltisi ise filtreden. Karanlıkta ° C'de -4 vitamin korumak.
| Vitaminler | Tutar (mg) | Nihai hacmi (mi) | Nihai vitamini konsantrasyonu (mg / L) |
| Biotin | 12.22 | 500 | 24.43 |
| B12 vitamini | 13.50 | 100 | 135.00 |
| Tiamin hidroklorür | 977,63 | 500 | 1,955.27 |
Tablo 2:. Vitamini çözeltisi tarifi Miktarları konsantre Solu hazırlanması için gerekli miktarlardıryon.
- Kısmen DW ile 20 L Otoklavlanabilir kabı dolduracak ve bir manyetik karıştırıcı çubuğu yerleştirin. Bir manyetik karıştırıcı plaka üstüne kabı yerleştirin ve (vitamin hariç) Tablo 3'te gösterilen kimyasal ekleyin birbiri ardına ve her tam eridikten sonra bunları bir ekleme. 20 L. ulaşmak için konteyner doldurunuz
| Bileşen | Tutar ortamına eklemek | Birim |
| NaCl | 350.00 | g |
| CaCI2 · 2H 2 O | 3.00 | g |
| KCI | 9.60 | g |
| Na 2 SiO 3 · 9H 2 O | 1.14 | g |
| MgSO 4 · 7H 2 O | 29.60 | g |
| 20.40 | g | |
| KH 2 PO 4 | 1.36 | g |
| Amonyum ferrik sitrat | 0.10 | g |
| Çözüm A | 20.00 | ml |
| Biotin solüsyonu * | 818,00 | ul |
| Vitamin B12 çözümü * | 296,20 | ul |
| Tiamin hidroklorür çözeltisi * | 521,60 | ul |
| * Soğutmalı otoklava medya ekle |
Tablo 3: N. salina orta tarifi. Miktarları besin açısından zengin bir ortamda 20 L hazırlanmasında gerekli miktarlar vardır.
- 30 120 ° C'de ve atmosfer basıncında dakika süre ile otoklavlama sureti orta sterilize edin. Orta coo edelimRT aşağı l.
- Bir manyetik karıştırıcı plaka üzerinde kap yerleştirin. Adım 3.2 hazırlanan vitamin ekleyin ve iyice orta karışımı sağlar.
4. İnorganik kirleticiler hamur hazırlama
- Kısmen DW ile Tablo 4'te belirtilen hacimsel şişeler dolgu ve listelenen bireysel tuz ekleyin. Gerekli nihai hacme DW ile doldurun ve iyice karıştırın. Bazı unsurları duvarları şişeyi adsorbe olarak bu stokları korumak etmeyin
DİKKAT: tuzlar işlerken Bu protokolde kullanılan çeşitli inorganik kirleticiler, kanserojenik, teratojenik ve mutajenik olan bir yüz maskesi, eldiven ve laboratuvar önlüğü giymek.
| Analit | Tuz kaynağı | Stokta hacmi hazırlamak için (L) | Tuz şişeye ekleyin60; (Mg tuzu) | Analit konsantrasyonu kültüre ilave (mg analit / L) |
| Olarak | NaAsO 2 | 0.1 | 14.8 | 7.74E-02 |
| CD | CDC 2 | 0.5 | 13.5 | 1.50E-02 |
| Co | CoCl2 .6H 2 O | 0.5 | 34.7 | 1.56E-02 |
| Cr | Na 2 Cr 2 O 7 · 2H 2 O | 0.1 | 40.6 | 1.29E-01 |
| Cu | CuCl 2 .2H 2 O | 0.1 | 38.3 | 1.30E-01 |
| Hg | HgCl 2 | 1.0 14.6 | 9.80E-03 | |
| Mn | MnCl2 .4H 2 O | 0.1 | 58.8 | 1.49E-01 |
| Ni | NiCl 2 'nin .6H 2 O | 0.1 | 112.0 | 2.51E-01 |
| Pb | PbCl 2 | 0.5 | 39.9 | 5.41E-02 |
| Sb | Sb 2 O 3 | 0.5 | 26.7 | 4.06E-02 |
| Se | Na 2 SEO 3 | 0.5 | 11.8 | 9.80E-03 |
| Sn | SnCl2 .2H 2 O | 0.5 | 3.9 | 3.76E-03 |
| V | V 2 O 5 | 0.1 | 22.2 | 1.13E-01 |
| Zn | ZnCl2 | 0.1 | 99.9 | 4.36E-01 |
Tablo 4:. 1.1 L PBR ortamına bu konsantre stok 1 ml konsantre inorganik kirletici maddeler hamur hazırlama Eklenen son sütunda gösterilen nihai konsantrasyon üretir.
- Steril 0.2 um şırınga filtresi üzerinden geçirilmesiyle inorganik kirletici stokları sterilize ve steril bir tüp içinde süzülen madde toplanır.
5. N. salina Aşı Üretim
- 500 ml'lik bir Erlenmeyer şişesi, adım 3'te hazırlanan ortam 200 ml ilave edilir ve daha sonra ağar, 3 g ekleyin. 120 ° C 'de 20 dakika süre ile alüminyum folyo ve otoklav ile şişesi örtün. Steril petri kaplarına çözüm dökün ve sertleşene kadar serin olsun. Bu, steril bir başlık ya da en azından kontaminasyon riskini azaltmak için temiz bir ortamda bir alev yakınında tamamlanmalıdır.
- Streak N. steril petri-dis içinde salina hücrelerihes steril tohumlama döngü kullanarak adım 5.1 hazırlanan. Oda sıcaklığında muhafaza T12 ışıkları ile aydınlatılmış bir masanın üzerine petri çanağı kültürleri yerleştirin. Koloniler görünür olana kadar mikroalg büyütelim.
- Aktarım kolonileri besleyici zengin ortam 200 ml aşama 3'te hazırlanan ve ışıklı çalkalama tablası (1000 RPM) üzerine tutmak içeren Erlenmeyer bölmeli şişeler, steril etmek. Orta yeşil olana kadar kültür büyümesine izin.
- 1.1 L steril PBR için mikroalglerin aktarın. Bir sirkülasyon soğutucu ve otomatik ısıtma sirkülasyon su banyosu kumanda ile 23 ° C'de 200 ľmol m -2 sn -1 T8 floresan ışıkları ile aydınlatılmış ve tutulan bir inokulum su banyosunda PBR yerleştirin. Sırasıyla -1 dk dk -1 2.5 L ve 25 cc hava ve CO 2 rotometers ayarlayın.
- Yeni ortamı içeren yeni 1 .1 L PBRs içine büyüme bölünmüş biyokütle bir hafta sonra ve kuru ağırlık biyokütle olan en az 28 gr toplam kadar büyümesine izinOptik yoğunluk yoluyla belirlenebilir iki reaktör arasında elde edilmiştir.
- Kirlenmesini önlemek için steril bir santrifüj şişeleri ve steril teknikler kullanılarak, 10 ° C'de 15 dakika boyunca 2054 x g'de santrifüjleme ile hasat biyokütle aşı. Süpernatant atınız ve gerektiği gibi hücre konsantrasyonunu devam edin.
- Bir kez tüm biyokütle santrifüjlenir, taze, steril ortam 300 ml hücrelerin yeniden askıya.
- DW 3 ml mikroalg kültürünün 0.1 ml seyreltilir ve daha sonra DW 3 ml yeni çözeltinin 0.1 ml seyreltin. Örnek sağlamak iyice karıştırılır. 750 nm'de mikroalg konsantresi optik yoğunluk (OD) ölçün () hemen bir spektrofotometre kullanılarak.
- (1) konsantre biyokütle miktarını belirlemek için denklem kullanın.
Denklem (1) N (g / L -1), total askıda katı madde karşılık arasındaki doğrusal regresyon analiziyle elde edildi: Not Salina (R = 0,9995 2). Denklem 1 spectr için geliştirilmiştirBaşka bir spektrofotometre modeli kullanılarak eğer Malzeme Tablo modeli ophotometer, yeni bir kalibrasyon oluşturur.- Denklem (2) kullanarak (L) mikroalg konsantresi hacmi hesaplamak (L), bir PBR 1.1 L hacminde bir 4 g / L -1 Kültür yoğunluğu elde etmek için gerekli.
- Steril teknik kullanılarak, mikroalg hacmi, 4 g / L-1 bir ilk kültür yoğunluğa ulaşmak için otoklavlanmış PBR adım 5.9 bulundu konsantre ekleyin. 6 PBRs aşılanır kadar 1.1 L. orta PBR doldurun bu adımı yineleyin. Inokulum su banyosunda PBRs yerleştirin.
- PBRs içinde mikroalg 8 gün büyümesine izin ve ardından (yinelenen adımlar 5,6-5,7) tarafından hasat biyokütle. Adımı yineleyin 5.8 başlangıç hesaplamak1 g / L -1 bir başlangıç kültürü yoğunluğu aşı hacmi.
6. Deneysel Reaktörler
- Kullanılarak steril teknikler 12 asit durulanmıştır steril PBRs her bir aşama 3'te hazırlanan ortamın yaklaşık 1 L ilave edin. Deneysel büyüme sisteminin su banyosunda PBRs yerleştirin. -1 Dk 1.5 L üzerinde serpme havayı açın.
- % 70 etanol ile temizleyerek kalibre pH metre sterilize edin. PBR ortamın pH'ı ölçün ve pH yaklaşık 7.0 olduğundan emin olun; değilse, 2 numaralı adımı yineleyin asit durulama aşamasından süzülen asidi uzaklaştırmak için.
- Etanol (% 70) kullanılarak problar dezenfekte etmek ve sonra da kapak PBRs bunları eklemek tamponu, pH 7 ile her bir pH denetleyicisi kalibre edin.
- (Kontrol PBRs hariç) her bir PBR kirleticilerin tamamen PBR karıştırın olsun aşama 4'te hazırlanan steril inorganik kirletici maddeler stoklar her 1 ml. PBRs inorganik kirleticilerin nihai konsantrasyonu göstermek vardırn Tablo 4'te son sütununda ve kömür yakıtlı enerji santrali entegrasyonu tahmin maksimum konsantrasyonları bekleniyor.
- Kontrol PBRs steril DW 14 ml ekleyin.
- 1 g / L -1 başlangıç kültürü yoğunluğunun elde edilmesi için, deneysel PBRs adım 5.11 'de elde edilen konsantre mikroalg inokulum ekleyin. Iyice biyokütle karışımı edelim.
- Yüksek ışık yoğunluğu ışıklar (984 ľmol m -2 sn -1) ve pH kontrolörleri açın ve 30 cc min 1 CO 2 ayarlayın. 50 cc dak CO 2 akışını -1 sonradan 3 gün artması. İlk düşük CO2 akış hızı nedeniyle gaz / sıvı transferi ve pH ölçümü gecikmelere pH büyük değişiklikler önlemek için kritik öneme sahiptir.
- Tedbir ve gerektiği gibi örnekler alabilir. Örnekleme sonra su seviyesini işaretlemek için emin olun. (DİKKAT: pbr bazı inorganik kirleticiler, kanserojenik, teratojenik ve mutajenik olduğu, kullanım eldiven ve capped konteynerler) örnekleri işlerken.
- Buharlaşmaya bağlı kayıpları telafi etmek için PBRs günlük steril DW ekleyin.
- Büyüme 7 gün sonra, 9936 x g santrifüjleme ile hasat biyokütle ve -80 ° C de, her iki, biyokütle ve süpernatan ortamı muhafaza eder.
- 0.1 mbar ve -50 ° CO / N de biyokütle kurumaya dondurun. Toz biyokütle (santrifüj tüp içinde toz biyokütle bir spatula kullanın). -80 ° C'de dondurularak kurutuldu biyokütle korur.
Numunelerin sindirimi Destekli 7. Mikrodalga
biyokütle örneklerinin sindirimi ICP-MS analizi için, bir ön işleme adımında, gereklidir.
Not: Bu adımlar kontrollü basınç rahatlaması ile kapalı bir kap mikrodalga sindirim sistemini kullanın. (DİKKAT: Yüksek basınç, asit sindirim sırasında geliştirmek sindirim gemileri ve kalkan fiziksel bütünlüğünü incelemek ve her kullanımdan önce mikrodalga sindirim damar kapaklarını yeniden şekillendirmek).
- Sabun ve suyla yıkayın Teflon mikrodalga sindirim gemiler, DW ile durulayın ve gemilerin hava kurumaya bırakın. Aşağıdaki adımlarda açıklandığı gibi damarlarda eser metal kontaminasyonu temizlemek için asit sindiremez.
- Mikrodalga sindirim damar kapakları yeniden şekillendirme ve sıkıca şişeleri kapatın.
- Her bir nitrik asit 10 ml ilave edilir.
- Emniyet kalkan gemi tanıtın. Hiçbir biyokütle, su ya da herhangi bir reaktif maddeler güvenli kalkan zarar görmesini önlemek amacıyla emniyet kalkanı duvarlarında ya da sindirim gemilerin dış duvarlarında kalmadığından emin olun. Emniyet valfi flakon bahar aynı hizada emin emniyet kalkanı Cap. Kapak delikleri, dış satırda ve içeri doğru iç satırda dışa bakacak şekilde rotor üzerindeki kalkan bulun.
- Damar bir numaralı günü, seramik termovel ve sıcaklık sensörü takın. Bu termometre şişede gerçek iç sıcaklığı izler ve sindirim progr yürütmek kontrol parametre olarak hizmet vermektedirduyuyorum. Şişe numara bir başka şişeleri aynı numune ve reaktif miktarlarını içerdiğinden emin olun.
- Girdi sindirim parametreleri Tablo 5'te gösterilen ve sindirim başlar. Program tamamlandığında onlar RT ulaşana kadar, hava şişeleri serin.
| Adım | Durulama Şişeler | Örnek sindirim | ||||
| Sıcaklık (° C) | Süre (dk) | Max. gücü (W) | Sıcaklık (° C) | Süre (dk) | Max. gücü (W) | |
| 1 | RT 190 | 25 | 1000 | RT 180 | 15 | 1000 |
| 2 | 190 | 10 | 1000 | 180 | 15 | 1000 |
| - | 20 | - | - | 20 | - |
Tablo 5: mikrodalga sindirim programda kullanılan parametreler.
- Davlumbaz içinde, kapak delikleri ile kalkan kapağındaki basınç tahliye aracı sizden uzağa işaret yerleştirin. (: Biyokütle sindirim asit kullanılarak beri davlumbaz içine her zaman açık sindirilir şişeler toksik dumanlar üreten DİKKAT) Basınç kapağını açık bırakılır kez.
- Asit atınız. DW 3 kez ile Teflon gemileri durulayın. Kuru hava flakon edelim.
- , Biyokütle sindirmek mikrodalga sindirim gemilere dondurularak kurutulmuş biyokütle 50 mg ekleyin. Kalite kontrol (KK) aşağıda şişeleri hazırlanması için: ekleme iki farklı şişelerde ya da seviye 7 ICPMS 5 ml ya da kademeleri 9.1 ve viyalden 10.1 (sindirilmiş olan çözelti içinde hazırlanmış Seviye 7 Hg CVAAS standart 5 mi takviye laboratuvar adlandırılır Boş (LFB)), başka bir şişe boş (sindirilmiş çözüm bırakınBu tüpten Laboratuar reaktifi olarak adlandırılan boş (LRB)).
- , Orta sindirmek 10 mi asidi durulandı mikrodalga sindirim damarları kuru süpernatan ortamı ekleyin. Kalite kontrol (KK) aşağıda şişeleri hazırlanması için: İki farklı şişeler içinde 10 ilave bir şişe adım 9.1 ve 10.1 (LFB adlandırılan bu şişeden sindirilmiş çözelti) hazırlanmıştır Seviye 7 ICPMS ya CVAAS metal standardı, 5 ml ilave DW ml (Bu şişeye sindirilen çözeltisi LRB olarak adlandırılır).
- Mikrodalga sindirim damar kapakları yeniden şekillendirme ve sıkıca şişeleri kapatın.
- Konsantre edilerek eser metal dereceli nitrik asit 7 ml ve her bir şişeye 3 ml hidrojen peroksit ekleyin. Yavaşça çözüm dönen tarafından içeriğini homojenize. (Tablo 5'te örnek sindirim için mikrodalga sindirim parametreleri kullanmak) adımları 7,4-7,7 tekrarlayarak flakon içeriğini Digest.
- Artan iyileşme DW gemiler durulama, 25 ml volümetrik şişeye sindirilen örnek ekleyin. DW ile ölçülü balona doldurunİşaretlemek.
- Transfer şapkalı kap örnekleri sindirmek. Analiz tamamlanana kadar 4 ° C'de örnekleri korur. Bu çalışmada analiz için Hg ve diğer elemanlar için üç gün içinde aynı gün yapılır.
8. Kalite Kontrol (QC) Örnekleri
Not: Deneysel örneklerden sonuçların güvenilirliğini sağlamak amacıyla QC örnekleri analiz edin.
- Kısmen DW ile 1 L hacimsel şişesi durulanır bir asit doldurun. (Bu çözüm de boş bir çözüm olarak adlandırılır) konsantre iz metal dereceli nitrik asit 280 ml ekleyin ve iyice karıştırın (DİKKAT: Her zaman ekzotermik reaksiyon şiddetli olabilir gibi asit su ekleyin, suya asit asla ekleyin). Oda sıcaklığına soğutun çözelti olsun.
- Adım 7.9 ve 7.10 hazırlanan kalite kontrol örnekleri ek olarak aşağıdaki QC örnekleri hazırlanır.
- Devam kalibrasyon doğrulama (CCV) için: bkz hazırlanması için kalibrasyon standardı ile bir polistiren tüp (Filladım 9.2 ve 10.1). CVAAS raf ve ICPMS ICPMS alıcısı içinde standart çözüm üzerinde Hg standart solüsyonu koyun.
- Ve devam eden kalibrasyon boş (CCB) için: Boş (adım 8.1) içinde hazırlanan solüsyon iki polistiren tüpler (16 mi) doldurun. Bir CVAAS rafa örnek ve ICPMS otomatik numune alıcı diğer örnek yerleştirin.
- Laboratuvar güçlendirilmiş matriks (LFM) için: rasgele numune her tür (örneğin, biyokütle veya orta) için her 12 numune 1 örnek seçin ve bir LFM hazırlamak için kullanabilirsiniz. ICPMS, bir polistiren tüp ICPMS standart seviyede 7 ve (biyokütle ya da ortam ya da gelen) ile sindirilmiş deney örneği 3 ml, 0.5 ml ilave ediniz.
- Içeriğini karıştırın ve ICPMS otomatik numune üzerinde şişeleri yerleştirin. CVAAS için bir polistiren tüp 2 ml Hg standart Seviye 7 ve (biyokütle veya orta birinden) sindirilmiş deneysel örnek 6 ml ekleyin. CVAAS rafa içeriği ve yeri şişeleri karıştırın.
- Yinelenen örnekler için: Rastgele şimdiye kadar 1 örnek seçinmatrisin her türü için 12 numune y (örneğin, biyo-kütle, orta LFM veya seyreltilmiş matris) ve flakon çoğaltmak için kullanılır. ICPMS otomatik numune alıcı ve CVAAS rafa tekrar şişeleri yerleştirin.
- Kopya örnekler için: Rasgele matris (örneğin, biyo-kütle, orta, LFM veya seyreltilmiş matris) her bir tipi için, her 12 örneklerinin 1. örnek seçmek ve şişe çoğaltmak için kullanılır. ICPMS otomatik numune alıcı ve CVAAS rafa tekrar şişeleri yerleştirin.
- Çalışmada veri kalite kriterlerini tanımlayın. Bu çalışmada için Eaton, Clesceri, Rice ve Greenberg 25 tarafından kurulan kalite kriterlerini çoğaltmak. QC kurulan parametreler şunlardır: ±% 10 25 ± 70-130% 25 içinde, LFB yüzde kurtarma (% R) (Pb ve Sb, tartışma bakın hariç), LFM yüzde dahilinde CCV için yüzde farkı (% D) kurtarma (% R) 75-125% 25 içinde, ve göreli yüzde farkı (RPD) ±% 20 25 içinde ve sürekli cayöntem raporlama limiti (MRL) 25 yaş altı libration boş (CCB). Adım 9.7 hesaplama denklemleri bakın.
Plazma Kütle Spektrometresi Coupled İndüktif tarafından 9. Kantitasyonu (ICPMS)
- Analiz gününde, polistiren tüpler için yaklaşık 5 mi sindirilmiş numunenin transferi ve ICPMS otomatik numune alıcı koyun. Polistiren tüplere sindirilmiş numune yaklaşık 15 ml ilave edilir ve CVAAS rafa yerleştirin.
- Analiz aynı gün kalibrasyon standartları hazırlamak. Satın alınan ICPMS standart solüsyonu ilave edin ve Tablo 6'da tarif edildiği gibi boş (adım 8.1) içinde hazırlanan solüsyon ile doldurmak asit durulanmıştır volumetrik balonlara (malzeme Tablo l'de standart çözelti açıklamasına bakınız).
| Parametre | Seviye 1 | Seviye 2 | Seviye 3 | Seviye 4 | Seviye 5 | Seviye 6 | Seviye 7 |
| Satın alınan standart eklenecek (ml) | - | - | - | - | - | - | 10.0 |
| Seviye 7 eklenecek (mi) | 0.0 | 1.0 | 2.5 | 5.0 | 20.0 | 25.0 | - |
| Nihai hacim * (ml) | - | 50.0 | 50.0 | 50.0 | 100.0 | 50.0 | 100.0 |
| Nihai konsantrasyon (ug / L), | |||||||
| 75 As | 0.0 | 2.0 | 5.0 | 10.0 | 20.0 | 50.0 | 1000,0 |
| 111 Cd | 0.0 | 1.0 | 2.5 | 5.0 | 10.0 | 25.0 | 50.0 |
| 59 Co | 0.0 | 10.0 | 25.0 | 50.0 | 100.0 | 250.0 | 500.0 |
| 52 Cr | 0.0 | 2.0 | 5.0 | 10.0 | 20.0 | 50.0 | 100.0 |
| 63 Cu | 0.0 | 5.0 | 12.5 | 25.0 | 50.0 | 125.0 | 250.0 |
| 55 Mn | 0.0 | 3,0 | 7.5 | 15.0 | 30.0 | 75.0 | 150.0 |
| 60 Ni | 0.0 | 8 | 20.0 | 40.0 | 80.0 | 200.0 | 400.0 |
| 208 Pb | 0.0 | 1.0 | 2.5 | 5.0 | 10.0 | 25.0 | 50.0 |
| 121 Sb | 0.0 | 12.0 | 30.0 | 60.0 | 120.0 | 300.0 | 600.0 |
| 51 V | 0.0 | 10.0 | 25.0 | 50.0 | 100.0 | 250.0 | 500.0 |
| 66 Zn | 4,0 | 10.0 | 20.0 | 40.0 | 100.0 | 200.0 | |
| * Aşama 8.1 hazırlanan çözeltisi ilave edilerek, bu hacim elde | |||||||
Tablo 6: Kalibrasyon standartlarının Yoğunlaşma 7 Düzeyleri 1..
- ICPMS gelen kozalakları çıkarın ve DW 1 dakika onları sonikasyon. Kozalakları kurutun ve enstrüman onları geri koydu.
- Su soğutucu açın, gazlar (Ar, H 2 O), ICPMS, iç standart fiş hatları ve otomatik numune kapları doldurmak durulama (DW,% 10 nitrik asit,% 1 nitrik asit +% 0.5 hidroklorik asit) .
- Tablo 7 parametrelere ayarlanmış yöntem Masshunter Workstation yazılımını açın ve plazma, melodi ICPMS açmak ve yükleyin.
| Parametreler Değerler | |||||||||
| İç standartlar | 72 Ge, 115, | ||||||||
| Rf güç | 1.500 W | ||||||||
| Plazma gaz akış hızı | 14.98 | ||||||||
| Nebülizatör gaz akış hızı | 1.1 L / dk (taşıyıcı ve seyreltme gaz kombine - 0.6 + 0.5 L / dk) | ||||||||
| Örnekleme konisi | X lens Nikel | ||||||||
| Kevgir koni | Nikel | ||||||||
| Örnek alım oranı | 0.3 rps | ||||||||
| Nebulizatör pompa | 0.1 rps | ||||||||
| S / C sıcaklık | 2 ° C | ||||||||
| Tarama koşulu | Süresi 1 sn, tekrarında 3 sayısını Dwell | ||||||||
| H2 gaz akımı | N / A | ||||||||
| O gaz akışı | 4.3 ml / dak | ||||||||
| Parametre | Seviye 1 | Seviye 2 | Seviye 3 | Seviye 4 | Seviye 5 | Seviye 6 |
| L7 Hg standart eklenecek (ml) | 0 | 1 | 2.5 | 5 | 20 | 25 |
| Nihai hacim * (ml) | - | 50 | 50 | 50 | 100 | 50 |
| Nihai konsantrasyon (ug / L), | 0 | 0.5 | 1.25 | 2.5 | 5 | 12.5 |
| * Aşama 8.1 hazırlanan çözeltisi ilave edilerek, bu hacim elde | ||||||
Tablo 8: Hg kalibrasyon standardının Konsantrasyon 6 Düzeyleri 1..
- Ar gaz ve hava vanasını açın, Atom absorbsiyometri açmakyon Spektrofotometre ve Akış Enjeksiyon Atomik Spektroskopi (FIAS). , CVAAS Winlab yazılımını açın Hg lambasını açmak ve yazılımın enerji parametresi 79. yükleyin Tablo 9'da parametrelerle Hg analizi için bir program erişene kadar ısınmasını bekleyin. Maksimum geçirgenlik vermek için enstrüman ışık yolu ayarlayın.
| Parametreler | Değerler |
| Taşıyıcı gaz | Argon, 100 ml / dakika |
| Lamba | Hg electrodeless deşarj lambası, 185 mA kurulum |
| Dalga boyu | 253.7 nm |
| Yarık | 0.7 nm |
| Hücre sıcaklığı | 100 ° C |
| Numune hacmi | 500 ul |
| Taşıyıcı | % 3 HCI, 9.23 ml / dakika |
| Indirgeyici | % 10 SnCl2, 5.31 ml / dakika |
| Ölçüm | Tepe yükseklik |
| Çoğaltır Oku | 3 |
Tablo 9: CVAAS çalışma koşulları.
- % 3 eser metal dereceli hidroklorik asit yapılmış taşıyıcı çözümüne hattını takın.
- % 3 eser metal derecesi, hidroklorik asit (Hg analizi için uygun olan)% 10 kalay klorür yapılan indirgeyici madde çözeltisine çizgiyi takın. Atmosferik oksidasyona eğilimli olduğu gibi bu çözüme analizinin aynı gün hazırlayın (DİKKAT: Kalay klorür çok tehlikeli olduğunu onunla çalışırken koruyucu aşınma kullanmak tehlikeli muhafaza içinde CVAAS atık toplamak ve düzgün atmayın.).
- CVAAS Winlab yazılımında CVAAS raf ve giriş sırası Hg standartları, QC örnekleri ve deneysel örnekleri yerleştirin. Standartlar çalıştırın ve kalibrasyon denklemini oluşturmak.
- Run QC samPles ve deneysel örnekler. CVAAS aracı haline numunenin yaklaşık olarak 5 ml çizer elemental Hg (Hg 0) gaz numune Hg mevcut azaltır ve kapalı bir sistem içerisinde bir taşıyıcı gaz (Ar) ile çözelti gaz temizler. Hg buharı Hg lamba yolunda bir hücreye geçer. Bir detektör 253.7 nm'de absorbe ışığı belirler ve konsantrasyona ilişkilendirir. (DİKKAT: Hg buharı zehirlidir, enstrüman egzoz kaput yerinde olduğundan emin olun).
- Analizi sırasında adımda 9.7% R,% D ve RPD hesaplayın ve proje veri kalitesi kriterlerine sonuçları karşılaştırın.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
Biyokütle verimleri
N. üretimi salina Bu çalışmada kullanılan PBR sistemi içinde 8.5, 1 g / L-1 ila ± 0.19 g / L-1 (n = 12), kontrol reaktörleri ve 4.0 ± 0.3 g / L-1 (n = 12) büyümüştür Çoklu metal 7 gün içinde kirlenmiş. Deneyler üçlü reaktörler ve çoklu toplu genelinde tekrarlanabilir veriler üretti. Şekil 2A üç bağımsız PBRs numune dayalı çok küçük standart hata ile ortalama kültür yoğunluğunu gösterir. Bu sonuç, izole bir sonuç değildi sağlamak için, üç toplu benzer sonuçlar ile büyütüldü. dört parti için kombine sonuçlar, Şekil 2B'de gösterilmiştir. Biyolojik çeşitlilik var olmasına karşın, bu çalışma N'ye inorganik kirleticilerin tutarlı bir olumsuz etkisi olduğunu göstermektedir salina üretimi. kirletici maruz PBRs biyokütle verimleri gelen kontrol PBRs için istatistiksel olarak anlamlı fark vardıgün 2 itibaren (ANOVA, p <0.05).
İnorganik kirletici nicelikleme Kalite Kontrol değerlendirmesi
Hiçbir kayıpları, hiçbir kazanç ve sindirim (Tablo 10) esnasında analitlerin çapraz kontaminasyon belirten% 100 yakın% R LFB% R tarafından gösterildiği gibi analiz ondört elemanlarının Oniki tam sindirim sonra geri kazanılabilir idi. Numuneler,% D ve RPD kantitatif analiz tüm analiz ve sonuçların ortalamasına ile izlendi sırasında Tablo 10'da gösterilmiştir. Gibi, Cd, Co, Cr, Cu, Hg, Mn, Ni, Pb, Sb, V ve Zn geçti Pb ve Sb için ancak% D% D ve RPD, yavaş yavaş analiz sırasında düştü. Bu elemanlar için% D koni temizlendikten sonra geliştirilir, ancak, sürekli koni temizliği pratik değildir ve bu nedenle Pb ve Sb için veri kalitesi hedefleri düşürülmüştür. Tüm analitler için CCB MRL altında da vardı. Matris etkileri LFM örnekleri analiz ve% R alarak değerlendirildi. While Co, Hg, V ve Sb o QC hedeflerin altında% R sonuçlanan sindirilmiş biyokütle numuneleri analiz edildiğinde As, Cd, Cr, Cu, Mn, Ni, Pb ve Zn geçti değildi, QC veri kriterlerini geçti. 3 (çözünen: çözücü) 1 bir oranında DW Matrix seyreltme veri kalitesi kriterleri geçti% R sonuçlandı. Matris etkileri de sindirilmiş süpernatant analizi sırasında gözlendi ve seyreltme enstrümanın algılama sınırı taviz vermedi emin aynı seyreltme oranı (Tablo 10) tarafından ele alındı. Se ve Sn tespiti ile ilgili sorunlar sırasıyla kararsız okumalar ve kirlilik sorunu dayalı gözlenen bulundu. Se için kararsız okumalar matrisinde 27 tuz atfedilir. Sn kirlenme sindirim aşamasında kullanılan bir asit geri takip edildi.
| Analit | R | CCV | LFB | Biyokütle örnekleri için LFM | Süpernatan örnekleri için LFM | ||||
| % D | % R | Sulandırma oranı | % R | RPD | Sulandırma oranı | % R | RPD | ||
| QC 25 sınırlar | 0,9950 | ± 10 | 70-130 | - | 75-125 | ± 20 | - | 75-125 | ± 20 |
| Olarak | 0,9998 | 1.8 | 101.0 | 1: 3 | 100.4 | 5.2 | 1: 3 | 92.5 | -0.5 |
| CD | 1,0000 | 1.4 | 102.6 | 1: 3 | 103.5 | 4.6 | Hiçbiri | 92.3 | 0.6 |
| Co | 0,9997 | 1.7 | 98,8 | Hiçbiri | 95.2 | -1.4 | Hiçbiri | 96.5 | -1.5 |
| Cr | 0,9999 | 1.5 | 99.8 | 1: 3 | 96.5 | 1.8 | 1: 3 | 90.1 | -0.8 |
| Cu | 0,9999 | 2.9 | 98.2 | 1: 3 | 101.4 | 4.8 | 1: 3 | 94.4 | -0.5 |
| Hg | 0,9983 | -1.7 | 103.0 | Hiçbiri | 98.7 | 1.5 | Hiçbiri | 98.0 | 0.3 |
| Mn | 0,9998 | 2.9 | 97.6 | 1: 3 | 83.2 | 1.8 | 1: 3 | 95.4 | -1.7 |
| Ni | 0,9999 | 103.5 | 1: 3 | 98.5 | 2.1 | Hiçbiri | 93.3 | -0.9 | |
| V | 0,9998 | 2.5 | 97.2 | Hiçbiri | 95.5 | -1.5 | Hiçbiri | 101.2 | -1.9 |
| Pb | 0,9998 | 12.6 | 105.2 | 1: 3 | 88.9 | 0.0 | Hiçbiri | 93.5 | -0.5 |
| Sb | 0,9998 | 1.1 | 105.7 | Hiçbiri | 101.8 | -9,6 | Hiçbiri | 90.8 | -1.2 |
| Zn | 0,9997 | 5.2 | 120.8 | 1: 3 | 90.7 | 1.4 | Hiçbiri | 89.2 | -1.9 |
Tablo 10: kalite kontrol örnekleri sonuçlarının özeti. R = correlation katsayısı,% D: yüzde fark,% R: solvent oranı: yüzde kazanım, RPD = rölatif yüzde fark, seyreltme oranı çözünen anlamına gelmektedir.
İnorganik kirletici konsantrasyonları
Ağır metal ve inorganik kirletici maddeler hem biyokütle ve süpernatan ortamı içinde bulundu. analiz 12 elemanları için biyokütle bulunan konsantrasyonları, Şekil 3'te gösterilmektedir., üçlü PBRs hasat biyokütle konsantrasyonlar (N = 3) 1. çok küçük bir standart hata (Şekil 3A) gösteren toplu. 4 partilerden üç nüsha PBRs verileri birleştirerek tutarlı inorganik kirleticiler biyokütle (N = 12) mevcut olduğunu göstermektedir. Süpernatan bir ortam içinde bulunan konsantrasyonları Şekil 4'te gösterilmektedir. Sonuçlar üçlü PBRs gösterir (n = 3) 1, aynı zamanda, küçük standart hata (Şekil 4A) ve çoğu kirleticiler tercihli olarak biyokütle l bulunan olduğunu göstermektedir toplu için #eading enstrümanın MRL yakın birkaç örnek konsantrasyonları ile süpernatant çok düşük konsantrasyonlar için. Dört partiden alınan sonuçlar Şekil 4B'de sunulmaktadır.
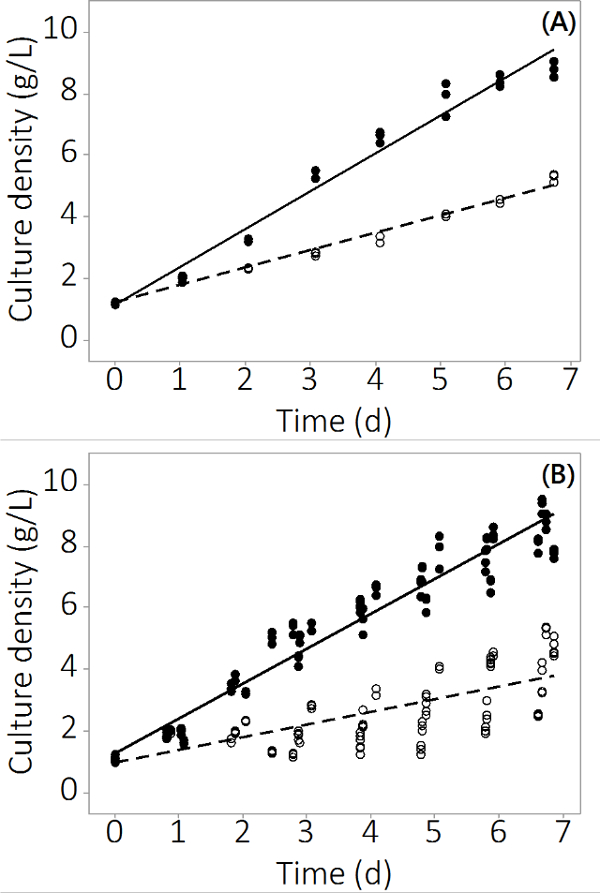
Şekil 2,. Kirlenmiş ve kumanda PBRs ekim süre boyunca Cı ulture konsantrasyonu. Toplu 1. (A) Kültür yoğunluğu, N = 3 PBRs kaynaklanır. 4 toplu olarak (B) 'Kültür yoğunluğu, N sonuçlar 12 PBRs =. Boş çevreler biyokütle kirlenmiş temsil, dolu daireler kontrolü temsil etmektedir.
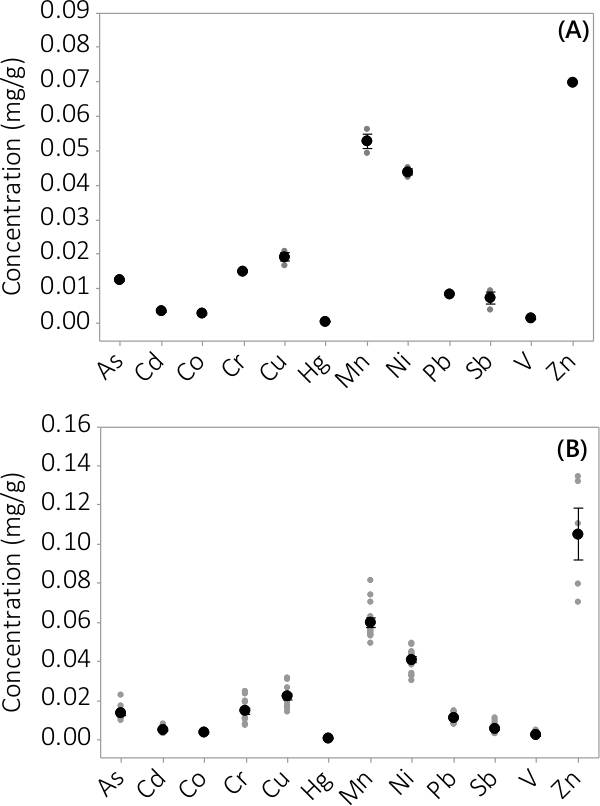
Biyokütle inorganik kirleticilerin Şekil 3. Konsantrasyon. (A) toplu # Yoğunlaşma1, N = 1 PBR Zn ve N = tüm analitler için 3 PBRs için sonuçlar, 4 gruplar (B) konsantrasyonu, N = 4 Zn PBRs ve N = tüm analitler için 12 PBRs kaynaklanır. Ortalama konsantrasyonları, siyah dolu daireler ile temsil edilmektedir, tek tek veri noktaları, gri dolu daireler ile temsil edilmiştir. Hata çubukları ortalamadan ± tek standart hata temsil etmektedir.
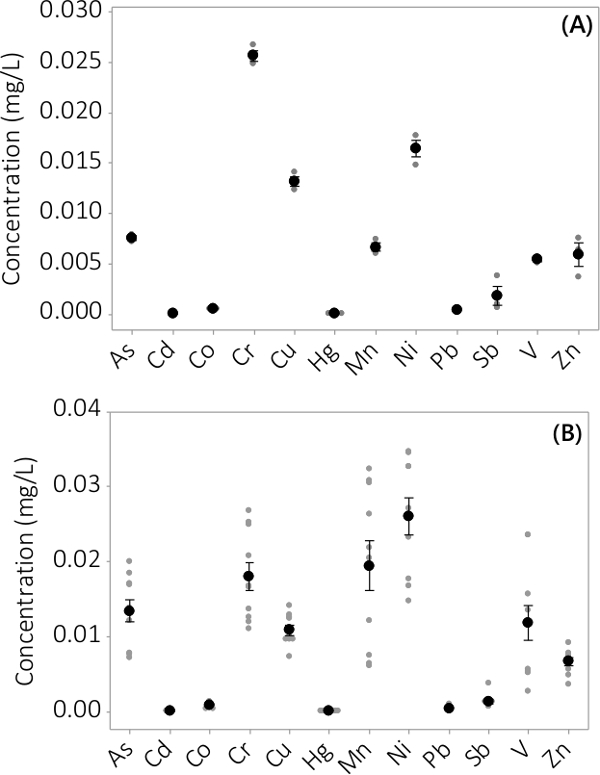
Süpernatan inorganik kirletici Şekil 4. Yoğunlaşma. Toplu 1. (A) konsantrasyonu, N = 3 PBRs, 4 gruplar (B) konsantrasyonu, N = 12 PBRs sonuçları kaynaklanır. Ortalama konsantrasyonları, siyah dolu daireler ile temsil edilmektedir, tek tek veri noktaları, gri dolu daireler ile temsil edilmiştir. Hata çubukları ortalamadan ± tek standart hata temsil etmektedir.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
Tuzlu mikroalg N. salina başarıyla tekrarlanabilir sonuçlar ve yüksek biyokütle verimleri ile tasarlanmış büyüme sisteminde yetiştirilen olabilir. Hava İkmal 7 gün büyüme dönemleri boyunca en az hesaplaşmanın veya biyolojik kirliliğe ile iyi karma askıya kültür için izin karıştırma. Floresan ışık banka genelinde minimum ışık değişkenliği de büyüme fark farklılıkları üretmek değil gösterilmektedir.
Çalışma ağır metal kömür baca gazı olumsuz etkiler biyokütle büyüme ile entegrasyon konsantrasyonları temsilcisi de medya kontamine gösterir. Çalışmada Tekrarlanabilirlik çoklu metal sistemi verimlilik üzerindeki etkisini vurgulamaktadır. Süreç içinde çeşitli adımlar büyümeyi olumsuz etkileyebilir ve çalışkan deneysel hazırlık gerektiren kirletmesine potansiyeline sahiptir. Deneye başlamadan önce, ortamın pH değeri belirlenmesi ortamı asitleştirilir olmadığını doğrulamak (ör resu sağlayan bir QC adımdır) asit iliklerine sonra durulama uygunsuz pbr dan sonuçtaki. Asitleştirilmiş orta besin biyoyararlanımını yosun büyümesini etkileyecek ve değiştirecek (örneğin, inorganik karbon türleşme ve metallerin türleşme değişiklikler) dolayısıyla alg bağlama yerleri, besin ve metaller arasındaki etkileşimleri etkileyen. Bu çalışmalar için laboratuar ekipmanları titiz hazırlanması kişiye metallerin doğru bir kütle dengesi gerçekleştirilebilir şekilde gerekli oldu. Süreçte diğer adımlar doğru dereceli solventler ve kimyasalların kullanımı ihtiyacını vurgulayarak metaller için hesaplanamayan tanıtmak potansiyeline sahiptir. Sürecinde uygun QC etkin bir ağır metal kirleticilerin giriş tanımlayabilirsiniz.
Sonuçlar tanıttı kirleticilerin biyokütle (Şekil 3), medya (Şekil 4) ve çevre arasında dağıtılır göstermektedir. Hasat N. bulunan inorganik kirleticiler salina Bu mikroalg incorporat olacağını düşündürmektedire baca gazında bulunan inorganik kirletici maddelerin çeşitli. Bu özümleme dolayı şarj bağlama yerleri, emme hücresi içinde bağlı metabolik etkinliğe ve orta 28, bu elemanlar ile oluşan komplekslerin çökelmesi hücre duvarlarına adzorpsiyon bir sonucu olabilir. Birkaç gün sonra inorganik kirleticiler ile Görme reaktörler kontrol reaktörlerinin koyu yeşil ile karşılaştırıldığında sarı renkte göründü. Kirlenmiş hasat biyokütle santrifüj hasat sonrası pelet oluşumundan sonra kirletici içermeyen biyokütle görsel farklı değildi. hasattan önce görsel renk farkı daha düşük yoğunluklu biyokütle atfedilen ve mikroalglerin vurguladı. Şekil 4'te gösterildiği gibi, biyokütle uzaklaştırıldı olmayan kirletici maddeler ortam içinde biriken potansiyeline sahiptir. Medyada Birikim ortam dönüştürme ekonomik uygunluk için bir zorunluluk temsil eder ölçeği sınırlamak için bir potansiyeli temsil eder. sınırlama dikte olacağınıtüre özgü olacak ağır metal kirletici maddeleri hoşgörü ile. Bu çalışmanın sonuçları daha iyi atık karbon kaynakları ile mikroalg büyüme sistemlerini entegre üzerindeki potansiyel olumsuz etkilerini anlamak için gereğini, özellikle kömür bazlı baca gazı vurgulayın. Bu çalışmadan elde edilen sonuçlar, poliklorlanmış dibenzo dioksin gibi sülfür ve nitrojen, ince toz ve organik kirletici maddeler oksitleri olarak baca gazı içinde mevcut olması beklenen diğer kirletici maddelerin verimliliği etkilerini anlamak gerekir vurgulamak ve furanlar dibenzo. Önceki ÇAY ve LCA değerlendirmeler gibi ağır metaller ve verimlilik üzerindeki inorganik kirleticiler olarak kirletici etkileri dikkate almadan sorunsuz bir entegrasyon varsaydım. Genel olarak bu çalışmanın sonuçları verimlilik üzerinde bir çok metal sisteminin etkisini vurgulamak ve kirletici biyoremidasyonu için mikroalglerin potansiyellerini anlamak için de kullanılabilir.
yöntem th izin sunduMikroalglerin için tekrarlanabilir sonuçlar inorganik kirleticilerin e çalışması. Bu deneyde kullanılan bazı inorganik kirletici maddeler geleneksel olarak düşük konsantrasyonlarda büyüme sistemleri bulunur, fakat diğerleri hücre içerisinde bilinen bir işlevi yoktur. Bunun bir sonucu olarak konsantrasyonda As, Cd, Co, Cr, Cu, Hg, Mn, Ni, Pb, Sb, Se, Sn, V ve Zn çok eleman karışımı Tablo 4 inhibe büyüme gösterilmektedir. Biyokütle kirletici miktarını miktarının çok metal sistemlerde zor kanıtlayabilirim. Genellikle, organik ve tuzların yüksek içerikli numuneler sonunda hatalı okumalar ve analitik doğruluk 29,30 kaybına yol açar koniler kurmak matris müdahaleler, Poliatomik müdahaleler, fiziksel müdahaleler ve tuz üretebilir. Kalite kontrol numuneleri okumalar doğruluğu ve kesinliğini belirlemeye yardımcı deneysel örnekleri ile birlikte çalışacak. Bu çalışma için geliştirilmiş protokollerin kullanılması ile analit ölçümü, bir olduğu gösterilmiştirÇalışma 25,29 Bu tip için kabul edilebilir bir performans içindedir kabul edilebilir geri kazanımlar üreten ccurate ve hassas. Mikrodalga fırın tarafından numune Sindirim N. için etkili olduğu gösterdi salina olarak sindirilmiş örnekler hücre artıkları veya karışmayan kısımlarının hiçbir varlığı ile netti. Bu deneylerde (alg biyokütlesi ve yapay deniz suyu) kullanılan matris matris seyreltme ile kurtulduk matris müdahaleler üretti. Ancak, bu deneyde kullanılan olanlardan daha yüksek biyokütle örnek boyutları matris girişimlere yol açabilir ve bu nedenle QC her özel senaryo için analiz edilmelidir.
Subscription Required. Please recommend JoVE to your librarian.
Materials
| Name | Company | Catalog Number | Comments |
| Chemicals | |||
| Sodium chloride | Fisher Scientific | S271-3 | |
| Calcium chloride dihydrate | Fisher Scientific | C79-500 | |
| Potassium chloride | Fisher Scientific | P217-500 | |
| Sodium meta silicate nonahydrate | Fisher Scientific | S408-500 | |
| Magnesium sulfate heptahydrate | Fisher Scientific | M63-500 | |
| Potassium nitrate | EMD Chemical | PX1520-5 | |
| Potassium phosphate monobasic | Fisher Scientific | P285-500 | |
| Ammonium ferric citrate | Fisher Scientific | I72-500 | |
| Boric acid | Fisher Scientific | A73-500 | |
| Sodium molybdate, dihydrate | EMD Chemical | SX0650-2 | |
| Manganese chloride tetrahydrate | Fisher Scientific | M87-500 | |
| Zinc sulfate heptahydrate | Fisher Scientific | Z68-500 | |
| Cupric sulfate pentahydrate | Fisher Scientific | C489-500 | |
| Biotin | Acros Organics | 230090010 | |
| Thiamine | Acros Organics | 148990100 | |
| Vitamin B12 | Acros Organics | 405920010 | |
| Copper (II) chloride dihydrate | Sigma-Aldrich | 221783-100G | Irritant, Dangerous to the Environment |
| Lead (II) chloride | Sigma-Aldrich | 268690-250G | Toxic, Dangerous to the Environment |
| Sodium dichromate dihydrate | Sigma-Aldrich | 398063-100G | Oxidizing, Highly Toxic, Dangerous to the Environment |
| Cobalt (II) chloride hexahydrate | Sigma-Aldrich | 255599-100G | Toxic, Dangerous to the Environment |
| Nickel (II) chloride hexahydrate | Sigma-Aldrich | 223387-500G | Toxic, Dangerous to the Environment |
| Sodium (meta) arsenite | Sigma-Aldrich | 71287 | Toxic, Dangerous to the Environment |
| Cadmium chloride | Sigma-Aldrich | 202908-10G | Highly Toxic, Dangerous to the Environment |
| Mercury (II) chloride | Sigma-Aldrich | 215465-100G | Toxic, Dangerous to the Environment |
| Tin (II) chloride dihydrate | Fisher Scientific | T142-500 | Corrosive. Suitable for Hg analysis. Very hazardous. |
| Manganese chloride tetrahydrate | Fisher Scientific | M87-500 | |
| Vanadium (V) oxide | Acros Organics | 206422500 | Dangerous to the Environment |
| Carbon dioxide | Air Liquide | I2301S-1 | Compressed |
| Hydrogen peroxide | H325-500 | Fisher Scientific | 30% in water |
| ICP-MS standard | ICP-MS-6020 | High Purity Standards | |
| Mercury standard | CGHG1-1 | Inorganic Ventures | 1000±6 µg/mL in 5% nitric acid |
| Argon | Air Liquide | Compressed | |
| Helium | Air Liquide | Compressed, ultra high purity | |
| Hydrogen | Air Liquide | Compressed, ultra high purity | |
| Nitric acid | Fisher Scientific | A509-P212 | 67-70% nitric acid, trace metal grade. Caution: manipulate under fume hood. |
| Hydrochloric acid | Fisher Scientific | A508-P212 | 35% hydrochloric acid, trace metal grade. Caution: manipulate under fume hood. |
| Equipment | |||
| Scientific prevacuum sterilizer | Steris | 31626A | SV-120 |
| Centrifuge | Thermo Fisher | 46910 | RC-6 Plus |
| Spectrophotometer | Shimadzu | 1867 | UV-1800 |
| pH controller | Hanna | BL981411 | X4 |
| Rotometer, X5 | Dwyer | RMA-151-SSV | T31Y |
| Rotometer, X5 | Dwyer | RMA-26-SSV | T35Y |
| Water bath circulator | Fisher Scientific | 13-873-45A | |
| Compact chiller | VWR | 13270-120 | |
| Freeze dryer | Labconco | 7752020 | |
| Stir plate | Fisher Scientific | 11-100-49S | |
| pH lab electrode | Phidgets Inc | 3550 | |
| Inductively coupled plasma mass spectrometer | Agilent Technologies | 7700 Series ICP-MS | Attached to autosampler CETAC ASX-520 |
| FIAS 100 | Perkin Elmer Instruments | B0506520 | |
| Atomic absorption spectrometer | Perkin Elmer Instruments | AAnalyst 800 | |
| Cell heater (quartz) | Perkin Elmer Instruments | B3120397 | |
| Microwave | Milestone | Programmable, maximum power 1,200 W | |
| Microwave rotor | Milestone | Rotor with 24-75 ml Teflon vessels for closed-vessel microwave assisted digestion. | |
| Materials | |||
| 0.2 μm syringe filter | Whatman | 6713-0425 | |
| 0.2 μm syringe filter | Whatman | 6713-1650 | |
| 0.45 μm syringe filter | Thermo Fisher | F2500-3 | |
| Polystyrene tubes | Evergreen | 222-2094-050 | 17 x 100 mm w/cap, 16 ml, polysteryne |
| Octogonal magnetic stir bars | Fisher scientific | 14-513-60 | Magnets encased in PTFE fluoropolymer |
References
- Dismukes, G. C., Carrieri, D., Bennette, N., Ananyev, G. M., Posewitz, M. C. Aquatic phototrophs: efficient alternatives to land-based crops for biofuels. Curr Opin Biotechnol. 19 (3), 235-240 (2008).
- Moody, J. W., McGinty, C. M., Quinn, J. C. Global evaluation of biofuel potential from microalgae. Proceedings of the National Academy of Sciences. 111 (23), 8691-8696 (2014).
- Pinto, E., et al. Heavy metal-induced oxidative stress in algae. J Phycol. 39 (6), 1008-1018 (2003).
- Gupta, A., Lutsenko, S. Evolution of copper transporting ATPases in eukaryotic organisms. Curr Genomics. 13 (2), 124-133 (2012).
- Perales-Vela, H. V., Peña-Castro, J. M., Cañizares-Villanueva, R. O. Heavy metal detoxification in eukaryotic microalgae. Chemosphere. 64 (1), 1-10 (2006).
- Sandau, E., Sandau, P., Pulz, O. Heavy metal sorption by microalgae. Acta Biotechnol. 16 (4), 227-235 (1996).
- Amer, L., Adhikari, B., Pellegrino, J. Technoeconomic analysis of five microalgae-to-biofuels processes of varying complexity. Bioresour Technol. 102 (20), 9350-9359 (2011).
- Benemann, J. R., Goebel, R. P., Weissman, J. C., Augenstein, D. C. Microalgae as a source of liquid fuels. Final Technical Report, US Department of Energy, Office of Research. , (1982).
- Benemann, J. R., Oswald, W. J. Report No. DOE/PC/93204--T5 Other: ON: DE97052880; TRN: TRN. Systems and economic analysis of microalgae ponds for conversion of CO2 to biomass. , (1996).
- Chisti, Y. Biodiesel from microalgae. Biotechnol Adv. 25 (3), 294-306 (2007).
- Davis, R., Aden, A., Pienkos, P. T. Techno-economic analysis of autotrophic microalgae for fuel production. Applied Energy. 88 (10), 3524-3531 (2011).
- Jones, S., et al. Process design and economics for the conversion of algal biomass to hydrocarbons: whole algae hydrothermal liquefaction and upgrading. U.S. Department of Energy Bioenergy Technologies Office. , (2014).
- Lundquist, T. J., Woertz, I. C., Quinn, N. W. T., Benemann, J. R. A realistic technology and engineering assessment of algae biofuel production. Energy Biosciences Institute. , Berkeley, CA. (2010).
- Nagarajan, S., Chou, S. K., Cao, S., Wu, C., Zhou, Z. An updated comprehensive techno-economic analysis of algae biodiesel. Bioresour Technol. 145, 150-156 (2011).
- Pienkos, P. T., Darzins, A. The promise and challenges of microalgal-derived biofuels. Biofuels Bioproducts & Biorefining-Biofpr. 3, 431-440 (2009).
- Richardson, J. W., Johnson, M. D., Outlaw, J. L. Economic comparison of open pond raceways to photo bio-reactors for profitable production of algae for transportation fuels in the Southwest. Algal Research. 1 (1), 93-100 (2012).
- Rogers, J. N., et al. A critical analysis of paddlewheel-driven raceway ponds for algal biofuel production at commercial scales. Algal Research. 4, 76-88 (1016).
- Sun, A., et al. Comparative cost analysis of algal oil production for biofuels. Energy. 36 (8), 5169-5179 (2011).
- Thilakaratne, R., Wright, M. M., Brown, R. C. A techno-economic analysis of microalgae remnant catalytic pyrolysis and upgrading to fuels. Fuel. 128, 104-112 (2014).
- Quinn, J. C., et al. Nannochloropsis production metrics in a scalable outdoor photobioreactor for commercial applications. Bioresour Technol. 117, 164-171 (2012).
- Borkenstein, C., Knoblechner, J., Frühwirth, H., Schagerl, M. Cultivation of Chlorella emersonii with flue gas derived from a cement plant. J Appl Phycol. 23 (1), 131-135 (2010).
- Douskova, I., et al. Simultaneous flue gas bioremediation and reduction of microalgal biomass production costs. Appl Microbiol Biotechnol. 82 (1), 179-185 (2009).
- Israel, A., Gavrieli, J., Glazer, A., Friedlander, M. Utilization of flue gas from a power plant for tank cultivation of the red seaweed Gracilaria cornea. Aquaculture. 249 (1-4), 311-316 (2012).
- Napan, K., Teng, L., Quinn, J. C., Wood, B. Impact of Heavy Metals from Flue Gas Integration with Microalgae Production. , Algal Research. (2015).
- Eaton, A. D., Clesceri, L. S., Rice, E. W., Greenberg, A. E. 3125B. Inductively coupled plasma/mass spectrometry (ICP/MS) method. Standard methods for the examination of water and wastewater. , (2005).
- Eaton, A. D., Clesceri, L. S., Rice, E. W., Greenberg, A. E. Standard methods for the examination of water and wastewater. , APHA-AWWA-WEF. (2005).
- Matrix effects in the ICP-MS analysis of selenium in saline water samples. Smith, M., Compton, J. S. Proceedings of the 2004 Water Institute of Southern Africa Biennial Conference, Cape Town, South Africa, , (2004).
- Mehta, S. K., Gaur, J. P. Use of algae for removing heavy metal ions from wastewater: progress and prospects. Crit Rev Biotechnol. 25 (3), 113-152 (2005).
- EPA, U. Method: 200.8: Determination of trace elements in waters and wastes by inductively coupled plasma - mass spectrometry. , (1994).
- Eaton, A. D., Clesceri, L. S., Rice, E. W., Greenberg, A. E. 3120B. Inductively coupled plasma (ICP) method. Standard methods for the examination of water and wastewater. , (2005).
Tags
Çevre Bilimleri Sayı 101 yosun ağır metaller,Get cutting-edge science videos from JoVE sent straight to your inbox every month.









