Snelle Fractionering en isolatie van volbloed componenten in monsters verkregen van een communautair gevestigde instelling
Summary
We outline a methodology for the processing of whole blood to obtain a variety of components for further analysis. We have optimized a streamlined protocol that enables rapid, high-throughput simultaneous processing of whole blood samples in a non-clinical setting.
Abstract
Verzameling en verwerking van hele bloedmonsters in een niet-klinische omgeving biedt een unieke kans om te evalueren thuiswonende mensen met en zonder reeds bestaande voorwaarden. Snelle verwerking van deze monsters is essentieel voor de afbraak van belangrijke cellulaire componenten voorkomen. Hier opgenomen zijn methoden voor het gelijktijdig perifere bloed mononucleaire cellen (PBMC), DNA, RNA en serum isolatie van een enkel bloed trekken uitgevoerd in de huizen van toestemming deelnemers over een grootstedelijk gebied, met verwerking begonnen binnen 2 uur van de collectie. We hebben deze technieken gebruikt worden om meer dan 1.600 bloedmonsters waardoor consistente, hoogwaardige materialen, die vervolgens werd gebruikt in succesvolle DNA-methylatie, genotypering, genexpressie en flowcytometrie analyseert verwerken. Enkele methoden zijn standaard; echter, in combinatie op de beschreven wijze, zij stellen efficiënte verwerking van monsters van deelnemers populatie- en / of community-op basis van studies die normaal niet in een klinische setting worden geëvalueerd. Daarom heeft dit protocol heeft het potentieel om monsters (en vervolgens data) die meer representatief zijn voor de algemene bevolking te verkrijgen.
Introduction
Meerdere studies hebben gekenmerkt verschillen in genexpressie, DNA methylatie en cel subsets in het bloed bij mensen met en zonder mentale (of andere) ziekten 1-4. Deze studies zijn echter verkregen uit klinische omstandigheden waarin ziektegeassocieerde verschillen kunnen worden vergroot als gevolg van het algemeen ernstiger aard van de aandoeningen waarvoor patiënten om behandeling. Als gevolg van de vooruitgang in de 'omics "aanpak, is de afgelopen tien jaar een explosie van belang bij het verkrijgen van biologische monsters van de gemeenschap en / of epidemiologische instellingen 5-7, met het oog op basis van de bevolking schattingen van de prevalentie van de ziekte te bieden en een breder beeld van de waargenomen omgevingsdeterminanten van deze mentale en / of lichamelijke ziekten.
Een belangrijke uitdaging in dit verband is het vereiste van een snelle verwerking van de verzamelde monsters. Degradatie van mononucleaire cellen, belangrijke immuunsysteem componenten die frequentl zijny gebruikte de gezondheid van een individu begint direct na bloedafname met een significante afname van herstel na 2 uur verzameld 8-10 te beoordelen. Om deze uitdaging aan te pakken, presenteren we een geoptimaliseerd protocol waarin meerdere onderdelen van het menselijk bloed gelijktijdig worden geïsoleerd uit monsters verkregen in huizen van de proefpersonen die in een groot stedelijk gebied. Het protocol is gebaseerd op onze samenstelling en modificatie van de huidige technieken, met inbegrip van opslag van "extra" fracties bij toekomstige technieken een verdere isolatie / analyse. Hoewel alternatieve werkwijzen of kits kunnen worden gebruikt in plaats van de afzonderlijke methoden beschreven, die beschreven zijn bewezen als een betrouwbare en efficiënte middelen voor het verwerken van monsters in een high-throughput manier. Hoogwaardige fracties (PBMC's, DNA, serum en RNA) vers bloed kan worden geproduceerd binnen 2 uur verzameld en alle assay ready monsters beschikbaar zijn binnen 2 dagen (figuur 1 kan worden).
Dit protocol werd ontwikkeld om de efficiënte verwerking van monsters van de gemeenschap-woning, volwassen inwoners van de stad Detroit voor het testen in de Detroit Buurt Health Study staat (DNHS; DA022720, RC1MH088283, DA022720-05-S1), een populatie-gebaseerde studie van de sociale en biologische determinanten van post-traumatische stress-stoornis (PTSS) en andere psychische aandoeningen. De prevalentie van PTSS in Detroit is meer dan twee keer het nationale gemiddelde 11,12. Het identificeren van de biologische determinanten van PTSS bij deze populatie kan helpen om passende farmacologische en / of cognitieve gedragstherapie interventies om mensen die lijden aan de aandoening te helpen ontwikkelen, zowel in de stedelijke bevolking, en in de andere een hoog risico populaties (bv terugkerende militaire veteranen). Ons laboratorium, voorheen gevestigd aan de Wayne State University in Detroit, Michigan, werd geselecteerd voor de verwerking op basis van onze expertise in het omgaan met verse weefselmonsters afkomstig van een verscheidenheidvan bronnen, de noodzaak om te beginnen met de verwerking van de monsters binnen 2 uur van de collectie, en onze nabijheid van de collectie sites. Met deze unieke gelegenheid voorhanden, ons doel was om de verwerking grootste opbrengst van DNA, RNA, serum en perifere bloed mononucleaire cellen (PBMC) van elk monster (totaal N = 1639 monsters na 5 golven specimeninzameling) te optimaliseren. De hier geschetste procedures kunnen gelijktijdig worden uitgevoerd in een niet-klinische omgeving, waarbij verkregen uitgangsmateriaal (zie tabel 1 voor de gemiddelde opbrengst) voor een veelvoud van stroomafwaartse toepassingen zoals microarray, epigenetische, real-time RT-PCR, en flowcytometrie analyse.
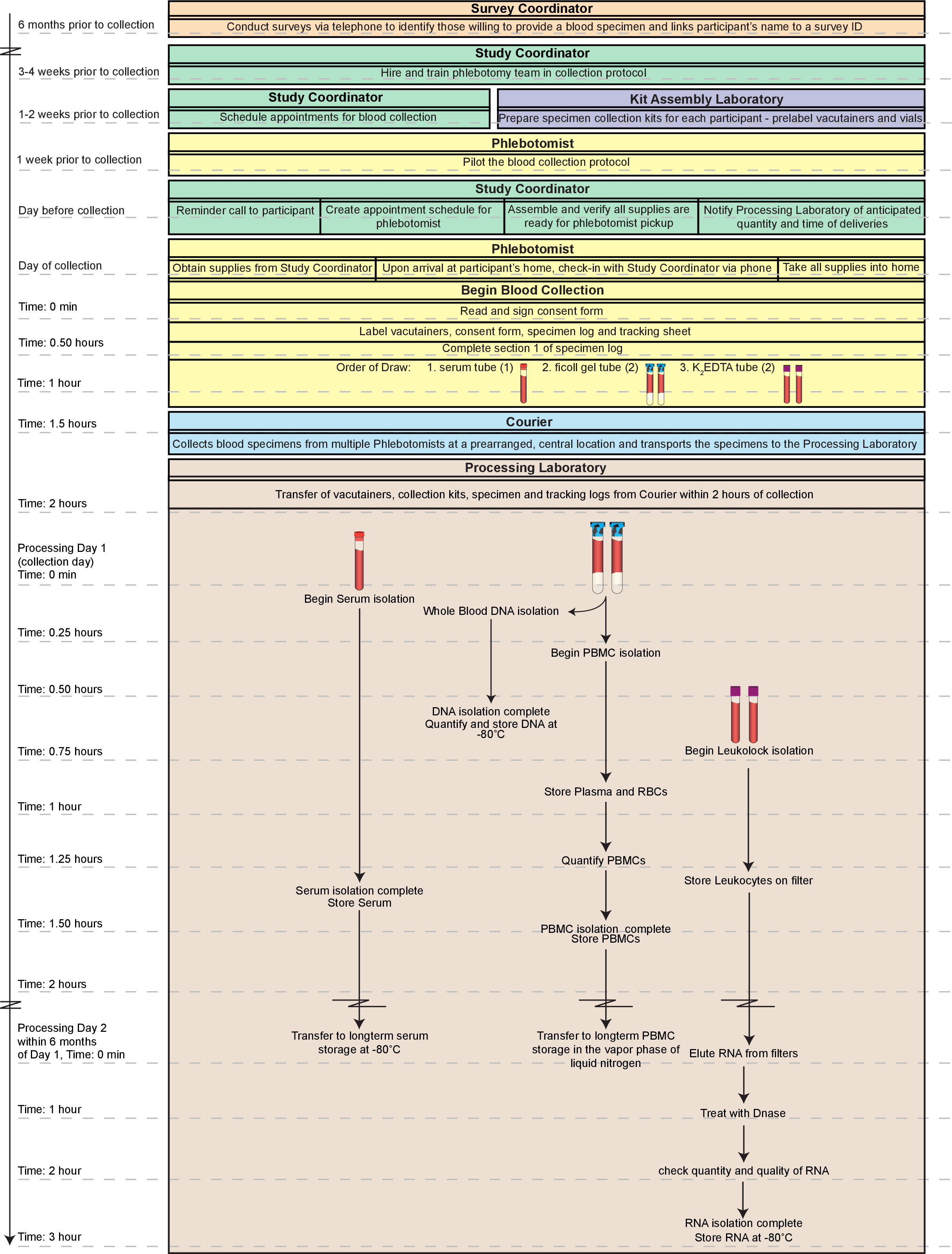
Figuur 1. Algemene workflow. Het totale proces hier afgebeelde omvat de logistiek van het verkrijgen van de bloedmonsters van de identificatie toestemming particmers om het bloed te trekken zelf. Hoge kwaliteit, fracties (perifere mononucleaire bloedcellen, PBMCs, DNA, serum en RNA) van vers volbloed kan worden geproduceerd binnen 2 uur van de collectie en alle test-klaar exemplaren kunnen beschikbaar zijn binnen 2 dagen. Bovendien is het door middel van deze werkwijze bereide fracties geschikt voor langdurige opslag als monsters niet direct worden getest. De gehele tijdslijn hier beschreven kan in één dag (~ 5 uur totaal) worden ingevuld. Toch zou zo'n dag zeer arbeidsintensief vooral voor een enkele technicus een aanzienlijke ervaring met de techniek. Dus, adviseren wij het verdelen van de procedures op dag 1 tussen ten minste twee technici en het invullen van het RNA processing op dag 2. Klik hier om een grotere versie van deze figuur te bekijken.
Protocol
Representative Results
Discussion
We hebben een gestroomlijnde protocol die met succes toegepast voor meer dan 1600 volbloedmonsters verwerken Detroit Wijk Health Study beschreven. Hoewel veel van deze technieken zijn in de literatuur, onze stap voor stap compilatie, waaronder juist getimede wijzigingen tussen elke stap, weerspiegelt een geoptimaliseerd, efficiënt protocol dat succes produceert diverse biologische monsters met uiteenlopende downstreamtoepassingen, waaronder DNA methylatie, mRNA expressie en immunologische analyse. Deze exemplaren zijn …
Disclosures
The authors have nothing to disclose.
Acknowledgements
We would like to thank Henriette Mair-Meijers for invaluable attention to detail and hours devoted to processing the blood collections. We are grateful for the graphic design expertise of Natalie Jameson Kiesling. We also appreciate the approval of the manufacturers (Qiagen (Valencia, CA), BD Biosciences (San Jose, CA), Life Technologies (Grand Island, NY)) mentioned herein to publish the use of their products as described. Funding for this work was generously provided by the National Institutes of Health award numbers DA022720, RC1MH088283, and DA022720-05-S1.
Materials
| QIAamp DNA Blood Mini Kit | Qiagen | 51104 | Day 1: DNA isolation |
| Phosphate-buffered saline (PBS) | Sigma | P5493-1L | Day 1: PBMC isolation |
| 5 ¾” Pasteur pipets | Fisher | 13-678-6A | Day 1: PBMC isolation |
| Fetal Bovine Serum (FBS), heat inactivated | Life Technologies | 10082147 | Day 1: PBMC isolation |
| Dimethyl Sulfoxide (DMSO) | Sigma | D8418-500ml | Day 1: PBMC isolation |
| RPMI Medium 1640, liquid | Invitrogen | 11875119 | Day 1: PBMC isolation |
| 0.4% trypan blue stain | Invitrogen | T10282 | Day 1: PBMC isolation |
| Countess Cell Counting Chamber | Invitrogen | C10283 | Day 1: PBMC isolation |
| Countess Automated Cell Counter or cell counting device such as a microscope and hemocytometer | Invitrogen | C10281 | Day 1: PBMC isolation |
| LeukoLOCK Fractionation & Stabilization Kit | Ambion | 1933 | Day 1: Leukocyte RNA isolation |
| 25G x 5/8 in. needles | Becton Dickinson | 305122 | Day 1: Leukocyte RNA isolation |
| Syringes (5ml) | Becton Dickinson | 309646 | Days 1 and 2: Leukocyte RNA isolation |
| Denaturing Lysis Solution | Ambion | 8540G | Day 2: Leukocyte RNA isolation |
| 5M NaCl | Life Technologies | 24740011 | Day 2: Leukocyte RNA isolation |
| TRI Reagent | Ambion | 9738 | Day 2: Leukocyte RNA isolation |
| Bromo-3-chloro-propane (BCP) | Sigma | B-9673 | Day 2: Leukocyte RNA isolation |
| spin cartridges | Ambion | 10051G | Day 2: Leukocyte RNA isolation |
| 0.1mM EDTA | Ambion | 9912 | Day 2: Leukocyte RNA isolation |
| DNA-free Kit | Ambion | AM1960 | Day 2: DNase treament |
| RNA 6000 Ladder | Agilent | 5067-1529 | Day 2: Bioanalyzer analysis |
| RNA 6000 Nano Series II Kit | Agilent | 5067-1511 | Day 2: Bioanalyzer analysis |
| RNaseZAP | Ambion | AM8782 | Day 2: Bioanalyzer analysis |
| Ethanol >99% | Sigma | E7023-500ml | |
| Isopropanol >99% | Sigma | I9516-500ml | |
| Nuclease-free ultra pure water | Invitrogen | 9938 | |
| Pipette tips (nuclease-free) | Eppendorf | 22491253 | |
| Pipetter (serological) | Eppendorf | 2223020-4 | |
| Pipetters (for volumes under 1ml) | Eppendorf | 3120000-054 | |
| Pipettes (serological) | Fisher | 13-678-27E | |
| Controlled rate freezing containers | Nalgene | 5100-0001 | |
| Cryoboxes (to hold 2ml and 5ml cryovials and 1.5ml microcentrifuge tubes) | Fisher | 03-395-464 | |
| Test tube rack | Thermo Scientific | 14-804-134 | |
| 15ml polypropylene tubes | Fisher | 14-959-49D | |
| 1.5ml and 0.65 microcentrifuge tubes | Fisher | 07-200-534 and 07-200-185 | |
| 2ml and 5ml cryovials | Fisher | 10-500-26 and 10-269-88F | |
| 8ml CPT vacutainer | BD Biosciences | 362761 | 2 tubes |
| 6ml K2 EDTA vacutainer | BD Biosciences | 367863 | 2 tubes |
| 8.5ml SST vacutainer | BD Biosciences | 367988 | 1 tube |
| Vortexer | Fisher | 2215365 | |
| Dry bath incubator with heating block for microcentrifuge tubes | Fisher | 11-715-1250 | |
| Filtration/vacuum system for use within the cell culture hood | Fisher | 01-257-87 | |
| Fixed-angle rotor for microcentrifuge tubes with aerosol-tight lid | Eppendorf | 22637002 | |
| Refrigerated centrifuge with a swing-bucket rotor and aerosol-tight caps for 16 x 125mm vacutainers and 15ml polypropylene tubes | Eppendorf | 22628157 | 2, one does not need to be refrigerated |
| Nanodrop 2000 (recommended for accuracy of small volumes) or other spectrophotometric device | Fisher | 13-400-411 | |
| Agilent Bioanalyzer | Agilent Technologies | G2940CA | |
| Liquid nitrogen tank | Thermo Scientific | 11-676-56 | |
| -80 ˚C freezer | Thermo Scientific | 992RAK | |
| Sharps container | Fisher | 22-037-970 | |
| Biological waste container | Thermo Scientific | 1223P52 | |
| Biosafety Level 2 certified cell culture hood | Thermo Scientific | 13-261-315 |
References
- Hernandez, M. E., Martinez-Fong, D., Perez-Tapia, M., Estrada-Garcia, I., Estrada-Parra, S., Pavon, L. Evaluation of the effect of selective serotonin-reuptake inhibitors on lymphocyte subsets in patients with a major depressive disorder. Eur Neuropsychopharmacol. 20, 88-95 (2010).
- Weigelt, K., et al. TREM-1 and DAP12 expression in monocytes of patients with severe psychiatric disorders EGR3, ATF3 and PU.1 as important transcription factors. Brain Behav Immun. 25, 1162-1169 (2011).
- Robertson, M. J., et al. Lymphocyte subset differences in patients with chronic fatigue syndrome, multiple sclerosis and major depression. Clin Exp Immunol. 141, 326-332 (2005).
- Rotter, A., Asemann, R., Decker, A., Kornhuber, J., Biermann, T. Orexin expression and promoter-methylation in peripheral blood of patients suffering from major depressive disorder. J Affect Disord. 131, 186-192 (2011).
- Klengel, T., et al. Allele-specific FKBP5 DNA demethylation mediates gene-childhood trauma interactions. Nat Neurosci. 16, 33-41 (2013).
- Segman, R. H., Shefi, N., Goltser-Dubner, T., Friedman, N., Kaminski, N., Shalev, A. Y. Peripheral blood mononuclear cell gene expression profiles identify emergent post-traumatic stress disorder among trauma survivors. Mol Psychiatry. 10, 500-513 (2005).
- Smith, B. H., et al. Cohort Profile: Generation Scotland: Scottish Family Health Study (GS:SFHS). The study, its participants and their potential for genetic research on health and illness. Int J Epidemiol. 42, 689-700 (2013).
- Mallone, R., et al. Isolation and preservation of peripheral blood mononuclear cells for analysis of islet antigen-reactive T cell responses: position statement of the T-Cell Workshop Committee of the Immunology of Diabetes Society. Clin Exp Immunol. 163, 33-49 (2011).
- Duvigneau, J. C., Hartl, R. T., Teinfalt, M., Gemeiner, M. Delay in processing porcine whole blood affects cytokine expression. J Immunol Methods. 272, 11-21 (2003).
- Debey, S., et al. Comparison of different isolation techniques prior gene expression profiling of blood derived cells: impact on physiological responses, on overall expression and the role of different cell types. Pharmacogenomics J. 4, 193-207 (2004).
- Uddin, M., et al. Epigenetic and immune function profiles associated with posttraumatic stress disorder. Proc Natl Acad Sci U S A. 107, 9470-9475 (2010).
- Kessler, R. C., Wang, P. S. The descriptive epidemiology of commonly occurring mental disorders in the United States. Annu Rev Public Health. 29, 115-129 (2008).
- . QIAamp® DNA Mini and Blood Mini Handbook Available from: https://www.qiagen.com/us/resources/resourcedetail?id=67893a91-946f-49b5-8033-394fa5d752ea (2010)
- Koenen, K. C., et al. SLC6A4 methylation modifies the effect of the number of traumatic events on risk for posttraumatic stress disorder. Depress Anxiety. 28, 639-647 (2011).
- Walsh, K., Uddin, M., Soliven, R., Wildman, D. E., Bradley, B. Associations between the SS variant of 5-HTTLPR and PTSD among adults with histories of childhood emotional abuse: Results from two African American independent samples. J Affect Disord. 161, 91-96 (2014).
- Bustamante, A. C., et al. Childhood maltreatment is associated with epigenetic differences in hypothalamic-pituitary-adrenal (HPA) axis genes in the Detroit Neighborhood Health Study. , (2013).
- Sipahi, L., et al. Longitudinal epigenetic variation of DNA methyltransferase genes is associated with vulnerability to post-traumatic stress disorder. Psychol Med. 44, 3165-3179 (2014).
- Uddin, M., Koenen, K. C., Aiello, A. E., Wildman, D., de los Santos, R., Galea, S. Epigenetic and inflammatory marker profiles associated with depression in a community-based epidemiologic sample. Psychol Med. 41, 997-1007 (2011).
- Uddin, M., et al. Post-traumatic stress disorder is associated with immunosenescent T cell phenotypes in the Detroit Neighborhood Health Study. , (2011).
- Uddin, M., et al. Post-traumatic stress disorder is associated with immunosenescent T cell phenotypes in the Detroit Neighborhood Health Study. , (2011).
- Uddin, M. Biological signatures of post-traumatic stress disorder in the Detroit Neighborhood Health Study. , (2010).
- Aiello, A. E. Cytomegalovirus antibodies as a marker of immunosenescence in the Detroit Neighborhood Health Study. , (2010).
- Bustamante, A. C., et al. . Distinct gene expression profiles characterize lifetime PTSD and childhood maltreatment in the Detroit Neighborhood Health Study. , (2013).

