Topluluk tabanlı Ayar Elde Edilen Örneklerin hızlı Fraksiyonlama ve Tam Kan Bileşenlerinin İzolasyonu
Summary
We outline a methodology for the processing of whole blood to obtain a variety of components for further analysis. We have optimized a streamlined protocol that enables rapid, high-throughput simultaneous processing of whole blood samples in a non-clinical setting.
Abstract
Olmayan bir klinik ortamda toplanması ve tam kan örneklerinin işlenmesi ve önceden var olan koşullar olmaksızın, hem toplum içinde yaşayan bireylerin değerlendirmek için eşsiz bir fırsat sunuyor. Bu örneklerin hızlı işlenmesi önemli hücresel bileşenlerin bozulmasını önlemek için önemlidir. Eş zamanlı periferik kan mononükleer hücre (PBMC), DNA yöntemleri burada Dahil, RNA ve işleme ile bir metropol boyunca katılımcılara rıza evlerinde yapılan tek bir kan beraberlik serum izolasyonu, toplama 2 saat içinde başlamıştır. Biz 1600 üzerinde kan örnekleri sonradan başarılı DNA metilasyonu, genotipleme, gen ifadesinde kullanılan ve akış sitometri analizleri olmuştur verimli tutarlı, yüksek kaliteli malzeme, işlemek için bu teknikleri kullandık. Kullanılan yöntemlerden bazıları standart; tarif edildiği şekilde bir araya getirildiğinde, ancak, bunlar popülasyon ve / veya Topluma katılımcı örnekler etkili olarak işlenmesini sağlarNormalde bir klinik ortamda değerlendirilecek olmaz dayalı çalışmalar. Bu nedenle, bu protokol, genel nüfusun temsilcisi (ve buna bağlı veriler) örnekleri elde etmek için bir potansiyele sahiptir.
Introduction
Birden fazla çalışmalar ve zihinsel (veya diğer) 1-4 Hastalıkları olmadan bireyler arasında kanda gen ifadesinin, DNA metilasyonu ve hücre alt kümesi farklılıkları nitelendirmiştir. Ancak bu çalışmalar, hastalıkla ilişkili farklar, hastaların tedaviye arayan olan hastalıkların genellikle daha ağır olmaları büyütülür olabilecek olan klinik elde edilmiştir. Nedeniyle "omik" yaklaşımlara gelişmeler, geçmiş on hastalık prevalansının toplum tabanlı tahminleri sağlamak amacıyla, topluluk ve / veya epidemiyolojik ayarlarından 5-7 den biyolojik numune alma ilgi bir patlama ve daha geniş bir resim gördü Bu zihinsel ve / veya bedensel hastalıkların çevresel belirleyicileri.
Bu bağlamda önemli bir zorluk toplanan numunelerin hızlı işlem için bir gerekliliktir. Tek-çekirdekli hücreleri, frequentl anahtar bağışıklık sistemi bileşenlerinin Parçalanmay, bir bireyin sağlık, toplama 8-10 2 saat sonra geri kazanım önemli bir azalma ile birlikte kan alımı üzerine hemen başlar değerlendirmek için kullanılan. Bu zorluğu gidermek için, insan tam kan birden fazla bileşen aynı anda büyük bir metropol bölgesinde yaşayan deneklerin evlerine elde edilen örneklerden izole edildiği optimize edilmiş bir protokol mevcut. Protokolü derlenmesi ve gelecek teknikler daha izolasyonu için izin halinde tüm "ekstra" fraksiyonların depolama dahil olmak üzere güncel teknikler, modifikasyonu üzerine kuruludur / analiz eder. Alternatif yöntemler veya kitleri burada açıklanan bireysel yöntemlerle, bu ana hatları yerine kullanılabilir ise bir yüksek verimli bir şekilde numune işleme için güvenilir ve etkili bir yol olduğu kanıtlanmıştır. Yüksek kaliteli parçalar (PBMC, DNA serumu ve RNA) taze kan, 2 gün (Şekil 1 içinde mevcut olabilir 2 toplama saat ve deney için hazır numuneler içinde üretilebilir).
Bu protokol toplum konut, Detroit Mahalle Sağlık Çalışmasında test için Detroit kentinin yetişkin sakinleri alınan örneklerin verimli işlenmesini sağlamak için geliştirilmiştir (DNHS; DA022720, RC1MH088283, DA022720-05-S1), bir toplum tabanlı post-travmatik stres bozukluğu (TSSB) ve diğer ruhsal hastalıkların sosyal ve biyolojik belirleyicileri çalışma. Detroit TSSB yaygınlığı iki ulusal ortalamanın 11,12 daha fazladır. Bu popülasyonda TSSB biyolojik belirleyicileri belirlenmesi, bu kentsel nüfus ve diğer yüksek risk gruplarında (örneğin, askeri gazileri dönen), hem bozukluktan muzdarip olanlar yardım etmek uygun farmakolojik ve / veya bilişsel-davranışçı müdahaleler geliştirmek için yardımcı olabilir. Daha önce Detroit, Michigan Wayne State Üniversitesi'nde bulunan Laboratuvarımız, çeşitli türetilen taze doku örnekleri ele bizim uzmanlık dayalı işlenmesine için seçildikaynakların, gerekliliği toplama 2 saat içinde numune işleme başlamak için, ve tahsilat sitelere bizim yakınlık. Ancak bu eşsiz fırsat, hedefimiz her örnekten DNA, RNA, serum ve periferik kan mononükleer hücreleri (PBMC'ler) büyük verim (örnek toplama 5 dalgaların üzerinde N = 1639 numunelerin toplam) için işleme optimize etmek oldu. Burada özetlenen işlemler dolayısıyla mikrodizide epigenetik, gerçek zamanlı RT-PCR dahil aşağı uygulamaların çok sayıda için malzeme (ortalama verim için bakınız Tablo 1) başlangıç üreten bir klinik olmayan bir ortamda eş zamanlı olarak gerçekleştirilen ve analizler akım sitometri edilebilir.
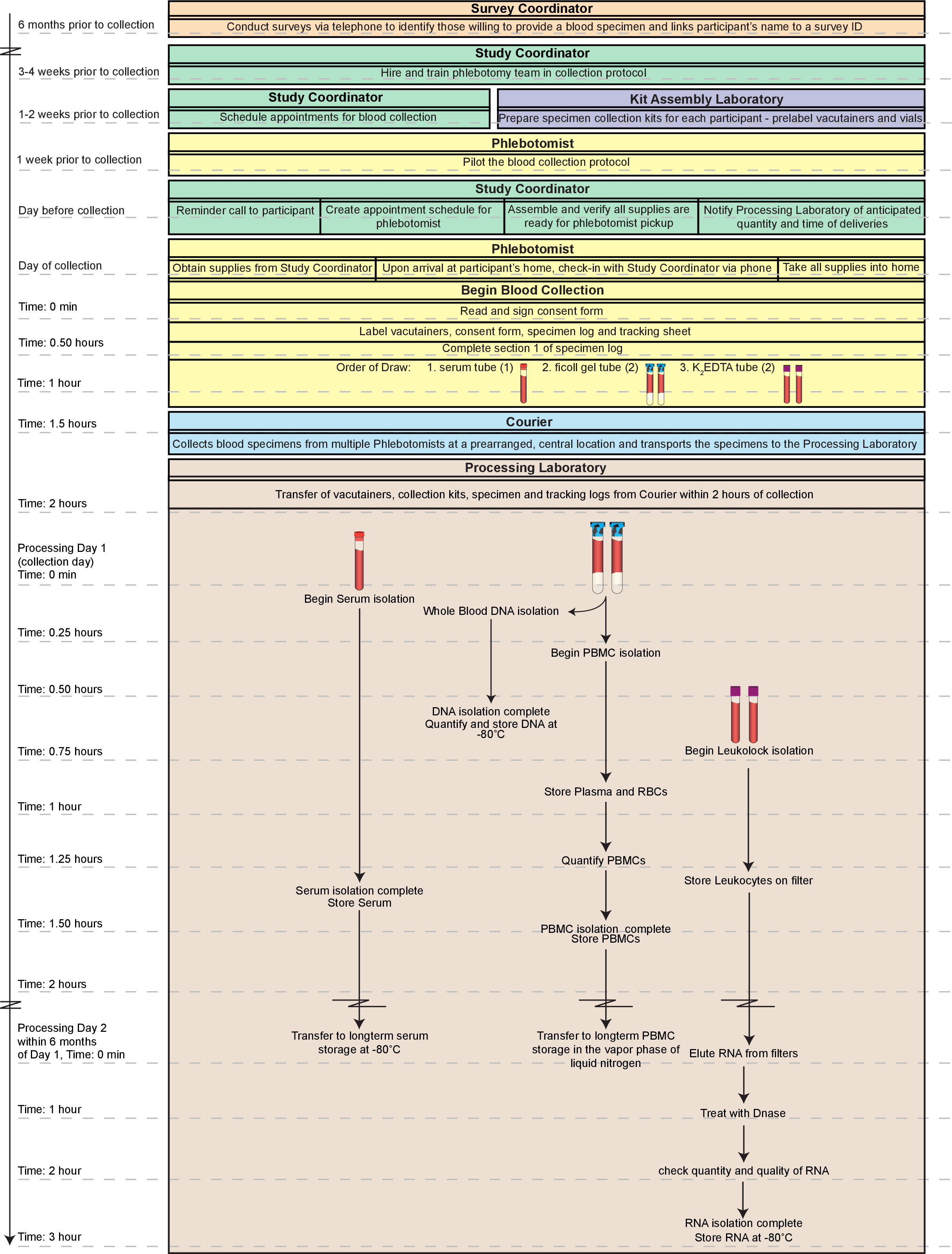
Şekil 1. Genel iş akışı. Burada gösterilen genel işlem rıza partic belirlenmesi kan örnekleri elde lojistik içerirkan ipants kendisini çizin. Yüksek kaliteli, fraksiyonlar (periferal kan tek-çekirdekli hücreleri PBMC DNA, serum, ve RNA), taze tam kan toplama 2 saat içinde üretilebilir ve deney için hazır numuneleri 2 gün içinde mevcut olabilir. Örnekler hemen test edilmesi değildir Dahası, bu metod ile hazırlanan fraksiyonlar, uzun süreli depolama için uygundurlar. Burada özetlenen tüm zaman çizelgesi tek bir gün (~ 5 saat toplam) tamamlanmış olabilir. Bununla birlikte, böyle bir gün, özellikle teknikleriyle büyük deneyim ile tek bir teknisyen için son derece emek-yoğun olacaktır. Böylece, en az iki teknisyen arasındaki Gün 1 prosedürleri bölünmesi ve Gün 2. RNA işleme tamamlayarak tavsiye bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
Protocol
Representative Results
Discussion
Biz başarıyla Detroit Mahalle Health Study 1.600'den fazla tam kan örnekleri işlemek için uygulanmış bir aerodinamik protokol tanımlanmıştır. Bu tekniklerin birçok mevcut literatürde mevcut olmasına rağmen, her adım arasında tam zamanlı değişiklikler dahil olmak üzere adım adım derleme başarıyla aşağı geniş bir uygulama yelpazesi ile biyolojik örneklerin çeşitli üretir optimize edilmiş, verimli protokol yansıtır, DNA metilasyonu, mRNA ifade ve immünolojik analizi dahil. Bu örnek…
Disclosures
The authors have nothing to disclose.
Acknowledgements
We would like to thank Henriette Mair-Meijers for invaluable attention to detail and hours devoted to processing the blood collections. We are grateful for the graphic design expertise of Natalie Jameson Kiesling. We also appreciate the approval of the manufacturers (Qiagen (Valencia, CA), BD Biosciences (San Jose, CA), Life Technologies (Grand Island, NY)) mentioned herein to publish the use of their products as described. Funding for this work was generously provided by the National Institutes of Health award numbers DA022720, RC1MH088283, and DA022720-05-S1.
Materials
| QIAamp DNA Blood Mini Kit | Qiagen | 51104 | Day 1: DNA isolation |
| Phosphate-buffered saline (PBS) | Sigma | P5493-1L | Day 1: PBMC isolation |
| 5 ¾” Pasteur pipets | Fisher | 13-678-6A | Day 1: PBMC isolation |
| Fetal Bovine Serum (FBS), heat inactivated | Life Technologies | 10082147 | Day 1: PBMC isolation |
| Dimethyl Sulfoxide (DMSO) | Sigma | D8418-500ml | Day 1: PBMC isolation |
| RPMI Medium 1640, liquid | Invitrogen | 11875119 | Day 1: PBMC isolation |
| 0.4% trypan blue stain | Invitrogen | T10282 | Day 1: PBMC isolation |
| Countess Cell Counting Chamber | Invitrogen | C10283 | Day 1: PBMC isolation |
| Countess Automated Cell Counter or cell counting device such as a microscope and hemocytometer | Invitrogen | C10281 | Day 1: PBMC isolation |
| LeukoLOCK Fractionation & Stabilization Kit | Ambion | 1933 | Day 1: Leukocyte RNA isolation |
| 25G x 5/8 in. needles | Becton Dickinson | 305122 | Day 1: Leukocyte RNA isolation |
| Syringes (5ml) | Becton Dickinson | 309646 | Days 1 and 2: Leukocyte RNA isolation |
| Denaturing Lysis Solution | Ambion | 8540G | Day 2: Leukocyte RNA isolation |
| 5M NaCl | Life Technologies | 24740011 | Day 2: Leukocyte RNA isolation |
| TRI Reagent | Ambion | 9738 | Day 2: Leukocyte RNA isolation |
| Bromo-3-chloro-propane (BCP) | Sigma | B-9673 | Day 2: Leukocyte RNA isolation |
| spin cartridges | Ambion | 10051G | Day 2: Leukocyte RNA isolation |
| 0.1mM EDTA | Ambion | 9912 | Day 2: Leukocyte RNA isolation |
| DNA-free Kit | Ambion | AM1960 | Day 2: DNase treament |
| RNA 6000 Ladder | Agilent | 5067-1529 | Day 2: Bioanalyzer analysis |
| RNA 6000 Nano Series II Kit | Agilent | 5067-1511 | Day 2: Bioanalyzer analysis |
| RNaseZAP | Ambion | AM8782 | Day 2: Bioanalyzer analysis |
| Ethanol >99% | Sigma | E7023-500ml | |
| Isopropanol >99% | Sigma | I9516-500ml | |
| Nuclease-free ultra pure water | Invitrogen | 9938 | |
| Pipette tips (nuclease-free) | Eppendorf | 22491253 | |
| Pipetter (serological) | Eppendorf | 2223020-4 | |
| Pipetters (for volumes under 1ml) | Eppendorf | 3120000-054 | |
| Pipettes (serological) | Fisher | 13-678-27E | |
| Controlled rate freezing containers | Nalgene | 5100-0001 | |
| Cryoboxes (to hold 2ml and 5ml cryovials and 1.5ml microcentrifuge tubes) | Fisher | 03-395-464 | |
| Test tube rack | Thermo Scientific | 14-804-134 | |
| 15ml polypropylene tubes | Fisher | 14-959-49D | |
| 1.5ml and 0.65 microcentrifuge tubes | Fisher | 07-200-534 and 07-200-185 | |
| 2ml and 5ml cryovials | Fisher | 10-500-26 and 10-269-88F | |
| 8ml CPT vacutainer | BD Biosciences | 362761 | 2 tubes |
| 6ml K2 EDTA vacutainer | BD Biosciences | 367863 | 2 tubes |
| 8.5ml SST vacutainer | BD Biosciences | 367988 | 1 tube |
| Vortexer | Fisher | 2215365 | |
| Dry bath incubator with heating block for microcentrifuge tubes | Fisher | 11-715-1250 | |
| Filtration/vacuum system for use within the cell culture hood | Fisher | 01-257-87 | |
| Fixed-angle rotor for microcentrifuge tubes with aerosol-tight lid | Eppendorf | 22637002 | |
| Refrigerated centrifuge with a swing-bucket rotor and aerosol-tight caps for 16 x 125mm vacutainers and 15ml polypropylene tubes | Eppendorf | 22628157 | 2, one does not need to be refrigerated |
| Nanodrop 2000 (recommended for accuracy of small volumes) or other spectrophotometric device | Fisher | 13-400-411 | |
| Agilent Bioanalyzer | Agilent Technologies | G2940CA | |
| Liquid nitrogen tank | Thermo Scientific | 11-676-56 | |
| -80 ˚C freezer | Thermo Scientific | 992RAK | |
| Sharps container | Fisher | 22-037-970 | |
| Biological waste container | Thermo Scientific | 1223P52 | |
| Biosafety Level 2 certified cell culture hood | Thermo Scientific | 13-261-315 |
References
- Hernandez, M. E., Martinez-Fong, D., Perez-Tapia, M., Estrada-Garcia, I., Estrada-Parra, S., Pavon, L. Evaluation of the effect of selective serotonin-reuptake inhibitors on lymphocyte subsets in patients with a major depressive disorder. Eur Neuropsychopharmacol. 20, 88-95 (2010).
- Weigelt, K., et al. TREM-1 and DAP12 expression in monocytes of patients with severe psychiatric disorders EGR3, ATF3 and PU.1 as important transcription factors. Brain Behav Immun. 25, 1162-1169 (2011).
- Robertson, M. J., et al. Lymphocyte subset differences in patients with chronic fatigue syndrome, multiple sclerosis and major depression. Clin Exp Immunol. 141, 326-332 (2005).
- Rotter, A., Asemann, R., Decker, A., Kornhuber, J., Biermann, T. Orexin expression and promoter-methylation in peripheral blood of patients suffering from major depressive disorder. J Affect Disord. 131, 186-192 (2011).
- Klengel, T., et al. Allele-specific FKBP5 DNA demethylation mediates gene-childhood trauma interactions. Nat Neurosci. 16, 33-41 (2013).
- Segman, R. H., Shefi, N., Goltser-Dubner, T., Friedman, N., Kaminski, N., Shalev, A. Y. Peripheral blood mononuclear cell gene expression profiles identify emergent post-traumatic stress disorder among trauma survivors. Mol Psychiatry. 10, 500-513 (2005).
- Smith, B. H., et al. Cohort Profile: Generation Scotland: Scottish Family Health Study (GS:SFHS). The study, its participants and their potential for genetic research on health and illness. Int J Epidemiol. 42, 689-700 (2013).
- Mallone, R., et al. Isolation and preservation of peripheral blood mononuclear cells for analysis of islet antigen-reactive T cell responses: position statement of the T-Cell Workshop Committee of the Immunology of Diabetes Society. Clin Exp Immunol. 163, 33-49 (2011).
- Duvigneau, J. C., Hartl, R. T., Teinfalt, M., Gemeiner, M. Delay in processing porcine whole blood affects cytokine expression. J Immunol Methods. 272, 11-21 (2003).
- Debey, S., et al. Comparison of different isolation techniques prior gene expression profiling of blood derived cells: impact on physiological responses, on overall expression and the role of different cell types. Pharmacogenomics J. 4, 193-207 (2004).
- Uddin, M., et al. Epigenetic and immune function profiles associated with posttraumatic stress disorder. Proc Natl Acad Sci U S A. 107, 9470-9475 (2010).
- Kessler, R. C., Wang, P. S. The descriptive epidemiology of commonly occurring mental disorders in the United States. Annu Rev Public Health. 29, 115-129 (2008).
- . QIAamp® DNA Mini and Blood Mini Handbook Available from: https://www.qiagen.com/us/resources/resourcedetail?id=67893a91-946f-49b5-8033-394fa5d752ea (2010)
- Koenen, K. C., et al. SLC6A4 methylation modifies the effect of the number of traumatic events on risk for posttraumatic stress disorder. Depress Anxiety. 28, 639-647 (2011).
- Walsh, K., Uddin, M., Soliven, R., Wildman, D. E., Bradley, B. Associations between the SS variant of 5-HTTLPR and PTSD among adults with histories of childhood emotional abuse: Results from two African American independent samples. J Affect Disord. 161, 91-96 (2014).
- Bustamante, A. C., et al. Childhood maltreatment is associated with epigenetic differences in hypothalamic-pituitary-adrenal (HPA) axis genes in the Detroit Neighborhood Health Study. , (2013).
- Sipahi, L., et al. Longitudinal epigenetic variation of DNA methyltransferase genes is associated with vulnerability to post-traumatic stress disorder. Psychol Med. 44, 3165-3179 (2014).
- Uddin, M., Koenen, K. C., Aiello, A. E., Wildman, D., de los Santos, R., Galea, S. Epigenetic and inflammatory marker profiles associated with depression in a community-based epidemiologic sample. Psychol Med. 41, 997-1007 (2011).
- Uddin, M., et al. Post-traumatic stress disorder is associated with immunosenescent T cell phenotypes in the Detroit Neighborhood Health Study. , (2011).
- Uddin, M., et al. Post-traumatic stress disorder is associated with immunosenescent T cell phenotypes in the Detroit Neighborhood Health Study. , (2011).
- Uddin, M. Biological signatures of post-traumatic stress disorder in the Detroit Neighborhood Health Study. , (2010).
- Aiello, A. E. Cytomegalovirus antibodies as a marker of immunosenescence in the Detroit Neighborhood Health Study. , (2010).
- Bustamante, A. C., et al. . Distinct gene expression profiles characterize lifetime PTSD and childhood maltreatment in the Detroit Neighborhood Health Study. , (2013).

