5.3: 산및염기: Ka,pKa,상대강점
이 단원에서는 산과 염기의 상대적 강점의 중요한 측면을 탐구합니다. 산의 강도는 물속의 물가베이스로산 해리와 하이드로늄 이온에 의해 평가된다. 강한 산의 완전한 해리는 매우 높은 농도의 하이드로늄 이온으로 확인된다. 그 결과, 불완전한 해리 공정은 약한 산을 확증한다. 따라서 평형은 이러한 반응에서 약한 산에 대한 강한 산과 후진에 대한 전진 방향에 있습니다.
따라서, 산 강도는 불균성 분자 및 하이드로늄 이온의 농도에 의해 정의된다. 약한 산은 평형 상수(Keq)를통해 추정될 수 있지만, 희석용용은 일정하며, 수분 농도의 변화는 무시할 수 있다. 이러한 관찰은 산도 상수 또는 해리 상수,Ka로알려진 변형된 평형 상수로 이어집니다. 산도의 척도인 산도 상수를 정의하려면 일반 산염 염기 반응을 고려하십시오.
그림 1: 물 에서 일반 산의 해리
여기서 HA는 일반 산을 나타내고 A- 그 컨쥬게이트 베이스를 나타냅니다. 다음 식은 이 반응에 대한 산도 상수를 나타낸다.
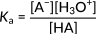
그림 2: 일반 산 해리에 대한 산성 상수
이 관계는 분자에 있는 하이드로늄 이온의 집중에 집중합니다. 따라서, 이러한 이온의 증가는 산도상수 증가와 강한 산으로 이어집니다. 유기산에서는, 전형적으로, Ka의 크기는 여러 순서에 걸쳐 퍼져. 따라서, 다른 산의 강도는 PK값의 관점에서 표현되며, Ka의음의 logarithm으로계산됩니다.
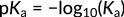
그림 3: pKa의 표정
여기서 빼기 기호는 pK값과 산도 사이의 역관계를 나타냅니다. 벤조산대 하이드로브롬산으로 해명됨에 따라, 값이 높을수록 K값이 더 낮은K값과 같으며 이는 산이 약하다는 것을 나타낸다.
상기 원리를 확장함으로써 pK값은 베이스의 강도를 확립할 수도 있다. 염기의 해리가 컨쥬게이트 산을 형성하기 때문에, 강한 컨쥬게이트 산은 약한 염기에 해당한다. 예를 들어, 메탄올 대 에틸라민을 고려하십시오. pK값을가진 메탄올의 컨쥬게이트산은 -3.8의값이 pK값을가진 에틸라민의 공주산보다 더 산성이며 10.6값이다. 따라서 메탄올은 에틸라민보다 약한 기지입니다.


