18.3: 伏打/ 伽凡尼电池
自发化学反应
自发的氧化还原反应在性质上非常强烈。 为遥控器供电的一次性 AA 电池中发生的化学反应就是自发氧化还原反应的一个例子。 另一个示例是将卷绕铜线浸入一个水性银硝酸盐溶液中。 反应表明,颜色从无色变为明亮的蓝色,并在铜线上形成灰色沉淀物,色彩逐渐,视觉上令人印象深刻。 在这项实验中,铜会被氧化以形成铜质离子,从而使溶液呈蓝色,而银色离子则会被还原为在电线上形成银沉淀。
这种反应可以归纳如下:
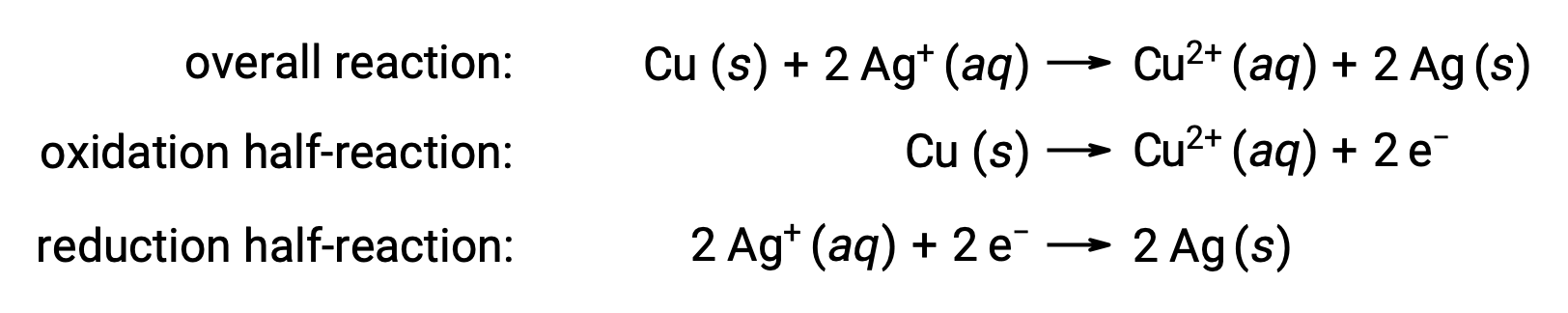
在这里,电子从铜线直接和自发地转移到水化银离子。
电化学细胞和原电池(伽凡尼电池)
假设设备包含氧化还原系统的所有反应物和生成物,但阻止反应物之间的物理接触。 因此,电子的直接传输是被阻止的;相反,它是通过与分离的反应物相接触的外部电路间接发生的。 这类装置通常称为电化学细胞。
电化学电池是一种仪器,在该仪器中,氧化还原反应产生电流,而反应原子之间不会直接接触。 因自发氧化还原反应而产生电流的电化学细胞称为电镀或伏打电池 (以 Luigi Galvani 和 Alessandro Volta 命名)。
原电池(伽凡尼电池)的组件
图 1 所示为基于铜和银 (i) 之间自发反应的原电池(伽凡尼电池)。 典型的原电池(伽凡尼电池)由两个半电池组成,每个共轭都包含一个氧化还原反应物对或一对单个。 左侧的半电池包含铜 (0) /Cu (II) 对数,形式为实心铜箔和硝酸铜水溶液。 右侧半电池包含 Ag (i) /Ag (0) 对数作为固体银箔和水化银硝酸盐溶液。 外部电路通过其实心箔连接到每个半电池,这意味着 Cu 和 Ag 箔各自充当电极。 反应发生在每个半电池反应混合物及其相应电极之间的接口处。 阳极是发生氧化的电极,它具有负电荷,而阴极是发生还原的电极,它具有正电荷。
这两个半电池通过盐桥连接,盐桥是一个倒 U 形管,其中含有一种凝胶或惰性电解质的糊状物,如氯化钾或硝酸铵。 盐桥有助于使反应混合物保持分离,同时确保反应的电荷平衡。 该细胞中的自发反应会在阳极半电池中产生 Cu2+ 阳离子,并在阴极半电池中消耗 AA+ 离子,从而产生来自盐桥的惰性离子补偿性流动,从而保持电荷平衡。 盐桥提供惰性离子的流动,确保通过中和阳极和阴极处的正负离子的积聚来继续反应。 因此,阳极半电池中 Cu2+ 浓度的增加是由盐桥流入 NO3− 来平衡的,而 Na+ 流入阴极半电池的流量补偿了 AA+ 浓度的下降。
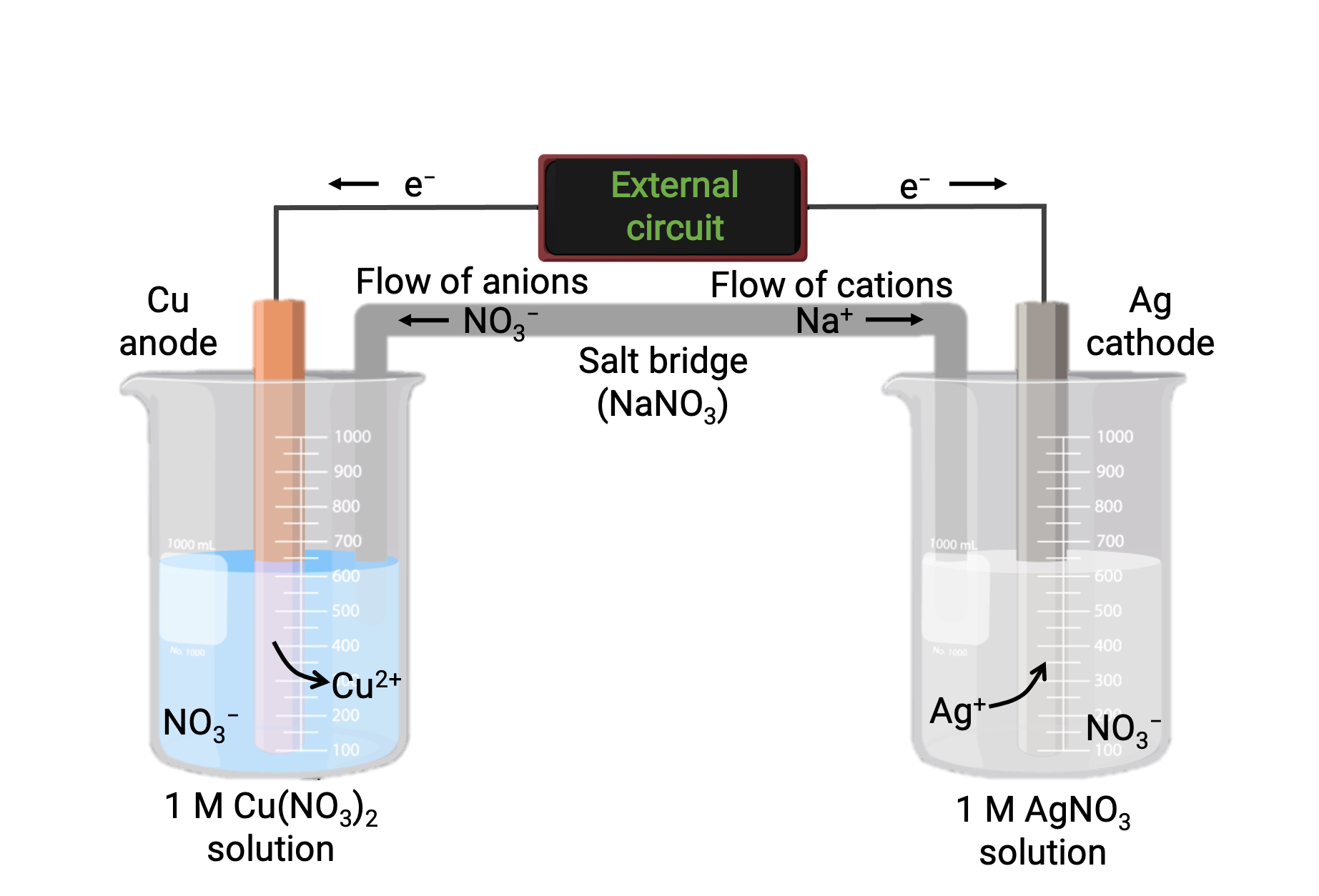
图 1 :基于铜离子和银离子之间自发反应的原电池(伽凡尼电池)。
使用电池示意图或电池符号表示原电池(伽凡尼电池)。
使用电池示意图或电池符号象征性地表示原电池(伽凡尼电池)。
• 在电池示意图中,组件相位之间的所有接口都由垂直平行线表示。
• 如果两个或多个组件在同一阶段存在,它们将以逗号分隔。
• 阳极在原理图的左侧表示,阴极在右侧表示。
• 双垂直线表示两个半反应之间的盐桥或多孔分区。
• 根据惯例,原理图以阳极开始,从左到右依次识别单元内遇到的相位和接口,最后是阴极。
例如,上述原电池(伽凡尼电池)由一个实心铜阳极组成,该阳极浸入通过盐桥连接到一个水银 (i) 硝酸盐溶液,其中是实心银阴极。 按照上述准则将此语句转换为符号,将生成单元格原理图:
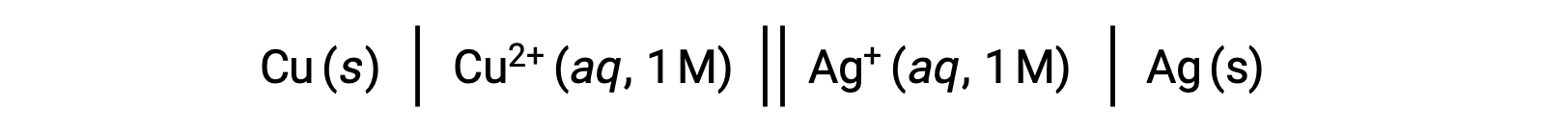
本文改编自 Openstax, 化学 2e, 第17.2节:原电池(伽凡尼电池)。


